Получение красного железоокисного пигмента
Иллюстрации
Показать всеИзобретение может быть использовано в лакокрасочной промышленности. Способ получения красных железоокисных пигментов включает получение раствора нитрата железа (II) и первого содержащего оксид азота потока путем реакции железа с азотной кислотой. Затем получают водную суспензию гематитовых ядер и второй содержащий оксид азота поток путем реакции железа с азотной кислотой. Получают суспензию гематитового пигмента путем реакции водной суспензии гематитовых ядер с раствором нитрата железа (II) и по меньшей мере одним щелочным осадителем в присутствии по меньшей мере одного содержащего кислород газа и/или путем реакции водной суспензии гематитовых ядер с раствором нитрата железа (II)), железа и по меньшей мере одного содержащего кислород газа. При этом получают третий содержащий оксид азота поток. Отделяют гематитовый пигмент от водной фазы. Окисляют второй содержащий оксид азота поток с получением окисленного второго содержащего оксид азота потока. Приводят в контакт первый содержащий оксид азота поток, и/или третий содержащий оксид азота поток, и/или окисленный второй содержащего оксид азота поток с водной промывочной фазой, получая предварительно очищенный газовый поток и промывочную фазу, обогащенную азотной кислотой. Удаляют монооксид диазота и/или нитрозные газы от предварительно очищенного газового потока нагреванием до температуры от 200 до 1400°С с получением очищенного газового потока. Изобретение позволяет повысить экологическую безопасность при получении красных железоокисных пигментов с широким цветовым спектром и высоким выходом. 20 з.п. ф-лы, 12 ил.
Реферат
Настоящее изобретение относится к улучшенному способу получения красных железоокисных пигментов посредством процесса Пеннимана с помощью нитрата (также называемого нитратным процессом или процессом конго красного) и к установке для осуществления этого процесса, а также к применению агрегата для производства красных железоокисных пигментов процессом Пеннимана с помощью нитрата.
Оксиды железа используются во многих областях промышленности. Их применяют, например, в качестве окрашивающих пигментов в керамике, строительных материалах, пластмассах, чернилах, красках и бумаге, они служат в качестве основы для различных катализаторов или подложек, и способны адсорбировать или абсорбировать загрязняющие вещества. Магнитные оксиды железа находят применение в магнитных запоминающих устройствах, тонирующих составах или ферромагнитных жидкостях, или в медицинских использованиях, таких как, например, в качестве контрастного вещества для магнитно-резонансной томографии.
Оксиды железа можно получить водным осаждением и реакциями гидролиза солей железа (Ullmann's Encyclopedia of Industrial Chemistry, VCH Weinheim 2006, Глава 3.1.1. Iron Oxide Pigments, стр. 61-67). Железоокисные пигменты посредством процесса осаждения получают из растворов солей железа и щелочных соединений в присутствии воздуха. Благодаря целевому контролю реакции также возможно таким образом получить мелкоизмельченные частицы гетита, магнетита и маггаемита. Однако красные пигменты, полученные этим процессом, проявляют относительно низкую интенсивность цвета и, следовательно, используются главным образом в промышленности строительных материалов.
Однако водное получение мелкоизмельченного гематита, соответствующего модификации α-Fe2O3, является намного более затруднительным. В результате применения стадии вылеживания также возможно получение гематита прямым водным осаждением с помощью добавления мелкоизмельченного оксида железа в модификации маггаемита, γ-Fe2O3, или модификации лепидокроцита, γ-FeOOH, в качестве нуклеирующего материала [US 5421878; ЕР 0645437; WO 2009/100767].
Дополнительным способом получения красных железоокисных пигментов является процесс Пеннимана (US 1327061; US 1368748; US 2937927; ЕР 1106577А; US 6503315). В этом процессе железоокисный пигмент получают растворением и окислением металлического железа с добавлением ядра соли железа и оксида железа. Соответственно в SHEN, Qing; SUN, Fengzhi; Wujiyan Gongye 1997, (6), 5-6 (CH), Wujiyan Gongye Bianjib, (CA 128:218378n) раскрыт процесс, в котором разбавленная азотная кислота действует на железо при повышенных температурах. Это производит суспензию гематитовых ядер. Эта суспензия формируется традиционным образом с образованием суспензии красного пигмента, и пигмент выделяют из этой суспензии при желании образом, который сам по себе является обычным. Интенсивность цвета красных пигментов, полученных этим процессом, однако является относительно низкой, подобно интенсивности цвета коммерческого продукта сорта 130, и, следовательно, эти пигменты применяют главным образом в промышленности строительных материалов. ЕР 1106577 А раскрывает вариант процесса Пеннимана, охватывающий воздействие на железо разбавленной азотной кислоты при повышенной температуре с целью получения ядер, т.е. мелкоизмельченных оксидов железа, имеющих размер частиц менее чем или равный 100 нм. Взаимодействие железа с азотной кислотой является сложной реакцией и в зависимости от условий эксперимента может привести или к пассивированию железа и, следовательно, к прекращению реакции, или к растворению железа с образованием растворенного нитрата железа. Оба варианта развития реакции являются нежелательными, и получение мелкоизмельченного гематита осуществляется только при определенных условиях. ЕР 1106577 А описывает подобные условия для получения мелкоизмельченного гематита. Здесь железо вводят в реакцию с разбавленной азотной кислотой при температурах между 90 и 99°С. WO 2013/045608 описывает процесс получения красных железоокисных пигментов, в котором улучшена реакционная стадия получения ядер, т.е. мелкоизмельченного гематита, имеющего размер частиц менее чем или равный 100 нм.
Эти по существу эффективные процессы, которые позволяют прямое получение высококачественных красных оксидов железа с большой вариацией в значениях цвета, тем не менее страдают от следующих недостатков:
1. Выделение оксидов азота формулы NOm, в которой азот может иметь различные степени окисления между +1 и +5. Оксиды азота могут быть токсичными (причем примерами являются нитрозные газы NO, NO2 и N2O4, также идентифицированные, в общем случае, как "NOx"); они генерируют смог, разрушают атмосферные озонный слой под действием УФ излучения и являются парниковыми газами. Конкретно монооксиды диазота являются более сильными парниковыми газами, чем диоксид углерода, на коэффициент, равный приблизительно 300. Кроме того, в настоящее время считают, что монооксид диазота является наиболее мощным разрушителем озона. В случае процесса Пеннимана с азотной кислотой нитрозные газы NO и NO2, а также монооксид диазота образуются в значительных количествах.
2. Процесс Пеннимана с азотной кислотой приводит к образованию содержащих азот сточных вод, которые содержат значительные количества нитратов, нитритов и аммиачных соединений.
3. Процесс Пеннимана с азотной кислотой является очень энергоемким, так как он включает нагревание больших объемов водных растворов до температур от 60°С до 120°С посредством внешнего энергопитания. Кроме того, в результате введения в реакционную смесь содержащих кислород газов в качестве окислителей энергоносители удаляются из реакционной смеси (отгонка паром), и их необходимо поставлять еще раз в форме тепла.
Следовательно, цель заключалась в предоставлении эффективного и экологически безопасного процесса получения красных железоокисных пигментов, который избегает приведенные выше недостатки, причем с одной стороны красные железоокисные пигменты получают с широким цветовым спектром с высоким выходом, и с другой стороны сводится к минимуму фракция содержащих азот побочных продуктов, выделяющихся в окружающую среду.
Обнаружен процесс получения красных железоокисных пигментов, который достигает эту цель, и также предоставляет установку, в которой можно проводить этот процесс в промышленном масштабе.
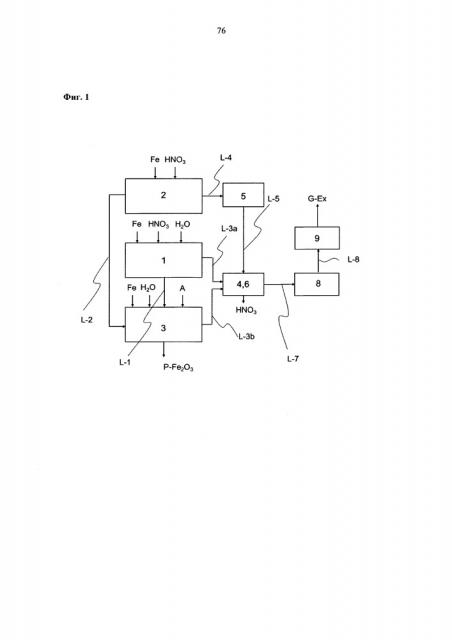
Способ согласно изобретению включает по меньшей мере стадии
a) получения раствора нитрата железа (II) путем реакции железа с азотной кислотой, получая таким образом первый содержащий оксид азота поток и необязательно далее отделения любого непрореагировавшего железа от раствора нитрата железа (II), полученного таким образом,
b) получения водной суспензии гематитовых ядер посредством взаимодействия железа с азотной кислотой, получая таким образом второй содержащий оксид азота поток, и необязательно далее отделения любого непрореагировавшего железа от суспензии гематитовых ядер, полученной таким образом,
c) получения водной суспензии гематитового пигмента посредством
I. взаимодействия водной суспензии гематитовых ядер из стадии b) с раствором нитрата железа (II) из стадии а) и по меньшей мере одного щелочного осадителя в присутствии по меньшей мере одного содержащего кислород газа, и/или путем реакции
II. взаимодействия водной суспензии гематитовых ядер из стадии b) с раствором нитрата железа (II) из стадии а), железа и по меньшей мере одного содержащего кислород газа,
получая таким образом третий содержащий оксид азота поток.
d) выделения гематитового пигмента, присутствующего в водной суспензии гематитового пигмента из водной фазы,
e) окисления второго содержащего оксид азота потока из стадии b), получая окисленный второй содержащий оксид азота поток.
f) контакт первого содержащего оксид азота потока и/или третьего содержащего оксид азота потока и/или окисленного второго содержащего оксид азота потока из стадии е) с водной промывочной фазой, получая таким образом предварительно очищенный газовый поток и промывочную фазу, обогащенную азотной кислотой.
g) Удаления монооксида диазота и/или нитрозных газов из предварительно очищенного газового потока из стадии f) нагреванием до температуры от 200 до 1400°С необязательно в присутствии по меньшей мере одного катализатора, предпочтительно от 250 до 500°С в присутствии по меньшей мере одного катализатора и/или от 800 до 1400°С в отсутствии катализатора, получая таким образом очищенный газовый поток.
В одном предпочтительно варианте выполнения процесс согласно изобретению включает дополнительно к стадиям от а) до g) стадию
h) удаления по меньшей мере аммиачных соединений и/или нитритных соединений и/или нитратных соединений, в особенности по меньшей мере аммиачный соединений, нитратных соединений и нитритных соединений из водной фазы из стадии d) посредством способов, известных специалистам сами по себе, получая очищенную сточную воду и необязательно обогащенную солями сточную воду.
В дополнительном предпочтительном варианте выполнения процесс согласно изобретению включает в себя дополнительно к стадиям от а) до g) или от а) до h) одну или более стадий из
i) возврата обогащенной азотной кислотой водной фазы, образованной на стадии f) к стадии а), и/или b) и/или с), и/или
j) использования нагретого очищенного газового потока из стадии g) для предварительного нагревания предварительно очищенного газового потока из стадии f), образуя предварительно нагретый предварительно очищенный газовый поток и охлажденный очищенный отработанный газ.
На данный момент можно отметить, что объем изобретения охватывает все желательные и возможные комбинации этих компонентов, интервалы значений и/или параметры процесса, которые даны выше и представлены ниже, или основные или установленные в предпочтительных интервалах.
Обычно применяемое железо содержит железо в форме проволоки, листов, гвоздей, узелков или грубых опилок. Отдельные куски в этом случае имеют любую желательную форму и традиционно имеют толщину (измеренную, например, как диаметр проволоки или толщину листа) от около 0,1 миллиметра вплоть до около 10 миллиметров. Размер бухт проволоки или листов, которые применяются в процессе, в основном определяется практическими целями. Следовательно, должно быть возможно загрузить реактор исходным материалом без трудностей, как правило, через смотровой люк. Подобное железо вырабатывается наряду с другими способами как лом или как побочный продукт в металлообрабатывающей промышленности, причем примерами являются перфорированные металлические листы.
Железо, применяемое в процессе согласно изобретению, как правило, имеет содержание железа, равное >90%. Примеси, встречающиеся в этом железе, являются обычно посторонними металлами, такими как, например, марганец, хром, кремний, никель, медь, и другими элементами. Однако можно также применять без вреда железо высокой чистоты.
Азотная кислота, применяемая на стадиях а) и b) в процессе согласно изобретению, имеет концентрации от 10 до 67 мас. % HNO3, предпочтительно от 20 до 67 мас. % HNO3. На стадиях b) и/или с), кроме азотной кислоты также возможно применять другую кислоту, такую как, например, соляная кислота или серная кислота. Предпочтительно никакую дополнительную кислоту, кроме азотной кислоты, не применяют на этих стадиях процесса. В этом заключается преимущество, что водная суспензия гематитовых ядер, получаемая процессом согласно изобретению, и гематит имеют очень низкое содержание серы и содержание хлора. В этом заключается преимущество для применения катализаторов, так как для определенных реакций сера и хлор являются известными каталитическими ядами.
Растворы нитрата железа (II) в основном имеют концентрации от 50 до 300 г/л Fe(NO3)2 (число на основе безводного твердого вещества). Кроме Fe(NO3)2, растворы нитрата железа (II) могут также включать количества от 0 до 50 г/л Fe(NO3)2. Однако выгодно очень низкое количество Fe(NO3)3.
Оксиды азота для целей настоящего изобретения представляют собой содержащие азот и кислород соединения общей формулы NOy. Эта группа включает нитрозные газы (также называемые NOx) общей формулы NOm, где азот может иметь различные степени окисления между +1 и +5. Их примерами являются NO (монооксид азота, m=1, степень окисления +2), NO2 (диоксид азота, m=2, степень окисления +4), и N2O5 (m=2,5, степень окисления +5). NO2 находится в зависимом от температуры и давлении равновесии со своим димером N2O4 (степень окисления обоих +IV). В дальнейшем, NO2 будет относиться как к самому NO2, так и к его димеру N2O4. N2O (монооксид диазота, веселящий газ, m=0,5, степень окисления +1) также принадлежит к группе оксидов азота общей формулы NOy, но не числится в группе нитрозных газов.
Первый содержащий оксид азота поток из стадии а) или третий содержащий оксид азота поток из стадии с) процесса согласно изобретению в основном содержит от 1 до 200 г/м3 нитрозных газов (вычисленных как г/м3 NO2) и/или от 0,5 до 50 г/м3 N2O. Количество нитрозных газов и монооксида диазота в этих потоках может колебаться в широких интервалах. Стадия а) процесса согласно изобретению, как правило, производит небольшие количества нитрозных газов и монооксида диазота, которые обычно накапливаются над реакционной смесью в реакторе, так как эти реакторы обычно являются закрытыми. Введение воздуха или инертных газов, таких как азот, также называемых внешним воздухом, в реактор всасыванием или продуванием продуцирует первый содержащий оксид азота поток.
На стадии b) процесса согласно изобретению, как правило, в соответствии с условиями реакции производятся значительно более высокие количества нитрозных газов и монооксида диазота, чем в случае стадии а), и эти количества таким же образом накапливаются над реакционной смесью в реакторе, если эти реакторы закрыты, или направляются в линии, соединенные с реактором, если реакторы открыты, когда, например, превышены допустимые давления. Благодаря введению воздуха или инертных газов, например, азота, также называемых внешним воздухом, в реактор всасыванием или продуванием, можно тогда генерировать потоки с определенными уровнями нитрозных газов и монооксида диазота. Тогда количество нитрозных газов и монооксида диазота в этих потоках зависит от количества этих газов, образованных в ходе взаимодействия, и от количества внешнего воздуха, загруженного в установку, и от продолжительности загрузки внешнего воздуха, и можно, следовательно, регулировать до желательных уровней, выгодных для дополнительных технологических стадий. Может быть выгодно комбинировать первый и второй содержащие оксид азота потоки после выхода из реакторов или вводить первый содержащий оксид азота поток как заместитель внешнего воздуха в реактор для стадии b). Полученные комбинированные первый и второй содержащие оксид азота потоки в основном содержат от 1 до 50 г/м3 нитрозных газов (вычисленных как г/м3 NO2) и/или от 1 до 50 г/м3 монооксида диазота.
Второй содержащий оксид азота поток из стадии b) процесса согласно изобретению в основном имеет концентрацию от 1 до 2000 г/м3 нитрозных газов (вычисленных как г/м3 NO2) и от 0,5 до 2000 г/м3 монооксида диазота. В результате введения по меньшей мере одного содержащего кислород газа в реактор в ходе взаимодействия генерируется второй содержащий оксид азота поток. Количество нитрозных газов и монооксида диазота можно поэтому также регулировать через скорость течения по меньшей мере одного содержащего кислород газа.
Окисленный второй содержащий оксид азота поток, полученный после стадии е), в основном содержит не более чем 50%, предпочтительно менее чем 30%, более предпочтительно менее чем 15% первоначальной фракции монооксида азота, т.е. фракции, присутствующей до стадии f).
Водная суспензия гематитовых ядер, полученная на стадии b), в основном имеет концентрации от 50 до 300 г/л гематита, предпочтительно от 80 до 150 г/л гематита. Гематитовые ядра, полученные в соответствии со стадией b) и присутствующие в водной суспензии гематитовых ядер, имеют размер частиц, например, менее чем или равный 100 нм и/или удельную площадь поверхности по БЭТ от 40 м2/г до 150 м2/г. Этот гематит (α-Fe2O3) может также содержать фракции других фаз, например, гетит (α-FeOOH) и/или ферригидрит (5 Fe2O3⋅9 H2O).
По меньшей мере один щелочной осадитель из стадии с) в варианте I. представляет собой, например, NaOH, КОН, Na2CO3, К2СО3, NH3 или NH4OH, или другие гидроксиды и карбонаты щелочных металлов и щелочноземельных металлов или любые желательные их смеси. Предпочтение отдается применению гидроксидов щелочных металлов или карбонатам щелочных металлов, особенно предпочтение применению NaOH.
По меньшей мере один содержащий кислород газ из стадии с) в варианте I или II. представляет собой, например, воздух, кислород, NO, NO2, О3 или смеси приведенных газов. Воздух является предпочтительным.
Отделение гематитового пигмента, присутствующего в водной суспензии гематитовых ядер, из водной фазы в соответствии со стадией d) выполняется предпочтительно осаждением, фильтрацией или центрифугированием. Удаленная водная фаза включает наряду с другими компонентами нитратные соединения, нитритные соединения и аммиачные соединения и, таким образом, в основном имеет общее содержание азота от 0,2 до 10 г/л азота, предпочтительно от 0,2 до 5 г/л азота (вычисленное в каждом случае на элементарный азот).
Красный железоокисный пигмент, полученный процессом согласно изобретению, также упоминается альтернативно как гематитовый пигмент в связи с этим изобретением, содержит предпочтительно от 80 до 100 мас. % α-Fe2O3, кристаллическую решетку α-Fe2O3, содержащую от 0 до 10 мас. % кристаллической воды. Гематит, полученный процессом согласно изобретению, обладает широким цветовым спектром. На окраску гематита влияет размер частиц, распределение размера частиц, количество кристаллической воды и/или введение внешних атомов. Значения цвета измеряют способами, известными специалистам.
Водная промывочная фаза в основном представляет собой воду или разбавленную азотную кислоту, предпочтительно разбавленную азотную кислоту, более предпочтительно азотную кислоту, которая перемещается по круговому движению.
Обогащенная азотной кислотой промывочная фаза в основном имеет содержание HNO3 от 1 до 67 мас. %, предпочтительно от 5 до 67 мас. %.
Катализаторы представляют собой предпочтительно альтернативно катализаторы для разложения нитрозных газов и/или для разложения монооксида диазота. Примерами катализаторов являются активированные угли, силикагель, молекулярные сита, ванадий-цинковые катализаторы или хром-цинковые катализаторы.
Предварительно очищенный газовый поток в основном имеет температуру от 20 до 90°С, предпочтительно от 30 до 80°С, и содержит предпочтительно не более чем 50%, более предпочтительно менее чем 30%, очень предпочтительно менее чем 15% первоначальной фракции нитрозных газов (вычисленных как NO2), т.е. фракции, присутствующей перед стадией f).
Предварительно нагретый предварительно от 250 до 500°С, более предпочтительно от 300 до 450°С и от 0,5 до 20 г/м3 нитрозных газов (вычисленных как г/м3 NO2), предпочтительно от 0,5 до 20 г/м3 нитрозных газов (вычисленных как г/м3 NO2) и/или от 1 до 40 г/м3 N2O.
Очищенный отработанный газ в основном имеет температуру от 150 до 1500°С, предпочтительно от 150 до 500°С. Очищенный отработанный газ в основном содержит от 0,001 до 0,3 г/м3 нитрозных газов (вычисленных как г/м3 NO2), предпочтительно от 0,005 до 0,3 г/м3 нитрозных газов (вычисленных как NO2) и/или от 0,001 до 0,3 г/м3 N2O, предпочтительно от 0,005 до 0,3 г/м3 N2O.
Охлажденный очищенный отработанный газ в основном имеет температуру от 80°С до 450°С, предпочтительно от 150 до 350°С. Охлажденный очищенный отработанный газ в основном содержит от 0,001 до 0,3 г/м3 нитрозных газов (вычисленных как г/м3 NO2), предпочтительно от 0,005 до 0,3 г/м3 нитрозных газов (вычисленных как NO2) и/или от 0,001 до 0,3 г/м3 N2O, предпочтительно от 0,005 до 0,3 г/м3 N2O.
Очищенная сточная вода содержит только небольшие остаточные количества растворенных соединений азота. Очищенная сточная вода в основном имеет общее содержание азота не более чем 0,2 г/л азота, предпочтительно не более чем 0,1 г/л азота, более предпочтительно не более чем 0,02 г/л азота (вычисленного в каждом случае на элементарный азот).
Обогащенная солями сточная вода в основном содержит соли, которые не удалены в предшествующих стадиях очистки. Обогащенная солями сточная вода предпочтительно содержит сульфат.
Стадии а) и/или b) могут происходить любым способом, известным специалисту, для взаимодействия железа с азотной кислотой.
Например, на стадии а) от 0,4 до 10 молей железа на моль азотной кислоты взаимодействуют при температуре, равной 60°С или менее, предпочтительно от 10 до 60°С, с получением раствора нитрата железа (II). В случае применения избытка железа раствор нитрата железа (II) можно легко отделить от непрореагировавшего железа. В следующей порции необязательно добавляют дополнительное железо и/или дополнительную азотную кислоту.
Стадии b) и с) процесса согласно изобретению могут происходить любым способом, известным специалисту. Стадии b) и с) предпочтительно осуществляют в соответствии с процессами, описанными в ЕР 1106577 А или WO 2013/045608.
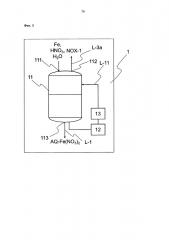
Это выполняется, например, применением стадии b) процесса согласно изобретению с генерацией суспензии гематитовых ядер, причем температура реакции воздействия азотной кислоты на железо составляет по меньшей мере 90°С, предпочтительно от 90 до 99°С.
В другом предпочтительном варианте выполнения стадии b) генерируют водную суспензию гематитовых ядер, причем азотная кислота имеет концентрацию от 2 до 6 мас. % HNO3 и применяется в молярном реакционном отношении железа к азотной кислоте (HNO3) от 1,5 до 16. В дополнительном предпочтительном варианте выполнения стадии b) генерируют водную суспензию гематитовых ядер, причем азотная кислота имеет концентрацию от 2 до 15 мас. % HNO3. В дополнительном предпочтительном варианте выполнения стадии b) применяют молярное реакционное отношение железа к азотной кислоте (HNO3) от 1,0 до 16.
В дополнительном предпочтительном варианте выполнения стадии b) получают водную суспензии гематитовых ядер, причем гематитовые ядра, присутствующие в водной суспензии гематитовых ядер, имеют размер частиц менее чем или равный 100 нм и удельную площадь поверхности по БЭТ от 40 м2/г до 150 м2/г, измеренную согласно DIN 66131, причем получение включает по меньшей мере стадии:
i) предоставления смеси железа и воды, имеющей температуру от 60 до 120°С,
ii) добавления азотной кислоты к смеси из стадии i), и
iii) необязательно дальнейшего отделения любого непрореагировавшего железа от водной суспензии гематитовых ядер, полученной таким образом.
В дополнительном предпочтительном варианте выполнения на стадии ii) азотную кислоту добавляют к смеси из стадии i) со скоростью такой, чтобы реакционная смесь предпочтительно нагревалась по меньшей мере на 15°С менее чем за 120 минут после окончания добавления азотной кислоты, даже без внешнего источника тепла. Подобным образом предпочтительно, чтобы реакционная смесь на стадии ii) достигала максимальной температуры от 105 до 160°С. Подобным образом предпочтительно, чтобы стадии i) и ii) протекали в сосуде под давлением. Подобным образом предпочтительно, чтобы после окончания добавления азотной кислоты на стадии ii), падение реакционной температуры до менее чем 100°С ожидалось до осуществления стадии iii).
В одном предпочтительном варианте выполнения варианта I. стадии с) температура в ходе взаимодействия составляет от 70 до 100°С, предпочтительно от 75 до 90°С. Дозируют раствор нитрата железа (II) из стадии а) и по меньшей мере один щелочной осадитель, и реакционную смесь окисляют по меньшей мере одним содержащим кислород газом, предпочтительно от 0,2 до 100 литров по меньшей мере одного содержащего кислород газа, предпочтительно воздуха, за час и на литр суспензии до тех пор, пока красный железоокисный пигмент не достигнет желательного оттенка цвета.
В одном предпочтительном варианте выполнения варианта II. стадии с) суспензию гематитового пигмента получают взаимодействием суспензии гематитовых ядер с железом и раствором нитрата железа (II) при температурах от 70 до 100°С, предпочтительно от 75 до 90°С, и окислением с помощью от 0,2 до 100 литров по меньшей мере одного содержащего кислород газа, предпочтительно воздуха, за час и на литр суспензии до тех пор, пока красный железоокисный пигмент не достигнет желательного оттенка цвета.
В дополнительном предпочтительном варианте выполнения варианта II. стадии с) водная суспензия гематитовых ядер из стадии b) взаимодействует с раствором нитрата железа (II) из стадии а) и железом, по меньшей мере одним содержащим кислород газом и по меньшей мере одной сульфатной солью, как например, сульфат железа (II) и/или сульфат щелочного металла или щелочноземельного металла, предпочтительно сульфатом железа (II) и/или сульфатом натрия, с получением красного железоокисного пигмента. Температура реакции составляет от 70 до 100°С, предпочтительно от 75 до 90°С. Применяемым по меньшей мере одним содержащим кислород газом является предпочтительно воздух, причем количество составляет предпочтительно от 0,2 до 50 л воздуха за час и на литр суспензии до тех пор, пока красный железоокисный пигмент не достигнет желательного оттенка цвета.
В дополнительном предпочтительном варианте выполнения стадии с) водная суспензия гематитовых ядер из стадии b) взаимодействует с раствором нитрата железа (II) из стадии а), по меньшей мере одним щелочным осадителем, железом, по меньшей мере одним содержащим кислород газом и необязательно по меньшей мере одной сульфатной солью, как, например, сульфат железа (II) и/или сульфат щелочного металла или сульфат щелочноземельного металла, предпочтительно сульфат железа (II) и/или сульфат натрия, с получением красного железоокисного пигмента. Температура реакции составляет от 70 до 100°С, предпочтительно от 75 до 90°С. По меньшей мере один щелочной осадитель добавляют к реакционной смеси более предпочтительно в конце взаимодействия, как, например, при остаточной концентрации ионов железа (II) менее чем или равной 10 г/л, очень предпочтительно при остаточной концентрации ионов железа (II) менее чем или равной 5 г/л., причем продолжают подачу содержащего кислород газа. Применяемый содержащий кислород газ предпочтительно содержит воздух, причем количество составляет предпочтительно от 0,2 до 50 л воздуха за час и на литр суспензии до тех пор, пока красный железоокисный пигмент не достигнет желательного оттенка цвета.
Подачу по меньшей мере одного содержащего кислород газа можно начинать во всех предпочтительных вариантах выполнения или во время фазы нагревания реакционной смеси, состоящей из суспензии гематитовых ядер из стадии b), раствора нитрата железа (II) из стадии а), и железа, или в конце фазы нагревания.
По меньшей мере одну сульфатную соль, например, сульфат железа (II) или сульфат щелочного металла или сульфат щелочноземельного металла, предпочтительно сульфат железа (II) и/или сульфат натрия, можно во всех предпочтительных вариантах выполнения применять в форме раствора, суспензии или твердого вещества. Твердое вещество в этом случае находится в форме безводного соединения или различных модификаций, содержащих кристаллическую воду. Сульфат железа (II) применяют предпочтительно в форме водного раствора или в форме твердого гептагидрата сульфата железа (II) или его суспензий.
В другом предпочтительном варианте выполнения стадии с) по меньшей мере одну сульфатную соль, например, сульфат железа (II) или сульфат щелочного металла или сульфат щелочноземельного металла, предпочтительно сульфат железа (II) и/или сульфат натрия, добавляют к реакционной смеси до и/или после начала подачи содержащего кислород газа. Преимущество заключается в том, что следует применять меньшее количество раствора нитрата железа (II) и что ускоряется осаждение гематитового пигмента, образованного в ходе взаимодействия, из суспензии гематитового пигмента. Это облегчает последующее отделение гематитового пигмента в стадии d) процесса согласно изобретению.
На стадии d) процесса согласно изобретению выполняется отделение красного железоокисного пигмента, присутствующего в суспензии, предпочтительно фильтрацией и/или осаждением и/или центрифугированием. Подобным образом предпочтительно осадок на фильтре промывают, и далее осадок на фильтре высушивают. Подобным образом предпочтительно до отделения красного железоокисного пигмента от водной фазы проводят одну или более стадию отсеивания, более предпочтительно с помощью сит различных размеров и с уменьшающимися размерами сит. Преимущество заключается в том, что посредством этих средств внешние вещества, например, металлические частицы, которые в противном случае загрязнили бы гематитовый пигмент, удаляются из суспензии гематитового пигмента.
Для отделения гематитового пигмента от водной фазы возможно осуществлять все способы, известные специалистам, например, осаждение с последующим удалением водной фазы или фильтрацию с применением фильтр-прессов, как, например, применение мембранных фильтр-прессов.
В одном предпочтительном варианте выполнения стадии d) по меньшей мере одну сульфатную соль, например, сульфат железа (II) или сульфат щелочного металла или сульфат щелочноземельного металла, предпочтительно сульфат железа (II) и/или сульфат натрия, можно добавлять к суспензии гематитового пигмента во время или до отсева и/или во время или до отделения. Преимущество заключается в том, что ускоряется осаждение гематитового пигмента из суспензии гематитового пигмента. Это облегчает последующее отделение красного железоокисного пигмента на стадии d) процесса согласно изобретению.
Далее необязательно присутствует по меньшей мере одна очистка осадка на фильтре или осадка, отделенного таким образом. После отделения и/или очистки необязательно красный железоокисный пигмент, отделенный таким образом, высушивают, например, с помощью фильтровальных осушителей, ленточных сушилок, пластицирующих сушилок, вращающихся распылительных сушилок, сушильных камер или распылительных сушилок. Высушивание происходит предпочтительно с применением ленточных сушилок, тарельчатых сушилок, пластицирующих сушилок и/или распылительных сушилок.
Окисление второго содержащего оксид азота потока из стадии b) на стадии е) осуществляется, например, посредством контакта второго содержащего оксид азота потока по меньшей мере с одним окислителем необязательно в присутствии одного или более катализаторов и/или высокоэнергетического излучения, например, УФ излучения. Окислителями являются в основном воздух, кислород, озон или пероксид водорода, предпочтительно воздух.
Окисление происходит, например, при температуре от 20 до 300°С.
Окисление происходит, например, при давлении от 0,08 МПа до 2 МПа (от 0,8 до 20 бар). Предпочтительно окисление происходит при давлениях между 0,08 МПа и 1 МПа (от 0,8 до 10 бар). В основном окисление ускоряется более высоким давлением. Одной из реакций во время окисления второго содержащего оксид азота потока является окисление NO до NO2.
На стадии f) первый содержащий оксид азота поток - и, в случае осуществления стадии с) в соответствии с вариантом II. также третий содержащий оксид азота поток - а также окисленный второй содержащий оксид азота поток из стадии е) контактируют с водной промывочной фазой для получения предварительно очищенного газового потока и обогащенной азотной кислотой промывочной фазы. В этой операции в частности, из содержащих оксид азота потоков стадий а) и с) или из окисленного содержащего оксид азота потока из стадии е) удаляют NO2.
Во время взаимодействия NO2 с водной промывочной фазой образуется азотная кислота и таким образом концентрация HNO3 водной промывочной фазы непрерывно возрастает в течение очистки содержащего NO2 потока, пока не будет достигнута желательная конечная концентрация. Конечная концентрация HNO3 составляет предпочтительно от 10 до 67 мас. %, более предпочтительно от 20 до 67 мас. %. Когда достигнута желательная конечная концентрация HNO3, образованную азотную кислоту удаляют из промывочного контура и замещают водой или азотной кислотой ниже желательной конечной концентрации HNO3.
Предварительно очищенный газовый поток, полученный согласно стадии f) процесса согласно изобретению, содержит, например, не более чем 50%, предпочтительно менее чем 30%, более предпочтительно менее чем 15% первоначальной фракции ΝΟ2, присутствующей до стадии f). NO, присутствующий в потоках, применяемых на стадии f), растворяется в водной фазе до намного меньшей степени, чем NO2, но содержание NO изменяется даже во время очистки частично посредством равновесных реакций или окисления. N2O является растворимым в водной фазе до значительно более низкой степени, чем NO2. Влияние очистки на концентрацию N2O газового потока в основном очень незначительно.
Стадию g) предпочтительно проводят в присутствии одного или более катализаторов. Соответствующие процессы достаточно хорошо известны специалистам как DeNOx процессы или даже SCR (Избирательное Каталитическое Восстановление) или NSCR (Не избирательное Каталитическое Восстановление) процессы. Также известен процесс для термического разложения монооксида диазота под названием DeN2O® процесс.
Предварительно очищенный газовый поток здесь в основном контактирует с аммиаком или химическим соединением, которое разлагается с образованием аммиака, например, мочевиной, в присутствии одного или более катализаторов, которые могут быть необязательно нанесены по меньшей мере на одну подложку. Катализаторы в основном включают диоксид титана, пентоксид ванадия и оксид вольфрама и/или цеолиты и/или платину и/или оксиды других металлов. Нитрозные газы и аммиак взаимодействуют здесь в реакции сопропорционирования с образованием азота и воды или с образованием азота, диоксида углерода и воды в случае применения мочевины, а не аммиака. В тоже время в зависимости от применяемого катализатора монооксид диазота термически расщепляется на азот и кислород (катализ разложения). Однако монооксид диазота может также расщепляться термически без катализатора до или после удаления других оксидов азота. Для этой цели монооксид диазота можно нагревать не непосредственно или непосредственно до требуемой температуры. Непосредственное нагревание происходит посредством сжигания углеродсодержащего топлива, например, природного газа или бензина, в присутствии отработанного газа, содержащего монооксид диазота. В этом случае диоксид углерода и азот образуются непосредственно. Стадию g) проводят предпочтительно в одну стадию и в присутствии по меньшей мере одного катализатора и в присутствии аммиака или по меньшей мере одного химического соединения, которое разлагается с образованием аммиака, например, мочевины. На этой стадии температура предварительно очищенного газового потока поднимается до температуры от 250 до 500°С, более предпочтительно от 300 до 450°С.
В другом варианте выполнения стадию g) осуществляют в две стадии. В этом случае предварительно очищенный газовый поток из стадии f)
i) нагревают до температуры от 250 до 500°С, более предпочтительно от 300 до 450°С, и далее
ii) нагревают до температуры от 800 до 1400°С.
В этом случае присутствует каталитическая реакция DeNOx, в которой разлагаются оксиды азота, такие как монооксид азота и диоксид азота, и на второй стадии происходит не каталитическое термическое разложение монооксида диазота.
На стадии h) процесса согласно изобретению в основном содержащие железо соединения, например, соли железа, особенно соли железа (II), и/или содержащие азот соединения, например, аммиачные соединения,