Субстратный раствор 3,3',5,5'-тетраметилбензидина гидрохлорида для иммуноферментного анализа
Иллюстрации
Показать всеИзобретение относится к биохимии, а именно к использованию готового субстратного раствора для иммуноферментного анализа. Для этого используют стабильный водный раствор 3,3',5,5'-тетраметилбензидина гидрохлорида и пероксида. следующего состава: 3,3',5,5'-тетраметилбензидин гидрохлорид - 0,35-0,40 г/л; пероксид водорода либо мочевины - 0,1-0,2 г/л; поливиниловый спирт - 1-2 г/л; гидроксипропилированный β-циклодекстрин - 2-3 г/л; маннитол - 30-60 г/л; динатриевая соль нитрилотриметилфосфоновой кислоты - 0,1-1,0 г/л; проклин 150 - 0,05 г/л в нитратном буфере при pH=3,7-3,8. Изобретение обеспечивает получение субстратного раствора для иммуноферментного анализа, отличающегося высокой активностью и высокой стабильностью при хранении. 2 табл., 7 пр.
Реферат
Настоящее изобретение относится к биохимии, а именно - к стабильному водному раствору 3,3',5,5'-тетраметилбензидина гидрохлорида (ТМБ⋅2HCl) и пероксида - пероксида водорода либо пероксида мочевины, готовому к использованию в качестве субстратного раствора в иммуноферментном анализе.
Иммуноферментный анализ (ИФА) применяют для определения наличия антигенов, чаще - антител к антигенам возбудителей различных инфекций. В основе ИФА лежит иммунная реакция антигена с антителом. Присоединение к антителам ферментной метки позволяет учитывать результат реакции антиген-антитело по скорости ферментативной активности. Наибольшее распространение получил твердофазный гетерогенный иммунный анализ - ELISA (enzyme linked immunosorbent assay). Анализ обычно проводят с использованием стандартных диагностических иммуноферментных наборов, основными компонентами которых являются полистирольные планшеты с иммобилизованными антителами или антигенами, конъюгаты антител или антигена с ферментом, субстраты ферментной метки. Во всех коммерческих тест-системах в качестве фермента используется пероксидаза хрена, а в качестве субстрата ферментативной реакции предложен в [Bos E.S., van der Doelen A.A., Van Rooy N., Schuurs A.H.W.M. // J. Immunoassay. - 1981. - V. 3-4. - P. 187-204] и наиболее часто применяется ТМБ. Продукт окисления ТМБ пероксидом водорода регистрируется фотометрически. Однако ТМБ в водном растворе пероксида плохо растворим и недостаточно стабилен. В связи с этим готовили свежий субстратный раствор непосредственно перед использованием, а именно смешиванием двух компонентов - раствора ТМБ из одного флакона и раствора пероксида водорода из другого флакона. Тем не менее, предпочтительно использование стабильного субстратного раствора, в состав которого входят и ТМБ, и пероксид. Это позволяет исключить стадию смешивания двух компонентов - ТМБ и пероксида - перед началом измерения ферментативной активности и использовать один и тот же набор в течение длительного времени.
В связи с тем, что ТМБ в воде нерастворим, его растворяют в органических растворителях (диметилсульфоксид, диметилформамид, спирты) или используют поверхностно-активные вещества.
Известен субстратный раствор, содержащий органические растворители [US Patent 5006461, заявлен 3 ноября 1989 г.], способ изготовления которого включает внесение ТМБ, растворенного в небольшом количестве диметилфурана, метанола или диметилсульфоксида, в нитратный буфер с добавкой поливинилпирролидона и пероксида водорода. Недостатком этой композиции является наличие в ее составе токсичного органического растворителя и недостаточная стабильность при хранении.
Известен [US Patent 5792618, заявлен 27 сентября 1996 г.] субстратный раствор для иммуноферментного анализа, который получают растворением ТМБ в диметилсульфоксиде, добавляют HCl, солюбилизируют в водном растворе гидроксипропилированного β-циклодекстрина. Добавки 1,2,6-гексантриола и этилендиаминтетрауксусной кислоты используют для стабилизации раствора к хранению, уксуснокислым натрием доводят рН до 4,28. Затем добавляют перекись водорода и изопропиловый спирт. Такой раствор может храниться до 18 месяцев при комнатной температуре. Недостатком этой композиции также является наличие в ее составе токсичного органического растворителя - диметилсульфоксида, а также недостаточная стабильность при хранении.
В качестве прототипа выбран субстратный раствор на чисто водной основе [Патент РФ №2268253, заявлен 28 сентября 2004 г] - композиция ТМБ гидрохлорида, пероксида мочевины, гидроксипропил-β-циклодекстрина, поливинилового спирта, проклина 150, гидрохлорида 2-меркаптоэтиламина и глицерина в цитратном буфере с рН 3,77, которая может дополнительно содержать моногидрат орцина. Гидрофильные комплексы включения ТМБ с гидроксипропил-β-циклодекстрином в водном растворе поливинилового спирта с добавкой глицерина создают устойчивую дисперсию, не склонную к расслоению. Гидрохлорид 2-меркаптоэтиламина и моногидрат орцина используют в качестве антиоксидантов, которые реагируют со свободными радикалами и таким образом предотвращают окисление ТМБ. Для предотвращения негативного влияния микрофлоры среды на стабильность препарата в качестве антибактериального средства добавляют проклин 150 в количестве 0,05 г/л, не оказывающем ингибирующего действия на пероксидазу. Использование этой композиции позволяет сохранять ТМБ в присутствии пероксида мочевины довольно длительное время и использовать ее в качестве субстратного раствора. Однако устойчивость композиции при хранении недостаточно высока - с течением времени активность субстратного раствора снижается.
Задача изобретения - создание устойчивого к длительному хранению водного раствора ТМБ и пероксида, не содержащего органических растворителей.
Поставленная задача решается композицией: гидрохлорид 3,3'5,5'-тетраметилбензидина (от 0,35 до 0,40 г/л), пероксид водорода либо мочевины (от 0,1 до 0,2 г/л), поливиниловый спирт (ПВС, от 1 до 2 г/л), гидроксипропилированный β-циклодекстрин (ЦД, от 2 до 3 г/л), маннитол (от 30 до 60 г/л), динатриевая соль нитрилотриметилфосфоновой кислоты (АФОН, от 0,1 до 1,0 г/л), проклин 150 (0,05 г/л) в среде цитратного буфера с рН от 3,7 до 3,8.
Согласно механизму окисления ТМБ [Кирейко А.В., Веселова И.А., Шеховцова Т.Н. // Биоорганическая химия. - 2006. - Т. 32. - №1. - С. 80-86] окисляется его основание, а не протонированная форма. Величина рКа перехода между основанием и протонированной формой составляет 3,25. При рН менее 2,5 ТМБ находится в виде хорошо растворимой в воде, но неактивной в процессе окисления протонированной формы. При рН более 4,0 ТМБ находится в форме нерастворимого в водной среде, но окисляющегося основания. В предлагаемой композиции оптимальными с точки зрения активности и растворимости ТМБ приняты согласованные значения концентрации ТМБ в пределах от 0,35 до 0,40 г/л и рН от 3,7 до 3,8.
Известно [Von Н. Gallati, I. Pracht. // J. Clin. Chem. Clin. Biochem. - 1985. - Vol. 23. - P. 453-460], что при концентрации пероксида менее 0,05 и более 0,2 г/л активность раствора снижается, концентрация пероксида в предлагаемой композиции (0,1-0,2 г/л) соответствует максимальной активности субстратного раствора. Концентрации ПВС, ЦЦ, маннитола и АФОН оптимизированы по устойчивости раствора к расслоению и антиоксидантному действию. Проклин 150 - консервант, в концентрации не более 0,05 г/л не оказывает ингибирующего действия на пероксидазу.
Предлагаемое изобретение иллюстрируется нижеприведенными примерами.
Примеры 1-6
Приготовление субстратного раствора.
В водном растворе цитратного буфера с рН 3,75 растворяют с разным соотношением концентраций (примеры №1-6, Таблица 1) следующие компоненты: ПВС, ЦД, маннитол, АФОН, проклин 150, ТМБ⋅2HCl. Композицию выдерживают при комнатной температуре не менее суток для образования комплекса включения ТМБ с ЦД. Вносят пероксид, перемешивают и убирают в холодильник. Через сутки субстратный раствор готов к испытаниям.
Оценка активности субстратного раствора
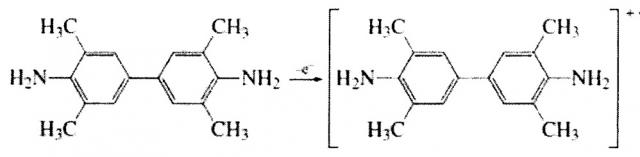
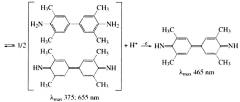
Продуктом одноэлектронного окисления ТМБ в ферментативной реакции является катион-радикал (Схема 1 [Кирейко А.В., Веселова И.А., Шеховцова Т.Н. // Биоорганическая химия. - 2006. - Т. 32. - №1. - С. 80-86.]), который находится в равновесии с бинарным комплексом, имеющим синюю окраску. Активность субстратного раствора оценивали спектрофотометрически по поглощению этого комплекса на длине волны максимума в электронном спектре при 655 нм.
Схема 1 - Схема окисления ТМБ
К 3 мл субстратного раствора прибавляют 0,2 мл свежеприготовленного и разбавленного до 1 мг в 100 л воды раствора пероксидазы. Через 15 мин инкубации измеряют плотность раствора при 655 нм.
Активность субстратных растворов по примерам №1-6 представлена в таблице 1.
Пример 7
Композиция отличается от приведенной в примере 1 тем, что вместо 0,13 г/л пероксида водорода используется 0,15 г/л пероксида мочевины. Активность субстратного раствора D655 нм составила 2,35.
Пример 8 (прототип)
Субстратный раствор по патенту РФ №2268253 следующего состава: ТМБ⋅2HCl (0,38 г/л), ПВС (1,28 г/л), ЦД (2,56 г/л), глицерин (62,5 г/л), гидрохлорид 2-меркаптоэтаноламина (0,0073 г/л), моногидраторцина (0,007 г/л), пероксид мочевины (0,157 г/л).
Активность субстратного раствора D655 нм составила 2,1.
Из данных примеров 1-7 следует, что субстратные растворы по предлагаемому техническому решению по активности не уступают, а в некоторых случаях превосходят прототип.
Сохраняемость субстратных растворов по примерам 1 и 8 оценивали по остаточной активности при хранении при температуре 37°С. Результаты испытаний на сохраняемость приведены в таблице 2.
Испытания на сохраняемость (таблица 2) демонстрируют существенно более высокую стабильность субстратных растворов по предлагаемому техническому решению по сравнению с прототипом. Снижение активности композиции (1) на 20% в течение 10 недель хранения при температуре 37°С соответствует гарантированному сроку хранения от 3 до 4 лет при температуре от 2°С до 8°С, рекомендованной зарубежными производителями субстратных растворов.
Водный субстратный раствор 3,3',5,5'-тетраметилбензидина гидрохлорида и пероксида для иммуноферментного анализа, содержащий поливиниловый спирт, гидроксипропил-β-циклодекстрин, проклин 150 и стабилизаторы для хранения, отличающийся тем, что в качестве стабилизаторов используют маннитол и динатриевую соль нитрилотриметилфосфоновой кислоты при следующем содержании компонентов:
| 3,3',5,5'-тетраметилбензидин гидрохлорид | 0,35-0,40 г/л |
| пероксид водорода либо мочевины | 0,1-0,2 г/л |
| поливиниловый спирт | 1-2 г/л |
| гидроксипропилированный β-циклодекстрин | 2-3 г/л |
| маннитол | 30-60 г/л; |
| динатриевая соль нитрилотриметилфосфоновой кислоты | 0,1-1,0 г/л |
| проклин 150 | 0,05 г/л |
| в среде цитратного буфера с рН | 3,7-3,8 |