Бифункциональное средство для дегазации и дезинфекции
Иллюстрации
Показать всеИзобретение относится к средствам комплексной дегазации высокотоксичных веществ и дезинфекции возбудителей опасных инфекционных болезней и может быть использовано при обработке защитной одежды и открытых участков кожи людей, оказавшихся в зоне заражения контаминантами химической и биологической природы, например, при выполнении мероприятий по ликвидации последствий техногенных аварий и чрезвычайных ситуаций. Бифункциональное средство представляет собой водный раствор окислителя - диоксида хлора - 0,2 мас.% и поверхностно-активного вещества - окиси алкилдиметиламина - 0,01 мас.%. Средство позволяет с высокой эффективностью и в короткие сроки снизить высокие уровни заражения контаминантами химической и биологической природы до достижения безопасного уровня обеззараживания. 13 табл., 6 пр.
Реферат
Изобретение относится к средствам комплексной дегазации высокотоксичных веществ (ВТВ) и дезинфекции возбудителей опасных инфекционных болезней (ВОБ) и может быть использовано при специальной обработке защитной одежды и открытых участков кожи людей, оказавшихся в зоне заражения контаминантами химической и биологической природы при выполнении мероприятий по ликвидации последствий техногенных аварий и чрезвычайных ситуаций.
В настоящее время известны два основных типа рецептур для дегазации ВТВ, некоторые из которых обладают и дезинфицирующей активностью [1, 2].
В состав таких рецептур входят вещества:
- имеющие выраженные окислительные свойства;
- имеющие выраженные основные свойства.
К первому типу рецептур, проявляющих окислительное действие, в первую очередь, относятся рецептуры на основе хлорсодержащих веществ, таких как гипохлорит кальция и натрия, натриевые соли хлорамидов бензол- и толуолсульфокислот (хлорамин Б и Т), дихлорамидов бензол- и толуолсульфокислот (дихлормины Б и Т), натриевая соль дихлоризоциануровой кислоты и другие, в которых в качестве окислителя выступает электрофильный реагент Сl+ [1].
К средствам окислительного действия также относятся вещества, реагирующие с выделением активного кислорода, на окислительной способности которого и основана дегазирующая активность таких соединений как пероксид водорода (перекись водорода, 30% раствор-пергидроль) и его органические и неорганические производные, например, гидроперит - комплексное соединение перекиси водорода и мочевины, соли пероксодисерной кислоты, пероксосольват фторида калия и другие носители перекиси водорода [3-6].
Известно средство химической дегазации ВТВ окислительного типа, включающее соль с анионом HSO3- (метадисульфит натрия) и сульфат меди. В процессе растворения этих компонентов в воде образуется анион SO5-, который является сильным окислителем, разрушающим ВТВ [7].
Для дегазации защитной одежды и оборудования, которые подверглись действию ВТВ из числа имитаторов кожно-нарывных и нервнопаралитических агентов, предложено использовать в газообразном виде соединения окислительного типа, такие как озон и диоксид хлора [8].
Известен ряд рецептур окислительного типа, состоящих из четвертичных аммониевых комплексов (бензилтриалкиламмоний хлориды) и окислителя (пероксид водорода или его производные) [9, 10], из клатрата додецилдиметиламмонийгалогенида с карбамидом [11].
Средства, предназначенные для дезинфекции воды, медицинских инструментов, хирургического инструмента и т.д., содержат такие окислители как перекись водорода, пергидроль, диоксид хлора и другие [12-17].
Ко второму типу дегазирующих средств, имеющих выраженный основный характер, относятся нуклеофильные реагенты, приводящие к гидролизу ВТВ, такие как щелочи (едкий натр, гидроокись кальция, карбонат натрия и другие), алкоголяты, амины.
В некоторых случаях эффект достигается за счет совместного использования реагентов, проявляющих как окислительные, так и основные свойства, например, водная суспензия дветретиосновной соли гипохлорита кальция (ДТС ГК), содержащая гипохлорит и гидроокись кальция.
Несмотря на эффективность и другие положительные качества, практически всем известным средствам свойственны те или иные существенные недостатки, не позволяющие широко использовать их по прямому назначению.
Наиболее существенными недостатками известных средств являются:
- недостаточно хорошая растворимость в воде (хлорсодержащие);
- раздражающее действие при попадании на кожу и в органы дыхания, а в случае попадания в глаза - тяжелые поражения (хлорсодержащие, пероксид водорода и его производные, щелочи);
- коррозионное действие, обесцвечивание тканей и лакокрасочных покрытий;
- разложение под действием тепла, влаги и углекислого газа, в связи с чем, средство необходимо хранить в герметичной таре в прохладном месте, укрытом от прямых солнечных лучей;
- содержание в своем составе примесей технических продуктов, которые являются нежелательными, а также пленкобразующих добавок, мешающих дальнейшему использованию оборудования, приборов и т.п.после высыхания средства.
Существует множество рецептур, но в основном, они предназначены только для дегазации ВТВ, либо только для дезинфекции ВОБ, и лишь некоторые из них являются бифункциональными, проявляющими одновременно дегазирующие и дезинфицирующие свойства [18-20].
Наиболее близким к заявляемому средству по назначению, функциональности и возможности обеспечивать высокий уровень эффекта в короткие сроки является средство, используемое при реализации способа дегазации тканей, зараженных ВТВ, представляющее собой газообразный диоксид хлора [8]. Газообразный диоксид хлора принят в качестве средства-прототипа
Для средства-прототипа, предложенного для дегазации различных тканей, зараженных ВТВ, характерен ряд недостатков. Прежде всего, его недостаточная эффективность в отношении ряда ВТВ. Если различные образцы тканей, зараженные 2-хлорэтилэтил-сульфидом, можно дегазировать полностью (100%) при экспозиции в течение 1 ч, то в случае заражения О-этилфторметилфосфонатом дегазация всех испытанных образцов проходит лишь частично (13-68%).
Кроме того, для проведения дегазации требуется замкнутая камера (палатка), в которую должен подаваться газообразный диоксид хлора из специальной установки (генератора) для его получения.
Персонал при нахождении в замкнутой камере во время проведения дегазации должен использовать средства защиты органов дыхания и глаз.
Нет сведений по дезинфицирующему действию средства-прототипа как на споровую, так и на вегетативную формы микроорганизмов.
Таким образом, средства для специальной обработки не только защитной одежды, но и открытых участков кожи людей, подвергшихся действию ВТВ и ВОБ, в доступных средствах информации не обнаружены.
Целью изобретения является создание бифункционального средства, отличающегося рядом свойств, благодаря которым его можно быстро получить, провести специальную обработку защитной одежды и открытых участков кожи людей, оказавшихся в зоне заражения высокотоксичными веществами и возбудителями особо опасных болезней:
- эффективность при дегазации различных типов высокотоксичных веществ;
- эффективность при дезинфекции микроорганизмов - возбудителей особо опасных болезней;
- хорошая растворимость в воде;
- простота получения;
- безвредность для кожи;
- безвредность для глаз;
- содержание в своем составе компонентов, которые доступны и выпускаются в промышленных условиях;
- простота и длительность хранения, удобство транспортировки.
Цель изобретения достигается за счет применения заявляемого средства, в состав которого входят сильный окислитель и поверхностно-активное вещество (ПАВ).
В качестве сильного окислителя используют диоксид хлора, благодаря чему заявляемое средство проявляет дегазирующие и дезинфицирующие свойства. В отличие от средства-прототипа диоксид хлора используют не в газообразном состоянии, а в виде водного раствора.
В качестве ПАВ в заявляемое средство введено четвертичное аммонийное соединение в виде окиси алкилдиметиламина. Указанное ПАВ дополнительно введено в состав заявляемого средства для усиления дегазирующих и дезинфицирующих свойств путем улучшения смачиваемости обрабатываемых поверхностей, изготовленных из различных материалов, в том числе сильно загрязненных и замасленных, а также для улучшения адгезии заявляемого средства с обрабатываемыми поверхностями. Принято во внимание и то, что используемое ПАВ проявляет самостоятельную дезинфицирующую активность при использовании его в концентрации, не превышающей принятую в заявляемом средстве.
Возможность достижения цели изобретения доказывается результатами экспериментальных исследований, представленными в следующих примерах.
Пример 1. Получение заявляемого средства.
Для получения заявляемого средства используют компоненты в следующем количестве, г:
| хлорит натрия (80%) | - 5,5; |
| бисульфат натрия | - 7,7; |
| окись алкилдиметиламина | - 0,1; |
| вода | - 1000 мл. |
Компоненты, входящие в состав заявляемого средства, отличаются хорошей растворимостью в воде.
Вначале получают диоксид хлора путем взаимодействия в водном растворе хлорита натрия и бисульфата натрия, взятых в соотношении 1:1,3. Избыток бисульфата натрия способствует более быстрому взаимодействию его с хлоритом натрия. Также существует мнение, что наличие в водном растворе диоксида хлора аниона HSCV приводит к стабилизации водного раствора диоксида хлора [21].
Для получения 1000 мл заявляемого средства к 1000 мл воды добавляют 5,5 г хлорита натрия и 7,7 г бисульфата натрия и дожидаются их полного растворения. К полученному раствору добавляют 0,1 г окиси алкилдиметиламина и перемешивают до полного его растворения. Заявляемое средство имеет желтоватый цвет и запах, похожий на запах хлора, с концентрацией диоксида хлора в водном растворе 0,2% (2 г/л). Продолжительность получения заявляемого средства составляет 15 мин при температуре 20°С.
Компоненты, входящие в состав заявляемого средства выпускаются в промышленных условиях и широко представлены на российском рынке в форме, удобной для хранения, транспортировки и получения заявляемого средства.
Пример 2. Оценка безопасности заявляемого средства.
Безопасность заявляемого средства оценивали путем определения токсикологических характеристик: токсического действия при внутрижелудочном введении, раздражающего действия на кожные покровы и глаза.
Оценка токсического действия.
Оценку токсического действия заявляемого средства проводили в соответствии с методическими указаниями по изучению общетоксического действия фармакологических веществ [22]. Токсическое действие было изучено на 24 белых крысах-самцах в возрасте 12 недель и массой 260-280 г, содержавшихся на стандартном режиме вивария: температура окружающего воздуха 22±2°С, 12-часовая синхронизированная смена светового периода, комбинированный корм и воду животные получали ad libitum.
В ходе эксперимента были сформированы 4 группы по 6 крыс в каждой: три опытные и одна контрольная.
Так как предполагается наружное применение заявляемого средства и возможность случайного попадания его внутрь незначительна, опытные группы получали заявляемое средство в теплом виде (37°С) внутрижелудочно в количествах: 1 мл, 1,5 мл и 2 мл.
Контрольная группа получала физиологический раствор в объеме 2 мл.
Наблюдение за подопытными животными проводилось в течение 14 суток, причем в первые сутки непрерывно. Фиксировалось общее состояние и поведение животных, прирост массы тела (1 раз в 7 суток), потребление корма и воды.
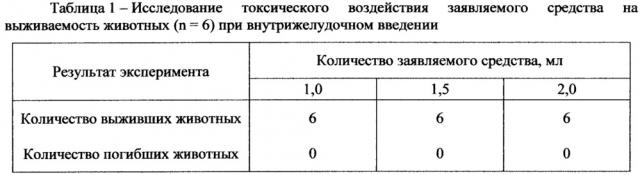
Критериями оценки токсического действия служили картина интоксикации и выживаемость животных (таблица 1).
Клиническое состояние всех подопытных животных в течение 14 суток наблюдения не выходило за пределы физиологической нормы, потребление корма и воды также соответствовало нормальным потребностям.
Введение заявляемого средства в количествах 1 мл, 1,5 мл и 2 мл не вызывало гибели подопытных животных. Не отмечали и какие-либо другие признаки негативного воздействия заявляемого средства. В частности, не отмечали какие-либо диспепсические явления. Во все дни наблюдения по общему состоянию и поведению животные трех опытных и контрольной групп не отличались.
Динамика изменения массы тела была положительной и практически не различалась во всех экспериментальных группах (таблица 2). Наблюдался равномерный прирост массы тела. Анализ прироста массы тела позволил установить, что введение заявляемого средства в указанных дозах не вызывает какие-либо достоверные отличия по сравнению с контрольной группой, получавшей физиологический раствор.
Таким образом, результаты наблюдений за подопытными животными на протяжении 14 суток после введения им заявляемого средства в указанных количествах показали, что при случайном попадании заявляемого средства внутрь организма оно не проявляет токсического воздействия.
Оценка раздражающего действия на кожные покровы.
Оценку раздражающего действия исследуемого средства на кожу проводили на крысах-самцах массой 250-300 г. В эксперименте участвовали две группы животных по 6 особей в каждой: опытная и контрольная.
В день опыта животных экспериментальных групп фиксировали на станках и ножницами освобождали от волосяного покрова участки кожи спины площадью 10 см2. Один раз в сутки в течение 7 суток животным опытной группы наносили заявляемое средство, животным контрольной группы - воду. Норма расхода составляла 1 мл/10 см2, температура воздуха - 16°С. Через 3 ч экспозиции каждый раз смывали заявляемое средство с кожи теплой водой.
Раздражающее действие заявляемого средства оценивали ежедневно визуально, а также путем измерения температуры поверхности кожи и толщины кожной складки в сравнении с контрольными измерениями, проведенными за 30 мин до опыта.
Измерение температуры поверхности кожи животных проводили с помощью прибора «ADA TemPro 300».
Измерение толщины кожной складки проводили с помощью микрометра МК 25-1 [23]. Взятую с двух сторон в складку кожу, слегка оттянутую, вводили между измерительными поверхностями микрометра. При появлении третьего звука трещотки измерение считали законченным.
В течение семидневного нанесения заявляемого средства на кожу и последующего наблюдения за животными визуально не отмечалось каких-либо признаков раздражения кожи (гиперемии, отека, инфильтрации, шелушения т.п.). Сами участки аппликации заявляемого средства животных не беспокоили, пальпация их была безболезненной. Температура поверхности кожи у подопытных животных практически не изменялась (таблица 3).
Измерение толщины кожной складки в местах аппликации заявляемого средства после трех- и семикратного нанесения показало, что она ни в одном случае достоверно не изменяется (р>0,05) по сравнению с исходными показателями. Результаты эксперимента объективно подтверждают отсутствие отека кожи после нанесения заявляемого средства (таблица 4).
Таким образом, семикратное ежедневное нанесение заявляемого средства на кожу крыс с аппликацией в течение 3 ч не сопровождалось раздражающим действием на кожу.
Кроме того, провели оценку кожно-резорбтивного действия заявляемого средства по показателям крови и относительной массе внутренних органов подопытных животных.
По клиническим показателям крови, определенным до начала эксперимента и по его окончании, различий не установлено (таблица 5).
Вскрытие животных опытной группы, проведенное через 7 суток, позволило установить, что органы грудной клетки не изменены. Легкие бледно-розовые, воздушные, без уплотнений на ощупь. Размеры сердца в пределах нормы. В полостях сердца содержится небольшое количество жидкой крови. Мышца сердца плотная, коричневой окраски.
Анализ изменений относительной массы и степени влажности внутренних органов подопытных животных позволил установить, что ежедневные аппликации заявляемого средства в течение семи суток не вызывают какие-либо достоверные отличия по сравнению с контрольной группой (таблицы 6 и 7).
Таким образом, в результате изучения кожно-резорбтивного действия установлено, что заявляемое средство не оказывает токсическое воздействие и не обладает способностью проникать в организм через неповрежденную кожу в количествах, вызывающих отравление подопытных животных, а также изменять функциональное состояние жизненно важных органов и систем организма при его ежедневном накожном нанесении в течение семи суток.
Патологоанатомические исследования животных, проведенные через семь суток после начала эксперимента показали отсутствие анатомо-морфологических различий между животными опытной и контрольной групп.
Таким образом, экспериментальные данные, полученные в ходе наблюдений за подопытными животными в семидневный период нанесения заявляемого средства, а также результаты патоморфологических исследований позволяют отнести заявляемое средство к безопасным.
Оценка раздражающего действия на глаза.
Раздражающее действие заявляемого средства на глаза животных изучали на кроликах путем оценки изменений слизистой оболочки и роговицы глаза, развившихся при внесении заявляемого средства в конъюнктивальный мешок.
В эксперименте участвовала группа кроликов из 6 особей. В опыт брали клинически здоровых кроликов без видимых повреждений глаз. В шприц набирали заявляемое средство и, применяя инъекционные иглы различного диаметра, подбирали каплю массой 10±1 мг. На протяжении всего эксперимента животные находились в свободном состоянии (не фиксированы). Шприцом через инъекционную иглу вносили одну каплю заявляемого средства в конъюнктивальный мешок при оттягивании нижнего века глаза, второй глаз служил контролем.
Оценку раздражающего действия заявляемого средства проводили визуально сразу после его внесения в конъюнктивальные мешки глаз, и затем через 1 ч, 2 ч, 48 ч и 72 ч. Оценку реакции слизистой оболочки глаза выражали в баллах по шкале, приведенной в ГОСТ Р ИСО 10993-10-2009 [24]. Оценка в баллах свидетельствовала: 0 - видимой реакции нет, 1 - легкое покраснение конъюнктивы, 2 - покраснение конъюнктивы и частично склеры, 3 - резкое покраснение конъюнктивы и всей склеры, гнойный офтальмит.
Помимо этого следили за появлением гиперемии, отечности, инъекции сосудов склеры и состоянием зрачков. Оценивали влияние заявляемого средства и по характеру конъюнктивита (поверхностный, глубокий), ожогам слизистой I, II и III-степени.
После введения заявляемого средства (непосредственно после инсталляции) наблюдалось неполное смыкание век глаза в течение от 5 мин до 15 мин.
Введение заявляемого средства не вызывало у подопытных животных обильного слезотечения, отека конъюнктивы и других симптомов.
Гиперемию слизистых оболочек глаз констатировали у всех подопытных животных, начиная сразу после нанесения заявляемого средства. Через одни сутки гиперемия слизистых оболочек глаз кроликов исчезла.
Общее состояние кроликов в экспериментах оставалось без изменений.
Таким образом, экспериментально доказано, что заявляемое средство при внесении его в конъюнктивальный мешок глаз кроликов, не оказывает существенного раздражающего действия на слизистую оболочки и роговицу глаз.
Пример 3. Исследование дегазирующей эффективности заявляемого средства в отношении 2,2'-дихлордиэтилсульфида.
При исследовании дегазирующей эффективности заявляемого средства в отношении 2,2'-дихлордиэтилсульфида в качестве тест-объектов использовали:
- ткань хлопкополиэфирную [25];
- белье альпинистское [26].
Заражение тест-объектов 2,2'-дихлордиэтилсульфидом перед проведением дегазации составляло 1 мг, что соответствовало уровню заражения образцов тканей 2-хлорэтилэтил-сульфидом при использовании средства-прототипа - 1 мг (8,8×10-6 моль) [8].
На указанные тест-объекты методом орошения наносили заявляемое средство с нормой расхода 0,4 л/м2 и выдерживали в течение 30 мин. Затем из-под тест-объекта извлекали сорбционные подложки из бязи, пропитанные дибутилфталатом и экстрагировали в этаноле. Экстракт анализировали для определения остаточного количества ВТВ, которое определяли колориметрическим методом с использованием реактива Т-135 [8].
Критерием дегазирующей эффективности заявляемого средства в отношении 2,2'-дихлордиэтилсульфида служило остаточное количество ВТВ на тест-объектах через 10 мин и 30 мин после начала дегазации.
Результаты экспериментов представлены в таблице 8. Как видно, в случае использования заявляемого средства необходимая полнота дегазации 2,2'-дихлордиэтилсульфида достигается после однократной обработки в течение 30 мин.
В случае же обработки средством-прототипом полная дегазация 2-хлорзтилэтил-сульфида (аналог 2,2'-дихлордиэтилсульфида) достигалась при обработке тест-объектов из различных тканей в течение 1 ч [8].
Таким образом, экспериментально установлено, что заявляемое средство пригодно для обработки тест-объектов из различных тканей при высокой степени зараженности 2,2'-дихлордиэтилсульфидом и при этом обладает такой же эффективностью как и средство-прототип, но в отличие от средства-прототипа полная дегазация обеспечивается при меньшем в 2 раза времени экспозиции заявляемого средства.
Пример 4. Исследование дегазирующей эффективности заявляемого средства в отношении О-этил-S-β-диизопропиламиноэтилметилфосфоната.
Оценку дегазирующей активности заявляемого средства в отношении О-этил-S-β-диизопропиламиноэтилметилфосфоната проводили орошением аналогично приведенному в примере 3. Норма расхода заявляемого средства составила 0,4 л/м2. В качестве тест-объектов также использовали ткань хлопкополиэфирную и белье альпинистское.
Заражение тест-объектов O-этил-S-β-диизопрошшаминоэтилметилфосфонатом перед проведением дегазации составляло 1 мг.
Критерием дегазирующей эффективности заявляемого средства в отношении используемого ВТВ служило остаточное количество O-этил-S-β-диизопропиламиноэтил-метилфосфоната на тест-объектах через 30 мин после начала дегазации.
Результаты экспериментов представлены в таблице 9 и свидетельствуют, что в случае использования заявляемого средства необходимая полнота дегазации О-этил-S-β-даизопропиламиноэтилметилфосфоната достигается после однократной обработки тест-объектов в течение 30 мин.
В случае же использования средства-прототипа степень дегазации различных тканей, зараженных О-этилфторметилфосфонатом (химическим аналогом О-этил-S-β-диизопропиламиноэтилметилфосфоната) после обработки тест-объектов в течение 1 ч составляла 13-68%.
Таким образом, экспериментально установлено, что при дегазации тест-объектов с высокой степенью зараженности O-этил-S-β-диизопропиламиноэтилметилфосфонатом заявляемое средство проявляет высокую эффективность при меньшем времени экспозиции.
Пример 5. Исследование дезинфицирующей эффективности заявляемого средства.
Дезинфицирующую эффективность заявляемого средства изучали по общепринятым методикам в отношении возбудителей опасных инфекционных болезней бактериальной природы с использованием вегетативных и споровых форм тест-микроорганизмов [27, 28]. В качестве тест-микроорганизмов вегетативных форм использовали кишечную палочку (Escherichia coli, штамм 1257) и золотистый стафилококк (Staphylococcus aureus, штамм 906), а в качестве тест-микроорганизмов споровых форм - Bacillus cereus, штамм 96 и сибиреязвенную живую сухую вакцину СТИ-1 для людей. Согласно руководящим документам, данные микроорганизмы применяются при оценке дезинфицирующей активности средств, применяемых для специальной обработки при заражении ВОБ [27, 28].
Заражение тест-объектов указанными тест-микроорганизмами проводили до проведения дезинфекции по общепринятым методикам, с использованием суспензии бульонной культуры, выращенной в термостате при температуре 37°С и содержащей тест-микроорганизмы в количестве 4-8×105 КОЕ/мл.
При исследовании дезинфицирующей способности заявляемого средства в отношении указанных тест-микроорганизмов в качестве тест-объектов использовали:
- пластикат листовой ПВХ марки 57-40 (пластины размером 100×100 мм и толщиной 0,5-3,0 мм) [29];
- ткань хлопкополиэфирную [25];
- белье альпинистское [26].
- нитриловые медицинские перчатки [30], надетые на руки испытателя.
Обеззараживание тест-объектов осуществляли способом орошения при норме расхода заявляемого средства 0,4 л/м2. Обработку проводили однократно и двукратно, изменяя время экспозиции. Тест-объекты располагали в горизонтальном положении для создания более удобных условий для проведения дезинфекции. При проведении исследований в каждом эксперименте использовали по 20 тест-объектов, опыты повторяли трехкратно.
Критерием дезинфицирующей эффективности заявляемого средства служило остаточное заражение тест-объекта используемым тест-микроорганизмов.
В ходе экспериментов установлено, что тест-объекты, зараженные вегетативными формами тест-микроорганизмов, в случае использования заявляемого средства при однократной обработке были продезинфицированы полностью уже через 2 мин. Роста микроорганизмов на них не обнаружено (таблица 10).
Тест-объекты, зараженные споровой формой микроорганизмов (Bacillus cereus, штамм 96), были продезинфицированы полностью с использованием заявляемого средства при однократной обработке и экспозиции 15 мин. Роста микроорганизмов на них не обнаружено (таблица 11).
В то же время, на тест-объектах, имитирующих кожные покровы человека (нитриловые медицинские перчатки), зараженных споровыми формами микроорганизмов, через 30 мин после окончания однократной дезинфекции с использованием заявляемого средства остаточное заражение Bacillus cereus, штамм 96 не превышало 0,13±0,003 КОЕ/см2, остаточное заражение СТИ-1 не превышало 1,28±0,005 КОЕ/см2. При двукратной обработке тест-объекты были продезинфицированы полностью. Роста микроорганизмов на них не обнаружено (таблица 12).
Таким образом, экспериментально установлено, что при заражении вегетативными и споровыми формами микроорганизмов дезинфекция с использованием заявляемого средства при норме расхода 0,4 л/м2 обеспечивает достижение полного обеззараживания тест-объектов при однократном проведении дезинфекции вегетативных форм микроорганизмов в течение 2 мин, при однократной дезинфекции споровой формы микроорганизмов Bacillus cereus, штамм 96 в течение 15 мин, при двукратной дезинфекции тест-объектов, имитирующих кожные покровы человека, в отношении споровых форм микроорганизмов в течение 30 мин.
Пример 6. Исследование стабильности заявляемого средства при хранении.
Исследование стабильности заявляемого средства при хранении было выполнено на примере дезинфекции тест-поверхности из пластиката листового ПВХ марки 57-40, зараженной тест-микроорганизмом споровой формы. В качестве тест-микроорганизма использовали Bacillus cereus, штамм 96.
Заражение тест-поверхностей указанным тест-микроорганизмом проводили по общепринятым методикам до проведения дезинфекции, с использованием суспензии бульонной культуры, выращенной в термостате при температуре 37°С и содержащей тест-микроорганизм в количестве 4-8×105 КОЕ/мл.
Обеззараживание тест-поверхностей осуществляли способом орошения при норме расхода заявляемого средства 0,4 л/м2. Обработку проводили однократно и двукратно при изменении времени экспозиции. Тест-поверхности при этом располагали в горизонтальном положении для удобства проведения дезинфекции. При проведении исследований в каждом эксперименте использовали по 6 тест-поверхностей, опыты повторяли трехкратно.
Стабильность заявляемого средства оценивали путем исследования изменения дезинфицирующей активности растворов, взятых после хранения в течение 1-14 суток.
Из результатов исследований видно, что заявляемое средство сохраняет требуемый уровень дезинфицирующей активности в течение 8 суток (таблица 13).
Таким образом, гарантированный срок хранения заявляемого средства составляет не менее 8 суток. Особые температурные условия хранения или использование специального оборудования при этом не требуются.
Согласно обобщенным экспериментальным данным, заявляемое средство достаточно просто получить, входящие в его состав компоненты выпускаются в промышленных условиях и доступны. Компоненты заявляемого средства хорошо растворимы в воде, удобны для хранения и транспортировки, могут храниться длительное время без потери свойств. Заявляемое средство безопасно при применении, не оказывает раздражающего действия на кожу и глаза, обеспечивает высокий уровень эффективности при дегазации различных высокотоксичных веществ, а также при дезинфекции вегетативных и споровых форм микроорганизмов - возбудителей особо опасных болезней.
Заявляемое средство в отличие от средства-прототипа позволяет дегазировать различные ткани с высокой степенью зараженности высокотоксичными веществами при меньшем времени экспозиции, а также надежно проводить дезинфекцию тканей и поверхностей, зараженных вегетативной и споровой формами микроорганизмов.
Это свидетельствует о достижении цели изобретения и пригодности заявляемого средства для использования при проведении специальной обработки (дегазации и дезинфекции) защитной одежды и открытых участков кожи людей, подвергшихся заражению высокотоксичными веществами и возбудителями особо опасных болезней.
Заявляемое средство может быть рекомендовано для использования:
- при проведении дегазации защитной одежды и открытых участков кожи людей, подвергшихся воздействию высокотоксичных веществ, при норме расхода 0,4 л/м2 и экспозиции 30 мин;
- для дезинфекции в очагах инфекционных заболеваний, вызванных как вегетативными, так и спорообразующими формами микроорганизмов, при норме расхода 0,4 л/м2 и экспозиции 2 мин для вегетативных форм микроорганизмов и 15 мин (обработка одежды) и 30 мин (обработка кожных покровов) для споровых форм микроорганизмов.
Заявляемое изобретение удовлетворяет критерию «новизна», так как впервые предложено высокоэффективное бифункциональное средство, обеспечивающее возможность проведения специальной обработки (дегазации и дезинфекции) не только защитной одежды, но и открытых участков кожи людей за счет комплексного воздействия диоксида хлора и окиси алкилдиметиламина.
Заявляемое изобретение удовлетворяет критерию «изобретательский уровень», так как из доступных источников информации не является очевидным целесообразность включения в состав заявляемого средства сильного окислителя в виде диоксида хлора и поверхностно-активного вещества в виде окиси алкилдиметиламина, оптимальное их соотношение в водном растворе, а также возможность обеспечения за счет их комплексного воздействия дегазации различных типов высокотоксичных веществ и дезинфекции относительно возбудителей опасных инфекционных болезней бактериальной природы.
Соответствие критерию «пригодность для применения» доказывается результатами выполненных исследований, подтверждающими, что заявляемое средство отличается высоким уровнем эффективности в отношении высокотоксичных веществ и возбудителей опасных инфекционных болезней, так как обладает высокой дегазирующей и дезинфицирующей активностью, и может найти широкое применение при специальной обработке защитной одежды и открытых участков кожи людей, подвергшихся заражению при выполнении мероприятий по ликвидации последствий техногенных аварий и чрезвычайных ситуаций. Приготовление заявляемого средства отличается простотой, а входящие в его состав компоненты выпускаются в промышленных условиях и свободно продаются на российском рынке. Гарантированный срок хранения компонентов, используемых для получения заявляемого средства, составляет 3 года, гарантированный срок хранения заявляемого средства в готовом виде без потери свойств - 8 суток. Заявляемое средство может использоваться для проведения специальной обработки с применением различных технических средств.
СПИСОК ЛИТЕРАТУРЫ
1. Франке 3. Химия отравляющих веществ Том 2/3. Франке, П. Франке, В. Варнке. - М.: «Химия», 1973. - 405 с.
2. Учебник сержанта войск радиационной, химической и биологической защиты. - М.: Военное издательство, 2006. - 556 с.
3. RU 2397792 С1, 27.08.2010.
4. RU 2248234 С2, 20.03.2005.
5. US 7282470 В2, 16.10.2007.
6. RU 2040275, 25.07.1995.
7. RU 2232613 С2, 20.07.2004.
8. US 4784699 А, 15.11.1988.
9. US 5850964 А, 12.01.1999.
10. US 6376436 В1, 23.04.2002.
11. RU 2290208 С2, 27.12.2006.
12. GB 1435228 А, 05.12.1976.
13. CN 101779668 А, 21.07.2010.
14 ЕР 2130796 А1, 09.12.2009.
15. US 4073888 А, 14.02.1978.
16. CN 101228868 А, 30.07.2008.
17. CN 1590281 А, 12.11.2008.
18. RU 2290208 С2, 27.12.2006.
19. RU 2248234 С2, 20.03.2006.
20. RU 2397792 С1, 27.08.2010.
21. RU 2466930 С2, 20.11.2012.
22. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / Под ред. Р.У. Хабриева. - 2 изд., перераб. и доп. - М.: Медицина, 2005. - 832 с.
23. ГОСТ 6507-90. Микрометры. Технические условия.
24. ГОСТ Р ИСО 10993-10-2009. Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 10. Исследования раздражающего и сенсибилизирующего действия
25. ТУ 8314-162-08570932-2009 «Ткань хлопкополиэфирная маскирующей расцветки».
26. ТУ 858-5895-2006 «Белье альпинистское нательное».
27. МУ 3.5.2435-09. Методические указания. 3.5. Дезинфектология. Методы изучения и оценки спороцидной активности дезинфицирующих и стерилизующих средств: Руководство. - М.: Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека, 2009. - 55 с.
28. Методы лабораторных исследований и испытаний медико-профилактических дезинфекционных средств для оценки их эффективности и безопасности: Руководство. - М.: Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека. 2009, - 740 с.
29. ТУ 2246-424-05761784-2000 «Пластикат ПВХ марки 57-40».
30. ГОСТ Р 52239-2004 «Перчатки медицинские диагностические одноразовые. Часть 1. Спецификация на перчатки из каучукового латекса или раствора».
Бифункциональное средство для обработки защитной одежды и открытых участков кожи людей, оказавшихся в зоне заражения контаминантами химической и биологической природы, включающее окислитель, в качестве которого содержит диоксид хлора, отличающееся тем, что представляет собой водный раствор диоксида хлора, который дополнительно включает поверхностно-активное вещество, в качестве которого содержит окись алкилдиметиламина при следующем соотношении компонентов, мас.%:
| диоксид хлора | 0,2 |
| окись алкилдиметиламина | 0,01 |
| вода | остальное |