Слитые белки для применения в терапии
Иллюстрации
Показать всеНастоящее изобретение относится к биотехнологии и медицине, в частности к одноцепочечному слитому белку для ингибирования клеточной секреции клетки-мишени, нуклеиновой кислоте, вектору экспрессии, способу получения слитого белка и трехцепочечного нецитотоксического белка при действии протеазы на слитый белок, а также применениям белков согласно изобретению для лечения патофизиологических состояний, связанных с клеточной гиперсекрецией. Указанный белок включает нецитотоксическую протеазу, нацеливающий фрагмент, способный к связыванию с участком связывания на клетке-мишени, домен транслокации, способный перемещать протеазу в цитозоль клетки-мишени, два участка протеолитического расщепления и ковалентную связь между нацеливающим фрагментом и доменом транслокации. Настоящее изобретение позволяет улучшить связывание за счёт наличия в структуре слитого белка определённых нацеливающих фрагментов. 8 н. и 15 з.п. ф-лы, 1 ил., 18 пр.
Реферат
Настоящее изобретение относится к конструкции нового класса нацеливаемых ингибиторов секреции (TSIs), к способу их активации и к активированному продукту.
Нецитотоксические протеазы представляют собой хорошо известную группу протеаз, которые воздействуют на клетки-мишени путем ограничения функции клеток. Важно отметить, что нецитотоксические протеазы не убивают клетки-мишени, на которых они действуют. Некоторые из наиболее известных примеров нецитотоксических протеаз включают клостридиальные нейротоксины (например, ботулинический нейротоксин, который продается под такими названиями как Dysport™, Neurobloc™ и Botox™) и IgA протеазы.
Нецитотоксические протеазы оказывают свое действие путем протеолитического расщепления внутриклеточных транспортных белков, известных как белки SNARE (например, SNAP-25, WAMP или Syntaxin) - см. Gerald K (2002) "Cell and Molecular Biology" (4th edition) John Wiley & Sons, Inc. Сокращение SNARE является производным от термина Soluble NSF Attachment Receptor (рецептор растворимого белка присоединения NSF), где NSF означает N-ethylmaleimide-Sensitive Factor (N-этилмалеимид-чувствительный фактор). Белки SNARE являются неотъемлемой частью внутриклеточного образования везикул и, таким образом, секреции молекул посредством транспортировки везикул из клетки. Соответственно, как только они доставлены в желаемую клетку-мишень, нецитотоксические протеазы способны ингибировать клеточную секрецию из клетки-мишени.
Нецитотоксические протеазы можно использовать в их нативных или в практически нативных формах (т.е. как голотоксины, например, в случае Dysport™, Neurobloc™ и Botox™), и в этом случае нацеливание протеаз на конкретные типы клеток зависит от (i) локализованного введения протеаз и/или (ii) собственной связывающей способности нативной протеазы. В качестве альтернативы, нецитотоксические протеазы могут быть использованы в перенацеленной форме, где нативная протеазы модифицирована таким образом, что она включает экзогенный лиганд, известный как нацеливающий фрагмент (TM). ТМ выбирают таким образом, чтобы он обеспечивал специфичность связывания для требуемой клетки-мишени и, как часть способа перенацеливания, нативная связывающая часть нецитотоксической протеазы может быть удалена.
Авторы настоящего изобретения первыми выдвинули концепцию и разработали технологию перенацеливания на основе клостридиальных нейротоксинов, и получающиеся слитые белки известны как нацеливаемые ингибиторы секреции (TSIs).
Замену ТМ можно осуществить с помощью стандартных методов химического сопряжения, которые хорошо известны специалистам. В связи с этим можно сослаться на Hermanson, G.T. (1996), Bioconjugate techniques, Academic Press и на Wong, S.S. (1991), Chemistry of protein conjugation and cross-linking, CRC Press.
Однако химическое сопряжение часто является неточным. Например, после конъюгации ТМ может быть присоединен к остальной части конъюгата более чем в одном месте прикрепления. Химическое сопряжение также трудно контролировать. Например, ТМ может быть присоединен к остальной части модифицированного токсина на участке прикрепления на компоненте протеазы и/или на компоненте транслокации. Это вызывает проблемы, когда для терапевтической эффективности желательно присоединение только к одному из указанных компонентов (предпочтительно на одном участке). Таким образом, химическое конъюгирование приводит к смешанной популяции модифицированных молекул токсинов, что нежелательно.
В качестве альтернативы химической конъюгации замену ТМ можно осуществить путем рекомбинантного получения одноцепочечного полипептида слитый белок. Получение подобных молекул описано в WO 98/07864. Однако авторы настоящего изобретения определили, что приведенная в WO 98/07864 методика не подходит для всех типов TM.
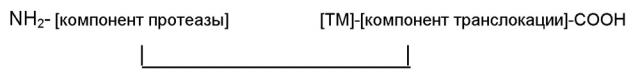
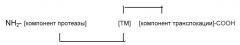
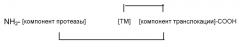
Альтернативная WO 98/07864 система описана в WO 2006/059093. Согласно WO 2006/059093, ТМ центрально-презентированы (СР) в одноцепочечном слитом белке между компонентом нецитотоксической протеазы и компонентом домена транслокации. Сказанное приводит к одноцепочечному слитому белку, имеющему следующую структуру:
NH2-[компонент протеазы]-[TM]-[компонент транслокации]-COOH
Вышеуказанные слитые белки активируются обработкой протеазой, которая способна осуществлять расщепление на участке, расположенном на С-конце компонента протеазы. Указанный процесс активации приводит к двухцепочечному белку, содержащему компонент протеазы, который ковалентно присоединен (посредством дисульфидной связи) к компоненту транслокации слитого белка. В случае WO 2006/059093 полученная двухцепочечная молекула имеет TM, который связан пептидной связью своим С-концом с N-концом компонента домена транслокации. Таким образом, N-концевая часть TM может свободно взаимодействовать и связывать желаемый рецептор. Подобное расположение имеет важное значение для класса TMs, которым для связывания с их рецептором необходим свободный N-конец или свободная N-концевая часть.
В качестве примера, после протеолитической активации, в WO 2006/059093 предлагаются полипептиды, имеющие следующую двухцепочечную конформацию:
В указанной двухцепочечной конформации ТМ и компоненты транслокации представлены в форме одноцепочечного слитого белка, в котором С-конец ТМ связан пептидной связью с N-концом компонента транслокации.
Авторы настоящего изобретения обнаружили, что системы, описанные в WO 98/07864 и WO 2006/059093, не являются оптимальными для представления всех типов TM, и, таким образом, могут приводить к получению слитых белков, имеющих нежелательную/сниженную способность связываться с намеченными клетками-мишенями.
Таким образом, существует потребность в альтернативной или усовершенствованной системе для конструкции TSIs.
Настоящее изобретение решает одну или несколько из вышеуказанных проблем, предлагая одноцепочечный полипептид слитый белок, который включает:
(a) нецитотоксическую протеазу или ее фрагмент, при этом указанная протеаза или фрагмент протеазы способны расщеплять белок по экзоцитозному пути клетки-мишени;
(b) нацеливающий фрагмент, способный к связыванию с участком для связывания на клетке-мишени, при этом участок для связывания способен подвергаться эндоцитозу с тем, чтобы быть включенным в эндосомы внутри клетки-мишени;
(c) домен транслокации, способный перемещать протеазу или фрагмент протеазы из эндосомы через мембрану эндосомы в цитозоль клетки-мишени;
(d) первый участок протеолитического расщепления, где слитый белок способен расщепляться первой протеазой, при этом первый участок протеолитического расщепления расположен между нецитотоксической протеазой и доменом транслокации;
(e) второй участок протеолитического расщепления, где слитый белок способен расщепляться второй протеазой, при этом второй участок протеолитического расщепления расположен между доменом транслокации и нацеливающим фрагментом; и
(f) ковалентную связь между нацеливающим фрагментом и доменом транслокации, где, после протеолитического расщепления на втором участке протеолитического расщепления, нацеливающий фрагмент остается связанным с доменом транслокации с помощью указанной ковалентной связи.
Система, описанная в WO 2006/059093, предоставляет TSIs, содержащие TM с N-концом, который свободен и может взаимодействовать с участком связывания на клетке-мишени. Тем не менее, авторы настоящего изобретения обнаружили, что система, описанная в WO 2006/059093, не подходит для TMs, которые для взаимодействия с участком связывания на клетке-мишени требуют наличия как свободного N-концевого домена, так и свободного С-концевого домена.
Таким образом, в отличие от WO 2006/059093, в настоящем изобретении предлагается система получения TSIs, где компонент TM имеет как свободный N-концевой домен, так и свободный С-концевой домен.
В одном варианте осуществления настоящего изобретения предлагается одноцепочечный слитый белок, имеющего следующую ориентацию от N-конца к С-концу, где Р1 и Р2 представляют собой первый и второй участок протеолитического расщепления:
NH2-[компонент протеазы]-[P1]-[TM]-[P2]-[компонент транслокации]-COOH
После расщепления на первом и втором участке расщепления указанный одноцепочечный слитый белок принимает вид следующей трехцепочечной структуры, в которой компонент TM и компонент транслокации ковалентно связаны друг с другом и в которой
А) компонент протеазы ковалентно связан с компонентом ТМ:
или В) компонент протеазы ковалентно связан с компонентом транслокации:
В другом варианте осуществления настоящего изобретения предлагается одноцепочечный слитый белок, имеющую следующие ориентацию от N-конца к С-концу, где Р1 и Р2 представляют собой первый и второй участок протеолитического расщепления:
NH2-[компонент протеазы]-[P1]-[компонент транслокации]-[P2]-[TM]-COOH
После расщепления на первом и втором участке расщепления указанный одноцепочечный слитый белок принимает вид следующей трехцепочечной структуры, в которой компонент TM и компонент транслокации ковалентно связаны друг с другом и в которой
А) компонент протеазы ковалентно связан с компонентом транслокации:
или В) компонент протеазы ковалентно связан с компонентом ТМ:
В другом варианте осуществления настоящего изобретения предлагается одноцепочечный слитый белок, имеющего следующую ориентацию от N-конца к С-концу, где Р1 и Р2 представляют собой первый и второй участок протеолитического расщепления:
NH2-[TM]-[P2]-[компонент протеазы]-[P1]-[компонент транслокации]-COOH
После расщепления на первом и втором участке расщепления указанный одноцепочечный слитый белок принимает вид следующей трехцепочечной структуры, в которой компонент TM и компонент транслокации ковалентно связаны друг с другом и в которой
А) компонент протеазы ковалентно связан с компонентом транслокации:
или В) компонент протеазы ковалентно связан с компонентом ТМ:
При его использовании полипептид TSI по настоящему изобретению связывается с клеткой-мишенью, при этом TM облегчает связывание. Компонент домена транслокации затем воздействует на транспортировку компонента нецитотоксической протеазы в цитозоль клетки-мишени. Оказавшись внутри, компонент нецитотоксической протеазы подавляет экзоцитозный путь клетки-мишени. Таким образом, за счет инактивации экзоцитозного пути клетки-мишени полипептид по настоящему изобретению ингибирует секрецию из клетки. Соответственно, полипептиды TSI по настоящему изобретению могут быть применены для подавления или лечения различных патофизиологических состояний или симптомов, связанных с клеточной секрецией.
Нецитотоксические протеазы
Биологически активный компонент TSI полипептидов по настоящему изобретению представляет собой нецитотоксическую протеазу. Таким образом, после доставки в цитозоль клетки-мишени, компонент нецитотоксической протеазы воздействует на расщепление SNARE внутри требуемой клетки-мишени. Поскольку белки SNARE являются важным компонентом секреторного процесса в клетках-мишенях млекопитающих, то их протеолитическая инактивации ингибирует/подавляет секрецию из указанных клеток-мишеней.
Нецитотоксические протеазы представляют собой отдельный класс молекул, которые не убивают клетки; вместо этого они действуют путем ингибирования клеточных процессов, отличных от синтеза белка. Нецитотоксические протеазы продуцируются различными высшими организмами (в частности, растениями и животными) - примером подобного высшего организма является бразильский скорпион. Кроме того, нецитотоксические протеазы продуцируются различными микроорганизмами, в частности бактериями, такими как Clostridium sp. и Neisseria sp.
Клостридиальные нейротоксины представляют собой основную группу молекул нецитотоксических токсинов и состоят из двух полипептидных цепей, соединенных друг с другом дисульфидной связью. Две цепи называют тяжелой цепью (Н-цепью), которая имеет молекулярную массу приблизительно 100 кДа, и легкой цепью (L-цепью), которая имеет молекулярную массу приблизительно 50 кДа. Именно L-цепь обладает функцией протеазы и проявляет высокую субстратную специфичность по отношению к везикулам и/или связанным с клеточной мембраной белкам (SNARE), участвующим в экзоцитозных процессах (например, таким как синаптобревин, синтаксин, SNAP и/или VAMP). Указанные субстраты являются важными компонентами механизма клеточной секреции.
Neisseria sp., в первую очередь вида N. gonorrhoeae, производят функционально подобные нецитотоксические молекулы токсина. Примером подобной нецитотоксической протеазы является протеаза IgA (см. WО 99/58571). Похожие протеазы IgA продуцируются стрептококками, такими как Streptococcus pneumoniae.
Таким образом, в одном варианте осуществления настоящего изобретения нецитотоксическая протеаза по настоящему изобретению может быть протеазой клостридиального нейротоксина или протеазой IgA (см., например, WO 99/032272). Другим примером нецитотоксических протеаз является протеаза яда скорпиона, например, протеаза из яда бразильского скорпиона Tityus serrulatus или протеаза антареаза (см., например, WO 2011/022357).
Нацеливающий фрагмент (TM)
Компонент TM по настоящему изобретению отвечает за связывание полипептида по настоящему изобретению с участком связывания на клетке-мишени. Таким образом, компонент TM представляет собой лиганд, посредством которого полипептид по настоящему изобретению связывается с выбранной клеткой-мишенью.
В контексте настоящего изобретения клетки-мишени могут быть клетками любого млекопитающего (предпочтительно, клетками человека). Таким образом, ТМ может связываться с клетками, отличными от нейронных клеток, и/или с нейронными клетками.
Компонент TM полипептидов по настоящему изобретению имеет как свободную N-концевую часть, так и свободную С-концевую часть. Так, в одном варианте осуществления настоящего изобретения ТМ способен взаимодействовать с участком связывания (в частности, рецептором или акцептором) на клетке-мишени посредством взаимодействия между N-концевой частью нацеливающего фрагмента и доменом участка связывания. В другом варианте осуществления настоящего изобретения ТМ способен осуществлять взаимодействие между С-концевой частью нацеливающего фрагмента и доменом участка связывания. В другом варианте осуществления настоящего изобретения ТМ способен на двойное взаимодействие, при котором N-концевая часть нацеливающего фрагмента взаимодействует с доменом участка связывания и C-концевая часть нацеливающего фрагмента взаимодействует с доменом участка связывания. В указанном последнем варианте осуществления настоящего изобретения N-концевая и С-концевая части TM могут связываться с теми же самыми или с различными доменами участка связывания и/или они могут связываться с доменами на разных участках связывания.
Подходящие TMs для использования в полипептидах по настоящему изобретению включают цитокины, факторы роста, нейропептиды, лектины и антитела, а указанный термин включает моноклональные антитела, связывающие белковые структуры, фрагменты антител, такие как Fab, F(ab)'2, Fv, ScFv, и одноцепочечные антитела, такие как камелиды и т.д.
В одном варианте осуществления настоящего изобретения компонент TM включает или состоит из лиганда пептида (в частности, пептидного гормона), который связывается с рецептором, присутствующим на клетке-мишени. В одном варианте осуществления настоящего изобретения указанный лиганд пептида имеет аминокислотную последовательность, содержащую 5-200 последовательных аминокислотных остатков. В качестве примера, указанный лиганд пептида включает или состоит из аминокислотной последовательности, содержащей 5-150, или 5-100, или 5-50, или 5-40, или 5-30, или 5-25, или 5-20, или 7-12, или примерно 10 последовательных аминокислотных остатков.
Компонент ТМ включает N-концевую часть и С-концевую часть. Каждая из указанных частей обычно содержит, по меньшей мере, 5, по меньшей мере, 10, по меньшей мере, 15, по меньшей мере, 20 или, по меньшей мере, 25 последовательных аминокислотных остатков.
В одном варианте осуществления настоящего изобретения TM включает или состоит из лиганда пептида (или его аналога), который связывается с рецептором, выбранным из MRGPRX1 (например, рецептора пептида бычьего мозгового вещества надпочечников (BAM)), рецептора опиоидного пептида, OPRM1 или OPRD1 (например, рецептора пептида бета-эндорфин), BDKRB1 или BDKRB2 (например, рецептора пептида брадикинин), OPRM1 или OPRD1 (например, рецептора пептида мет- или лей-энкефалин), OPRK1 (например, рецептора пептида динорфин), GALR1, GALR2 или GALR3 (например, рецептора пептида галанин), OPRL1 (например, рецептора пептида ноцицептин) и TACR1, TACR2 или TACR3 (например, рецептора пептида вещества Р).
В одном варианте осуществления настоящего изобретения TM включает или состоит из лиганда пептида (или его аналога), выбранного из пептида бычьего мозгового вещества надпочечников (BAM), опиоидного пептида, пептида бета-эндорфин, пептида брадикинин, пептида мет- или лей-энкефалин, пептида динорфин, пептида галанин, пептида ноцицептин и пептида вещества P.
В одном варианте осуществления настоящего изобретения TM включает или состоит из пептида гонадотропин-высвобождающего гормона (GnRH). GnRH представляет собой составленный из 10 аминокислот пептидный гормон. N-концевые аминокислоты GnRH играют определенную роль в активации рецептора, в то время как С-концевые аминокислоты необходимы для высокоаффинного связывания с рецептором GnRH (см. публикацию Flanagan, Millar & Illing (1997) Reviews of Reproduction, 2, 113-120, которая во всей своей полноте включена в данное описание посредством ссылки). Функция GnRH в условиях in vivo заключается в воздействии на рецепторы GnRH, расположенные на передней доле гипофиза, и стимулируют синтез и высвобождение гонадотропинов, например, лютеинизирующего гормона (LH) и фолликулостимулирующего гормона (FSH). Ссылка на пептид GnRH охватывает все функциональные связывающие фрагменты, их варианты и аналоги. В качестве примера, термин пептид GnRH охватывает пептид GnRH, в котором аминокислота цистеин (ограниченная с боков двумя ахиральными аминокислотными остатками, такими как глицин и/или аланин) вставлена в качестве замены аминокислоты в положении 6 пептида GnRH. GnRH также известен как лютропин-высвобождающий гормон (LHRH). Дополнительные примеры включают пептиды GnRHI, пептиды GnRHII и пептиды GnRHIII, а также полноразмерный предшественник полипептида GnRH, содержащий 92 аминокислоты, и отдельные их части.
В одном варианте осуществления настоящего изобретения TM включает или состоит из пептида кортикотропин-высвобождающего фактора (CRF). CRF представляет собой состоящий из 41 аминокислот пептидный гормон гипоталамуса, который взаимодействует с рецепторами CRF1 и CRF2. Основная функция CRF в условиях in vivo заключается в стимулировании высвобождения ACTH из кортикотропов в передней доле гипофиза. Ссылка на пептид CRF охватывает полноразмерный CRF, урокортин 1 и урокортин 2, а также все функциональные связывающие фрагменты, варианты и их аналоги.
В одном варианте осуществления настоящего изобретения TM включает или состоит из гастрин-высвобождающего пептида (GRP). GRP представляет собой содержащий 27 аминокислот пептидный гормон. GRP регулирует многочисленные функции желудочно-кишечного тракта и центральной нервной систем, в том числе высвобождение желудочно-кишечных гормонов, сокращение клеток гладких мышц и пролиферацию эпителиальных клеток, и является действенным митогеном для опухолевых тканей. Ссылка на пептид GRP охватывает все функциональные связывающие фрагменты, варианты и их аналоги.
В одном варианте осуществления настоящего изобретения TM включает или состоит из нейромедина B. Нейромедин В представляет собой содержащий 10 аминокислот пептидный гормон. Функция нейромедина B заключается в воздействии на рецепторы BB1 в условиях in vivo, и он является действенным митогеном и фактором роста для нормальных и опухолевых тканей легких и тканей желудочно-кишечного эпителия. Ссылка на пептид нейромедин B охватывает все функциональные связывающие фрагменты, варианты и их аналоги. Ссылка на нейромедин B охватывает пептидный гомолог человека, бомбезин, и включает в себя полноразмерный бомбезин - состоящий из 14-аминокислот пептид, первоначально выделенный из кожи лягушки - а также отдельные его части и его пептидные аналоги.
В одном варианте осуществления настоящего изобретения TM включает или состоит из гастрина или холецистокинина (ССК). Гастрин представляет собой содержащий 17 аминокислот пептидный гормон, а ССК представляет собой содержащий 8 аминокислот пептидный гормон. И гастрин, и холецистокинин действуют на рецепторы CCK1 и CCK2 в условиях in vivo, в основном в желудочно-кишечном тракте и центральной нервной системе, с целью модулирования секреции ферментов поджелудочной железы и сокращения гладких мышц желчного пузыря и желудка, тревоги, обезболивания, возбуждения и нейролептической активности. Ссылка на пептиды гастрин и холецистокинин охватывает все функциональные связывающие фрагменты, варианты и их аналоги.
В одном варианте осуществления настоящего изобретения TM включает или состоит из пептида соматостатин (SST). Примеры подходящих TMs пептида SST включают полноразмерный SST и кортистатин (CST), а также отдельные их части и их пептидные аналоги, такие как BIM 23052, BIM 23056 или BIM23268; октреотидные пептиды, ланреотидные пептиды, BIM23027, CYN154806, BIM23027, вапреотидные пептиды, сенглитидные пептиды и SOM230. Указанные ТМ связываются с рецепторами sst, такими как рецепторы sst1, sst2, sst3, sst4 и sst5. SST и CST обладают значительной структурной гомологией и связываться со всеми известными рецепторами sst. Ссылка на пептиды SST или CST охватывает все функциональные связывающие фрагменты, варианты и их аналоги.
В одном варианте осуществления настоящего изобретения TM включает или состоит из пептида гормона, высвобождающего гормон роста (GHRH). GHRH известен также как соматотропин-высвобождающий фактор (GRF или GHRF) или соматокринин. Подходящие пептиды GHRH включают полноразмерный пептид GHRH (1-44) и отдельные его части, такие как GHRH (1-27, 1-28, 1-29), GHRH (1-37) и GHRH (1-40, 1-43)-OH, а также пептидные аналоги, такие как BIM-28011 или NC-9-96. Ссылка на пептид GHRH охватывает все функциональные связывающие фрагменты, варианты и их аналоги.
В одном варианте осуществления настоящего изобретения TM включает или состоит из пептида активированного протеиназой рецептора (PAR), например PAR1. Пептиды PAR представляют собой уникальную подтип связанных с G-белком рецепторов 7-трансмембранного рецептора, особенность которых заключается в том, что они протеолитически модифицированы с освобождением нового внеклеточного N-конца, который действует в качестве связанного активирующего лиганда. Были идентифицированы агонисты PAR1 (такие как TFLLR), которые активируют их родственный рецептор. Ссылка на пептид PAR охватывает все функциональные связывающие фрагменты, варианты и их аналоги.
В одном варианте осуществления настоящего изобретения TM включает или состоит из паратиреоидного гормона (PTH). PTH представляет собой пептид, который высвобождается паращитовидной железой и связывается с рецептором РТН-1. Указанный рецептор широко распространен, но особенно много его содержится в тканях-мишенях РТН, преимущественно, в почках и в костях. Ссылка на пептид PTH охватывает все функциональные связывающие фрагменты, варианты и их аналоги.
В одном варианте осуществления настоящего изобретения TM включает или состоит из пептида, который связывается с секреторной клеткой слизистых оболочек или с нервной клеткой, контролирующей или направляющей секрецию слизи. Например, ТМ связывается с (а) клетками, секретирующими муцин, такими как эпителиальные бокаловидные клетки и секреторные клетки подслизистой железы, (b) клетками, которые секретируют водные компоненты слизи, таких как клетка Клара и белковая клетка, и/или (c) клетками, которые управляют или направляют секрецию слизи, такими как "сенсорно-афферентные" С-волокна или волокна NANC нейронной системы. Особо следует упомянуть следующие пептиды TMs: VIP; агонисты бета2 адренорецептора; гастрин-высвобождающий пептид; и пептид, связанный с геном кальцитонина. Ссылка на указанные пептиды TMs охватывает все функциональные связывающие фрагменты, варианты и их аналоги. Так, TSIs по данному варианту осуществления настоящего изобретения находят терапевтическое применение при лечении гиперсекреции слизи, астме и/или хроническом обструктивном заболевании легких.
В другом варианте осуществления настоящего изобретения TM включает или состоит из пептида, который связывается с эндокринной клеткой. Особо следует упомянуть здесь GHRH; тиреотропный гормон (TSH), инсулин, инсулиноподобный фактор роста; TSH высвобождающий гормон (протирелин); FSH/LH-высвобождающий гормон (гонадорелин); кортикотропин-высвобождающий гормон (CRH); и ACTH. Ссылка на указанные пептидные TMs охватывает все функциональные связывающие фрагменты, варианты и их аналоги. Так, TSIs по данному варианту осуществления настоящего изобретения находят терапевтическое применение при лечении: неоплазии железы внутренней секреции, в том числе MEN; тиреотоксикоза и других заболеваний, зависимых от гиперсекреции щитовидной железы; акромегалии, гиперпролактинемии, болезни Кушинга и других заболеваний, зависимых от гиперсекреции передней доли гипофиза; гиперандрогенизма, хронической ановуляции и других заболеваний, связанных с синдромом поликистозных яичников.
В другом варианте осуществления настоящего изобретения TM включает или состоит из пептида, который связывается с воспалительной клеткой. Особо здесь следует упомянуть пептиды TMs (i) для тучных клеток, такие как С4-домен Fc IgE; (ii) для эозинофилов, такие как лиганды рецептора комплемента C3a/C4a-R, антигены, активные по отношению к рецептору комплемента CR4; (iii) для макрофагов и моноцитов, такие как макрофагальный стимулирующий фактор, (iv) для нейтрофилов, такие как антиген, связанный с рецептором комплемента iC3b, или IL8. Ссылка на указанные пептиды TMs охватывает все функциональные связывающие фрагменты, варианты и их аналоги. Так, TSIs по данному варианту осуществления настоящего изобретения находят терапевтическое применение при лечении аллергии (сезонного аллергического ринита (сенной лихорадки), аллергического конъюнктивита, вазомоторного ринита и пищевой аллергии), эозинофилии, астмы, ревматоидного артрита, системной красной волчанки, дискоидной красной волчанки, язвенного колита, болезни Крона, геморроя, зуда, гломерулонефрита, гепатита, панкреатита, гастрита, васкулита, миокардита, псориаза, экземы, хронического радиационно-индуцированного фиброза, рубцевания легких и других фиброзных расстройств.
В другом варианте осуществления настоящего изобретения TM включает или состоит из пептида, который связывается с экзокринной клеткой. Особо здесь следует упомянуть пептид, активирующий аденилциклазу гипофиза (РАСАР-38). Ссылка на указанные пептиды TMs охватывает все функциональные связывающие фрагменты, варианты и их аналоги. Так, TSIs по данному варианту осуществления настоящего изобретения находят терапевтическое применение при лечении гиперсекреции слизи секреторными клетками слизистых оболочек, расположенными в желудочно-кишечном тракте, в частности, в толстой кишке.
В еще одном варианте осуществления настоящего изобретения TM включает или состоит из пептида, который связывается с иммунологическими клетками. Здесь следует упомянуть такие лиганды, как фрагмент/элемент поверхности вируса Эпштейна-Барра. Ссылка на указанные пептиды TMs охватывает все функциональные связывающие фрагменты, варианты и их аналоги. Так, TSIs по данному варианту осуществления настоящего изобретения находят терапевтическое применение при лечении тяжелой псевдопаралитической миастении, ревматоидного артрита, системной красной волчанки, дискоидной красной волчанки, при трансплантации органов, трансплантации тканей, трансплантации жидкостей, при лечении болезни Грейвса, тиреотоксикоза, аутоиммунного диабета, гемолитической анемии, тромбоцитопенической пурпуры, нейтропении, хронического аутоиммунного гепатита, аутоиммунного гастрита, злокачественной анемии, тиреоидита Хашимото, болезни Аддисона, синдрома Шегрена, первичного билиарного цирроза, полимиозита, склеродермии, системного склероза, пузырчатки обыкновенной, буллезного пемфигоида, миокардита, ревмокардита, гломерулонефрита (гудпасчерова типа), увеита, орхита, неспецифического язвенного колита, васкулита, атрофического гастрита, злокачественной анемии, сахарного диабета 1 типа.
В еще одном варианте осуществления настоящего изобретения TM включает или состоит из пептида, который связывается с сердечно-сосудистой клеткой. Здесь состоит упомянуть тромбин и TRAP (пептидный агонист тромбинового рецептора) и лиганды, которые связываются с сердечно-сосудистыми эндотелиальными клетками, такие как антиген-распознающие антитела поверхности GP1b. Ссылка на указанные пептиды TMs охватывает все функциональные связывающие фрагменты, варианты и их аналоги. Так, TSIs по данному варианту осуществления настоящего изобретения находят терапевтическое применение при лечении сердечно-сосудистых заболеваний и/или гипертензии.
В еще одном варианте осуществления настоящего изобретения TM включает или состоит из пептида, который связывается с костной клеткой. Здесь следует упомянуть лиганды, которые связываются с остеобластами при лечении заболевания, выбранного из остеопетроза и остеопороза, и включают кальцитонин, а также лиганды, которые связываются с остеокластами, в том числе факторами дифференцировки остеокластов (в частности, TRANCE, или RANKL, или OPGL). Ссылка на указанные пептиды TMs охватывает все функциональные связывающие фрагменты, варианты и их аналоги. Так, TSIs по данному варианту осуществления настоящего изобретения находят терапевтическое применение при лечении заболеваний костной ткани.
Линейные и циклические интегрин-связывающие последовательности представляют собой еще одну группу пептидов TMs по настоящему изобретению. Многие интегрины распознают тройную пептидную последовательность Arg-Gly-Asp (RGD) (Ruoslahti, 1996). Фрагмент RGD можно найти более чем в 100 белках, включая фибронектин, тенасцин, фибриноген и витронектин. Взаимодействие RGD и интегрина используется многими патогенами, включая вирус Коксаки (Roivaninen et al., 1991) и аденовирус (Mathias et al., 1994), как консервативный механизм проникновение в клетку. Было показано, что линейные и циклические пептидные последовательности, соответственно, PLAEIDGIEL и CPLAEIDGIELC, связывают и интернализуют ДНК в клетках, экспрессирующих интегрин α9β1 (Schneider et al., 1999). Ссылка на указанные пептиды TMs охватывает все функциональные связывающие фрагменты, варианты и их аналоги.
Другие TMs по настоящему изобретению, включают TMs, обнаруженные методами фагового отображения, в частности TMs, которые нацеливаются и интернализуются эпителиальными клетками дыхательных путей человека. Они включают линейные и циклические пептиды THALWHT (Jost et al., 2001); LEBP-1 (QPFMQCLCLIYDASC), LEBP-2 (RNVPPIFNDVYWIAF) и LEBP-3 (VFRVRPWYQSTSQS) (Wu et al., 2003); CDSAFVTVDWGRSMSLC (Florea et al., 2003); SERSMNF, YGLPHKF, PSGAARA, LPHKSMP, LQHKSMP (Writer et al., 2004); FSLSKPP, HSMQLST и STQAMFQ (Rahim et al., 2003). Ссылка на указанные пептиды TMs охватывает все функциональные связывающие фрагменты, варианты и их аналоги.
В одном варианте осуществления настоящего изобретения TM включает или состоит из первой и второй частей (в частности, доменов). В одном варианте осуществления настоящего изобретения первая и вторая части нацеливающего фрагмента могут быть получены из того же самого лиганда (например, из любого из вышеуказанных лигандов TM). Первая и вторая части могут связываться с одним и тем же из различных участков на одном и том же рецепторе. В качестве альтернативы, первая и вторая части могут связывать участки на различных рецепторах.
Первую и вторую части нацеливающего фрагмент можно получить из различных лигандов (например, любых из вышеуказанных лигандов TM), которые могут связываться с тем же самыми или различными рецепторами. Соответственно, TM может быть гибридом двух TM. Первая и вторая части могут связываться с теми же самыми или различными участками одного и того же рецептора. В качестве альтернативы, первая и вторая части могут связывать участки на различных рецепторах.
TM может дополнительно включать третью и/или последующие части из других TMs (например, любого из вышеуказанных лигандов TM).
В одном варианте осуществления настоящего изобретения первая часть (например, домен) включает или состоит из лиганда, который связывается посредством свободной N-концевой части (например, свободного N-конца) с его рецептором-мишенью. Примером подобного лиганда является лиганд, который связывается с опиоидными рецепторами (например, лиганд, который связывается с рецептором ORL1, таким как опиоидный пептид). Другие примеры опиоидных пептидов включают ноцицептин, динорфин, бета-эндорфин и энкефалин. Другие отличные от опиоидных пептидов лиганды TM включают BAM, галанин, вещество Р, GnRH, CRF, GRP, нейромедин В, бомбезин, гастрин, CCK, SST, CST и пептиды GHRH (а также отдельные их части, варианты и аналоги).
В другом (или том же самом) варианте осуществления настоящего изобретения вторая часть (например, домен) включает или состоит из лиганда, который связывается посредством свободной С-концевой части (например, свободного С-конца) с его рецептором-мишенью. Примером подобного лиганда является лиганд, который связывается с рецептором брадикинина (например, с пептидом брадикинин) или рецептором вещества Р (например, пептидом вещества Р). Другие лиганды пептида TM включают BAM, галанин, вещество Р, GnRH, CRF, GRP, нейромедин В, бомбезин, гастрин, CCK, SST, CST и пептиды GHRH (а также отдельные их части, варианты и аналоги).
В качестве примера гибридный TM содержит первую часть, которая включает или состоит из пептида ноцицептин, и вторую часть, которая включает или состоит из пептида брадикинин (или пептида вещества Р). В других примерах первая часть включает или состоит из пептида ноцицептин, а вторая часть включает или состоит из пептида, выбранного из пептида BAM, опиоидного пептида, пептида бета-эндорфин, пептида брадикинин, пептида энкефалин, пептида динорфин, пептида галанин и пептида вещества P.
В другом примере гибридный TM содержит первую часть, которая включает или состоит из пептида динорфин, и вторую часть, которая включает или состоит из пептида брадикинин (или пептида вещества Р). В других примерах первая часть включает или состоит из пептида динорфин, а вторая часть включает или состоит из пептида, выбранного из пептида BAM, опиоидного пептида, пептида бета-эндорфин, пептида брадикинин, пептида энкефалин, пептида ноцицептин, пептида галанин и пептида вещества P.
В другом примере гибридный TM содержит первую часть, которая включает или состоит из пептида галанин, и вторую часть, которая включает или состоит из пептида брадикинин (или пептида вещества Р). В других примерах первая часть включает или состоит из пептида галанин, а вторая часть включает или состоит из пептида, выбранного из пептида BAM, опиоидного пептида, пептида бета-эндорфин, пептида брадикинин, пептида энкефалин, пептида ноцицептин, пептида динорфин и пептида вещества P.
В другом примере гибридный TM содержит первую часть, которая включает или состоит из пептида BAM, и вторую часть, которая включает или состоит из пептида брадикинин (или пептида вещества Р). В других примерах первая часть включает или состоит из пептида BAM, а вторая часть включает или состоит из пептида, выбранного из опиоидного пептида, пептида бета-эндорфин, пептида брадикинин, пептида энкефалин, пептида ноцицептин, пептида динорфин, пептида галанин и пептида вещества P.
В другом примере гибридный TM содержит первую часть, которая включает или состоит из пептида бета-энд