Способ комплексного лечения больных с остеосаркомой нижней челюсти
Иллюстрации
Показать всеИзобретение относится к области медицины, предпочтительно к стоматологии, онкологии, и может быть использовано в комплексном лечении больных с остеосаркомой нижней челюсти. Проводят пред- и послеоперационную химиотерапию, оперативное лечение в виде резекции пораженного участка нижней челюсти с первичной аутопластикой дефекта. Со второго дня после операции проводят сеансы мезодиэнцефальной модуляции (МДМ-терапии). Назначают МДМ-терапию вначале два раза в день с шестичасовым интервалом в течение трех дней и далее один раз в день на протяжении последующих семи дней. Осуществляют МДМ-терапию через электроды, которые фиксируют на голове пациента по лобно-затылочной методике: анод – на середину лба, катод – на середину затылка. Используют для МДМ-терапии импульсные токи с частотой 10000 Гц, модулированные в низкочастотном диапазоне от 20 до 100 Гц. Подбирают силу тока индивидуально до появления у пациента ощущений «ползания мурашек», и/или незначительного жжения или вибрации, и/или отдельных толчков, и/или незначительного давления. Далее проводят сеанс терапии на подобранной силе тока. Длительность сеанса составляет 30 минут. Способ обеспечивает профилактику метастазирования и рецидива опухолеобразования, создание условий для развития локального и системного антистрессового эффекта, быстрое уменьшение выраженности болевого синдрома, ускорение восстановления функции за счет раннего уменьшения отечности, регенерации слизистой оболочки, ускорения костной репарации, психоэмоционального восстановления. 3 ил., 3 табл., 10 пр.
Реферат
Изобретение относится к области медицины, а именно к стоматологии, онкологии.
По данным научной литературы в настоящее время отмечается рост онкологической патологии челюстно-лицевой области от 1,5 - 2% до 3 -3,5% [Casaroto A.R. et al. Ewing's Sarcoma Family Tumors in the Jaws: Case Report, Immunohistochemical Analysis and Literature Review. In Vivo. 2017. 31(3): 481-491; Mahmoud O. et al. Adjuvant therapies utilization pattern and survival outcomes in high-grade head and neck soft tissue sarcoma; a population based study. Oral Oncol. 2017 Mar; 66:28-37].
Своевременное лечение и подбор методов терапии и реабилитации крайне важен для сохранения качества жизни данных больных и прогноза на выздоровление. Обеспокоенность медицинского сообщества, в контексте заболеваемости остеосаркомой, вызывает частота инвалидизации онкологических пациентов вследствие нарушения у них целого ряда важнейших функций обеспечения жизнедеятельности и социального взаимодействия. Медицинское сопровождение онкологических пациентов представляет собой сложную и взаимосвязанную систему решения целого аспектов: патоморфологического, функционального, эстетического (косметического), психологического.
Длительный послеоперационный период, осложнения и побочные эффекты оперативных вмешательств, преимущественно в виде продолжительно сохраняющегося болевого синдрома, деформации лицевого черепа, приводящих к функциональным нарушениям и эстетическим дефектам, нарушений эмоциональной сферы не только приводят к сложностям в дальнейшем ведении пациентов, но и способны значительно ухудшить социальное функционирование и качество жизни больных.
Основным методом терапии остеосарком остается хирургическое лечение с последующей остеопластикой [Tomar D. et al. (2016) Central Telangiectatic Osteosarcoma of the Mandible in a Paediatric Patient: A Rarity. J. Clin Diagn Res., 10(12), XD01-XD03; Chen Y. et al. (2017) Intentional marginal resection of periosteal osteosarcoma in combination with neoadjuvant chemotherapy: A report of two cases and a review of the literature. Oncol Lett., 13(3):1343-1347].
В последнее время широко практикуются операции с применением имплантов из костной ткани. Это могут быть как ауто-, так и аллоимпланты [Kim D. et al. (2017) Sacral Reconstruction with a 3D-Printed Implant after Hemisacrectomy in a Patient with Sacral Osteosarcoma: 1-Year Follow-Up Result. Yonsei Med J., 58(2):453-457].
Остеопластика зачастую дополняется осуществлением ортопедического протезирования участка образовавшегося дефекта, вследствие хирургического вмешательства [Utjuzh A.S., Jumashev A.V., LushkovR.M. (2016) Clinical example of orthopedic treatment of a patient after mandible resection caused by sarcoma with the use of dental implants. Clinical dentistry, 4 (80), 56-58].
Недостаточное удовлетворение имеющимися методами терапии остеосарком медицинских запросов заставляет совершенствовать прежние и разрабатывать новые методы лечения.
Имеются отдельные указания на возможность разрушения остеосаркомы и ингибирование метастазов посредством применения нано-импульсной стимуляции [Chen X. et al. (2017) Nano-pulse stimulation (NPS) ablates tumors and inhibits lung metastasis on both canine spontaneous osteosarcoma and murine transplanted hepatocellular carcinoma with high metastatic potential. Oncotarget. 2017 Apr 18]. Некоторые авторы фиксируют положительный терапевтический эффект чрезкожного применения С02 в рамка противоопухолевой терапии [Ueha Т. et al. (2017) Optimization of antitumor treatment conditions for transcutaneous C02 application: An in vivo study. Oncol Rep. 2017 Jun; 37(6): 3688-3694]. Также на стадиях разработки находятся исследования, посвященные применению тканевой инженерии в терапии указанной группы пациентов. С ее помощью предполагается достичь восстановления удаленного участка пораженной кости [El-Sayed MM et al. In vitro kinetic investigations on the bioactivity and cytocompatibility of bioactive glasses prepared via melting and sol-gel techniques for bone regeneration applications. Biomed Mater. 2017 Feb 24;12(l):015-029].
Последнее время внимание исследователей в области онкологии, в том числе, онкостоматологии, привлекают физиотерапевтические методы реабилитации, применяемые в послеоперационном периоде [Punzalan М., Hyden G. (2009) The role of physical therapy and occupational therapy in the rehabilitation of pediatric and adolescent patients with osteosarcoma. Cancer Treat Res., 152, 367-384; Yumashev A.V., Gorobets T.N., Admakin O.I., Kuzminov G.G., Nefedova I.V. (2016) Aspects of adaptation syndrome development and anti-stress effects of mesodiencephalic modulation. Indian journal of science and technology. Vol. 9(19), 1-10 - прототип].
Согласно современным исследованиям, физиотерапевтические методы в онкостоматологии и челюстно-лицевой хирургии применяются не только для ускорения местного регенерационного эффекта, нивелирования болевого компонента, но и нормализации психоэмоционального состоянии больных. Так, отмечается, что пациенты, страдающие онкологической патологией, подвергаются нозогенному, операционному и медикаментозному стрессу. Известно, что данное состояние лежит в основе выраженных иммунодепрессивного, противовоспалительного, ишемического, вегетодестабилизирующего процессов, а также способно приводить к замедлению течение процессов нормальной репарации и регенерации тканей [Matsumoto М., Watanabe К., Ishii К., Tsuji Т., Takaishi Н., Nakamura М., Toyama Y., Chiba К., Imanishi Y., Kishi К., Kawana H. (2010) Complicated surgical resection of malignant tumors in the upper cervical spine after failed ion-beam radiation therapy. Spine (Phila Pa 1976); 35(11), E505-9; Heymann P. G., Ziebart Т., Kammerer P. W., Mandic R., Saydali A., Braun A., Neff A., Draenert G. F. (2016) The enhancing effect of a laser photochemotherapy with cisplatin or zolendronic acid in primary human osteoblasts and osteosarcoma cells in vitro. J. Oral Pathol, 45(10), 803-809]. Для его купирования рядом авторов предлагается к использованию новый метод мезодиэнцефальной модуляции (МДМ) в качестве дополнительного в рамках послеоперационной реабилитации онкобольных [Matsumoto М., Watanabe К., Ishii К., Tsuji Т., Takaishi Н., Nakamura М., Toyama Y., Chiba К., Imanishi Y., Kishi К., Kawana H. (2010) Complicated surgical resection of malignant tumors in the upper cervical spine after failed ion-beam radiation therapy. Spine; 35(11), E505-9; Yumashev A.V., Gorobets T.N., Admakin O.I., Kuzminov G.G., Nefedova I.V. (2016) Aspects of adaptation syndrome development and anti-stress effects of mesodiencefhalic modulation. Indian journal of science and technology. Vol.9 (19), 1-10].
Следует отметить, что наличие либо отсутствие воспалительной реакции в послеоперационном периоде является важным предиктором безрецидивной выживаемости пациентов с опухолевым процессом [Lacigova S., Tomesova J, Gruberova J, Rusavy Z, Rokyta R. (2013) "Mesodiencephalic" modulation in the treatment of diabetic neuropathy. Neuro Endocrinol Lett. 34(2), 135-42; Dutta S., Crumley A.B., Fullarton G.M., Horgan P.G., McMillan D.C. (2011) Comparison of the prognostic value of tumour- and patient-related factors in patients undergoing potentially curative resection of oesophageal cancer. World J Surg., 35(8): 1861-6]. Поэтому противовоспалительный эффект мезодиэнцефальной модуляции так важен в онкостоматологии.
В лечении пациентов с остеосаркомой не менее важны манипуляции направленные на препятствование рецидива опухоли после ее первичного удаления, а также предупреждение метастазирования [Morhij R., Mahendra A., Jane М., McMillan D.C. The modified Glasgow prognostic score in patients undergoing surgery for bone and soft tissue sarcoma. J Plast Reconstr Aesthet Surg., 70(5):618-624. doi: 10.1016/j.bjps.2017.01.016. Epub 2017 Feb 24; Robl B., Botter S.M., Boro A., Meier D., Neri D., Fuchs B. (2017) Evaluation of F8-TNF-a in Models of Early and Progressive Metastatic Osteosarcoma. Transl Oncol., 24;10(3):419-430].
На практике в большинстве случаев предлагается ограничиться восстановительной операцией, возобновляющей жевательную функцию и эстетический вид - остеопластикой с ортопедическим протезированием [Aksu А.Е., Dursun Е., Calis М., Ersu В., Safak Т., Tozum T.F. Intraoral use of extraoral implants for oral rehabilitation of a pediatric patient after resection of ewing sarcoma of the mandible and reconstruction with iliac osteocutaneous free flap.J Craniofac Surg. 2014 May;25(3):930-3; Hutchison I.L., Dawood A., Tanner S. Immediate implant supported bridgework simultaneous with jaw reconstruction for a patient with mandibular osteosarcoma. Br Dent J. 2009 Feb 14;206(3): 143-6].
Однако дентальная имплантация сама по себе выступает в виде фактора риска развития осложнений, в том числе остеомелиелита и остеопороза.
В связи с чем, лечение с применением дентальных имплантов должно осуществляться с применением профилактических манипуляций с целью исключения риска развития осложнений.
Вышеизложенное делает актуальным поиск новых методов улучшения качества лечения больных в онкостоматологической практике, в том числе с применением современных физиотерапевтических методик, с целью снижения инвалидизации и повышения качества жизни данной категории пациентов.
Решаемой проблемой явилась разработка комплексного метода лечения больных остеосаркомой нижней челюсти, позволяющего минимизировать риск развития осложнений и рецидивов.
Достигаемым техническим результатом является:
- профилактика метастазирования и рецидива опухолеобразования;
- создание условий для развития локального и системного антистрессового эффекта;
- быстрое уменьшение выраженности болевого синдрома;
- ускорение восстановления функции за счет раннего уменьшения отечности, регенерации слизистой, ускорения кострой репарации, а также психоэмоционального восстановления.
В результате проведенных исследований, нами был разработан комплексный метод лечения, основанный на сочетании хирургических вмешательств с таким физиотерапевтическим методом как мезодиэнцефальная модуляция (МДМ) у больных с остеосаркомой нижней челюсти, а также определенная последовательность осуществления каждого из компонентов лечения.
Так, нами было выявлено, что на достижение указанных результатов оказывает влияние следующее сочетание в оригинальной последовательности компонентов лечебного комплекса:
- резекция пораженного опухолью участка челюсти, восстановление пострезекционного дефекта с применением аутоимпланта,
- применение МДМ-терапии.
МДМ-терапия обеспечивает ускорение местной регенерации тканей, за счет улучшения кровоснабжения тканей, купирования болевого синдрома и сопутствующего местного дискомфорта. Применение МДМ, на наш взгляд, также способно выступить в роли профилактического фактора развития осложнений вследствие применения имплантов. Целенаправленное воздействие импульсными токами при МДМ-терапии способно влиять на подкорково-стволовые структуры головного мозга, что приводит к активации и нормализации работы ряда антистрессовых систем организма и влечет за собой нормализацию психоэмоционального состояния пациента, а также, опосредованно, нормализацию иммунного статуса организма, что способствует не развитию воспаления в месте имплантации либо меньшей его выраженности, и улучшению кровообращения, что обеспечивает ускорение регенерации тканей. Мы выдвинули допущение, что применение МДМ-терапии у пациентов с опухолевой патологией особенно целесообразно, ввиду наличия данной категории больных в группе риска развития нозогений; дополнительные оперативные инвазивные вмешательства способны нарушить и без того дискредитированное психоэмоциональное состояние данных пациентов и привести к более выраженным психическим и психосоматическим нарушениям, чем у других категорий больных.
Нормализация психоэмоционального состояния пациентов, благодаря МДМ-терапии, в свою очередь, оказывает влияние на приверженность пациента к проводимому лечению, обеспечивая возможность проведения полного курса лечебных мероприятий, опосредованно способствует улучшению регенерации тканей и скорейшему уменьшению воспаления за счет недопущения развития психосоматических реакций, психогенно обусловленного угнетения иммунного ответа организма.
Нами было проведено клиническое рандомизированное контролированное исследование. На базе клинических баз кафедры ортопедической стоматологии Первого Московского государственного медицинского университета им. И.М. Сеченова было выполнено обследование и лечение 21 пациента с диагнозом Остеогенная саркома нижней челюсти (С41.1 по МКБ-10). Из них 8 женщин и 13 мужчин. Средний возраст пациентов составил (26,6±1,06) лет.
Всем больным предварительно проводилось гистологическое исследование ткани опухоли с получением патоморфологического и иммуногистохимического заключения.
Критерии включения: наличие единичной первичной остеосаркомы нижней челюсти, Tis N0 М0 либо Т1 N0 М0 по международной классификации стадий злокачественных новообразований (система TNM).
Критерии исключения: множественные очаги поражения нижней челюсти, вторичное метастатическое поражение нижней челюсти, прорастание первичной опухоли в близлежащие ткани, Т2-4 N1-x М1-х по системе TNM, а также следующие гистологические типы опухолей костной ткани: саркома Юинга, паростальная саркома, хондросаркома, ретикулосаркома, возраст больного более 70 лет, наличие тяжелой сопутствующей соматической патологии.
Пациенты были разделены на две группы исследования согласно проводимого лечения.
В основную группу (ОГ) вошли 10 пациентов с диагнозом Остеогенная саркома нижней челюсти, которые получали лечение согласно разработанной нами комплексной программе лечения больных остеосаркомой нижней челюсти с применением остеопластики с последующей корректирующей операцией и МДМ в постоперационном периоде. Из них 4 женщины и 6 мужчин. Средний возраст в группе составил (25,8±1,24) лет.
Группу сравнения (ГС) составили 11 пациентов с диагнозом Остеогенная саркома нижней челюсти, которые получали лечение с применением остеопластики с последующей корректирующей операцией без МДМ. Пациенты ГС получали дополнительную фармакотерапию в виде нестероидных противовоспалительных препаратов, направленную на нивелирование местного воспаления и болевого компонента, как одного из факторов, способствующих развитию психоэмоционального стресса.
Пациенты ОГ такую фармакотерапию не получали. Среди них 4 женщины и 7 мужчин. Средний возраст в группе составил (26,4±1,09) лет.
Методы исследования: клинико-анамнестический, клинический, физикальный, гистологический, психодиагностический, статистический.
В рамках мониторинга эффективности лечения пациентов использовался опросник MOS 36-Item Short Form Health Survey (MOS SF-36) - с целью оценки качества жизни пациентов. Показатели каждой из 8 шкал опросника варьируют между 0 и 100 баллов, где 0 баллов - полное неблагополучие, 100 баллов отражает полное благополучие в контексте рассматриваемого показателя.
Комплексная программа лечения больных остеосаркомой нижней челюсти состояла из ряда этапов (фиг. 1). При этом длительность этапов может быть и иной.
I. Этап предоперационной химиотерапии. Данный этап проводился с целью профилактики метастазирования и уменьшения объема первичной опухоли. Химиотерапия проводилась с применением препаратов ифосфамид и этопозид в течение 1-3 месяцев в дозах не превышающих стандартные, режим дозирования устанавливался индивидуально. Данный этап проводился пациентам как ОГ, так и ГС.
II. Этап оперативного лечения. Данный этап состоял из двух подэтапов, следовавших последовательно:
А) Первый подэтап - резекция пораженного участка нижней челюсти. Оперативное лечение в виде резекции нижней челюсти в пределах здоровой ткани проводилось всем пациентам ОГ и ГС наружным доступом. В зависимости от масштабов вовлечения костной ткани в опухолевый процесс и локализации остеосаркомы выполнялись сегментарная или половинная резекция с экзартикуляцией опухолевой ткани.
Б) Второй подэтап - первичная пластика дефекта нижней челюсти.
Остеопластика выполнялась путем реконструкции с применением аутоимпланта в виде свободного лоскута на сосудистой ножке из кости пригодной для остеопластики (может быть использована, например, малоберцовая кость, реберная кость). В ОГ фрагменты челюсти и аутоимпланта соединялись в единый блок при помощи позиционирующих устройств, выполненных индивидуально (фиг. 2. Ортопантомограмма пациента в послеоперационном периоде после восстановления контура нижней челюсти фрагментом малоберцовой кости).
Для удержания фрагмента нижней челюсти и профилактики смещения участка кости применять пластмассовые или металлические назубные шины с наклонной плоскостью (фиг. 3. Ортопантомограмма пациента в послеоперационном периоде после восстановления контура нижней челюсти фрагментом малоберцовой кости с применением металлической назубной шины).
Этап оперативного лечения завершался послойным сшиванием и дренированием операционной раны.
III. Этап послеоперационной реабилитации. Послеоперационная реабилитация включала две составляющие, следовавшие параллельно:
А) Послеоперационная химиотерапия. Данный этап, как и этап предоперационной химиотерапии, реализовывался с целью профилактики метастазирования и рецидива опухолеобразования. Использовались препараты ифосфамид и этопозид в индивидуально переносимых дозах, не превышающих стандартные. Продолжительность этапа - 6 месяцев.
Б) Мезодиэнцефальная модуляция. Данный этап реализовывался посредством применения к пациентам ОГ МДМ-терапии - современного метода физиотерапии, направленного на достижение локального и системного антистрессового эффекта посредством дозированного воздействия импульсными токами на подкорково-стволовую область головного мозга.
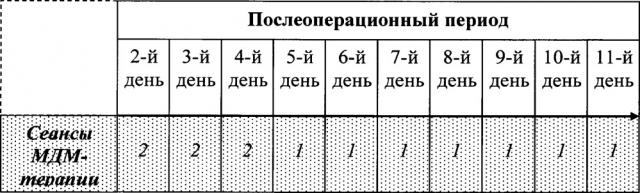
Со второго дня послеоперационного периода всем пациентам ОГ проводился десятидневный курс МДМ-терапии, состоящий из 13 получасовых сеансов (табл. 1).
Таблица 1. Схема сеансов МДМ-терапии у пациентов с остеосаркомой нижней челюсти в послеоперационном периоде.
Сеансы МДМ-терапии проводились два раза в день с шестичасовым интервалом в первые три дня и один раз в день на протяжении последующих семи дней.
Электроды при МДМ-терапии фиксировались на голове пациента по лобно-затылочной методике: анод - на середину лба, катод - на середину затылка. Между кожей и пластиной электрода помещалась одноразовая шестнадцатислойная фланелевая прокладка, увлажненная водой.
Для МДМ-терапии использовались импульсные токи с частотой 10000 Гц, модулированные в низкочастотном диапазоне от 20 до 100 Гц. Сила тока менялась индивидуально в указанном диапазоне до появления у пациента ощущений «ползания мурашек», незначительного жжения или вибрации, отдельных толчков, незначительного давления, и далее сеанс проводили на подобранной силе тока. Длительность сеанса МДМ-терапии составляет 30 минут.
Стимуляцией оказывались задействованы основные регуляторные центры, локализирующиеся в глубоких (мезодиэнцефальных) мозговых структурах. Это позволяет рассчитывать на нивелирование всех возможных патогенетических звеньев, принимающих участие в инициации и поддержании стрессовой реакции, как неотъемлемой составляющей послеоперационного периода.
Результаты исследования продемонстрировали достоверное сокращение сроков послеоперационной реабилитации у всех пациентов ОГ по сравнению с ГС на (0,5±0,98) месяца (р<0,01).
У пациентов ОГ на фоне МДМ-терапии отмечался антиалгический, противоотечный, противовоспалительный, иммунотропный, положительный трофический, антиспастический, регенераторно-репараторный, а также общий се дативный эффекты.
Клинические обследование установило, что у пациентов ОГ локальная отечность и гиперемия в области послеоперационной раны подвергались более скорому регрессу - в течение (2,5±0,12) дней, по сравнению с ГС (3,8±0,22 дней) (р<0,01). Сроки начала эпителизации в ОГ также были достоверно более ранними (с 3,9±0,25 дня) по сравнению ГС (5,7±0,23 дня) (Р<0,01).
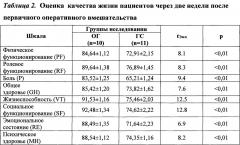
Психодиагностическое обследование с применением опросника MOS SF-36 через две недели после первичного оперативного вмешательства показало достоверно более высокое психическое и физическое благополучие в ОГ по сравнению с ГС (р<0,01) (табл. 2).
Общий уровень качества жизни в ОГ достигал 704,26 баллов, что на 119,36 баллов превышало показатели ГС.
Наиболее выраженные позитивные отличия отмечались по шкалам «боль» (на 18,31 балл), социальное функционирование (17,86 баллов), эмоциональное состояние (на 16,85 баллов), жизнеспособность (на 16,07 баллов).
Данное исследование в квантифицированном виде продемонстрировало в ОГ по сравнению с ГС более быстрое нивелирование и меньшую выраженность болевого синдрома, более быстрое восстановление функции за счет раннего уменьшения отечности, регенерации слизистой, ускорения кострой репарации, а также более быстрое психоэмоциональное восстановление в виде нормализации, что в целом обусловило рост показателей ролевого, социального и физического функционирования, а также общего и психического здоровья.
Полученные данные свидетельствуют в пользу использования МДМ-терапии в комплексе лечебных мероприятий в рамках лечения пациентов с остеосаркомой нижней челюсти.
Таким образом, разработанная комплексная программа лечения больных остеосаркомой нижней челюсти - комплекс методов лечения и их оригинальная последовательность выполнения, показала свою высокую эффективность как в области улучшения качества костной регенерации, так и сокращения реабилитационного периода после оперативного вмешательства; она позволяет осуществить не только излечение пациентов с остеосаркомой нижней челюсти, но и достичь функциональной и эстетической реабилитации данных пациентов путем установления аутоимпланта (фрагмента малоберцовой кости) с последующей имплантацией дентального протеза в аутоимплант.
Способ осуществляется следующим образом.
Проводят комплексную программу лечения больных остеосаркомой нижней челюсти, состоящую из следующих этапов:
I. Этап предоперационной химиотерапии.
Данный этап проводится с использованием стандартных схем химиотерапевтического лечения такого рода больных.
П. Этап оперативного лечения. Данный этап состоит из двух подэтапов, следовавших последовательно:
А) Первый подэтап - резекция пораженного участка нижней челюсти.
Выполняют резекцию нижней челюсти в пределах здоровой ткани. В зависимости от масштабов вовлечения костной ткани в опухолевый процесс и локализации остеосаркомы, выполняют сегментарную или половинную резекцию с экзартикуляцией опухолевой ткани.
Б) Второй подэтап - первичная пластика дефекта нижней челюсти. Остеопластику выполняют путем реконструкции с применением аутоимпланта в виде свободного лоскута на сосудистой ножке из малоберцовой кости. Фрагменты челюсти и аутоимпланта соединялись в единый блок при помощи позиционирующих устройств, выполненных индивидуально.
Для удержания фрагмента нижней челюсти и профилактики смещения участка кости следует использовать пластмассовые или металлические назубные шины с наклонной плоскостью.
Этап оперативного лечения завершается послойным сшиванием и дренированием операционной раны.
III. Этап послеоперационной реабилитации. Послеоперационная реабилитация включает две составляющие, реализуемые параллельно:
А) Послеоперационная химиотерапия. Данный этап, как и этап предоперационной химиотерапии, проводится с использованием стандартных схем химиотерапевтического лечения такого рода больных.
Б) Мезодиэнцефальная модуляция.
Со второго дня послеоперационного периода проводят десятидневный курс МДМ-терапии, состоящий из 13 получасовых сеансов (табл 3).
Таблица 3. Схема сеансов МДМ-терапии у пациентов с остеосаркомой нижней челюсти в послеоперационном периоде.
Сеансы МДМ-терапии проводят два раза в день с шестичасовым интервалом в первые три дня и один раз в день на протяжении последующих семи дней.
Электроды при МДМ-терапии фиксировались на голове пациента по лобно-затылочной методике: анод - на середину лба, катод - на середину затылка. Между кожей и пластиной электрода помещалась одноразовая шестнадцатислойная фланелевая прокладка, увлажненная водой.
Для МДМ-терапии использовались импульсные токи с частотой 10000 Гц, модулированные в низкочастотном диапазоне от 20 до 100 Гц. Сила тока менялась индивидуально в указанном диапазоне до появления у пациента ощущений «ползания мурашек», незначительного жжения или вибрации, отдельных толчков, незначительного давления.
Способ лечения первичной остеосаркомы нижней челюсти начальных стадий, включающий пред- и послеоперационную химиотерапию, оперативное лечение в виде резекции пораженного участка нижней челюсти с первичной аутопластикой дефекта, отличающийся тем, что
со второго дня после операции проводят сеансы мезодиэнцефальной модуляции (МДМ-терапии) вначале два раза в день с шестичасовым интервалом в течение трех дней и далее один раз в день на протяжении последующих семи дней;
при этом МДМ-терапию осуществляют через электроды, которые фиксируют на голове пациента по лобно-затылочной методике: анод - на середину лба, катод - на середину затылка;
для МДМ-терапии используют импульсные токи с частотой 10000 Гц, модулированные в низкочастотном диапазоне от 20 до 100 Гц, силу тока подбирают индивидуально до появления у пациента ощущений «ползания мурашек», и/или незначительного жжения или вибрации, и/или отдельных толчков, и/или незначительного давления, и далее сеанс проводят на подобранной силе тока, длительность сеанса составляет 30 минут.