Рнк-проводники для подавления репликации вируса гепатита b и для элиминации вируса гепатита b из клетки-хозяина
Иллюстрации
Показать всеИзобретение относится к биотехнологии, а именно к генной инженерии. Описан РНК-проводник (направляющих РНК) для подавления экспрессии вируса гепатита B в клетке-хозяине и для элиминации ДНК вируса гепатита В из клетки-хозяина, где указанный РНК-проводник содержит первую нуклеотидную последовательность, выбранную из SEQ ID NO: 1 и SEQ ID NO: 2, и вторую нуклеотидную последовательность SEQ ID NO: 5, фланкирующую первую последовательность с 3´-конца и представляющую собой РНК-шпильку, причём указанная первая последовательность способна связываться с целевым высококонсервативным участком генома вируса гепатита B, а указанная вторая последовательность содержит РАМ-мотив, способный распознаваться РНК-направляемой ДНК-эндонуклеазой Cas9 Streptococcus pyogenes с обеспечением элиминации вируса гепатита B. Также описан РНК-проводник для подавления экспрессии вируса гепатита B в клетке-хозяине и для элиминации ДНК вируса гепатита В из клетки-хозяина, где указанный РНК-проводник содержит первую нуклеотидную последовательность, выбранную из SEQ ID NO: 3 и SEQ ID NO: 4, и вторую нуклеотидную последовательность SEQ ID NO: 6, фланкирующую первую последовательность с 3´-конца и представляющую собой РНК-шпильку, причём указанная первая последовательность способна связываться с целевым высококонсервативным участком генома вируса гепатита B, а указанная вторая последовательность способна распознаваться РНК-направляемой ДНК-эндонуклеазой Cas9 Streptococcus thermophilus с обеспечением элиминации вируса гепатита B. Изобретения могут быть использованы в системах CRISPR-Cas9 для воздействия на высококонсервативные области генома вируса гепатита В (HBV) с последующей элиминацией ДНК вируса HBV, включая кольцевую ковалентно замкнутую ДНК (ккзДНК) HBV, из клетки-хозяина, такой как клетка млекопитающего (например, человека), в частности из гепатоцита человека, а также для подавления репликации вируса гепатита B. По сравнению с известными из уровня техники РНК-проводниками, используемыми в системах CRISPR-Cas9 для воздействия на ДНК HBV, РНК-проводники по изобретению обеспечивают усиленное действие таких систем на высококонсервативные области генома вируса гепатита В и сокращение сроков элиминации вирусной ДНК из клетки-хозяина. 2 н. и 8 з.п. ф-лы, 8 ил., 2 табл., 3 пр.
Реферат
Изобретение относится к области медицины и генной инженерии, а именно к числу средств – РНК-проводников (направляющих РНК), которые могут быть использованы в системах CRISPR-Cas9 для воздействия на высококонсервативные области генома вируса гепатита В (HBV) с последующей элиминацией ДНК вируса HBV, включая кольцевую ковалентно замкнутую ДНК (ккзДНК, cccDNA) HBV, из клетки-хозяина, такой как клетка млекопитающего (например, человека), в частности из гепатоцита человека, а также для подавления репликации вируса гепатита B. По сравнению с известными из уровня техники РНК-проводниками, используемыми в системах CRISPR-Cas9 для воздействия на ДНК HBV, РНК-проводники по изобретению обеспечивают усиленное действие таких систем на высококонсервативные области генома вируса гепатита В и сокращение сроков элиминации вирусной ДНК из клетки-хозяина.
Вирус гепатита В (HBV) является высококонтагиозным вирусом, способным инфицировать человека и вызывать острый или хронический гепатит В. Случаи заражения вирусным гепатитом В отмечаются по всему миру, с наибольшей распространенностью в странах Среднего и Ближнего Востока, Азии, странах Карибского Бассейна, Африки и Южной Америки. По данным ВОЗ, ежегодно регистрируются 350 млн новых случаев заражения вирусным гепатитом В, из которых 1 млн человек ежегодно погибает от его последствий, цирроза печени или гепатоцеллюлярной карциномы (ГЦК) (Custer B et al., 2004; Wright TL, 2006). В Российской Федерации, как и в странах Западной Европы, США, Канаде, Австралии, мероприятия по вакцинации против HBV значительно снизили заболеваемость острым гепатитом В, однако ежегодно в нашей стране регистрируется более сорока тысяч новых случаев хронической инфекции HBV, основной причины цирроза и рака печени (гепатоцеллюлярной карциномы), причем абсолютно большая доля заболевших гепатитом В приходится на молодое трудоспособное население (90%). Распространенность вирусного гепатита B в Российской Федерации составляет 2% от общего населения страны, то есть около 3 млн человек. Заболеваемость вирусом гепатита В – одна из самых серьезных проблем российского здравоохранения. (Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека, Государственный доклад «О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации в 2013 году», 24.06.2014, http://rospotrebnadzor.ru/documents/details.php?ELEMENT_ID=1984).
Острая форма инфекции HBV чаще всего протекает бессимптомно и характеризуется спонтанной элиминацией вируса. Однако в некоторых случаях острая форма инфекции может перетекать в хроническую. Как показано в литературе, хроническая форма инфекции (ХГВ) развивается у 95% новорожденных, у 20-30% детей в возрасте от 1 до 5 лет и менее чем у 5% взрослых (Trépo, et al. Lancet, 2014, 384(9959): 2053-63). В литературе показано, что у 1-2% взрослых с хроническим гепатитом B развивается цирроз печени, у 2-5% - гепатоцеллюлярная карцинома (Liaw et al, Hepatology, 1988, 8: 493-496; Fattovich et al, Gastroenterology, 2004; 127: S35-S50). У детей, страдающих ХГВ, риск развития гепатоцеллюлярной карциномы существенно повышен: показано, что она развивается у 25-50% детей, инфицированных HBV. В целом, как показано, примерно у 40% людей, страдающих ХГВ, рано или поздно развивается цирроз печени, гепатоцеллюлярная карцинома или печеночная недостаточность (Perz et al, Journal of Hepatology, 2006; 45: 529-538).
В качестве наиболее близкого аналога настоящего изобретения выбрана работа Kennedy E.M., et al. (“Suppression of hepatitis B virus DNA accumulation in chronically infected cells using a bacterial CRISPR/Cas RNA-guided DNA endonuclease” // Virology, 2015, 476: 196-205, URL: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4323668), в которой использование РНК-проводников совместно с белками Cas9 Streptococcus pyogenes позволяет воздействовать на различные стадии жизненного цикла вируса гепатита В, что позволяет не только уменьшить общий уровень вирусной ДНК HBV примерно в 1000 раз, но и снизить уровень ккзДНК HBV примерно в 10 раз; использование РНК-проводников совместно с белками Cas9 позволяет также инактивировать остаточную ккзДНК HBV.
Задачей изобретения является разработка новых средств – РНК-проводников (направляющих РНК), которые могут быть использованы в системах CRISPR-Cas9 с белками Cas9, такими как белки Cas9 Streptococcus pyogenes или Streptococcus thermophilus, для элиминации ДНК и прегеномной РНК вируса гепатита В из клетки-хозяина (например, из эукариотической клетки, такой как клетка гепатоцита млекопитающего или, более конкретно, клетка гепатоцита человека), и воздействия на различные стадии жизненного цикла вируса гепатита В (в том числе на стадии, способные к хронической персистенции в организме хозяина и приводящие к развитию у инфицированного лица цирроза печени и/или гепатоцеллюлярной карциномы). Изобретение обеспечивает повышение эффективности лечения острого и хронического вирусного гепатита B, а также повышение эффективности профилактики цирроза печени и гепатоцеллюлярной карциномы, вызванных хронической персистенцией кольцевой ковалентно замкнутой ДНК вируса гепатита B в организме хозяина.
Достигаемый технический результат является комплексным и включает в себя:
- повышение степени элиминации прегеномной РНК (пгРНК, pgRNA) вируса HBV - коррелята активной транскрипции при HBV инфекции;
-- сокращение продолжительности курса терапии, необходимого для элиминации ккзДНК HBV;
- повышение степени элиминации ккзДНК HBV – коррелята хронической персистенции HBV в организме хозяина, имеющей исход в гепатоцеллюлярную карциному и/или в цирроз печени;
- сокращение сроков элиминации ккзДНК HBV из гепатоцитов;
- уменьшение секретируемой ДНК HBV;
- уменьшение поверхностного антигена HBV (HBsAg);
- уменьшение кор-белка, компонента вирионов и регулятора транскрипции ккзДНК;
- уменьшение Х белка HBV, основного про-онкогенного фактора, одного из ключевых компонентов развития фиброза и ГЦК;
- расширение арсенала средств, которые могут использоваться в системе CRISPR-Cas9 для воздействия на высококонсервативные участки генома вируса гепатита B для элиминации различных стадий жизненного цикла вируса гепатита В, включая пгРНК HBV и ккзДНК HBV.
Задача решается, а технический результат достигается созданием молекулы РНК-проводника для подавления экспрессии вируса гепатита B в клетке-хозяине и для элиминации ДНК вируса гепатита В из клетки-хозяина, где указанный РНК-проводник содержит первую нуклеотидную последовательность, выбранную из SEQ ID NO: 1 (TCCGCAGTATGGATCGGCAG) и SEQ ID NO: 2 (GCAGATGAGAAGGCACAGAC), и вторую нуклеотидную последовательность SEQ ID NO: 5, фланкирующую первую последовательность с 3'-конца и представляющую собой РНК-шпильку, причём указанная первая последовательность способна связываться с целевым высококонсервативным участком генома вируса гепатита B, а указанная вторая последовательность содержит РАМ-мотив, способный распознаваться РНК-направляемой ДНК-эндонуклеазой Cas9 Streptococcus pyogenes с обеспечением элиминации вируса гепатита B.
Согласно предпочтительным вариантам реализации указанный технический результат также достигается тем, что:
- РНК-направляемая ДНК-эндонуклеаза Cas9 Streptococcus pyogenes распознаёт последовательность ДНК, содержащую PAM-мотив NGG;
- клетка-хозяин представляет собой клетку млекопитающего, инфицированную вирусом гепатита В, или клетку млекопитающего, в которой персистирует вируc гепатита В;
- ДНК вируса гепатита B представляет собой кольцевую ковалентно замкнутую ДНК (ккзДНК).
Молекула РНК-проводника по п. 1, отличающаяся тем, что вирус гепатита B имеет генотип, который выбран из группы, включающей генотипы A, В, С, D, Е, F, G и H.
Задача также решается, а технический результат достигается созданием молекулы РНК-проводника для подавления экспрессии вируса гепатита B в клетке-хозяине и для элиминации ДНК вируса гепатита В из клетки-хозяина, где указанный РНК-проводник содержит первую нуклеотидную последовательность, выбранную из SEQ ID NO: 3 (GGCGGGGTTTTTCTTGTTGA) и SEQ ID NO: 4 (GGCACTAGTAAACTGAGCCA), и вторую нуклеотидную последовательность SEQ ID NO: 6, фланкирующую первую последовательность с 3'-конца и представляющую собой РНК-шпильку, причём указанная первая последовательность способна связываться с целевым высококонсервативным участком генома вируса гепатита B, а указанная вторая последовательность способна распознаваться РНК-направляемой ДНК-эндонуклеазой Cas9 Streptococcus thermophilus с обеспечением элиминации вируса гепатита B.
Согласно предпочтительным вариантам реализации указанный технический результат также достигается тем, что:
- РНК-направляемая ДНК-эндонуклеаза Cas9 Streptococcus thermophilus распознаёт последовательность ДНК, содержащую PAM-мотив NNAGAAW;
- клетка-хозяин представляет собой клетку млекопитающего, инфицированную вирусом гепатита В, или клетку млекопитающего, в которой персистирует вируc гепатита В;
- ДНК вируса гепатита B представляет собой кольцевую ковалентно замкнутую ДНК (ккзДНК);
- вирус гепатита B имеет генотип, который выбран из группы, включающей генотипы A, В, С, D, Е, F, G и H.
Также изобретение поясняется чертежами.
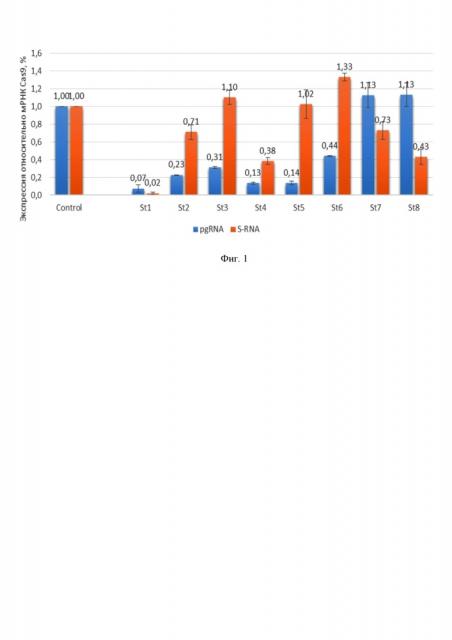
На фиг. 1 приведено снижение транскрипции HBV при ко-трансфекции систем S. thermophiles CRISPR/Cas9 и плазмиды 1.1merHBV в клетках HepG2 уже на 3 сутки после трансфекции. РНК-проводник SEQ ID NO: 4 (St4) снижает pgRNA и S-RNA (S-РНК HBV) на 87% и 62%, соответственно, в то время как SEQ ID NO: 3 (St3) снижает транскрипцию HBV только по pgRNA на 69%.
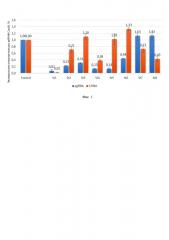
На фиг. 2 приведено противовирусное действие систем S. thermophiles CRISPR/Cas9 с РНК-проводниками SEQ ID NO: 3 (St3) и SEQ ID NO: 4 (St4). Высокоэффективная нуклеофекция клеток-модели хронической инфекции HBV HepG2-1.1merHBV, плазмидами, кодирующими StCas9-T2A-Blasticidin и ПЦР-продукты с U6-промотором и РНК-проводниками St3 и St4, с последующей негативной селекцией нетрансфицированных клеток. St3 и St4 приводят к значительному снижению всех показателей вирусного цикла (pgRNA на 56% и 61%, S-RNA на 63% и 64%, секретируемого HBsAg на 0,45 МЕ/мл и 1,65 МЕ/мл, секретируемой ДНК HBV на 59% и 53%, ккзДНК на 60% и 74% для St3 и St4, соответственно).
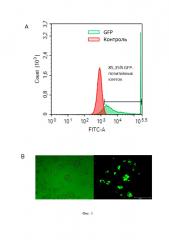
На фиг. 3 показана нуклеофекция клеток HepG2-1.1merHBV. На фиг. 3A – результаты FACS-анализа нуклеофицированных клеток по зеленому каналу FITC-A; на фиг. 3В – иммунофлуоресцентные фотографии нуклеофицированных клеток в светлом поле (слева) и на канале FITC-А (справа). Эффективность нуклеофекции воспроизводимо составляет 85±2%.
На фиг. 4 показано сравнение противовирусной эффективности пятидесяти РНК-проводников системы CRISPR/Cas9. На модели ко-трансфекции клеток HepG2 системами CRISPR/Cas9 и плазмиды, запускающей цикл HBV (1.1merHBV) была проведена оценка противовирусной активности пятидесяти индивидуальных РНК-проводников, среди которых Sp37 (SEQ ID NO: 2), Sp31, Sp20 (SEQ ID NO: 1), Sp15, Sp12, Sp11, Sp9 и Sp8 показали высокую эффективность по снижению транскрипции HBV.
На фиг. 5 приведено противовирусное действие S.pyogenes CRISPR/Cas9. На 7-е сутки после нуклеофекции клеток HepG2-1.1merHBV плазмидой, кодирующей Cas9-T2A-Blasticidin, и ПЦР-продуктами с U6-промотором и РНК-проводником Sp20 или Sp37 приводит к снижению транскрипции HBV pgRNA на 85% и 86%, S-RNA на 70% и 43% и ккзДНК на 79% и 82% для Sp20 (SEQ ID NO: 1) и Sp37 (SEQ ID NO: 2), соответственно.
На фиг. 6 показана трансфекция CRISPR/Cas9 с эффективными РНК-проводниками снижает выработку HBcAg HBV. При ко-трансфекции клеток HepG2 системами CRISPR/Cas9 с плазмидой, запускающей цикл HBV, происходит снижение выработки кор-антигена HBV – белка, участвующего в сборке вирионов и транскрипции ккзДНК (представлено изображение по действию Sp20). Иммуноцитохимическое окрашивание клеток HepG2, красный канал (594 нм) HBcAg; синий канал (365 нм) Hoechst33342, ядра клеток, Merged – наложение изображений.
На фиг. 7 показана трансфекция CRISPR/Cas9 с эффективными РНК-проводниками снижает выработку HBxAg HBV. Ко-трансфекция клеток HepG2 снижает продукцию HBx белка HBV, основного про-онкогенного белка HBV, играющего ключевую роль в злокачественной трансформации гепатоцитов и развития гепатоцеллюлярной карциномы. Иммуноцитохимическое окрашивание клеток HepG2, красный канал (594 нм) HBxAg; синий канал (365 нм) Hoechst33342, ядра клеток, Merged – наложение изображений.
На фиг. 8 показано внесение разрывов в ккзДНК HBV. Выделение ккзДНК HBV на 7-е сутки после нуклеофекции проводили с помощью Hirt-экстракции и обработки изолятов ферментом Plasmid-safe ATP-dependent DNase, разрушающим все виды ДНК, кроме кольцевых форм. Секвенирование нового поколения с помощью MiSeq проводили на ампликонах, полученных с помощью специфических праймеров с участка, охватывающего сайт нуклеолитического разрыва. Как видно из чертежа, РНК-проводник Sp20 с плазмидой, кодирующей S.pyogenes Cas9, вносит многочисленные мутации (на чертеже представлены делеции), включая делеции, инсерции, инверсии, рекомбинации и SNP в зоне разрыва.
Далее приводятся примеры осуществления изобретения, которые иллюстрируют, но не охватывают все возможные варианты осуществления изобретения и не ограничивают изобретение.
Примеры осуществления изобретения
Пример 1
В экспериментах были использованы 4 вида систем CRISPR/Cas9, полученных из 4 видов бактериальных организмов: Cas9 Streptococcus pyogenes (SpCas9), Cas9 Streptococcus thermophiles (StCas9), Cas9 Neisseria meningitides (NmCas9) и Cas9 Francicella novicida (FnCas9). Отличие этих систем состоит в разных консенсусах участка PAM: NGG для SpCas9 и FnCas9 (при этом SpCas9 может расщеплять только ДНК, в то время как для FnCas9 была также показана активность в отношении РНК), NmCas9 с РАМ NNNNGATT и NNAGAAW для StCas9.
Первым этапом настоящей работы стал подбор последовательностей-мишеней в ккзДНК для создания РНК-проводников, с этой целью мы использовали современные алгоритмы in silico и программы, находящиеся в открытом доступе, включая BroadInstitute (https://portals.broadinstitute.org/gpp/public/analysis-tools/sgrna-design) и Center for Organismal Studies, Heidelberg (http://crispr.cos.uni-heidelberg.de/). Был составлен перечень участков на геноме HBV с теоретически рассчитанной вероятностью их расщепления в консервативных и относительно консервативных участках генома.
Второй этап – синтез ПЦР-продуктов, содержащих U6-промотор и участок, соответствующий РНК-проводнику, с помощью двухэтапного мутагенного ПЦР (Cong L et al., 2013). Промежуточные продукты и ПЦР-продукты очищали на колонках Qiagen (QIAquick gel extraction kit) после вырезания из геля. Чистоту и концентрации ПЦР-продуктов оценивали по оптическому светопоглощению на спектрофотометре Nanodrop 2000. Для проверки точного совпадения полученных нуклеотидных последовательностей с заявленными последовательностями ПЦР-продуктов проводили клональное секвенирование. ПЦР-продукты получали в реакциях с высокоточной Q5-полимеразой (New England Biolabs).
Третий этап – проверка эффективности разрезания выбранных участков в культурах клеток-моделях хронической инфекции HBV in vitro. В основе этого этапа лежат два подхода.
Первый этап состоит в ко-трансфекции линии клеток гепатомы человека HepG2 векторами, кодирующими геном HBV под индуцибельным tet-on промотором (HBV генотипа D, 1.1mer-геном, предоставлено Dieter Glebe, Giessen University), плазмидами, кодирующими белки Cas9 (Addgene#63592 – SpCas9; Addgene#48669 – StCas9; Addgene#48670 – NMCas9; Addgene#68705 – FnCas9) и синтезированными ПЦР-продуктами, кодирующими РНК-проводник. Клетки ко-трансфицировали с помощью реагента полиэтиленимина или реагента Lipofectamine 2000, транскрипцию HBV активировали в течение 24 часов обработкой доксициклином (100 нг/мл). Оценку противовирусного действия систем CRISPR/Cas9 проводили через 3 суток по основным транскриптам ккзДНК HBV – прегеномной РНК HBV и S-РНК HBV методом ПЦР в режиме реального времени с помощью пары специфических праймеров и зондов после выделения нуклеиновых кислот, обработки ДНКазой I типа без РНКазной активности и обратной транскрипции.
Второй этап состоит в нуклеофекции модели хронической инфекции HBV, трансгенной линии клеток человека со вставкой 1.1mer генома HBV под индуцибельным tet-on промотором. Клетки HepG2-1.1merHBV воспроизводят полноценный цикл репликации HBV, в том числе образование полноценной ккзДНК, секрецию HBsAg и пр. Постановку нуклеофекции осуществляли на приборе Lonza с помощью наборов Amaxa 4D Nucleofector (V4XC-2024). В смесь для нуклеофекци входили: (1) вектор, кодирующий Cas9 белок с белком антибиотикорезистентности к бластицидину и (2) ПЦР-продукт, кодирующий РНК-проводник. Клетки нуклеофицировали, активировали сразу после нуклеофекции в течение 24 часов в среде с доксициклином (100 нг/мл). Эффективность нуклеофекции по данным проточной цитофлюориметрии составляла 80-85%. Для удаления не трансфицированных клеток проводили негативную селекцию путем инкубации клеток в полной среде с выбранной концентрацией бластицидина. Снятие клеток и выделение нуклеиновых кислот производили на 5 сутки после нуклеофекции. Противовирусное действие систем CRISPR/Cas9 оценивали по экспрессии прегеномной РНК HBV, S-РНК HBV, количествам секретируемого HBsAg, секретируемой ДНК HBV и относительному количеству ккзДНК. Остаточные матрицы ккзДНК в экспериментальных образцах с системами CRISPR/Cas9 использовали для амплификации участка нуклеолитического расщепления и секвенирования продуктов ПЦР методом NGS (MiSeq). Частоту мутаций подсчитывали в программе Geneious 6.1.8.
Пример 2
Для работы обоих типов систем (S.thermophiles и S.pyogenes) необходим РНК-проводник, состоящий из целевого участка, прилежащего к РАМ-последовательности (NGG и NNAGAAW, соответственно), и шпильки, распознаваемой белком Cas9.
На модели скрининга – ко-трансфекции клеток HepG2 плазмидой, кодирующей Cas9 белок, плазмидой 1.1merHBV, запускающей цикл вируса, и ПЦР-продуктами, кодирующими соответствующие РНК-проводники, по влиянию на снижение транскрипции HBV были отобраны РНК-проводники с наивысшими значениями противовирусного действия (см. фиг. 1, 3). Дальнейший анализ выявил РНК-проводники в высококонсервативных регионах генома HBV (см. таблицу 1), что позволяет использовать указанные РНК-проводники для лечения большинства пациентов с хроническим гепатитом B вне зависимости от генотипа или пригодных для большинства генотипов.
Таблица 1. Процент абсолютных (точных) совпадений последовательностей РНК-проводников с учетом РАМ-распознающих последовательностей для S.pyogenes CRISPR/Cas9 (NGG) и S.thermophiles CRISPR/Cas9 (NNAGAAW) среди всех генотипов HBV (А-Н). Процент был рассчитан в программе Geneious 6.1.8 с полногеномными последовательностями HBV, взятыми из базы данных GenBank. Все выбранные РНК-проводники с учетом РАМ-распознающих участков, располагаются в высококонсервативных областях, идентичных для большинства генотипов и абсолютного большинства субтипов внутри каждого генотипа.
| РНК-проводник | A (794), % | B (1450), % | C (1830), % | D (882), % | E (250), % | F (227), % | G (36), % | H (26), % | Противовирусная активность (pgRNA, %) |
| Sp20 | 98,7 | 83,7 | 90,3 | 91,6 | 86,4 | 96,5 | 100 | 88,5 | 90,7 |
| Sp37 | 97,1 | 81,1 | 91,5 | 97,8 | 75,6 | 1,8 | 11,1 | 0 | 87,4 |
| St3 | 95,6 | 3,0 | 88,7 | 93,5 | 0 | 0,9 | 97,2 | 0 | 69,8 |
| St4 | 98,6 | 97,2 | 92,7 | 97,3 | 98 | 0,9 | 100 | 3,8 | 86,6 |
Эксперименты по нуклеофекции на модели хронической инфекции HepG2-1.1merHBV (см. фиг. 2, 3, 5) выявили, что S.thermophiles и S.pyogenes CRISPR/Cas9 снижают все показатели цикла HBV: транскрипцию (pgRNA, S-RNA), а главное, ключевой компонент вирусного цикла, ответственный за хронизацию инфекции, кольцевую ковалентно замкнутую ДНК (снижение ккзДНК на 60%-74% для S.thermophiles и на 79%-82% для S.pyogenes CRISPR/Cas9). Стоит отметить, что в прототипе и других объектах из уровня техники снижение ккзДНК происходит на 67% (Kennedy E.M., et al. “Suppression of hepatitis B virus DNA accumulation in chronically infected cells using a bacterial CRISPR/Cas RNA-guided DNA endonuclease” // Virology. 2015, 476: 196-205) и 71% (Ramanan V., et al. “CRISPR/Cas9 cleavage of viral DNA efficiently suppresses hepatitis B virus” // Scientific Reports. 2015; 5:10833), что хуже показателей по снижению ккзДНК, которых удалось достичь авторам настоящего изобретения – 79-82 %.
Кроме того, в обеих вышеупомянутых работах результаты были получены к 13-м суткам или к 21-м суткам после внесения CRISPR/Cas9 систем, в то время как в условиях настоящего изобретения все результаты получены на 7-е сутки, причем на одной из лучших моделей хронического гепатита клетках HepG2-1.1merHBV, которые воспроизводят полноценный цикл репликации и наиболее близки по характеристикам к естественному циклу HBV. В целом, это говорит о значительно более выраженном противовирусном эффекте выбранных РНК-проводников. Более того, в отличие от всех ранее опубликованных в уровне техники данных в настоящем изобретении впервые использовали системы S.thermophiles CRISPR/Cas9 на модели хронического гепатита. Известно, что S.thermophiles CRISPR/Cas9 обладают меньшим размером, большей специфичностью действия и меньшей вероятностью внесения внецелевых разрывов в сравнении с классическим белком S.pyogenes Cas9, что связано с особенностями структуры белка S.thermophiles и более длинным РАМ (NNAGAAW – семь букв против NGG – трёх букв у S.pyogenes Cas9) (Müller M., et al. “Streptococcus thermophilus CRISPR-Cas9 Systems Enable Specific Editing of the Human Genome” // Molecular Therapy. 2016, 24(3): 636-644).
Пример 3
Также были получены данные по снижению секреции HBsAg, HBV DNA и снижению интенсивности окрашивания клеток на HBcAg HBV и HBxAg (Рис. 2, 5, 7). Методом секвенирования нового поколения было продемонстрировано, что оставшиеся матрицы ккзДНК содержат индел мутации и другие полиморфизмы в сайтах РНК-проводников (Рис. 6, Табл. 2), что указывает на прямое нуклеолитическое действие систем CRISPR/Cas9 на ккзДНК.
Таблица 2. Сводная таблица по внесению мутаций в ккзДНК под действием CRISPR/Cas9 систем с РНК-проводником Sp20. Результаты были получены на ккзДНК на 7 сутки после нуклеофекции CRISPR/Cas9 системы. Ампликоны, охватывающие участок нуклеолитического расщепления, были наработаны с ккзДНК и секвенированы методом NGS на секвенаторе MiSeq (97,079 прочтений). Результаты обрабатывали в программе Geneious 6.1.8.
| Делеции (1-4 nts),% | Делеции (5-10 nts),% | Делеции(13 nts),% | Общие делеции,% | Инсерции(1-4 nts),% | Общие инсерции,% | SNP,% | |
| Частота варианта | 17,40 | 1,12 | 0,50 | 19,10 | 0,35 | 35,10 | 0,49 |
| Частота мутаций со сдвигом рамок считывания | 10,20 | 1,10 | 0,50 | 11,80 | 0,21 | 21,10 | 0,49 |
| Доля мутаций со сдвигом рамок считывания | 61,80 | 60,10 | 100 |
Таким образом, угнетение вирусного цикла и внесение мутаций в матрицы ккзДНК, не подвергшиеся нуклеолитической деградации, связаны с действием выбранных CRISPR/Cas9 систем с указанными РНК-проводниками. В отличие от технологии siRNA и miRNA, которые используют короткие РНК для интерференции с транскриптами HBV и не оказывают прямого влияния на ккзДНК, действие CRISPR/Cas9 систем связано с прямым нуклеолитическим действием Cas9 белка на целевую мишень (ккзДНК). HBV – генетически гетерогенный вирус, поэтому получение высокоэффективных РНК-проводников, направляющих Cas9 белок к консервативным участкам HBV, – один из ключевых этапов в создании перспективного противовирусного средства. Мишени полученных РНК-проводников находятся в высококонсервативных регионах (доля абсолютных совпадений с учетом прилежащих РАМ-последовательностей выше 90% по большинству генотипов HBV), вызывают расщепление целевой мишени (ккзДНК) либо вносят многочисленные мутации и оказывают мощное противовирусное действие на всех использованных моделях.
1. Молекула РНК-проводника для подавления экспрессии вируса гепатита B в клетке-хозяине и для элиминации ДНК вируса гепатита В из клетки-хозяина, где указанный РНК-проводник содержит первую нуклеотидную последовательность, выбранную из SEQ ID NO: 1 и SEQ ID NO: 2, и вторую нуклеотидную последовательность SEQ ID NO: 5, фланкирующую первую последовательность с 3´-конца и представляющую собой РНК-шпильку, причём указанная первая последовательность способна связываться с целевым высококонсервативным участком генома вируса гепатита B, а указанная вторая последовательность содержит РАМ-мотив, способный распознаваться РНК-направляемой ДНК-эндонуклеазой Cas9 Streptococcus pyogenes с обеспечением элиминации вируса гепатита B.
2. Молекула РНК-проводника по п. 1, отличающаяся тем, что РНК-направляемая ДНК-эндонуклеаза Cas9 Streptococcus pyogenes распознаёт последовательность ДНК, содержащую PAM-мотив NGG.
3. Молекула РНК-проводника по п. 1, отличающаяся тем, что клетка-хозяин представляет собой клетку млекопитающего, инфицированную вирусом гепатита В, или клетку млекопитающего, в которой персистирует вируc гепатита В.
4. Молекула РНК-проводника по п. 1, отличающаяся тем, что ДНК вируса гепатита B представляет собой кольцевую ковалентно замкнутую ДНК (ккзДНК).
5. Молекула РНК-проводника по п. 1, отличающаяся тем, что вирус гепатита B имеет генотип, который выбран из группы, включающей генотипы A, В, С, D, Е, F, G и H.
6. Молекула РНК-проводника для подавления экспрессии вируса гепатита B в клетке-хозяине и для элиминации ДНК вируса гепатита В из клетки-хозяина, где указанный РНК-проводник содержит первую нуклеотидную последовательность, выбранную из SEQ ID NO: 3 и SEQ ID NO: 4, и вторую нуклеотидную последовательность SEQ ID NO: 6, фланкирующую первую последовательность с 3´-конца и представляющую собой РНК-шпильку, причём указанная первая последовательность способна связываться с целевым высококонсервативным участком генома вируса гепатита B, а указанная вторая последовательность способна распознаваться РНК-направляемой ДНК-эндонуклеазой Cas9 Streptococcus thermophilus с обеспечением элиминации вируса гепатита B.
7. Молекула РНК-проводника по п. 6, где РНК-направляемая ДНК-эндонуклеаза Cas9 Streptococcus thermophilus распознаёт последовательность ДНК, содержащую PAM-мотив NNAGAAW.
8. Молекула РНК-проводника по п. 6, отличающаяся тем, что клетка-хозяин представляет собой клетку млекопитающего, инфицированную вирусом гепатита В, или клетку млекопитающего, в которой персистирует вируc гепатита В.
9. Молекула РНК-проводника по п. 6, отличающаяся тем, что ДНК вируса гепатита B представляет собой кольцевую ковалентно замкнутую ДНК (ккзДНК).
10. Молекула РНК-проводника по п. 6, отличающаяся тем, что вирус гепатита B имеет генотип, который выбран из группы, включающей генотипы A, В, С, D, Е, F, G и H.