Способ создания биорезорбируемого клеточного скаффолда на основе фибрина плазмы крови
Иллюстрации
Показать всеИзобретение относится к области клеточной биологии и биотехнологии, конкретно к созданию биорезорбируемого клеточного скаффолда на основе фибрина плазмы крови. Способ включает смешивание плазмы крови или криопреципитата плазмы крови с раствором коллагена I типа, имеющим рН 7,4, введение суспензии животных клеток и добавление тромбин-кальциевой смеси в соотношении 3,94:2,86:1:1,09 соответсвенно. Изобретение позволяет получить биорезорбируемый клеточный скаффолд, имеющий 3D структуру и содержащий равномерно распределенные по всей толще клетки. 6 ил., 3 пр.
Реферат
Предлагаемое изобретение относится к медицине, биотехнологии, регенеративной медицине и представляет собой способ создания биорезорбируемого клеточного скаффолда на основе фибрина плазмы крови для тканевой инженерии.
Известны фибриновые гидрогели, широко применяемые в качестве скаффолдов для регенерации различных типов ткани. Фибриноген и фибрин являются естественной ранозаживляющей матрицей, которая обеспечивает 3D каркас для клеток, их миграцию и адгезию в область раны. При создании скаффолдов широко используются различные методы изготовления трехмерных структур - электроспиннинг, фазовая сепарация, сублимационная сушка и другие.
Однако эти методы достаточно агрессивны и не позволяют вводить клетки в скаффолды в процессе их изготовления. Как правило, эти способы характеризуются сложностью технологического процесса и требуют дорогостоящей аппаратуры. С этой точки зрения фибриноген является идеальным материалом, процесс полимеризации которого абсолютно инертен для клеток и не нуждается в специализированном оборудовании.
В качестве прототипа выбран способ создания фибринового гидрогеля, представленного в качестве скаффолда для тканевой инженерии (см. Rowe SL, Lee S, Stegemann JP. Influence of thrombin concentration on the mechanical and morphological properties of cell-seeded fibrin hydrogels. Acta Biomater. 2007; 3(1):59-67.) и содержащего клетки, которые вводятся непосредственно в фибриновый гидрогель до его полимеризации, катализируемой тромбином. Данный способ заключается в том, что после смешивания раствора лиофилизированного фибриногена и клеток проводят полимеризацию фибрина, катализируемую тромбином в следующих соотношениях по объему 50:10:40 - раствор фибриногена: эмбриональная бычья сыворотка: раствор тромбина. В данном прототипе доказано, что тромбин катализировал образование микроволокон фибрина, в результате чего создавалась трехмерная структура, в которой клетки были "встроены" в фибриновый гель во время его образования. Сам тромбин не снижал жизнеспособности и не препятствовал пролиферации клеток.
Однако способ имеет следующие недостатки: отсутствие в фибриновом скаффолде необходимых ростовых факторов и компонентов, обеспечивающих его каркасную функцию.
Задача предлагаемого изобретения - усовершенствование способа.
Техническим результатом предлагаемого изобретения является:
- создание клеточного скаффолда на основе фибрина плазмы крови с включением в него ростовых факторов, в композиции с коллагеном I типа и обеспечением 3D структуры;
- увеличение концентрации в скаффолде фибриногена, фибронектина, XIII фактора, ингибиторов фибринолиза, циркулирующих молекул клеточной адгезии, а также ростовых факторов за счет использования вместо плазмы крови, полученного из нее криопреципитата со стандартизированной концентрацией в нем фибриногена.
Поставленный технический результат достигается за счет того, что в способе, включающем смешивание раствора фибриногена и клеток, проведение полимеризации фибрина, катализируемой тромбином, источником растворенного фибриногена является плазма крови, обеспечивающая присутствие в скаффолде ростовых факторов, в композиции с коллагеном I типа, полимеризация которого, после доведения pH до 7,4, происходит после полимеризации фибрина, что обеспечивает объемную 3D структуру скаффолда.
Для увеличения концентрации в скаффолде фибриногена, фибронектина, XIII фактора, ингибиторов фибринолиза, циркулирующих молекул клеточной адгезии, а также ростовых факторов плазму крови заменяют криопреципитатом со стандартизированной концентрацией в нем фибриногена.
Для стандартизации концентрации фибриногена в скаффолде определяют его концентрацию в криопреципитате и доводят до стандартной концентрации путем добавления полученного при криообработке плазмы супернатанта.
Предложенный способ создания биорезорбируемого клеточного скаффолда на основе фибрина плазмы крови по п. 1 может быть реализован согласно следующей методике:
1. К уксуснокислому коллагену I типа (0,2% раствор) добавляют раствор NaOH до достижения pH 7,4.
2. К плазме крови добавляют раствор коллагена.
3. В полученный композитный раствор (см. п. 2) вводят суспензию клеток (фибробластов, мезенхимальных мультипотентных стромальных клеток или других клеток мезенхимального происхождения) в ростовой среде DMEM (среда Игла в модификации Дульбекко), содержащей 10% эмбриональной телячьей сыворотки (для экспериментальных исследований) или 10% аутологичной сыворотки (для использования в регенеративной медицине).
4. Композитный раствор, содержащий суспензию клеток, в объеме 2,5 мл заливают в форму для скаффолда (например, в чашку Петри, диаметром 3,5 см, предварительно обработанную силиконом).
5. После завершения манипуляций согласно п. 4 к композитному раствору, содержащему суспензию клеток, немедленно добавляют тромбин-кальциевую смесь.
6. Выдерживают полученный скаффолд в форме в течение 20 минут (для более полной полимеризации фибрина), затем перемещают его в пластиковую чашку Петри и заливают 5 мл ростовой среды DMEM, содержащей 10% сыворотки. Помещают чашку Петри с полученным скаффолдом в CO2 инкубатор при 5% CO2 и температуре 37°С. В течение последующих 3 часов происходит полная полимеризация содержащихся в скаффолде коллагена и фибриногена.
7. Соотношение компонентов - плазма крови: раствор коллагена с pH 7,4: суспензия клеток: тромбин-кальциевая смесь 3,94:2,86:1:1,09 соответственно.
Предлагаемый способ создания биорезорбируемого клеточного скаффолда на основе фибрина плазмы крови по п. 2 может быть реализован согласно следующей методике:
1. Криопреципитат готовится путем оттаивания свежезамороженной плазмы крови при температуре 1-6°С и ее центрифугирования при той же температуре при 4000 об/мин в течение 25 минут с последующим удалением супернатанта. Нерастворимый на холоде преципитат помещается в холодильную камеру в течение часа после извлечения из рефрижераторной центрифуги.
2. Для стандартизации концентрации фибриногена в скаффолде определяют его концентрацию в супернатанте и в криопреципитате и доводят его концентрацию в последнем до необходимого уровня путем смешивания супенатанта и криопреципитата.
3. К уксуснокислому коллагену I типа (0,2% раствор) добавляют раствор NaOH до достижения pH 7,4.
4. К криопреципитату плазмы крови добавляют раствор коллагена.
5. В полученный композитный раствор (см. п. 4) вводят суспензию клеток (фибробластов, мезенхимальных мультипотентных стромальных клеток, или других клеток мезенхимального происхождения) в культуральной среде DMEM (среда Игла в модификации Дульбекко), содержащей 10% эмбриональной телячьей сыворотки (для экспериментальных исследований) или 10% аутологичной сыворотки (для использования в регенеративной медицине).
6. Композитный раствор, содержащий суспензию клеток, в объеме 2,5 мл заливают в форму для скаффолда (например, в чашку Петри, диаметром 3,5 см, предварительно обработанную силиконом).
7. После завершения манипуляций согласно п. 4 к композитному раствору, содержащему суспензию клеток, немедленно добавляют тромбин-кальциевую смесь.
8. Выдерживают полученный скаффолд в форме в течение 20 минут (для более полной полимеризации фибрина), затем перемещают его в пластиковую чашку Петри и заливают 5 мл ростовой среды DMEM, содержащей 10% сыворотки. Помещают чашку Петри с полученным скаффолдом в CO2 инкубатор при 5% CO2 и температуре 37°С. В течение последующих 3 часов происходит полная полимеризация содержащихся в скаффолде коллагена и фибриногена.
9. Соотношение компонентов - криопреципитат плазмы крови: раствор коллагена с pH 7,4: суспензия клеток: тромбин-кальциевая смесь 3,94:2,86:1:1,09 соответственно.
Использование в качестве источника фибриногена плазмы крови в биорезорбируемой биополимерной клеточно-инженерной конструкции в значительной степени устраняет недостаток фибринового гидрогеля - отсутствие ростовых факторов, представленного в прототипе в качестве скаффолда для тканевой инженерии (см. Platelet-rich plasma scaffolds for tissue engineering: More than just growth factors in three dimensions / E. Anitua, R. Prado, S. Padilla, G. Orive // Platelets - 2014. - Vol. 7104 - N3 - P. 1-2). В плазме крови содержатся необходимые для роста и размножения клеток аминокислоты. В ней содержится и фибронектин - один из ключевых белков межклеточного матрикса, который, в частности, увеличивает клеточную адгезию, обеспечивает ответ клеток на факторы роста и является одним из элементов управления клеточного цикла за счет способности связываться с трансмембранными интегринами (см. Morla А. A Fibronectin Self-Assembly Site Involved in Fibronectin Matrix Assembly: Reconstruction in a Synthetic Peptide / A. Morla, E. Ruoslahti, E.J. Fogerty, V.E. Koteliansky, D.E. Mosher J Biol Chem // J. Cell Biol. - 1992. - Vol. 118 - N 2 - P. 421-429; Morla A. Superfibronectin is a functionally distinct form of fibronectin. / A. Morla, Z. Zhang, E. Ruoslahti // Nature - 1994. - Vol. 367 - N 6459 - P. 193-196). Показано, что мультипотентные мезенхимальные стромальные клетки человека (ММСК) собирают фибронектин плазмы в фибриллы своего экстрацеллюлярного матрикса в течение 24 часов. Затем ММСК активно натягивают собранные фибриллы внеклеточного матрикса (см. Mesenchymal Stem Cells Exploit Extracellular Matrix as Mechanotransducer / B. Li, C. Moshfegh, Z. Lin, J. Albuschies, V. Vogel // Sci. Rep. - 2013. - Vol. 3 - P. 2425).
В плазме крови содержится XIII фактор, который обеспечивает естественное сшивание нитей фибрина за счет образования ковалентных связей между глутамил- и лизиновыми остатками соседних молекул фибрина. Он же может задерживать разрушение скаффолда in vivo путем фибринолиза и протеолиза. Антифибринолитическим действием обладает и ингибитор активатора плазминогена, содержащийся в плазме крови.
Кроме плазмы крови в предлагаемую клеточно-инженерную конструкцию входит коллаген I типа, составляющий основу соединительной ткани организма и обеспечивающий ее прочность и эластичность. Коллаген имеет несколько преимуществ, которые позволяют использовать данный материал для получения скаффолдов в тканевой инженерии: биосовместимость, волокнистая структура, хорошая сочетаемость с другими материалами, биодеградируемость. По данным Brougham С.М. (см. Brougham С.М. Incorporation of fibrin into a collagen-glycosaminoglycan matrix results in a scaffold with improved mechanical properties and enhanced capacity to resist cell-mediated contraction / С.М. Brougham, T.J. Levingstone, S. Jockenhoevel, Т.С. Flanagan, F.J. O'Brien // Acta Biomater. - 2015. - Vol. 26 - P. 205-214) введение коллагена в состав фибринового скаффолда многократно увеличивает его прочность. Кроме того, следует отметить, что коллаген обладает свойствами, обуславливающими высокую клеточную адгезию скаффолда.
Предлагаемый способ создания биорезорбируемого клеточного скаффолда позволяет не только не повреждать клетки, вводимые в скаффолд в процессе его изготовления, но и сформировать его трехмерную структуру за счет того, что полимеризация коллагена происходит на фоне уже образовавшихся фибриновых волокон, которые и определяют направление волокон коллагена. Согласно данным Gillette В.М. и др. (см. Gillette В.М. In situ collagen assembly for integrating microfabricated three-dimensional cell-seeded matrices. / В.M. Gillette, J. a Jensen, B. Tang, G.J. Yang, A. Bazargan-Lari, M. Zhong, S.K. Sia // Nat. Mater. - 2008. - Vol. 7 - N 8 - P. 636-640) рост и зарождение новых коллагеновых волокон, в том числе в фибриновых скаффолдах, может происходить из предварительно сформированных волокон коллагена.
Однако концентрация этих факторов в небольшом объеме плазмы, формирующей скаффолд, явно недостаточна. Увеличение концентрации белков плазмы крови, формирующих каркас скаффолда, повышающих его прочность и стабильность в малом объеме скаффолда может быть осуществлено за счет использования криопреципитата плазмы крови.
Известно, что криопреципитат плазмы крови содержит фибриноген, фибронектин, фактор XIII, ингибиторы фибринолиза, циркулирующие молекулы клеточной адгезии (Е-селектин, V-CAM, I-CAM) в значительно большей концентрации, чем плазма крови (см. Руководство по клиническому применению донорской крови и ее компонентов. Бишкек, 2015, с. 56; Жидков Ю.Б., Колотилов Л.В., Современная инфузионно-трансфузионная терапия, 2007, глава 2). Появились исследования, свидетельствующие об усилении регенерации цирротической печени при внутрипеченочном введении криопреципитата (см. Черноусов А.Ф., Хоробрых Т.В., Карпова Р.В. и др. Регенерация цирротической печени кроликов при внутрипеченочном введении криопреципитата // Бюл. эксперим. биол. и мед. - 2012. - №9. - С. 384-386), что дает дополнительное основание для использования криопреципитата плазмы крови в регенеративной медицине.
Пример 1
На Фиг. 1 изображен внешний вид биорезорбируемого клеточного скаффолда на основе фибрина плазмы крови, выполненного в виде формоустойчивой, эластичной, прозрачной, плотной, гелеобразной структуры.
Пример 2
На основе данных световой микроскопии и флуоресцентной микроскопии с прижизненной окраской ядер установлено, что предложенный биорезорбируемый клеточный скаффолд не является цитотоксичным, клетки в нем сохраняют жизнеспособность и пролиферативную активность на протяжении до 14 суток наблюдения и формируют развитую клеточную сеть с 3D структурой.
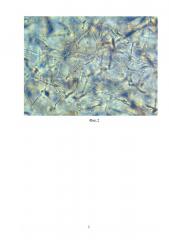
На Фиг. 2 показаны дермальные фибробласты человека в структуре биорезорбируемого клеточного скаффолда на основе фибрина плазмы крови (по п. 1), образование 3D клеточной сети, 5 сутки инкубации, световая микроскопия (x100).
На Фиг. 3. показаны дермальные фибробласты человека в структуре биорезорбируемого клеточного скаффолда на основе фибрина плазмы крови (по п. 2), образование 3D клеточной сети, 5 сутки инкубации, световая микроскопия (x100; фазовый контраст).
На Фиг. 4. показаны делящиеся мезенхимальные стромальные клетки в структуре биорезорбируемого клеточного скаффолда (по п. 2), 8 сутки инкубации (x200; фазовый контраст).
На Фиг. 5 показаны ядра дермальных фибробластов человека в толще биорезорбируемого клеточного скаффолда (по п. 2), 14 сутки эксперимента (x400; многофункциональный фотометр-имиджер Cytation 5; прижизненная окраска Hoechst 33342).
Пример 3
Распределение клеток по всей толще скаффолда подтверждается результатами гистологических исследований биорезорбируемого клеточного скаффолда.
На Фиг. 6 показан гистологический поперечный срез биорезорбируемого клеточного скаффолда (по п. 1), дермальные фибробласты человека распределены по всей толще (окраска гематоксилин-эозин, x100).
Способ создания биорезорбируемого клеточного скаффолда на основе фибрина плазмы крови, включающий смешивание плазмы крови или криопреципитата плазмы крови, обеспечивающих присутствие в скаффолде ростовых факторов, с раствором коллагена I типа, имеющим рН 7,4, введение суспензии животных клеток и добавление тромбин-кальциевой смеси в соотношении плазма крови или криопреципитат : раствор коллагена I типа с рН7,4 : суспензия животных клеток : тромбин-кальциевая смесь – 3,94 : 2,86 : 1 : 1,09 соответственно.