Реакционное средство, содержащее пористую подложку, пропитанную органическим соединением, способным образовывать газовые клатраты, и его использование для отделения и хранения со2
Иллюстрации
Показать всеИзобретение относится к реакционному средству, содержащему пористую подложку, на которую нанесено органическое соединение в твердой форме, способное образовывать газовые клатраты. Описано реакционное средство, содержащее пористую подложку, на поверхность и/или внутрь пор которой нанесено органическое соединение в твердой форме, выступающее в качестве молекулы-хозяина, образующей клатрат, отличающееся тем, что массовый процент нанесенного органического соединения составляет от 5% до 60% по массе в расчете на общую массу указанного реакционного средства, причем указанное органическое соединение выбрано из гидрохинона и его производных и фенола и его производных. Также описаны способ выделения СО2 из газовой смеси и реактор для выделения СО2 из газовой смеси. Технический результат: получено реакционное средство эффективное в отношении улавливания газов, в частности CO2. 4 н. и 12 з.п. ф-лы, 10 ил., 4 табл., 3 пр.
Реферат
Настоящее изобретение относится к реакционному средству, содержащему пористую подложку, пропитанную органическим соединением, способным образовывать газовые клатраты, к способам получения такого средства, а также его использованию, в частности, в промышленных методах разделения газов.
Природный газ в настоящее время представляет собой третий наиболее используемый во всем мире источник энергии после нефти и угля. В цепочке действий по обработке природного газа по экономическим или техническим причинам необходимо отделять присутствующие в нем загрязняющие вещества. Среди таких загрязняющих веществ CO2 является наиболее часто встречаемым веществом, которое, как правило, присутствует в потоке подлежащего обработке газа в наибольшей концентрации. В настоящее время существует много методов выделения CO2 из природного газа, такие как абсорбция за счет физических или гибридных химических растворителей, адсорбция на твердых частицах (адсорбентах), использование мембран и криогенных методов, в частности, как описано Rufford et al., Journal of Petroleum Science and Engineering, 2012, 94-95, 123-154. Указанные различные методы, тем не менее, имеют недостаток, заключающийся в высокой стоимости.
Для того чтобы уменьшить эту стоимость исследуются альтернативные способы выделения CO2, такие как, например, использование газовых клатратов. Газовый клатрат представляет собой комплекс включения, состоящий из нескольких молекул, где так называемые «молекулы-хозяева» формируют молекулярную клетку вокруг молекулы газа. В таких структурах молекулы-хозяева, таким образом, образуют открытую структуру с полостями или каналами, в которых физически захватываются, инкапсулируются атомы или молекулы газа, имеющие подходящий размер. Молекулы, заключенные в эти клетки, обозначаются как «приглашенные молекулы» («молекулы-гости»). Так как молекулярная сетка, формирующая клетку, стабилизируется слабыми связями типа водородных, то сформированные таким образом структуры также обозначаются аббревиатурой HOFs ("Hydrogen-bonded Organic Frameworks" или «Органическая Каркасная структура, связанная водородными связями»).
Молекулы, которые могут в присутствии молекул-гостей подходящего размера приводить к клатратам (или HOFs), должны иметь определенные характеристики, с тем чтобы позволить этим молекулам связываться друг с другом, образуя полости.
Такие молекулы-хозяева, создающие клатраты, должны, сперва, быть в состоянии сформировать между собой слабые связи типа водородной связи. В качестве примера можно назвать воду, которая может в определенных условиях образовать клатраты, обычно называемые «гидратами», одним из самых известных является клатрат, образуемый с метаном (гидрат метана). Органические молекулы-хозяева, образующие клатраты, также известны специалисту в данной области техники, и являются предметом многих исследований и научных публикаций.
В качестве примеров, но не ограничиваясь сказанным, можно упомянуть:
1. Гидрохинон и его производные
Замещение водорода в пара-положении фенола OH-группой приводит к гидрохинону (А) (семейство хинонов), модельного соединения, хорошо известного как склонного к формированию клатратов (Mak et al., Hydroquinone, Encyclopedia of Supramolecular Chemistry, Vol. 1, Editors J.L. Atwood и J.W. Steed, 2004, CRC Press, Taylor & Francis, pages 679-686).
Среди производных гидрохинона можно, в частности, упомянуть молекулы гидрохинона, в которых одна или две гидроксильные группы -ОН замещены тиольной группой -SH.
2. Фенол (В) и его производные
В частности, можно упомянуть:
В качестве производного фенола можно, в частности, упомянуть монозамещенные фенолы, такие как п-крезол, п-бромфенол, этилфенол, трет-бутилфенол, фенилфенол, п-фторфенол, м-фторфенол и о-фторфенол (MacNicol et al. Structure and design of inclusion compounds: the clathrate of hydroquinone, phenol, Dianin's compound and related systems, pages 1-45; J.L. Atwood, J.E.D. Davies, D.D. MacNicol, Inclusion compounds, Vol.2,1984, Academic Press Inc., London).
3. Мочевина (C)
См. также Harris et al., Urea inclusion compounds, Encyclopedia of Supramolecular Chemistry, Vol. 2, Editors J.L. Atwood and J.W. Steed, 2004, CRC Press, Taylor & Francis, pages 1538-1549.
4. Соединение Дианина (4-п-гидроксифенил-2,2,4-триметилхроман) (D)
См. также MacNicol et al., Structure and design of inclusion compounds: the clathrate of hydroquinone, phenol, Dianin's compound and related systems, pages 1-45, in J.L. Atwood, J.E.D. Davies, D.D. MacNicol, Inclusion compounds, Vol. 2, 1984, Academic Press Inc., London.
5. Производные соединения Дианина (D), где позиции R1, R2, R3 и R4 могут быть замещены, например, метильной группой (Me=-CH3):
где R2=R3=R4=Н; R1=Me, например (MacNicol et al., Structure and design of inclusion compounds: the clathrate of hydroquinone, phenol, Dianin's compound and related systems, pages 1-45 in J.L. Atwood, J.E.D. Davies, D.D. MacNicol, Inclusion compounds, Vol. 2, 1984, Academic Press Inc., London).
6. Производные (D), полученные замещением углеродов (C2) и (C4)
где R2=Н; R1=R3=Me, например (MacNicol et al., Structure and design of inclusion compounds: the clathrate of hydroquinone, phenol, Dianin's compound and related systems, pages 1-45 in J.L. Atwood, J.E.D. Davies, D.D. MacNicol, Inclusion compounds, Vol. 2, 1984, Academic Press Inc., London).
7. Производные (D), полученные изменением природы группы, ответственной за водородную связь
например, замещением ОН на SH:
(MacNicol. Structure and design of inclusion compounds: the clathrate of hydroquinone, phenol, Dianin's compound and related systems, pages 1-45 in J.L. Atwood, J.E.D. Davies, D.D. MacNicol., Inclusion compounds, Vol. 2, 1984, Academic Press Inc., London).
8. Хиназолинон (E)
где Z=O
2-фенил-3-п-(2,2,4-триметилхроман-4-ил)фенилхиназолин-4(3H)-он
См. также MacNicol et al., Structure and design of inclusion compounds: the clathrate of hydroquinone, phenol, Dianin's compound and related systems, pages 1-45 in J.L. Atwood, J.E.D. Davies, D.D. MacNicol, Inclusion compounds, Vol. 2, 1984, Academic Press Inc., London.
9. Соединения, полученные из указанных выше молекул, где кислород замещен серой или селеном:
- Пример 1: Производные (C)
См. также Takemoto et al., Inclusion compounds of urea, thiourea and selenourea, pages 48-67 in J.L. Atwood, J.E.D. Davies, D.D. MacNicol., Inclusion compounds, Vol.2, 1984, Academic Press Inc., London.
- Пример 2: Производные (D): 4-п-гидроксифенил-2,2,4-триметилтиахроман и 4-и-гидроксифенил-2,2,4-триметилселенхроман
4-п-гидроксифенил-2,2,4-триметилтиахроман
См. также. MacNicol et al., Structure and design of inclusion compounds: the clathrate of hydroquinone, phenol, Dianin's compound and related systems, pages 1-45 in J.L. Atwood, J.E.D. Davies, D.D. MacNicol, Inclusion compounds, Vol. 2, 1984, Academic Press Inc., London.
- Пример 3: Производные (E) от замещения кислорода серой
где Z=S
См. также MacNicol et al., Structure and design of inclusion compounds: the clathrate of hydroquinone, phenol, Dianin's compound and related systems, pages 1-45 in J.L. Atwood, J.E.D. Davies, D.D. MacNicol, Inclusion compounds, Vol. 2, 1984, Academic Press Inc., London.
10. Соединения, полученные из молекул выше, объединяющие нескольких модификаций, уже описанных выше: Например, модификация (D), касающаяся как ее гетероатома (замена кислорода на серу), так и заместителя кольца (замена водорода метилом)
где R2=R3=R4=Н; R1=Me
См. также MacNicol et al., Structure and design of inclusion compounds: the clathrate of hydroquinone, phenol, Dianin's compound and related systems, pages 1-45 in J.L. Atwood, J.E.D. Davies, D.D. MacNicol, Inclusion compounds, Vol. 2, 1984, Academic Press Inc., London.
Стоит отметить, что газовые гидраты, в которых молекулы-хозяева представляют собой молекулы воды, уже изучались в связи с улавливанием CO2. Тем не менее, использование газовых гидратов не дает возможность получить высокую селективность по отношению к CO2, например в том случае, когда CO2 отделяют от некоторых газовых смесей, например смеси CO2 и CH4. В самом деле, из-за близости кривых термодинамического равновесия гидратов CO2 и CH4, гидрат, который образуется, когда вода находится в контакте со смесью CO2/CH4 содержит значительное количество CH4, что делает применение этого метода для выделения CO2 невозможным в промышленном масштабе, как это описано Van Denderen et al., Industrial & Engineering Chemistry Research, 2009, 48, 5802-5807 and Ricaurte et al., Industrial & Engineering Chemistry Research, 2013, 52, 899-910.
С другой стороны, органические клатраты, в составе которых молекулы-хозяева представляют собой органические молекулы, являются селективными в отношении некоторых газов, таких как CO2, как показано Lee and Yoon, The Journal of Physical Chemistry, С 2011, 115, 22647-22651, and Lee et al., ChemPhysChem 2011, 12, 1-4, в случае органического клатрата гидрохинона. Однако гидрохинон, применяемый в этих исследованиях, является измельченным коммерческим твердым гидрохиноном, и этот тип обработки твердого вещества невозможно использовать в промышленном способе для обработки газа. Действительно, он имеет несколько недостатков, в частности потому, что это порошок кристаллов, площадь поверхности обмена газ/твердое вещество относительно невелика, и может иметь место блокировка контакторов и его использование приводит к образованию тонкодисперсных частиц. Кроме того, образование органических газовых клатратов требует особых условий давления и температуры, которые могут меняться в зависимости от среды, в которой они формируются.
Поэтому существует необходимость в системах, в составе которых можно получать органические газовые клатраты и которая может быть использована в промышленном процессе и имеет удовлетворительную эффективность в отношении захвата представляющих интерес газов, в частности посредством значительной площади поверхности обмена газ/твердое вещество.
Неожиданно, авторы настоящего изобретения обнаружили, что органические газовые клатраты можно сформировать внутри пористой подложки, на которую наносят органическое соединение, способное образовывать клатраты. Кроме того, неожиданно, авторы изобретения заметили, что эффективность улавливания газа, в частности CO2, полученного с использованием такой подложки, оказалась удовлетворительной.
В следующем далее тексте описания и в документе вообще под «органическим соединением(ями)» в контексте настоящего изобретения подразумевают органическое соединение(я), известное из уровня техники, в частности из литературы, которое способно выступать как молекулы-хозяева для образования клатрата, т.е. способны собираться вместе, чтобы сформировать газовые клатраты. Эти органические соединения могут быть, в частности, соединениями, упомянутыми выше.
Также, под термином «клатрат» понимают комплекс включения, состоящий из одного или нескольких молекул-хозяев, образующих молекулярную клетку (фиг. 1А). Термин «газовый клатрат» в таком случае означает узел, образованный молекулярной клеткой и молекулами газа, расположенными внутри клетки (фиг. 1B). Реакция улавливания молекул газа посредством клатрата описывается как «вовлечение в клатрат» («enclathration»), в то время как реакция освобождения молекулы газа газовым клатратом описывается как «извлечение из клатрата» («declathration»).
Кроме того, под термином «реакционное средство» подразумевается средство или система, способные взаимодействовать посредством химической реакции и/или физического и/или физико-химического процесса в условиях, когда они находятся в присутствии подходящих химических соединений.
Под термином «пористая подложка» подразумевается твердый материал, содержащий поры, на который может быть нанесено рассматриваемое соединение. Согласно изобретению, органическое соединение, способное образовывать газовые клатраты, осаждают на пористой подложке. Это органическое соединение придает средству по изобретению реактивность, по крайней мере отчасти благодаря своей способности образовывать газовые клатраты.
Таким образом, настоящее изобретение описывает реакционное средство, содержащее пористую подложку, на поверхность и/или внутри пор которой нанесено органическое соединение в твердой форме, выступающее в качестве молекулы-хозяина, образующей клатрат. В указанном средстве массовый процент указанного нанесенного органического соединения составляет от 5% до 60% по массе в расчете на общую массу указанного реакционного средства.
Указанное органическое соединение может быть, в частности, выбрано из гидрохинона и молекул гидрохинона, в котором одна или обе -OH группы замещены -SH; фенола, п-крезола, п-бромфенола, этилфенола, трет-бутилфенола, фенилфенола, п-фторфенола, м-фторфенола и о-фторфенола; соединения Дианина и его производных, в которых атомы кислорода замещены атомами серы; хиназолинона; мочевины, тио-мочевины, селеномочевины.
Подходящие пористые подложки, попадающие в объем настоящего изобретения, должны подходить для использования в промышленных процессах, в частности для разделения газа и, в частности, не должны разрушаться в условиях температуры и/или давления, используемых в этих процессах. Они должны иметь большую механическую прочность для того, чтобы избежать любых явлений (истирание и фрагментации), которые могут изменить размер подложки.
Предпочтительно пористую подложку выбирают из группы, состоящей из диоксида кремния, оксида алюминия, активированного угля, молекулярных сит и цеолитов.
Предпочтительно пористая подложка представляет собой диоксид кремния или оксид алюминия. Оксид алюминия может быть бета или гамма типа.
Гамма-оксид алюминия получают нагреванием гидроксидов алюминия при низкой температуре, и его также называют низкотемпературный переходный оксид алюминия; он кристаллизуется в соответствии со структурой шпинели с дефектами.
Бета-оксид алюминия представляет собой алюминат натрия, полученный на основе оксида алюминия Al2O3 и содержащий несколько процентов оксида натрия (Na2O) с очень небольшими количествами диоксида кремния и оксида железа. Особенностью этой структуры является его двумерная природа: кристалл выполнен с тонкими параллельными слоями плотного оксида алюминия, отделенными друг от друга редко расположенными плоскостями, в которых удерживаются ионы натрия.
Предпочтительно пористая подложка содержит поры с размером от 2 нм до 150 нм, предпочтительно от 20 нм до 120 нм.
Пористая подложка, например, содержит поры 50 нм или 100 нм.
В соответствии с одним вариантом осуществления размер пор пористой подложки является таким, что органическое соединение может быть нанесено в виде твердого вещества внутрь пор и образовывать в ней газовые клатраты, когда реакционное средство оказывается в присутствии газа.
Как правило, пористая подложка находится в виде пористых частиц, в частности со средним размером от 20 мкм до 5 мм, предпочтительно от 40 мкм до 700 мкм для способа с псевдоожиженном слоем, и от 1 мм до 5 мм для операций в неподвижном слое или в подвижном слое.
Как правило, используют шарики пористого материала, например шарики оксида кремния.
Выбор размера пористых частиц, как правило, зависит от желаемой области применения, и, следовательно, изменяется в соответствии со стадией промышленного способа, в которой желательно применить реакционное средство. Тем не менее эффективность улавливания газа часто улучшается с уменьшением размера частиц. Поэтому предпочтительно будут выбираться пористые частицы малого размера, например от 45 до 500 мкм.
В соответствии с одним вариантом осуществления изобретения пористая подложка имеет удельную площадь поверхности от 30 м2/г до 1000 м2/г.
При использовании пористой подложки, имеющей высокую удельную поверхность, площадь поверхности обмена газ/твердое вещество значительно увеличивается. Чем больше удельная площадь поверхности, тем больше увеличивается количество нанесенного органического соединения и тем больше становится количество сайтов захвата молекул газа, т.е. органических клатратов, что приводит к лучшей эффективности улавливания.
Как правило, массовое процентное содержание твердого нанесенного вещества составляет от 5% до 60%, предпочтительно от 10% до 30% по массе в расчете на общую массу указанного реакционного средства.
Массовая доля твердого нанесенного вещества может быть определена с помощью методов термогравиметрического анализа (ТГА) и методов дифференциальной сканирующей калориметрии (ДСК).
Для данного массового процентного содержания твердого нанесенного вещества толщина нанесенного вещества, как правило, зависит от среднего диаметра пор пористой подложки. Это нанесенное вещество должно быть достаточно толстым, чтобы газовый клатрат мог сформироваться, и достаточно тонким, чтобы избежать блокировки пор, что сократит доступ молекул газа к клатратам. В частном случае, в котором поры будут полностью заполнены твердым нанесенным веществом, молекулы газа будут иметь доступ только к области входа поверхности пор. Доступ к клатратам затем может быть возможен путем постепенной диффузии газа в заблокированные поры, что делает реакцию образования клатрата крайне медленной и неприменимой в промышленном процессе.
В соответствии с изобретением пористая подложка содержит твердое нанесенное вещество органического соединения, способное образовывать газовые клатраты.
В соответствии с одним вариантом осуществления органическое соединение выбирают из группы, состоящей из гидрохинона и его производных, фенола и его производных, соединений Дианина и его производных, хиназолинона и мочевины и ее производных.
Предпочтительно органическое соединение представляет собой гидрохинон и фенол.
В соответствии с одним конкретным вариантом осуществления указанное органическое соединение представляет собой гидрохинон. Последний образует клатраты, которые являются селективными в отношении некоторых газов, в частности CO2. Таким образом, его использование дает возможность получения реакционного средства, имеющего высокую селективность в отношении CO2, что позволяет легко отделить CO2 от газовой смеси, например смеси CO2/CH4 или CO2/H2.
Настоящее изобретение также относится к способу получения реакционного средства в соответствии с изобретением, включающему следующие стадии:
a) пропитку пористой подложки указанным органическим соединением, способным образовывать газовые клатраты в жидкой фазе, и
b) сушку полученной таким образом пропитанной пористой подложки.
Стадия a) состоит из пропитки пористой подложки раствором, содержащим органическое соединение, что приводит к получению пористой подложки, пропитанной органическим соединением в жидкой форме. Следующая затем стадия b) состоит из сушки пропитанной пористой подложки для получения твердого отложения органического соединения на поверхности и в порах подложки.
Стадию сушки b) осуществляют, например, в печи.
Как правило, пористую подложку, например шарики диоксида кремния, погружают в раствор, содержащий органическое соединение, а затем сушат в печи, для того чтобы получить тонкий слой твердого нанесенного вещества, покрывающего поры пористой подложки.
Стадии a) и b) способа, как определено выше, могут быть осуществлены в нескольких различных аппаратах (пропитка с помощью введения жидкости) или в одном аппарате.
В соответствии с альтернативным вариантом метод пропитки с помощью введения жидкости может дополнительно включать стадию фильтрации пористой подложки между стадией пропитки a) и стадией сушки b).
Указанная стадия фильтрации позволяет вдавливать избыток раствора, содержащего органическое соединение в пористую подложку, что дает возможность, после сушки, получать тонкий слой нанесенного органического соединения на пористой подложке.
В соответствии с одним вариантом осуществления растворитель раствора, содержащего органическое соединение, который может быть описан как «раствор для пропитки», представляет собой растворитель, в котором органическое соединение является стабильным и растворимым. Концентрация органического соединения в растворе для пропитывания и, следовательно, количество органического соединения, которое может быть нанесено на пористую подложку, как правило, зависят от природы растворителя.
В соответствии с одним вариантом осуществления органическое соединение представляет собой гидрохинон, применяемый в качестве спиртового раствора, насыщенного гидрохиноном.
Под «спиртовым раствором» подразумевается раствор, в котором растворитель представляет собой спирт, в частности этанол.
Настоящее изобретение также относится к реакционному средству, которое может быть получено по способу, описанному выше.
Объектом настоящего изобретения является также применение реакционного средства по настоящему изобретению для улавливания CO2.
Таким образом, согласно другому аспекту изобретения настоящее изобретение относится к способу выделения CO2 из газовой смеси, содержащей CO2 и по меньшей мере один газ, отличный от CO2; в указанном способе улавливание CO2 достигается за счет вовлечения газа в клатрат (enclathration) с помощью реакционного средства в соответствии с изобретением.
Способ по изобретению может быть периодическим, полунепрерывным или непрерывным.
Улавливание CO2 вовлечением в клатрат в реакционном средстве по изобретению имеет то преимущество, что оно является обратимым. Действительно, если осуществить извлечение газа из клатрата (declathration) в вакууме с целью выпустить газ из клатратов, эти клатраты могут затем снова уловить CO2, а это процесс, идентичный предыдущей реакции улавливания. В частности, реакция улавливания CO2 воспроизводима в том, что касается скорости реакции и количества уловленного газа. Реакционное средство по данному изобретению, таким образом, может быть использовано повторно, после его регенерации посредством извлечения газа из клатрата.
Настоящее изобретение также относится к использованию реакционного средства по настоящему изобретению для выделения CO2 из смеси газа, содержащей CO2 и по крайней мере один газ, отличный от CO2.
Как правило, реакционное средство по изобретению может быть использовано для выделения CO2 из смеси, содержащей CO2 и CH4, или CO2 и другие насыщенные газообразные углеводороды, или CO2 и N2, или же еще дополнительно многосоставных смесей, содержащих CO2, H2, CH4 и другие газообразные углеводороды.
Разделение особенно эффективно, когда используется реакционное средство, содержащее гидрохинон, поскольку реакция улавливания газа посредством клатратов гидрохинона гораздо более селективна по отношению к CO2, чем к CH4 или H2 (Lee et al., ChemPhysChem 2011, 12, 1-4).
Настоящее изобретение также относится к применению реакционного средства по настоящему изобретению для обработки природного газа, синтез-газа перед сгоранием или дымовых газов после сгорания.
Под «обработкой синтез-газа перед сгоранием» подразумевают обработку горючих материалов, таких как нефть и уголь, выше по технологическому потоку от стадии сжигания. Такая обработка состоит из отделения CO2 от смеси CO2/H2, так называемого «синтез-газа».
Под «обработкой дымового газа после сгорания» подразумевается обработка газовых выбросов после сжигания горючих материалов, таких как нефть и уголь, в воздухе. Такая обработка состоит из отделения CO2 от смеси CO2/N2, которая может содержать небольшую долю так называемых «захваченных» газов, таких как кислород, монооксид углерода (CO), оксиды серы (SOx) или оксиды азота (NOx).
Целью настоящего изобретения являются также различные применения, описанные выше в периодическом, полунепрерывном или непрерывном промышленном способе.
При периодическом режиме работы способ может быть осуществлен с помощью установки, включающий реактор или колонну, имеющую разделительные клапаны, средства для создания избыточного давления в реакторе, а также средства для регулирования давления, такие как, например, расширительный клапан или автоматический клапан, устройство регулирования давления, например датчик или манометр, средства нагревания и охлаждения, такие как, например, рубашка или внутренний теплообменник, устройство, предусматривающее измерение количество газа, поступающего в реактор, такое как, например, индикатор расхода, устройство для регистрации и управления реактором для того, чтобы проверять температуру и давление с течением времени. Реакционное средство сначала загружают в реактор, а затем вводят в контакт с подлежащим обработке газом в условиях надлежащих температуры и давления, так что органические молекулы, нанесенные на реакционное средство, образуют клатраты с газом, присутствующим в реакторе. Реакционное средство может подвергаться стадии подготовки или регенерации перед реакцией, например стадии нагревания или создания вакуума. Реакционное средство, применяемое в качестве реакционно-способных частиц, может быть неподвижным или находиться в движении в реакторе (например, ротационная корзина). Так как реакция вовлечения в клатрат происходит внутри средства, она изменяет состав первоначально введенного газа. После завершения реакции, все еще присутствующий газ продувают через один из клапанов реактора и рабочие условия в реакторе модифицируют таким образом, что газовый клатрат больше не был стабилен и мог высвободить газ, например путем увеличения температуры реактора или путем уменьшения давления. Таким образом, извлеченный газ имеет состав, отличный от исходного газа, например он имеет более высокое содержание CO2, чем в исходном газе. Другая рабочая альтернатива заключается в транспортировке реакционного средства после реакции в другое устройство, так называемый реактор или колонна диссоциации, для того, чтобы осуществить этап высвобождения газа. Такой периодический способ схематически показан на фиг. 4.
При полунепрерывном режиме работы способ чаще всего осуществляется с использованием нескольких отдельных сепараторов, работающих либо с неподвижным слоем или с псевдоожиженным слоем, по меньшей мере один из которых регенерируют, в то время как остальные работают, осуществляя реакцию. В соответствии с одним вариантом осуществления неподвижный слой является реактором или колонной, содержащими неподвижный слой свободно расположенных реакционно-способных частиц, через которые может циркулировать газ, тогда как внутри псевдоожиженного слоя, частицы находятся в движении с потоком газа, поступающего в реактор. Реактор с неподвижным слоем или с псевдоожиженным слоем включает те же элементы, что и для периодического режима работы, с добавлением устройства для подачи и отбора газа. Частицы имеют узкий размер гранул, но их средний размер может варьироваться от 40 микрон до 5 миллиметров в соответствии с проводимыми операциями. Перепад давления через слой часто является определяющим фактором в выборе размера гранулы, но производительность улавливания часто улучшается с уменьшением размера частиц. При адекватной схеме расстановки клапанов можно имитировать непрерывный способ. Например, на фиг. 5 пример иллюстрирует работу в двух колоннах с неподвижным слоем, одна из которых работает в фазе реакции, а другая находится в фазе регенерации. Фиг. 6 иллюстрирует функционирование в многоступенчатом псевдоожиженном слое, в котором подлежащий обработке газ последовательно пересекает несколько слоев псевдоожиженных частиц.
При непрерывном режиме работы твердые частицы и жидкость, как правило, циркулируют в противотоке. Реакционное средство регенерируют с захваченным потоком газа перед возвратом на рецикл (фиг. 7). Таким образом, весь блок включает в себя две секции: одну для улавливания, и одну для регенерации твердого вещества с рециклизацией. Контакт газ-твердое вещество происходит либо в подвижных слоях или дополнительно в многоступенчатых кипящих слоях с рециркуляцией твердого вещества между стадиями (фиг. 8).
Настоящее изобретение также относится к использованию реакционного средства по настоящему изобретению для хранения газа, такого как CH4, CO2 или дополнительно H2.
Действительно, интересующие газы могут быть захвачены реакцией вовлечения в клатрат внутри реакционного средства по настоящему изобретению и уловленные газы могут быть сохранены в нем. При необходимости, улавливаемые газы могут высвобождаться за счет реакции извлечения из клатрата.
В соответствии с другим аспектом настоящее изобретение также относится к способу обработки природного газа, синтез-газа перед сгоранием или дымовых газов после сжигания, включающему способ выделения CO2 по изобретению.
В соответствии с другим аспектом настоящее изобретение также относится к реактору для выделения CO2 из газовой смеси, состоящей из CO2 и по меньшей мере одного газа, отличного от CO2; где реактор включает:
- камеру,
- средство для приложения и поддержания в указанной камере определенного рабочего давления,
- средство для приложения и поддержания в указанной камере определенной рабочей температуры,
- средство для циркуляции указанной смеси газа через указанную камеру;
отличающемуся тем, что указанная камера содержит реакционное средство по изобретению, как определено ранее.
В соответствии с одним вариантом осуществления реактор работает с псевдоожиженным слоем.
В соответствии с другим вариантом осуществления указанный реактор работает с неподвижным слоем.
В соответствии с одним вариантом осуществления рабочее давление находится в диапазоне от 0 до 100 бар.
В соответствии с одним вариантом осуществления указанная рабочая температура составляет от 0 до 150°C. В самом деле, Lee and Yoon The Journal of Physical Chemistry, С 2011, 115, 22647-22651, и Lee et al., ChemPhysChem 2011, 12, 1-4, сообщили о режиме работы при низких температурах, таких как 0°C.
Стадия регенерации может быть проведена в вакууме (P=0) или при высокой температуре (обычно 150°C или ниже, причем следует понимать, что эта температура регенерации, как правило, меньше, чем температура разложения органического соединения, т.е. около 120°C для гидрохинона, около 40°C для фенола).
Изобретение будет более понятно при ознакомлении с нижеследующим описанием, которое приводится лишь в качестве примера и сопровождается ссылками на прилагаемые чертежи, где:
- Фиг. 1 показывает (А) пример гексагонального расположения органического клатрата типа 1, образованного молекулами гидрохинона и (В) пример газового органического клатрата, в котором сфера представляет собой молекулу газа;
- Фиг. 2 представляет собой график, представляющий массу в граммах (г) CO2, захваченного реакционным средством по изобретению, в зависимости от времени в минутах (мин) в течение двух последовательных циклов вовлечения в клатрат, первый цикл показан кружками и второй цикл - квадратами;
- Фиг. 3 представляет собой график, представляющий молярный состав газа (в мольных %) в зависимости от времени (в мин) в течение двух последовательных формирований, когда реакционное средством по изобретению помещают в присутствии смеси CO2/N2 с начальным составом, соответствующим 49,9 мол. % CO2. Кружочки и треугольники соответствуют концентрации CO2 в газе в течение первого и второго формирования, соответственно. Квадраты и кресты соответствуют концентрации N2 в газе в течение первого и второго формирования, соответственно.
- Фиг. 4 схематически иллюстрирует периодический способ по изобретению.
- Фиг. 5, 6, 7 и 8 иллюстрируют различные типы способов по изобретению: (5) - полунепрерывный, (6) - полунепрерывный в многостадийном псевдоожиженном слое, (7) - непрерывный, (8) - непрерывный в псевдоожиженном слое.
- Фиг. 9 и 10 иллюстрируют спектры Рамана реакционного средства до и после эксперимента 3 в таблице 4 ниже, соответственно.
ПРИМЕРЫ
Пример 1: Получение реакционного средства по изобретению.
Реакционное средство по изобретению было получено путем пропитки пористых частиц спиртовым раствором насыщенным органическим соединением.
Пористая подложка состоит из диоксида кремния, оксида алюминия или активированного угля. Пропитку осуществили путем погружения пористой подложки в спиртовой раствор, насыщенный органическим соединением, и подложку затем сушат в печи.
Проводили анализы методом ATG/DSC.
Приведенные ниже таблицы обобщают различные испытания, проведенные с различными подложками и органическими соединениями.
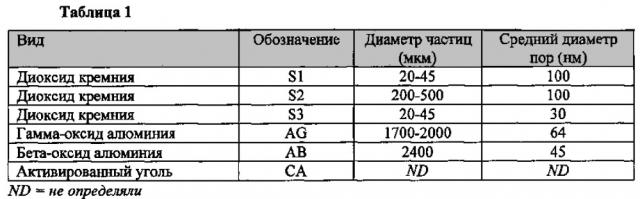
Характеристики первичных подложек, используемых в качестве пористой подложки, приведены в таблице 1:
Характеристики органических соединений, используемых в качестве молекул-хозяев, приведены в таблице 2:
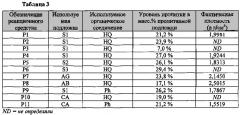
Характеристики полученного реакционного средства, приведены в таблице 3:
Пример 2: Использование реакционного средства по настоящему изобретению для улавливания CO2.
Реакционно-способное средство, полученное в примере 1, испытывали в присутствии чистого CO2.
Эксперименты проводились с использованием весов с магнитной подвеской марки RUBOTHERM, чтобы очень точно измерить массу газа, вступающего в реакцию с органическим соединением (с точностью до 10-5 г). Соответствующий аппарат описан Casas et al., 10th European Symposium on Thermal Analysis and Calorimetry (ESTAC), August 22-27, 2010, Rotterdam, The Netherlands.
Независимые эксперименты проводили при различных давлениях чистого CO2 и при различных температурах, где в каждом эксперименте выполняли два цикла вовлечения в клатрат-извлечения из клатрата. Эксперименты показали, что реакционное средство по изобретению улавливает CO2, что процесс улавливания является обратимым (после стадии извлечения из клатрата газа в вакууме следующая стадия вовлечения в клатрат газа происходит точно так же, как и предыдущая стадия), и что эксперименты прекрасно воспроизводимы в отношении скорости реакции и количества захваченного газа (фиг. 2).
Рабочие условия и полученные результаты приведены в таблице 4 (смотри ниже).
Пример 3: Использование реакционного средства по настоящему изобретению для выделения CO2 из смеси CO2/N2.
Реакционное средство получали в соответствии с той же процедурой, что и описанная в примере 1. Проведенный анализ дал возможность измерить, что количество гидрохинона, присутствующего в этом реакционном средстве, было равно 27% по массе.
Реакционное средство массой 66 г в виде частицы вводили в реактор, работающий в периодическом режиме, со ссылкой на уже описанные выше рабочие режимы. Реактор установлен на температуру 25°C с использованием его рубашки, в которой циркулирует жидкий теплоноситель. Температура в реакторе измеряется с помощью датчика PT100. Затем частицы вводят в контакт с газом, содержащим 49,9 мол. % CO2 путем загрузки в реактор при давлении 35 бар с помощью расширительного клапана и регулирования давления с помощью датчика давления, размещенного на реакторе. Давление и температура в зависимости от времени регистрируются системой сбора данных, подключенной к компьютеру, на частоте 1 Гц. Технические детали установки приведены в et al., Chemical Engineering Science, 2012, 82, 1-13. Реактор затем изолируют путем закрытия клапана подачи и изменение зависимости от времени состава газа, присутствующего в реакторе, отслеживают in situ с помощью газовой хроматографии. Осуществляли два последовательных формирования, причем между двумя формированиями присутствовала стадия для регенерации частиц, осуществляемая в течение 48 ч в вакууме. Фиг. 3 показывает, что состав газа действительно менялся с течением времени в отношении мольной доли CO2, которая уменьшалась, и мольной доли азота, которая увеличивалась. В конце эксперимента концентрация CO2 снижалась с 9,8% и 9,5% в первом и втором эксперименте, соответственно. Эти результаты, которые зависят от количества реакционного средства, введенного первоначально, воспроизводимы на двух полученных образованиях. Это показывает, что имеет место реакция вовлечения в клатрат, что эта реакция является селективной по отношению к CO2, и что реакция осуществляется с относительно быстрой кинетикой (менее, чем один час до достижения конечной концентрации).