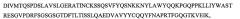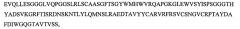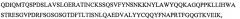Новые антитела к фосфорилхолину
Иллюстрации
Показать всеНастоящее изобретение относится к области иммунологии. Предложены антитело и фрагмент антитела, способные к связыванию с фосфорилхолином и/или конъюгатом фосфорилхолина. Также рассмотрена фармацевтическая композиция, нуклеиновая кислота, кодирующая антитело или его фрагмент, экспрессирующий вектор, клетка-хозяин и способ получения антитела или фрагмента антитела. Кроме того, описан способ приготовления варианта антитела, способного связываться с фосфорилином и/или конъюгатом фосфорилхолина, или фрагмента такого антитела. Данное изобретение может найти дальнейшее применение в терапии различных состояний, в частности, сердечно-сосудистых заболеваний и болезни Альцгеймера. 7 н. и 9 з.п. ф-лы, 7 ил., 5 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к новым антителам, связывающимся с фосфорилхолином (ФХ) и/или конъюгатами ФХ, и обладающим удивительно эффективными свойствами in vivo.
Предшествующий уровень техники
Перечисление или обсуждение в данном описании документа, явно опубликованного ранее, не обязательно является подтверждением того, что данный документ является частью существующего уровня техники или относится к общеизвестным знаниям.
Несмотря на доступные способы лечения сердечно-сосудистых заболеваний, острый коронарный синдром (ОКС) является главной причиной смерти в промышленно-развитых странах. ОКС происходит в результате образования тромба в полости коронарной артерии, что связано с хроническим воспалением стенки артерии. Воспаление артерии начинается с образования липидного ядра и инфильтрации воспалительных клеток, что приводит к образованию бляшки. Нестабильные бляшки содержат по существу некротизированное ядро и апоптотические клетки, разрушающие эндотелий и способные приводить к разрыву бляшки с обнажением подлежащего коллагена, фактора Виллебранда (фВ), тканевого фактора, липидов, и гладких мышц, обеспечивающих инициацию адгезии, активации и агрегации тромбоцитов (Libby et al. 1996. Macrophages and atherosclerotic plaque stability. Curr Opin Lipidol 7, 330-335 («Макрофаги и стабильность атеросклеротической бляшки»)). ОКС лечат с применением комбинации антитромбоцитарных средств, медикаментов для снижения холестерина (например, статинов), антикоагулянтов, а также хирургической реканализации посредством чрескожной коронарной ангиопластики (ЧКА) и имплантации стентов.
Антитромбоцитарные средства, такие как ингибиторы ЦОГ-1 (циклооксигеназы-1) (например, аспирин), антагонисты рецептора АДФ (например, тиклопедин и клопидогрел) и антагонисты гликопротеиновых рецепторов IIb/IIIa, как было показано, снижают частоту тяжелых сердечных приступов (ТСП) в ряде различных клинических испытаний (Dupont et al., 2009. ʺAntiplatelet therapies and the role of antiplatelet resistance in acute coronary syndromeʺ. Thromb Res 124, 6-13 («Антитромбоцитарная терапия и роль антитромбоцитарной резистентности при остром коронарном синдроме»)). Однако у части пациентов при долговременной антитромбоцитарной терапии продолжаются сердечно-сосудистые приступы. Далее, хроническая профилактическая терапия может занимать до двух лет, прежде чем будут достигнуты максимальные благоприятные эффекты, и многие пациенты подвержены высокому риску рецидива заболевания. Имеется период вплоть до 6-12 месяцев после инфаркта миокарда, когда пациент подвержен последующим тяжелым сердечным приступам, часто из-за повторной окклюзии, обусловленной рестенозом (Tabas. 2010. Macrophage death and defective inflammation resolution in atherosclerosis. Nat Rev Immunol 10, 36-46 («Гибель макрофагов и дефектное разрешение воспаления при атеросклерозе»)).
Соответственно, имеется существенная потребность в средствах лечения, направленных специально на профилактику дальнейшего прогрессирования развития бляшки и стимуляцию регрессии бляшки, позволяющую существенно уменьшить приступы во время этого периода.
Фосфорилхолин, группа полярной головки на некоторых фосфолипидах, играет существенную роль в сердечно-сосудистых заболеваниях. Активные формы кислорода, образуемые при коронарном воспалении, вызывают окисление липопротеина низкой плотности (ЛПНП) с образованием окисленного ЛПНП (оЛПНП). Фактически, сердечнососудистые заболевания (ССЗ), такие как атеросклероз, нестабильная стенокардия, или острый коронарный синдром, как было показано, связаны с повышенными уровнями о ЛПНП в плазме крови (Itabe and Ueda. 2007. Measurement of plasma oxidized low-density lipoprotein and its clinical implications. J Atheroscler Thromb 14, 1-11 («Измерение уровня окисленного липопротеина низкой плотности в плазме и его клиническое значение»)). ЛПНП является циркулирующей липопротеиновой частицей, содержащей липиды с ФХ группой полярной головки и белок апо-В100.
При окислении ЛПНП образуются ФХ-содержащие нео-эпитопы, не присутствующие в немодифицированном ЛПНП. Вновь экспонированный ФХ на оЛПНП распознается фагоцитарными рецепторами на макрофагах, такими как CD36, и образовавшийся о ЛПНП, поглощенный макрофагом, приводит к образованию провоспалительных пенистых клеток в стенке сосуда. Окисленный ЛПНП также распознается рецепторами на поверхности эндотелиальных клеток, и как отмечалось, стимулирует ряд ответов, включая эндотелиальную дисфункцию, апоптоз, и реакцию на несвернутые белки (Gora et al. 2010. Phospholipolyzed LDL induces an inflammatory response in endothelial cells through endoplasmic reticulum stress signaling. FASEB J 24(9):3284-97 («Фосфолиполизированный ЛПНП индуцирует воспалительный ответ в эндотелиальных клетках посредством передачи стрессовых сигналов через эндоплазматический ретикулум»)). ФХ нео-эпитопы также экспонируются на ЛПНП после модификации фосфолипазой А2 или аминовыми активными метаболитами заболеваний, такими как альдегиды, образуемые при окислении гликозилированных белков. Эти поочередно измененные частицы ЛПНП также являются провоспалительными факторами ССЗ.
Было показано, что антитела к фосфорилхолину (ФХ) связываются с окисленным или иным образом модифицированным ЛПНП и блокируют провоспалительную активность оЛПНП в исследованиях in vitro или на моделях in vivo (Shaw et al. 2000. Natural antibodies with the T15 idiotype may act in atherosclerosis, apoptotic clearance, and protective immunity. J Clin Invest 105, 1731-1740 («Натуральные антитела с T15 идиотипом могут действовать при атеросклерозе, апоптотическом расщеплении, и защитном иммунитете»); Shaw et al. 2001. Human-derived anti-oxidized LDL autoantibody blocks uptake of oxidized LDL by macrophages and localizes to atherosclerotic lesions in vivo. Arterioscler Thromb Vase Biol 21, 1333-1339 («Человеческие антитела к окисленным ЛПНП блокируют поглощение окисленных ЛПНП макрофагами и локализованы в атеросклеротических поражениях in vivo»)).
Далее, исследование клинических данных показало, что низкие уровни натуральных IgM анти-ФХ антител связаны с повышенным риском ТСП у больных с ОКС (Frostegard, J. 2010. Low level natural antibodies against phosphorylcholine: a novel risk market and potential mechanism in atherosclerosis and cardiovascular disease. Clin Immunol 134, 47-54 («Низкий уровень натуральных антител к фосфорилхолину: новый маркер риска и потенциальный механизм атеросклероза и сердечно-сосудистого заболевания»)).
Соответственно, имеется потребность в молекулах анти-ФХ антител, которые можно эффективно применять в терапии, в частности, полных человеческих анти-ФХ антителах, пригодных для лечения человека. Как известно авторам заявки, на сегодняшний день известный уровень техники не позволяет обеспечить терапевтически эффективные человеческие анти-ФХ антитела. Идентификация таких антител затруднена тем фактом, что способы скрининга человеческих антител с анти-ФХ-связывающей активностью in vitro плохо обеспечивают прогноз терапевтической активности in vivo.
С учетом этого, в данной области техники имеется потребность в молекулах человеческих анти-ФХ антител, обладающих эффективными и выгодными свойствами при использовании в системах in vivo, в частности, при использовании в лечении у человека.
Описание изобретения
Настоящая заявка описывает получение и анализ новых антител и фрагментов антител, содержащих новые антигенсвязывающие участки, способные связывать фосфорилхолин и/или конъюгаты фосфорилхолина.
В первом аспекте настоящее изобретение обеспечивает антитело или фрагмент антитела, способный связываться с фосфорилхолином и/или конъюгатом фосфорилхолина, где антитело или фрагмент антитела содержит вариабельный домен тяжелой цепи (VH) и/или вариабельный домен легкой цепи (VL), и где:
(a) VH домен содержит аминокислотную последовательность, включающую один, два, или предпочтительно три гипервариабельных участка (CDR), выбранных из группы, состоящей из:
- последовательности CDR1, содержащей аминокислотную последовательность, обладающую по меньшей мере 25%, 50%, 75% или 100%-ной идентичностью с последовательностью SEQ ID NO: 17;
- последовательности CDR2, содержащей аминокислотную последовательность, обладающую по меньшей мере 5%, 11%, 17%, 23%, 29%, 35%, 47%, 52%, 58%, 64%, 70%, 76%, 82%, 94% или 100%-ной идентичностью с последовательностью SEQ ID NO: 18; и
- последовательности CDR3, содержащей аминокислотную последовательность, обладающую по меньшей мере 4%, 9%, 13%, 18%, 22%, 27%, 31%, 36%, 40%, 45%, 50%, 54%, 59%, 63%, 68%, 72%, 77%, 81%, 86%, 90%, 95% или 100%-ной идентичностью с последовательностью SEQ ID NO: 19. 20, 21 или 22; и/или
(b) VL домен содержит аминокислотную последовательность, включающую один, два, или предпочтительно три гипервариабельных участка (CDR), выбранных из группы, состоящей из:
- последовательности CDR4, содержащей аминокислотную последовательность, обладающую по меньшей мере 5%, 11%, 17%, 23%, 29%, 35%, 47%, 52%, 58%, 64%, 70%, 76%, 82%, 94% или 100%-ной идентичностью с последовательностью SEQ ID NO: 23 или 24;
- последовательности CDR5, содержащей аминокислотную последовательность, обладающую по меньшей мере 14%, 28%, 42%, 57%, 71%, 85% или 100%-ной идентичностью с последовательностью SEQ ID NO: 25;
- последовательности CDR6, содержащей аминокислотную последовательность, обладающую по меньшей мере 11%, 22%, 33%, 44%, 55%, 66%, 77%, 88% или 100%-ной идентичностью с последовательностью SEQ ID NO: 26.
В одном варианте осуществления в соответствии с первым аспектом настоящего изобретения, антитело или фрагмент антитела содержит VH домен, включающий аминокислотную последовательность, содержащую последовательность CDR1, последовательность CDR2 и CDR3, как указано выше, и/или VL домен, включающий аминокислотную последовательность, содержащую последовательность CDR4, последовательность CDR5 и CDR6, как указано выше.
В другом варианте осуществления первого аспекта настоящего изобретения, антитело или фрагмент антитела включает:
- VH домен, содержащий аминокислотную последовательность, включающую все три из последовательностей CDR1, CDR2 и CDR3, присутствующие в аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 1, 3, 5, 7, 9, 11, 13 или 15, или аминокислотной последовательности, обладающей по меньшей мере 80%, 85%, 90% или 95%-ной идентичностью с аминокислотной последовательностью из любой из SEQ ID NO: 1, 3, 5, 7, 9, 11, 13 или 15; и/или
- VL домен, содержащий аминокислотную последовательность, включающую все три из последовательностей CDR4, CDR5 и CDR6, присутствующие в аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 2, 4, 6, 8, 10, 12, 14 или 16, или аминокислотной последовательности, обладающей по меньшей мере 80%, 85%, 90% или 95%-ной идентичностью с аминокислотной последовательностью из любой из SEQ ID NO: 2, 4, 6, 8, 10, 12, 14 или 16.
В другом варианте осуществления первого аспекта настоящего изобретения антитело или фрагмент антитела включает вариабельный домен тяжелой цепи (VH) и/или вариабельный домен легкой цепи (VL), где:
- VH домен содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1, 3, 5, 7, 9, 11, 13 или 15, или аминокислотную последовательность, обладающую по меньшей мере 50%, 60%, 70%, 80%, 85%, 90% или 95%-ной идентичностью аминокислотной последовательности к любой из SEQ ID NO: 1, 3, 5, 7, 9, 11, или 15; и
- VL домен содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 2, 4, 6, 8, 10, 12, 14 или 16, или аминокислотную последовательность, обладающей по меньшей мере 50%, 60%, 70%, 80%, 85%, 90% или 95%-ной идентичностью аминокислотной последовательности к любой из SEQ ID NO: 2, 4, 6, 8, 10, 12, 14 или 16.
SEQ ID NO: 1 является вариабельным доменом тяжелой цепи (VH) антитела X19-А05, как описано в следующих примерах, и имеет последовательность:
и включает гипервариабельные участки (CDR):
VH CDR1: GYWM (SEQ ID NO: 17);
VH CDR2: YISPSGGGTHYADSVKG (SEQ ID NO: 18);
VH CDR3: VRFRSVCSNAVCRPTAYDAFDI (SEQ ID NO: 19).
SEQ ID NO: 2 является вариабельным доменом легкой цепи (VL) антитела Х19-А05, и имеет последовательность:
и включает гипервариабельные участки (CDR):
VL CDR4: KSSQSVFYQSNKKNYLA (SEQ ID NO: 23);
VL CDR5: WASTRES (SEQ ID NO: 25);
VL CDR6: QQYFNAPRT (SEQ ID NO: 26).
SEQ ID NO: 3 является вариабельным доменом тяжелой цепи (VH) антитела М99-В05, как описано в следующих примерах, и имеет последовательность:
и включает гипервариабельные участки (CDR):
VH CDR1: GYWM (SEQ ID NO: 17);
VH CDR2: YISPSGGGTHYADSVKG (SEQ ID NO: 18);
VH CDR3: VRFRSVCSNGVCRPTAYDAFDI (SEQ ID NO: 20),
SEQ ID NO: 4 является вариабельным доменом легкой цепи (VL) антитела М99-В05, и имеет последовательность:
и включает гипервариабельные участки (CDR):
VL CDR4: KSSQSVFYNSNKKNYLA (SEQ ID NO: 24);
VL CDR5: WASTRES (SEQ ID NO: 25);
VL CDR6: QQYFNAPRT (SEQ ID NO: 26),
SEQ ID NO: 5 является вариабельным доменом тяжелой цепи (VH) антитела X19-А01, как описано в следующих примерах, и имеет последовательность:
и включает гипервариабельные участки (CDR):
VH CDR1: GYWM (SEQ ID NO: 17);
VH CDR2: YISPSGGGTHYADSVKG (SEQ ID NO: 18);
VH CDR3: VRFRSVCSNGVCRPTAYDAFDI (SEQ ID NO: 20).
SEQ ID NO: 6 является вариабельным доменом легкой цепи (VL) антитела Х19-А01, и имеет последовательность:
и включает гипервариабельные участки (CDR):
VL CDR4: KSSQSVFYNSNKKNYLA (SEQ ID NO: 24);
VL CDR5: WASTRES (SEQ ID NO: 25);
VL CDR6: QQYFNAPRT (SEQ ID NO: 26),
SEQ ID NO: 7 является вариабельным доменом тяжелой цепи (VH) антитела X19-А03, как описано в следующих примерах, и имеет последовательность:
и включает гипервариабельные участки (CDR):
VH CDR1: GYWM (SEQ ID NO: 17);
VH CDR2: YISPSGGGTHYADSVKG (SEQ ID NO: 18);
VH CDR3: VRFRSVCSNAVCRPTAYDAFDI (SEQ ID NO: 19).
SEQ ID NO: 8 является вариабельным доменом легкой цепи (VL) антитела Х19-А03, и имеет последовательность:
и включает гипервариабельные участки (CDR):
VL CDR4: KSSQSVFYQSNKKNYLA (SEQ ID NO: 23);
VLCDR5: WASTRES (SEQ ID NO: 25);
VL CDR6: QQYFNAPRT (SEQ ID NO: 26).
SEQ ID NO: 9 является вариабельным доменом тяжелой цепи (VH) антитела X19-А07, как описано в следующих примерах, и имеет последовательность:
и включает гипервариабельные участки (CDR):
VH CDR1: GYWM (SEQ ID NO: 17);
VH CDR2: YISPSGGGTHYADSVKG (SEQ ID NO: 18);
VH CDR3: VRFRSVCSNGVCRPTAYDAFDI (SEQ ID NO: 20),
SEQ ID NO: 10 является вариабельным доменом легкой цепи (VL) антитела X19-А07, и имеет последовательность:
и включает гипервариабельные участки (CDR):
VL CDR4: KSSQSVFYNSNKKNYLA (SEQ ID NO: 24);
VL CDR5: WASTRES (SEQ ID NO: 25);
VL CDR6: QQYFNAPRT (SEQ ID NO: 26).
SEQ ID NO: 11 является вариабельным доменом тяжелой цепи (VH) антитела X19-А09, как описано в следующих примерах, и имеет последовательность:
и включает гипервариабельные участки (CDR):
VH CDR1: GYWM (SEQ ID NO: 17);
VH CDR2: YISPSGGGTHYADSVKG (SEQ ID NO: 18);
VH CDR3: VRFRSVCSNGVCRPTAYDAFDI (SEQ ID NO: 20),
SEQ ID NO: 12 является вариабельным доменом легкой цепи (VL) антитела X19-А09, и имеет последовательность:
и включает гипервариабельные участки (CDR):
VL CDR4: KSSQSVFYNSNKKNYLA (SEQ ID NO: 24);
VLCDR5: WASTRES (SEQ ID NO: 25);
VL CDR6: QQYFNAPRT (SEQ ID NO: 26),
SEQ ID NO: 13 является вариабельным доменом тяжелой цепи (VH) антитела X19-А11, как описано в следующих примерах, и имеет последовательность:
и включает гипервариабельные участки (CDR):
VH CDR1: GYWM (SEQ ID NO: 17);
VH CDR2: YISPSGGGTHYADSVKG (SEQ ID NO: 18);
VH CDR3: VRFRSVSSNGVSRPTAYDAFDI (SEQ ID NO: 21).
SEQ ID NO: 14 является вариабельным доменом легкой цепи (VL) антитела X19-A11, и имеет последовательность:
и включает гипервариабельные участки (CDR):
VL CDR4: KSSQSVFYNSNKKNYLA (SEQID NO: 24);
VL CDR5: WASTRES (SEQ ID NO: 25);
VL CDR6: QQYFNAPRT (SEQ ID NO: 26).
SEQ ID NO: 15 является вариабельным доменом тяжелой цепи (VH) антитела X19-С01, как описано в следующих примерах, и имеет последовательность:
и включает гипервариабельные участки (CDR):
VH CDR1: GYWM (SEQ ID NO: 17);
VH CDR2: YISPSGGGTHYADSVKG (SEQ ID NO: 18);
VH CDR3: VRFRSVSSNAVSRPTAYDAFDI (SEQ ID NO: 22).
SEQ ID NO: 16 является вариабельным доменом легкой цепи (VL) антитела X19-С01, и имеет последовательность:
и включает гипервариабельные участки (CDR):
VL CDR4: KSSQSVFYQSNKKNYLA (SEQ ID NO: 23);
VL CDR5: WASTRES (SEQ ID NO: 25);
VL CDR6: QQYFNAPRT (SEQ ID NO: 26).
Итоговая сводка SEQ ID NO, как определено выше, показана далее:
В другом варианте осуществления первого аспекта изобретения, антитело или фрагмент антитела основаны на VH и/или VL доменах Х19-А05 антитела, и таким образом:
VH домен (i) содержит аминокислотную последовательность, обладающую по меньшей мере 80%, 85%, 90%, 95% или 100%-ной идентичностью с последовательностью SEQ ID NO: 1 и/или (ii) содержит CDR1 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 25%, 50%, 75% или 100%-ной идентичностью с последовательностью SEQ ID NO: 17; CDR2 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 5%, 11%, 17%, 23%, 29%, 35%, 47%, 52%, 58%, 64%, 70%, 76%, 82%, 94% или 100%-ной идентичностью с последовательностью SEQ ID NO: 18; и CDR3 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 4%, 9%, 13%, 18%, 22%, 27%, 31%, 36%, 40%, 45%, 50%, 54%, 59%, 63%, 68%, 72%, 77%, 81%, 86%, 90%, 95% или 100%-ной идентичностью с последовательностью SEQ ID NO: 19; и/или
- VL домен (iii) содержит аминокислотную последовательность, обладающую по меньшей мере 80%, 85%, 90%, 95% или 100%-ной идентичностью с последовательностью SEQ ID NO: 2, и/или (iv) содержит CDR4 последовательность, включающую аминокислотную последовательность, обладающую по меньшей мере 5%, 11%, 17%, 23%, 29%, 35%, 47%, 52%, 58%, 64%, 70%, 76%, 82%, 94% или 100%-ной идентичностью с последовательностью SEQ ID NO: 23; CDR5 последовательность, включающую аминокислотную последовательность, обладающую по меньшей мере 14%, 28%, 42%, 57%, 71%, 85% или 100%-ной идентичностью с последовательностью SEQ ID NO: 25; и CDR6 последовательность, включающую аминокислотную последовательность, обладающую по меньшей мере 11%, 22%, 33%, 44%, 55%, 66%, 77%, 88% или 100%-ной идентичностью с последовательностью SEQ ID NO: 26. Может быть предпочтительно, чтобы VH домен содержал последовательность SEQ ID NO: 1, a VL домен содержал последовательность SEQ ID NO: 2.
Антитело или фрагмент антитела из данного варианта осуществления может дополнительно содержать константную область тяжелой цепи (СН) или ее фрагмент, где фрагмент может содержать, например, по меньшей мере 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 120, 140, 160, 180, 200, 220, 240, 260, 280, 300, 320 или больше аминокислот в СН области. СН область или ее фрагмент могут быть соединены с VH доменом. Не имеется конкретного ограничения СН области, хотя в одном варианте осуществления она является человеческой СН областью. В данной области техники имеется много примеров человеческих СН областей. Примерные человеческие СН области для применения в данном контексте включают:
SEQ ID NO: 27 является СН областью М99-В05, и имеет последовательность СН области человеческого IgGl (UniProtKB/Swiss-Prot: P01857,1). SEQ ID NO: 28 является СН областью Х19-А05. SEQ ID NO: 28 отличается от SEQ ID NO: 27 по удаленному терминальному К (Lys) в СН области SEQ ID NO: 28, что позволяет снизить или устранить возможность разрушения пептидазами.
Антитело или фрагмент антитела из данного варианта осуществления может в дополнение или альтернативно содержать константную область легкой цепи (CL) или ее фрагмент, который может содержать, например, по мере 10, 20, 30, 40, 50, 60, 70, 80, 90, 100 или больше аминокислот из CL области. CL область или ее фрагмент могут быть соединены с VL доменом. Не имеется конкретных ограничений CL области, хотя в одном варианте осуществления она является человеческой CL областью. В данной области техники имеется много примеров человеческих CL областей. Примерная человеческая CL область для применения в настоящем изобретении включает:
SEQ ID NO: 29 является CL областью M99-B05 и Х19-А05, и имеет последовательность CL области человеческой каппа цепи (UniProtKB/Swiss-Prot: Р01834Д).
В соответствии с настоящим вариантом осуществления может быть предпочтительно, чтобы VH домен содержал последовательность из SEQ ID NO: 1, связанную с СН областью SEQ ID NO: 28, a VL домен содержал последовательность из SEQ ID NO: 2, связанную с CL областью из SEQ ID NO: 29.
В другом варианте осуществления первого аспекта настоящего изобретения антитело или фрагмент антитела основаны на VH и/или VL доменах антитела М99-В05, и таким образом:
- VH домен (i) содержит аминокислотную последовательность, обладающую примерно 80%, 85%, 90%, 95% или 100%-ной идентичностью с последовательностью SEQ ID NO: 3 и/или (ii) содержит CDR1 последовательность, содержащей аминокислотную последовательность, обладающую по меньшей мере 25%, 50%, 75% или 100%-ной идентичностью с последовательностью SEQ ID NO: 17; CDR2 последовательность, включающую аминокислотную последовательность, обладающую по меньшей мере 5%, 11%, 17%, 23%, 29%, 35%, 47%, 52%, 58%, 64%, 70%, 76%, 82%, 94% или 100%-ной идентичностью с последовательностью SEQ ID NO: 18; и CDR3 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 4%, 9%, 13%, 18%, 22%, 27%, 31%, 36%, 40%, 45%, 50%, 54%, 59%, 63%, 68%, 72%, 77%, 81%, 86%, 90%, 95% или 100%-ной идентичностью с последовательностью SEQ ID NO: 20; и/или
- VL домен (iii) содержит аминокислотную последовательность, обладающую по меньшей мере 80%, 85%, 90%, 95% или 100%-ной идентичностью с последовательностью SEQ ID NO: 4 и/или (iv) содержит CDR4 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 5%, 11%, 17%, 23%, 29%, 35%, 47%, 52%, 58%, 64%, 70%, 76%, 82%, 94% или 100%-ной идентичностью с последовательностью SEQ ID NO: 24, CDR5 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 14%, 28%, 42%, 57%, 71%, 85% или 100%-ной идентичностью с последовательностью SEQ ID NO: 25, и CDR6 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 11%, 22%, 33%, 44%, 55%, 66%, 77%, 88% или 100%-ной идентичностью с последовательностью SEQ ID NO: 26. Может быть предпочтительно, чтобы VH домен содержал последовательность из SEQ ID NO: 3, a VL домен содержал последовательность из SEQ ID NO: 4.
Антитело или фрагмент антитела из данного варианта осуществления может дополнительно содержать константную область тяжелой цепи (СН) или ее фрагмент, где фрагмент может содержать, например, по меньшей мере 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 120, 140, 160, 180, 200, 220, 240, 260, 280, 300, 320 или больше аминокислот из СН области. СН область или ее фрагмент могут быть соединены с VH областью. Нет конкретного ограничения для СН области, хотя в одном варианте осуществления она является человеческой СН областью. В данной области техники имеется много примеров человеческих СН областей. Примерные человеческие СН области для применения в данном контексте включают SEQ ID NO: 27 и SEQ ID NO: 28.
Антитело или фрагмент антитела из данного варианта осуществления могут в дополнение или альтернативно дополнительно содержать константную область легкой цепи (CL) или ее фрагмент, где фрагмент может включать, например, по меньшей мере 10, 20, 30, 40, 50, 60, 70, 80, 90, 100 или более аминокислот из CL области. CL область или ее фрагмент могут быть соединены с VL доменом. Нет конкретного ограничения CL области, хотя в одном варианте осуществления она является человеческой CL областью. В данной области техники имеется много примеров человеческих CL областей. Примерная человеческая CL область для применения в данном контексте включает SEQ ID NO: 29.
В соответствии с этим вариантом осуществления может быть предпочтительно, чтобы VH домен содержал последовательность из SEQ ID NO: 3, связанную с СН областью из SEQ ID NO: 27 или 28, a VL домен содержал последовательность из SEQ ID NO: 4, связанную с CL областью из SEQ ID NO: 29.
В другом варианте осуществления первого аспекта настоящего изобретения, антитело или фрагмент антитела основаны на VH и/или VL доменах из антитела Х19-А01, и таким образом:
- VH домен (i) содержит аминокислотную последовательность, обладающую по меньшей мере 80%, 85%, 90%, 95% или 100%-ной идентичностью с последовательностью SEQ ID NO: 5 и/или (ii) содержит CDR1 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 25%, 50%, 75% или 100%-ной идентичностью с последовательностью SEQ ID NO: 17, CDR2 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 5%, 11%, 17%, 23%, 29%, 35%, 47%, 52%, 58%, 64%, 70%, 76%, 82%, 94% или 100%-ной идентичностью с последовательностью SEQ ID NO: 18, и CDR3 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 4%, 9%, 13%, 18%, 22%, 27%, 31%, 36%, 40%, 45%, 50%, 54%, 59%, 63%, 68%, 72%, 77%, 81%, 86%, 90%, 95% или 100%-ной идентичностью с последовательностью SEQ ID NO: 20; и/или
- VL домен (i) содержит аминокислотную последовательность, обладающую по меньшей мере 80%, 85%, 90%, 95% или 100%-ной идентичностью с последовательностью SEQ ID NO: 6; и/или (iv) содержит CDR4 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 5%, 11%, 17%, 23%, 29%, 35%, 47%, 52%, 58%, 64%, 70%, 76%, 82%, 94% или 100%-ной идентичностью с последовательностью SEQ ID NO: 24; CDR5 последовательность, включающую аминокислотную последовательность, обладающую по меньшей мере 14%, 28%, 42%, 57%, 71%, 85% или 100%-ной идентичностью с последовательностью SEQ ID NO: 25; и CDR6 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 11%, 22%, 33%, 44%, 55%, 66%, 77%, 88% или 100%-ной идентичностью с последовательностью SEQ ID NO: 26. Может быть предпочтительно, чтобы VH домен содержал последовательность из SEQ ID NO: 5, a VL домен содержал последовательность из SEQ ID NO: 6.
Антитело или фрагмент антитела из данного варианта осуществления может дополнительно содержать константную область тяжелой цепи (СН) или ее фрагмент, где фрагмент может содержать, например, по меньшей мере 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 120, 140, 160, 180, 200, 220, 240, 260, 280, 300, 320 или больше аминокислот из СН области. СН область или ее фрагмент могут быть соединены с VH доменом. Нет конкретного ограничения СН области, хотя в одном варианте осуществления она является человеческой СН областью. В данной области техники имеется много примеров СН областей. Примерные человеческие СН области для применения в данном контексте включают SEQ ID NO: 27 и SEQ ID NO: 28.
Антитело или фрагмент антитела из данного варианта осуществления может в дополнение или альтернативно дополнительно содержать константную область легкой цепи (CL) или ее фрагмент, где фрагмент может содержать, например, по меньшей мере 10, 20, 30, 40, 50, 60, 70, 80, 90, 100 или больше аминокислот из CL области. CL область или ее фрагмент могут быть соединены с VL доменом. Нет конкретного ограничения CL области, хотя в одном варианте осуществления она является человеческой CL областью. В данной области техники имеется много примеров человеческих CL областей. Примерная человеческая CL область для применения в данном контексте включает SEQ ID NO: 29.
В соответствии с этим вариантом осуществления может быть предпочтительно, чтобы VH домен содержал последовательность из SEQ ID NO: 5, связанную с СН областью из SEQ ID NO: 27 или 28, a VL домен содержал последовательность из SEQ ID NO: 6, связанную с CL областью из SEQ ID NO: 29.
В другом варианте осуществления первого аспекта настоящего изобретения антитело или фрагмент антитела основаны на VH и/или VL доменах антитела Х19-А03, и таким образом:
- VH домен (i) содержит аминокислотную последовательность, обладающую по меньшей мере 80%, 85%, 90%, 95% или 100%-ной идентичностью с последовательностью SEQ ID NO: 17; CDR2 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 5%, 11%, 17%, 23%, 29%, 35%, 47%, 52%, 58%, 64%, 70%, 76%, 82%, 94% или 100%-ной идентичностью с последовательностью SEQ ID NO: 18; и CDR3 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 4%, 9%, 13%, 18%, 22%, 27%, 31%, 36%, 40%, 45%, 50%, 54%, 59%, 63%, 68%, 72%, 77%, 81%, 86%, 90%, 95% или 100%-ной идентичностью с последовательностью SEQ ID NO: 19; и/или
- VL домен (iii) содержит аминокислотную последовательность, обладающую по меньшей мере 80%, 85%, 90%, 95% или 100%-ной идентичностью с последовательностью SEQ ID NO: 8 и/или (iv) содержит CDR4 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 5%, 11%, 17%, 23%, 29%, 35%, 47%, 52%, 58%, 64%, 70%, 76%, 82%, 94% или 100%-ной идентичностью с последовательностью SEQ ID NO: 23; CDR5 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 14%, 28%, 42%, 57%, 71%, 85% или 100%-ной идентичностью с последовательностью SEQ ID NO: 25; и CDR6 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 11%, 22%, 33%, 44%, 55%, 66%, 77%, 88% или 100%-ной идентичностью с последовательностью SEQ ID NO: 26. Может быть предпочтительно, чтобы VH домен содержал последовательность из SEQ ID NO: 7, a VL домен содержал последовательность из SEQ ID NO: 8.
Антитело или фрагмент антитела из этого варианта осуществления может дополнительно содержать константную область тяжелой цепи (СН) или ее фрагмент, где фрагмент может содержать, например, по меньшей мере 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 120, 140, 160, 180, 200, 220, 240, 260, 280, 300, 320 или больше аминокислот из СН области. СН область или ее фрагмент могут быть соединены с VH доменом. Нет конкретных ограничений СН области, хотя в одном варианте осуществления она является человеческой СН областью. В данной области техники содержится много примеров человеческих СН областей. Примерные человеческие СН области для применения в этом контексте включают SEQ ID NO: 27 и SEQ ID NO: 28.
Антитело или фрагмент антитела из данного варианта осуществления может в дополнение или альтернативно дополнительно содержать константную область легкой цепи (CL) или ее фрагмент, где фрагмент может содержать, например, по меньшей мере 10, 20, 30, 40, 50, 60, 70, 80, 90, 100 или больше аминокислот из CL области. CL область или ее фрагмент могут быть соединены с VL доменом. Нет конкретного ограничения CL области, хотя в одном варианте осуществления она является человеческой CL областью. В данной области техники имеется много примеров человеческих CL областей. Примерная человеческая CL область для применения в данном контексте включает SEQ ID NO: 29.
В соответствии с этим вариантом осуществления может быть предпочтительно, чтобы VH домен содержал последовательность из SEQ ID NO: 7, связанную с СН областью из SEQ ID NO: 27 или 28, a VL домен содержал последовательность из SEQ ID NO: 8, связанную с CL областью из SEQ ID NO: 29.
В другом варианте осуществления первого аспекта настоящего изобретения антитело или фрагмент антитела основаны на VH и/или VL доменах антитела Х19-А07, и таким образом:
- VH домен (i) содержит аминокислотную последовательность, обладающую по меньшей мере 80%, 85%, 90%, 95% или 100%-ной идентичностью с последовательностью SEQ ID NO: 9, и/или (ii) содержит CDR1 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 25%, 50%, 75% или 100%-ной идентичностью с последовательностью SEQ ID NO: 17; CDR2 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 5%, 11%, 17%, 23%, 29%, 35%, 47%, 52%, 58%, 64%, 70%, 76%, 82%, 94% или 100%-ной идентичностью с последовательностью SEQ ID NO: 18; и CDR3 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 4%, 9%, 13%, 18%, 22%, 27%, 31%, 36%, 40%, 45%, 50%, 54%, 59%, 63%, 68%, 72%, 77%, 81%, 86%, 90%, 95% или 100%-ной идентичностью с последовательностью SEQ ID NO: 20; и/или
- VL домен (iii) содержит аминокислотную последовательность, обладающую по меньшей мере 80%, 85%, 90%, 95% 100%-ной идентичностью с последовательностью SEQ ID NO: 10; и/или (iv) содержит CDR4 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 5%, 11%, 17%, 23%, 29%, 35%, 47%, 52%, 58%, 64%, 70%, 76%, 82%, 94% или 100%-ной идентичностью с последовательностью SEQ ID NO: 24; CDR5 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 14%, 28%, 42%, 57%, 71%, 85% или 100%-ной идентичностью с последовательностью SEQ ID NO: 25; и CDR6 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 11%, 22%, 33%, 44%, 55%, 66%, 77%, 88% или 100%-ной идентичностью с последовательностью SEQ ID NO: 26. Может быть предпочтительно, чтобы VH домен содержал последовательность SEQ ID NO: 9, a VL домен содержал последовательность SEQ ID NO: 10.
Антитело или фрагмент антитела из данного варианта осуществления может дополнительно содержать константную область тяжелой цепи (СН) или ее фрагмент, где фрагмент может содержать, например, по меньшей мере 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 120, 140, 160, 180, 200, 220, 240, 260, 280, 300, 320 или больше аминокислот из СН области. СН область или ее фрагмент могут быть соединены с VH доменом. Нет конкретного ограничения СН области, хотя в одном варианте осуществления она является человеческой СН областью. В данной области техники имеется много примеров СН областей. Примерные человеческие СН области для применения в данном контексте включают SEQ ID NO: 27 и SEQ ID NO: 28.
Антитело или фрагмент антитела из данного варианта осуществления может в дополнение или альтернативно дополнительно содержать константную область легкой цепи (CL) или ее фрагмент, где фрагмент может содержать, например, по меньшей мере 10, 20, 30, 40, 50, 60, 70, 80, 90, 100 или больше аминокислот из CL области. CL область или ее фрагмент могут быть соединены с VL доменом. Нет конкретного ограничения CL области, хотя в одном варианте осуществления она является человеческой CL областью. В данной области техники имеется много примеров человеческих CL областей. Примерная человеческая CL область для применения в данном контексте включает SEQ ID NO: 29.
В соответствии с этим вариантом осуществления может быть предпочтительно, чтобы VH домен содержал последовательность из SEQ ID NO: 9, связанную с СН областью из SEQ ID NO: 27 или 28, a VL домен содержал последовательность из SEQ ID NO: 10, связанную с CL областью из SEQ ID NO: 29.
В другом варианте осуществления первого аспекта настоящего изобретения антитело или фрагмент антитела основаны на VH и/или VL доменах Х19-А09 антитела, и таким образом:
- VH домен (i) содержит аминокислотную последовательность, обладающую по меньшей мере 80%, 85%, 90%, 95% или 100%-ной идентичностью с последовательностью SEQ ID NO: 11; и/или (ii) содержит CDR1 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 25%, 50%, 75% или 100%-ной идентичностью с последовательностью SEQ ID NO: 17; CDR2 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 5%, 11%, 17%, 23%, 29%, 35%, 47%, 52%, 58%, 64%, 70%, 76%, 82%, 94% или 100%-ной идентичностью с последовательностью SEQ ID NO: 18; и CDR3 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 4%, 9%, 13%, 18%, 22%, 27%, 31%, 36%, 40%, 45%, 50%, 54%, 59%, 63%, 68%, 72%, 77%, 81%, 86%, 90%, 95% или 100%-ной идентичностью с последовательностью SEQ ID NO: 20; и/или
- VL домен (iii) содержит аминокислотную последовательность, обладающую по меньшей мере 80%, 85%, 90%, 95% или 100%-ной идентичностью с последовательностью SEQ ID NO: 12; и/или (iv) содержит CDR4 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 5%, 11%, 17%, 23%, 29%, 35%, 47%, 52%, 58%, 64%, 70%, 76%, 82%, 94% или 100%-ной идентичностью с последовательностью SEQ ID NO: 24; CDR5 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 14%, 28%, 42%, 57%, 71%, 85% или 100%-ной идентичностью с последовательностью SEQ ID NO: 25; и CDR6 последовательность, содержащую аминокислотную последовательность, обладающую по меньшей мере 11%, 22%, 33%, 44%, 55%, 66%, 77%, 88% или 100%-ной идентичностью с последовательностью SEQ ID NO: 26. Может быть предпочтительно, чтобы VH домен содержал последовательность SEQ ID NO: 11, a VL домен содержал последовательность SEQ ID NO: 12.
Антитело или фрагмент антитела из данного варианта осуществления может дополнительно содержать константную область тяжелой цепи (СН) или ее фрагмент, где фрагмент может содержать, например, по меньшей мере 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 120, 140, 160, 180, 200, 220, 240, 260, 280, 300, 320 или больше аминокислот из СН области. СН область или ее фрагмент могут быть соединены с VH доменом. Нет конкретного ограничения СН области, хотя в одном варианте осуществления она является человеческой СН областью. В данной области техники имеется много примеров СН областей. Примерные человеческие СН области для применения в данном контексте включают SEQ ID NO: 27 и SEQ ID NO: 28.
Антитело или фрагмент антитела из данного варианта осуществления может в дополнение или альтернативно дополнительно содержать константную область легкой цепи (CL) или ее фрагмент, где фрагмент может содержать, например, по меньшей мере 10, 20, 30, 40, 50, 60, 70, 80, 90, 100 или больше аминокислот из CL области. CL область или ее фрагмент могут быть соединены с VL доменом. Нет конкретного ограничения CL области, хотя в одном варианте осуществления она является человеческой CL областью. В данной области техники имеется много примеров человеческих CL областей. Примерная человеческая CL область для применения в данном контексте включает SEQ ID NO: 29.
В соответствии с этим вариантом осуществления может быть предпочтительно, чтобы VH домен содержал п