8-(1-{ 4-{ (5-хлор-4-{ (2-(диметилфосфорил)фенил)амино} пиримидин-2-ил)амино)-3-метоксифенил} пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он и его фармацевтически приемлемые соли в качестве модулятора alk и eger, предназначенные для лечения рака
Иллюстрации
Показать всеИзобретение относится к новым 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-ону формулы 1, указанной ниже, и его фармацевтически приемлемым солям. Соединения обладают свойствами ингибитора киназы анапластической лимфомы (ALK) и рецептора эпидермального фактора роста (EGFR) и предназначены для лечения рака, в частности рака, который представляет собой немелкоклеточный рак легких (NSCLC), в том числе с метастазами в головном мозге.
Изобретение также относится к противораковой фармацевтической композиции; к применению соединения общей формулы 1 для использования с дополнительным противораковым веществом для одновременного, раздельного или последовательного введения при лечении рака. Изобретение относится к способу получения соединения формулы 1 путем взаимодействия 8-(1-{4-амино-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-она гидрохлорида с 2,5-дихлор-N-[2-(диметилфосфорил)фенил]пиримидин-4-амином. Изобретение также относится к способу изготовления лекарственного средства смешением соединения общей формулы 1 и фармацевтически приемлемых наполнителей, с последующим формированием таблетки, капсулы или инъекции, помещенной в фармацевтически приемлемую упаковку. 11 н. и 4 з.п. ф-лы, 2 табл., 10 пр.
Реферат
Настоящее изобретение относится к 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-ону и его фармацевтически приемлемым солям - ингибиторам киназы анапластической лимфомы (ALK) и рецептора эпидермального фактора роста (EGFR), предназначенным для лечения рака.
Протеинкиназы представляют собой большое семейство белков, которые играют центральную роль в регуляции широкого круга клеточных процессов и осуществляют контроль над клеточными функциями. Аномальная активность протеинкиназы связана с несколькими заболеваниями, в том числе псориазом и раковыми заболеваниями.
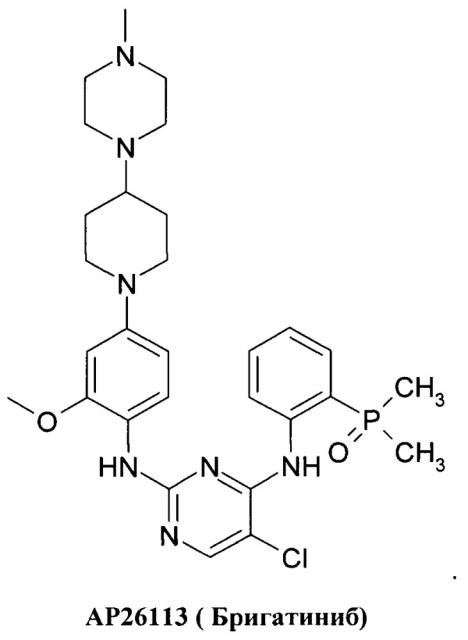
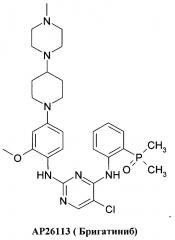
Известны ингибиторы киназы анапластической лимфомы (ALK), представляющие собой производные фосфора, запатентованные ARIAD Pharmaceuticals [США 2014/0066406 A1, WO 2009/143389]. В этой серии соединений самым продвинутым является АР26113, также известный как Бригатиниб (Brigatinib), оральный ингибитор рецепторов тирозинкиназ, таких как киназы анапластической лимфомы (ALK) и рецептора эпидермального фактора роста (EGFR), предназначенный для лечения рака. Двойной ALK/EGFR ингибитор АР26113 связывает и ингибирует ALK и гибридные ALK белки, а также EGFR и его мутантные формы
В настоящее время Бригатиниб (АР26113) получил разрешение FDA для лечения ALK-положительного немелкоклеточного рака легких (NSCLC). В связи с большим количеством протеинкиназ и множеством связанных с ними заболеваний, создание новых классов селективных ингибиторов протеинкиназ для лечения заболеваний, обусловленных повышенной активностью протеинкиназ, остается актуальной задачей.
Ниже приведены определения терминов, которые использованы в описании данного изобретения.
«Активный компонент» (лекарственное вещество, лекарственная субстанция, drug-substance) означает физиологически активное вещество синтетического или иного (биотехнологического, растительного, животного, микробного и прочего) происхождения, обладающее фармакологической активностью и являющееся активным началом фармацевтической композиции, используемой для производства и изготовления лекарственного препарата (средства).
«Лекарственное средство (препарат)» - вещество (или смесь веществ в виде фармацевтической композиции) в виде таблеток, капсул, инъекций, мазей и других готовых форм, предназначенное для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней, диагностики, анестезии, контрацепции, косметологии и прочего.
«Фармацевтическая композиция» обозначает композицию, включающую в себя активный компонент и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных, распределяющих и воспринимающих средств, средств доставки, таких как консерванты, стабилизаторы, наполнители, измельчители, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от природы и способа назначения и дозировки. Примерами суспендирующих агентов являются этоксилированный изостеариловый спирт, полиоксиэтилен, сорбитол и сорбитовый эфир, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант, а также смеси этих веществ. Защита от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как парабены, хлорбутанол, сорбиновая кислота и подобные им соединения. Композиция может включать также изотонические агенты, например сахара, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например моностеарат алюминия и желатин. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, а также их смеси, растительные масла (такие, как оливковое масло) и инъекционные органические сложные эфиры (такие, как этилолеат). Примерами наполнителей являются лактоза, молочный сахар, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Примерами измельчителей и распределяющих средств являются крахмал, альгиновая кислота и ее соли, силикаты. Примерами лубрикантов являются стеарат магния, лаурилсульфат натрия, тальк, а также полиэтиленгликоль с высоким молекулярным весом. Фармацевтическая композиция для перорального, сублингвального, трансдермального, внутримышечного, внутривенного, подкожного, местного или ректального введения активного начала, одного или в комбинации с другим активным началом, может быть введена животным и людям в стандартной форме введения в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, желатиновые капсулы, пилюли, порошки, гранулы, жевательные резинки и пероральные растворы или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, такие как мази и кремы, подкожные, внутримышечные, внутривенные, интраназальные или внутриглазные формы введения и ректальные формы введения.
«Фармацевтически приемлемая соль» означает относительно нетоксичные органические и неорганические соли кислот и оснований, заявленных в настоящем изобретении. Эти соли могут быть получены in situ в процессе синтеза, выделения или очистки соединений или приготовлены специально. В частности, соли оснований могут быть получены специально, исходя из очищенного свободного основания заявленного соединения и подходящей органической или неорганической кислоты. Примерами полученных таким образом солей являются гидрохлориды, гидробромиды, сульфаты, бисульфаты, фосфаты, нитраты, ацетаты, оксалаты, валериаты, олеаты, пальмитаты, стеараты, лаураты, бораты, бензоаты, лактаты, тозилаты, цитраты, малеаты, фумараты, сукцинаты, тартраты, мезилаты, малонаты, салицилаты, пропионаты, этансульфонаты, бензолсульфонаты, сульфаматы и им подобные (Подробное описание свойств таких солей дано в Berge S.M., et al., "Pharmaceutical Salts" J. Pharm. Sci. 1977, 66: 1-19). Соли заявленных кислот также могут быть специально получены реакцией очищенной кислоты с подходящим основанием, при этом могут быть синтезированы соли металлов и аминов. К металлическим относятся соли натрия, калия, кальция, бария, цинка, магния, лития и алюминия, наиболее желательными из которых являются соли натрия и калия. Подходящими неорганическими основаниями, из которых могут быть получены соли металлов, являются гидроксид, карбонат, бикарбонат и гидрид натрия, гидроксид и бикарбонат калия, поташ, гидроксид лития, гидроксид кальция, гидроксид магния, гидроксид цинка. В качестве органических оснований, из которых могут быть получены соли заявленных кислот, выбраны амины и аминокислоты, обладающие достаточной основностью, чтобы образовать устойчивую соль, пригодные для использования в медицинских целях (в частности, они должны обладать низкой токсичностью). К таким аминам относятся аммиак, метиламин, диметиламин, триметиламин, этиламин, диэтиламин, триэтиламин, бензиламин, дибензиламин, дициклогексиламин, пиперазин, этилпиперидин, трис(гидроксиметил)аминометан и подобные им. Кроме того, для солеобразования могут быть использованы гидроокиси тетраалкиламмония, например, такие как холин, тетраметиламмоний, тетраэтиламмоний и им подобные. В качестве аминокислот могут быть использованы основные аминокислоты - лизин, орнитин и аргинин.
Цель настоящего изобретения заключается в создании новых ингибиторов киназы анапластической лимфомы ALK и рецептора эпидермального фактора роста EGFR для лечения рака.
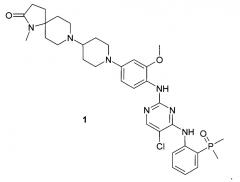
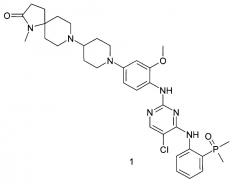
Поставленная цель достигается 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-оном формулы 1 и его фармацевтически приемлемыми солями.
Предметом настоящего изобретения является 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1 и его фармацевтически приемлемые соли
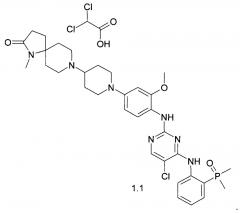
Более предпочтительным соединением является 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1 и 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-она дихлороацетат формулы 1.1
Настоящее изобретение также включает фармацевтически приемлемые соли 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-она формулы 1. Примеры фармацевтически приемлемых солей включают, но не ограничиваются ими, соли минеральных или органических кислот соединения формулы 1, таких как карбоновые кислоты, например, соли дихлоруксусной кислоты, а также соли хлористоводородной кислоты, фосфорной кислоты или сульфокислоты. Фармацевтически приемлемые соли по настоящему изобретению включают обычные нетоксичные соли исходного соединения, образованные, например, из нетоксичных неорганических или органических кислот. Фармацевтически приемлемые соли по настоящему изобретению могут быть синтезированы из исходного соединения, которое содержит основную или кислотную группу, обычными химическими способами. Как правило, такие соли могут быть получены взаимодействием свободных кислотных и основных форм соединений общей формулы 1 со стехиометрическим количеством соответствующего основания или кислоты в воде или в органическом растворителе или в смеси двух растворителей. Как правило, предпочтительны неводные среды, такие как эфир, этилацетат, этанол, изопропанол, ацетон или ацетонитрил (ACN). Списки подходящих солей можно найти в справочнике фармацевтических солей [Р.Н. Stahl, C.G. Wermuth (Eds.). Handbook of Pharmaceutical Salts, Properties, Selection, and Use. VHCA, Verlag Helvetica Chimica Acta, Switzerland, and Wiley-VCH, Weinheim, Germany. 2002.].
Предметом настоящего изобретения являются модуляторы киназ, в том числе и ALK и EGFR, которые представляют собой 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1 или его фармацевтически приемлемые соли.
Новое соединение 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1 и его фармацевтически приемлемые соли, например дихлорацетат формулы 1.1 обладают in vitro активностью по отношению к биомишеням ALK и EGFR, превышающей активность Бригатиниба (Таблицы 1 и 2). Так, например соединение формулы 1.1 в 3,2 раза превышает активность Бригатиниба по отношению к ALK и в 2,1 раза превышает активность Бригатиниба по отношению к EGFR (Таблица 1).
Предметом настоящего изобретения являются 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1 и его фармацевтичеки-приемлемые соли, предназначенные для лечения у пациента рака и других заболеваний, в том числе для лечения немелкоклеточного рака легких (NSCLC), в том числе с метастазами в головном мозге.
Предметом изобретения является фармацевтическая композиция в форме таблетки, капсулы или инъекции, содержащая, по меньшей мере, одно соединение 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1 или его фармацевтически приемлемую соль, и, по меньшей мере, один фармацевтически приемлемый наполнитель или добавку. Такая композиция может быть введена субъекту в случае необходимости подавлять рост, развитие рака и/или метастазов рака, в том числе твердых опухолей (например, рака предстательной железы, рака толстой кишки, поджелудочной железы и яичников, рака молочной железы, немелкоклеточного рака легкого (NSCLS), нейронных опухолей, таких как глиобластомы и нейробластомы; карциномы, рака мягких тканей); различных форм лимфомы, различных форм лейкемии и в том числе раковых заболеваний, устойчивых к другой обработке, в том числе тех, которые устойчивы к обработке другими ингибиторами киназ, и, как правило, для лечения и профилактики заболеваний или нежелательных состояний, обусловленых одной или более киназой, которые ингибируются соединениями по настоящему изобретению.
В соответствии с данным изобретением фармацевтическая композиции может быть в форме, подходящей для перорального применения (например, в виде таблеток, пастилок, твердых или мягких капсул, водных или масляных суспензий, эмульсий, диспергируемых порошков или гранул, сиропов или эликсиров), для местного применения (например, в виде кремов, мазей, гелей или водных или масляных растворов или суспензий), для введения путем ингаляции (например, в виде тонкоизмельченного порошка или жидкого аэрозоля), для введения путем инсуффляции (например, в виде тонкоизмельченного порошка) или для парентерального введения (например, в виде стерильного водного или масляного раствора для внутривенного, подкожного, внутримышечного введения дозы или в виде суппозиториев для ректального введения дозы).
Фармацевтическая композиция по изобретению может быть получена обычными способами с использованием обычных фармацевтических наполнителей, хорошо известных в данной области. Таким образом, фармацевтические композиции, предназначенные для перорального применения, могут содержать, например, один или несколько окрашивающих, подслащивающих, вкусовых компонентов и/или консервант.
Соединение 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1 или его фармацевтически-приемлемую соль обычно вводят теплокровному животному в единичной дозе в диапазоне 5-5000 мг/м2 площади тела животного, то есть примерно 0,1-100 мг/кг, и это обычно обеспечивает терапевтически эффективную дозу. Форма единичной дозы, такой как таблетка или капсула, обычно содержит, например, 1-250 мг активного ингредиента. Суточная доза обязательно будет варьироваться в зависимости от пациента, конкретного пути введения и тяжести заболевания, которое лечат. Соответственно, врач, который лечит конкретного пациента, может определить оптимальную дозу, учитывая ингибирующую активность против ALK и EGFR соединений общей формулы 1 и их таутомеров, стереоизомеров, фармацевтически приемлемых солей и сольватов, предназначенных для лечения заболеваний или медицинских состояний, обусловленных активностью ALK и EGFR, например, рака. Типы рака, которые могут быть восприимчивы к лечению с использованием соединений общей формулы 1 и их таутомеров, стереоизомеров, фармацевтически приемлемых солей и сольватов включают, но не ограничиваются лечением пациентов с немелкоклеточным раком легких (NSCLC), в том числе с метастазами в головном мозге.
Согласно другому аспекту настоящего изобретения соединение 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1, как определено выше, или его фармацевтически приемлемые соли предназначены для использования в качестве лекарственного средства.
В соответствии с настоящим изобретением предлагаются 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1 и их фармацевтически приемлемые соли для лечения заболевания, обусловленного активностью ALK и EGFR, в том числе для лечения ракового заболевания, обусловленного активностью ALK и EGFR.
Предметом настоящего изобретения является также способ производства лекарственного средства для лечения заболевания, обусловленного ALK и EGFR, предусматривающий использование соединения 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1 или его фармацевтически приемлемой соли.
Предметом настоящего изобретения является также способ лечения рака, обусловленного ALK и EGFR, предусматривающй использование соединения 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1 и его фармацевтически приемлемой соли.
Предметом настоящего изобретения является также способ получения противоракового эффекта у пациента, нуждающегося в таком лечении, который включает введение указанному пациенту эффективного количества соединения 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1 или его фармацевтически приемлемой соли.
В соответствии с настоящим изобретением предложен способ лечения человека, страдающего от заболевания, в том числе рака, при котором предпочтительно ингибирование ALK и EGFR. Лечение осуществляется путем введения нуждающемуся в этом человеку терапевтически эффективного количества соединения 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1 или его фармацевтически приемлемой соли.
В любом из аспектов или вариантов упомянутый в данном описании рак, указанный в общем смысле, может быть выбран из твердых опухолей (например, рака предстательной железы, рака толстой кишки, поджелудочной железы и рака яичников, рака молочной железы, немелкоклеточного рака легкого (NSCLS), нейронных опухолей, таких как глиобластомы и нейробластомы; карциномы, рака мягких тканей); различных форм лимфомы, таких как неходжкинская лимфома (NHL), известная как анапластическая крупноклеточная (ALCL), различные формы лейкемии; и в том числе рака, который устойчив к другим лекарствам, в том числе тех, которые устойчивы к ингибированию других киназ, и, как правило, для лечения и профилактики заболеваний или нежелательных состояний, обусловленных одной или более киназами, которые ингибируются соединениями по настоящему изобретению.
Настоящее изобретение относится также к способу лечения рака. Способ включает введение (в виде монотерапии или в комбинации с одним или несколькими другими противораковыми агентами, одним или несколькими агентами для облегчения побочных эффектов, излучение и т.д.) терапевтически эффективного количества соединения по настоящему изобретению, нуждающемуся в этом человеку или животному, чтобы ингибировать, замедлить или уменьшить рост, развитие или распространение рака у реципиента, в том числе твердых опухолей или других форм рака, таких как лейкозы. Такое введение представляет собой способ лечения или профилактики заболеваний, обусловленных одной или несколькими киназами, путем их ингибирования одним из соединений общей формулы 1 или или его таутомером, стереоизомером, фармацевтически приемлемой солью или его сольватом или его фармацевтически приемлемым производным. Термин "введение" включает доставку соединения общей формулы 1 или его пролекарства или другого его фармацевтически приемлемого производного с использованием любого подходящего состава или способа введения. Обычно соединение вводят один или несколько раз в месяц, часто один или более раз в неделю, например, ежедневно, через день, 5 дней/неделя, и т.д. Наиболее предпочтительными являются оральный и внутривенный способы введения.
Способ лечения рака, описанный выше, может быть примен в качестве единственной терапии или может включать в дополнение использование соединения по настоящему изобретению к обычной хирургии или лучевой терапии или химиотерапии или иммунотерапии. Такая химиотерапия может вводиться одновременно, одновременно-последовательно или раздельно с лечением соединением по настоящему изобретению и может включать один или более противоопухолевых агентов из следующих категорий: антипролиферативные/противоопухолевые препараты и их комбинации, используемые в медицинской онкологии; цитостатические агенты; агенты анти-вторжение; ингибиторы функции фактора роста; антиангиогенные агенты; сосудистые средства; антагонисты эндотелиновых рецепторов; антисмысловые терапии; подходы генной терапии и подходы иммунотерапии.
Предметом настоящего изобретения является также фармацевтическая композиция для комбинированного лечения рака, включающая соединение 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1 или его фармацевтически приемлемую соль и дополнительно противоопухолевое вещество, как определено выше. Термин "совместное лечение" используют по отношению к комбинированной терапии, причем, это может относиться к одновременному, раздельному или последовательному введению. В одном аспекте изобретения "комбинированное лечение" относится к одновременному введению. В другом аспекте настоящего изобретения "комбинированное лечение" относится к раздельному введению. В третьем аспекте настоящего изобретения "комбинированное лечение" относится к последовательному введению. Если введение последовательное или раздельное, задержка во введении второго компонента должна быть такой, чтобы сохранить эффективность эффекта, возникающего в результате использования комбинации.
Таким образом, одним из вариантов изобретения является применение соединения 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1 или его фармацевтически приемлемой соли и дополнительно противоопухолевого вещества для совместной терапии рака.
Предметом настоящего изобретения является также способ получения противоракового эффекта у нуждающегося в таком лечении теплокровного животного и человека, который включает введение указанным млекопитающим соединения 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1 или фармацевтически приемлемой соли и одновременное, раздельное или последовательное введение дополнительного противоопухолевого вещества указанному млекопитающему в количествах, совместно обеспечивающих получение противоракового эффекта.
Предметом данного изобретения является способ получения соединения 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1 путем взаимодействия соединения общей формулы 2 с 2,5-дихлор-N-[2-(диметилфосфорил)фенил]пиримидин-4-амином формулы 3.
Ниже изобретение описано более подробно с помощью конкретных примеров. Следующие примеры представлены с целью иллюстрации и не предназначены для ограничения изобретения каким-либо образом. Специалисты в данной области техники легко поймут различие некритических параметров, которые могут быть изменены или модифицированы, для получения таких же результатов.
Пример 1. Трет-бутил 4-(1-метил-2-оксо-1,8-диазаспиро(4.5)дек-8-ил)пиперидин-1-карбоксилат (2.1) был получен в соответствии со Схемой 1
Схема 1
К суспензии 1-метил-1,8-диазаспиро[4.5]декан-2-она (1.64 г, 9.75 ммоль) в 0.1 л дихлорметана были добавлены N-бок-4-пиперидон (1.95 г, 9.75 ммоль) и триацетоксиборогидрид натрия (3.1 г, 14.6 ммоль). Реакционная смесь перемешивалась при комнатной температуре в течение 24 ч. После окончания реакции был добавлен насыщенный водный раствор карбоната натрия, органическая фаза была отделена, промыта брайном, высушена над сульфатом натрия, профильтрована, затем фильтрат был упарен. Остаток после упаривания очищался на колонке с силикагелем, с дихлорметаном в качестве элюэнта. Трет-бутил 4-(1-метил-2-оксо-1,8-диазаспиро(4.5)дек-8-ил)пиперидин-1-карбоксилат (2.1) был получен с выходом 2.5 г (73%). LC-MS (ESI) 352.5 (M+H)+.
Пример 2. 8-(1-{4-амино-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он гидрохлорид формулы 2 был получен в соответствии со Схемой 2.
Схема 2
Раствор трет-бутил 4-(1-метил-2-оксо-1,8-диазаспиро(4.5)дек-8-ил)пиперидин-1-карбоксилата формулы 2.1 (2.5 г, 7.1 ммоль) в 25 мл 3М раствора HCl в диоксане и 15 мл метанола перемешивался при комнатной температуре 3 ч, затем он был частично упарен и выпавший осадок был отфильтрован. К осадку были добавлены 2-нитро-5-фторанизол (1.27 н, 7.45 ммоль) и диизопропилэтиламин (3.5 г, 27 ммоль) в 15 мл диметилформамида. Реакционная смесь перемешивалась при 70°C в течении 16 ч, затем выпаривалась и остаток промывался водой. Осадок отфильтровывался, промывался водой и эфиром и сушился на воздухе. Затем осадок был добавлен к суспензии Pd 10% на активированном угле в 100 мл метанола и подвергнут гидрированию в течение 3 ч при давлении 5 psi. По окончании реакции катализатор был отфильтрован, реакционная смесь обработана 5 мл 3М раствора HCl в диоксане и реакционная масса была выпарена, выход 8-(1-{4-амино-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-она гидрохлорида 1.01 г (35%). LC-MS (ESI) 373.5 (M+H)+.
Пример 3. 8-(1-{4-{(5-Хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1 был получен в соответствии со Схемой 3.
Схема 3
К суспензии 8-(1-{4-амино-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-она гидрохлорида формулы 2 (1 г, 2.25 ммоль) в 10 мл метоксиэтанола был добавлен 2,5-дихлор-N-(2-(диметилфосфорил)фенил)пиримидин-4-амин (0.82 г, 2.6 ммоль) и реакционная масса перемешивалась при кипении 15 ч. По окнчании реакции растворители были отогнаны при пониженном давлении и остаток перетирался с этанолом. Осадок отфильтровывался, промывался холодным этанолом, нейтрализовывался насыщенным водным раствором натрия гидрокарбоната, отфильтровывался и промывался ацетоном. 8-(1-{4-{(5-хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он был получен в количестве 420 мг (29%) после сушки осадка в вакууме. LC-MS (ESI) 653.2 (M+H)+. 1H NMR (DMSO-d6, 400 MHz) δ 11.16 (s, 1H), 8.49 (br, 1H), 8.07 (s, 1H) 8.04 (s, 1H), 7.53 (m, 1H), 7.35 (m, 2H), 7.10 (t, J=7.6 Hz, 1H), 6.63 (s, 1H), 6.48 (d, 1H), 3.76 (s, 3H), 3.7 (m, 2H), 2.85 (m, 2H), 2.7 (m, 2H), 2.6 (s, 3H), 2.4 (m, 1H), 2.15-2.35 (m, 4H), 1.8-1.9 (m, 6H), 1.78 (s, 3H), 1.74 (s, 3H), 1.6 (m, 2H), 1.34 (m, 2H).
Пример 4. Хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-она дихлорацетат формулы 1.1 был получен нейтрализацией хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-она дихлоруксусной кислотой.
К раствору хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-она (0.1 г, 0.15 ммоль) в смеси ацетона (4 мл) и этанола (4 мл) была добавлена дихлоруксусная кислота (0.02 г, 0.15 ммоль) в ацетоне (1 мл). Реакционная масса перемешивлась 24 часа при 20°C. Выпавшие кристаллы отфильтровывались и сушились в вакууме. Выход хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-она дихлорацетата - 0.097 г (79%).
1H NMR (DMSO-d6, 400 MHz) δ 11.21 (s, 1H), 8.52 (br s, 1H), 8.09 (s, 1H) 8.02 (s, 1H), 7.56 (m, 1H), 7.39 (m, 3H), 7.11 (t, J=7.6 Hz, 1H), 6.70 (s, 1H), 6.37 (d, 1H), 6.12 (s, 1H), 3.72 (s, 3H), 3.65 (m, 2H), 2.88 (m, 2H), 2.67 (m, 2H), 2.62 (s, 3H), 2.3 (m, 1H), 2.15-2.35 (m, 4H), 1.7-1.9 (m, 6H), 1.73 (s, 3H), 1.78 (s, 3H), 1.64 (m, 2H), 1.31 (m, 2H).
Пример 5. Эссей ALK. Вещества тестировали по влиянию на активность киназы ALK с помощью скрининговой платформы ADP Hunter Plus (DiscoverRX Corporation). Концентрация ДМСО в реакционной смеси составляла 1%. 4 мкл 100-кратных стоков исследуемых веществ в 100% ДМСО разбавляли в 36 мкл киназного буфера (50 мМ HEPES pH 7.5, 0.01% BRIJ-35, 10 мМ MgCl2, 1 мМ EGTA) и добавляли к 5 мкл 2-кратной смеси Субстрат/Киназа (ALK/Srctide, финальные концентрации - 1 мкг/мл ALK и 20 мкМ Srctide) в 384-луночном планшете (черные, малого объема, производство Corning, кат. #3676). Вещества преинкубировали с киназами в течение 10 мин при комнатной температуре. После этого для начала реакции добавляли 4 мкл 2.5-кратного раствора АТФ (конечная концентрация АТФ в реакционной смеси 100 мкМ). После 30 сек инкубации на шейкере реакцию инкубировали в течение 60 мин при комнатной температуре. После этого добавляли 5 мкл Реагента А и 10 мкл Реагента В и инкубировали еще 30-60 мин при комнатной температуре. Измеряли флуоресценцию при возбуждении длиной волны 530 нм и эмиссии 585 нм. Степень фосфорилирования пептидного субстрата рассчитывали по формуле ниже (если отношение эмиссии низкое - пептид фосфорилирован, т.е. нет ингибирования активности киназы, если отношение высокое - пептид не фосфорилирован, т.е. киназа ингибирована).
% фосфорилирования рассчитывается как
% ингибирования рассчитывается как
где:
C100%=средний сигнал эмиссии кумарина контроль 100% фосфорилирования,
С0%=средний сигнал эмиссии кумарина контроль 0% фосфорилирования,
F100%=средний сигнал эмиссии флуоресцеина контроль 100% фосфорилирования,
F0%=средний сигнал эмиссии флуоресцеина контроль 0% фосфорилирования.
Полученные результаты представлены в Таблице 1.
Пример 6. Эссей EGFR. Соединения общей формулы 1 тестировали по влиянию на активность киназ EGFR(L858R/T790M) b EGFR wt (все ферменты предоставлены Invitrogen Corp., каталожные номера PV3872, PV4128 and PV4803, соответственно) с помощью скрининговой платформы Z`-LYTE (производство Life Technologies). Концентрация ДМСО в реакционной смеси составляла 1%. 5 мкл 2-кратной смеси Субстрат/Киназа (Tyr4/EGFRwt или EGFR-L858R или EGFR-T790M, конечные концентрации - 0.5 мкМ для субстрата Tyr 4 и 1000, 250, 1000 нг/мл для EGFRwt или EGFR-L858R или EGFR-T790M соответственно) добавляли в 384-луночные планшеты (черные, малого объема, производство Corning, кат. #3676). 1.5 мкл 100-кратных стоков исследуемых веществ в 100% ДМСО разбавляли в 10 раз в 13.5 мкл киназного буфера (50 мМ HEPES pH 6.5, 0.01% BRIJ-35, 10 мМ MgCl2, 1 мМ EGTA, 0.02% NaN3) и затем 1 мкл разбавленных веществ добавляли к смеси Субстрат/Киназа. Вещества преинкубировали с киназами в течение 10 мин при комнатной температуре. После этого для начала реакции добавляли 4 мкл 2.5-кратного раствора АТФ (конечная концентрация АТФ в реакционной смеси была 180 или 100 или 40 мкМ для EGFRwt, EGFR-L858R и EGFR-T790M соответственно). После 30 сек инкубации на шейкере, реакцию инкубировали в течение 60 мин при комнатной температуре. После этого добавляли 5 мкл Реагента В (разбавленного 1:500) и инкубировали еще 60 мин при комнатной температуре. Измеряли флуоресценцию при возбуждении длиной волны 400 нм и эмиссии при 445 и 520 нм. Степень фосфорилирования пептидного субстрата рассчитывали по формуле ниже (если отношение эмиссии низкое - пептид фосфорилирован, т.е. нет ингибирования активности киназы, если отношение высокое - пептид не фосфорилирован, т.е. киназа ингибирована).
% фосфорилирования рассчитывается как
% ингибирования рассчитывается как
где:
С100%=средний сигнал эмиссии кумарина контроль 100% фосфорилирования,
С0%=средний сигнал эмиссии кумарина контроль 0% фосфорилирования,
F100%=средний сигнал эмиссии флуоресцеина контроль 100% фосфорилирования,
F0%=средний сигнал эмиссии флуоресцеина контроль 0% фосфорилирования.
Концентрационная кривая зависимости активности киназы от концентрации тестируемых веществ была построена с использованием сигмоидной модели. Полученные результаты представлены в Таблице 2.
Пример 7. Ингибирование пролиферации клеток.
Клетки выращивали в пластиковых культуральных флаконах Т75 и Т175 (Greiner Bio-One) в среде ДМЕМ или RPMI, содержащей 10% сыворотки (FBS), 1% смесь антибиотиков (AAS) при 37°C и 5% CO2. Пересевали клетки при достижении ~90% конфлюентности. Клетки снимали с культуральных флаконов с помощью раствора TryplExpress. Для этого удаляли из флакона культуральную среду, заливали клетки 2 мл раствора TryplExpress, ополаскивали этим раствором поверхность флакона, инкубировали клетки 5 минут при 37°C. Затем суспендировали клетки в новой культуральной среде. Клетки рассевали в пропорции 1:2-1:8.
День №1. Посадка клеток.
Клетки сажали в концентрации 500-2000 клеток в лунку в среде RPMI 1640+10% FBS, 40 мкл в лунку. Вертикальный ряд №24 контроль: среда без клеток.
Инкубация 24 часа, 37°C, 5% CO2.
День №2. Добавление соединений.
Соединения растворяли в ДМСО до концентрации 20 мМ. Затем в зависимости от максимальной тестируемой концентрации разбавляли соединения ДМСО до 400-кратной максимальной концентрации. Далее делали серийные разведения в ДМСО с шагом 3,16. Каждую концентрацию тестировали в двух повторах, каждый эксперимент повторяли как минимум 2 раза. Также в каждой плашке были контроли только с ДМСО без соединений. Затем делали промежуточное разведение соединений в 80 раз в клеточной среде 1640+10% FBS. Далее добавляли 10 мкл этих растворов к 40 мкл клеток. Итоговое разведение соединений в 400 раз и финальная концентрация ДМСО 0,25%.
Инкубация 72 часа, 37°C, 5% CO2.
День №3. Детекция.
В каждую лунку плашки добавляли 15 мкл реагента CellTiter-Glo, инкубировали 10 минут при комнатной температуре и детектировали люминесцентный сигнал на многофункциональном микропланшетном ридере Tecan Infinite M1000 PRO.
Обсчет результатов.
Для обсчета результатов использовали GraphPad Prizm5. Для первичных расчетов в качестве 0% живых клеток использовали лунки без клеток, а лунки с ДМСО без соединений как максимальное количество живых клеток 100%. Полученные результаты представлены в Таблице 2.
Пример 8. Приготовление лекарственного вещества в виде таблеток. Смешивали, а затем спресовывали в брусок 1600 мг крахмала, 1600 мг измельченной лактозой, 400 мг талька и 1000 мг соединения 1.8. Полученный брусок измельчали в гранулы и просеивают через сита, собирая гранулы размером 14-16 меш. Полученные гранулы таблетировали в таблетки, пригодных форм весом 500 мг каждая.
Пример 9. Приготовление лекарственного вещества в виде капсул. Соединение 1.8 тщательно смешивали с порошком лактозы в соотношении 2:1. Полученную порошкообразную смесь упаковывали по 600 мг в желатиновые капсулы подходящего размера.
Пример 10. Приготовление лекарственного вещества в виде композиций для внутримышечных, внутрибрюшинных или подкожных инъекций. Смешивали 500 мг соединения 1.8, 300 мг хлорбутанола, 2 мл пропиленгликоля и 100 мл воды для инъекций. Раствор фильтровали и помещали в 1 мл в ампулы, которые укупоривали.
Специалисты в данной области техники легко определят, некритические параметры, которые могут быть изменены или модифицированы для достижения результатов, представленных в изобретении. Различные модификации изобретения, в дополнение к описанным здесь, станут очевидными специалистам в данной области техники из приведенного выше описания.
1. 8-(1-{4-{(5-Хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1 и его фармацевтически приемлемые соли
2. Соединение по п. 1 или его фармацевтически приемлемые соли в качестве ингибиторов киназы анапластической лимфомы ALK и рецептора эпидермального фактора роста EGFR.
3. Соединение по п. 1 выбранное из ряда:
8-(1-{4-{(5-Хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-он формулы 1;
8-(1-{4-{(5-Хлор-4-{(2-(диметилфосфорил)фенил)амино}пиримидин-2-ил)амино)-3-метоксифенил}пиперидин-4-ил)-1-метил-1,8-диазаспиро(4.5)декан-2-она дихлороацетат формулы 1.1.
4. Соединение общей формулы 1 или его фармацевтически приемлемая соль по п. 1 ил