Производные бензилиденгуанидина и их терапевтическое применение для лечения заболеваний, связанных с неправильным сворачиванием белков
Иллюстрации
Показать всеИзобретение относится к применению соединений, описываемых формулой (I), или их фармацевтически приемлемых солей или таутомерных форм для лечения расстройств, связанных со стрессом, обусловленным неправильным сворачиванием белков, в частности с накоплением неправильно свернутых белков. Расстройства выбраны из нейропатии Шарко-Мари-Тута; тяжелого синдрома Дежерина-Сотта; заболеваний сетчатки, предпочтительно пигментного ретинита, цилиопатии сетчатки, макулярной дегенерации или диабетической ретинопатии или бокового амиотрофического склероза (ALS). В формуле (I) R1 представляет собой алкил, Cl, F или Br; R2 представляет собой H или F; R3 выбирают из H и алкила; R4 выбирают из H, COалкила и COOалкила; R5 представляет собой H; или R4 и R5 соединены, образуя оксодигидротриазиновую группу, которая необязательно является замещенной одной или более алкильными группами R10; X и Z независимо друг от друга представляют собой CR11, Y выбирают из CR11 и N; R11 представляет собой H или F, причем алкил означает C1-20-алкил. Изобретение относится также к различным вариантам соединений формулы (I) и фармацевтической композиции для использования в лечении расстройств, связанных со стрессом, обусловленным неправильным сворачиванием белков, в частности с накоплением неправильно свернутых белков. 6 н. и 8 з.п. ф-лы, 6 ил., 2 табл., 16 пр.
Реферат
Данное изобретение относится к соединениям, которые можно использовать для терапевтического применения при лечении расстройств, связанных со стрессом, обусловленным неправильным фолдингом (сворачиванием) белков, в частности с накоплением неправильно свернутых белков. В частности, в данном изобретении предлагаются соединения, способные оказывать защитное действие в отношении цитотоксического стресса эндоплазматического ретикулума.
Уровень техники
Соединение 2-(2,6-дихлорбензилиден)гидразинкарбоксимидамид, называемое также гуанабензом, является агонистом α2-адренергических рецепторов, применяемым в качестве средства против гипертензии.
Сообщалось также о различных производных гуанабенза. Например в патенте US №3,982,020 (Sandoz, Inc.) описываются замещенные бензилиденгидразины и их применение в качестве агентов, противодействующих гипергликемии, ожирению и воспалению. В публикации заявки на патент US №2004/0068017 (Bausch & Lomb Inc.) описываются замещенные бензилиденгидразины, способные повышать активность желатиназы А в клетках глаза. Эти соединения нашли применение в лечении первичной открытоугольной глаукомы. В публикации WO 2008/061647 (Acure Pharma АВ) описывается использование N-(2-хлор-3,4-диметоксибензилиденамино)гуанидина в качестве ингибитора рецепторов фактора роста эндотелия сосудов (VEGFR) и связанные с ним применения при лечении или предотвращении нежелательного образования кровеносных сосудов в ходе опухолевого роста и/или при воспалительных состояниях. В публикации WO 2005/031000 (Acadia Pharmaceuticals, Inc.) описываются замещенные бензилиденгидразины и их применение при лечении острой боли и хронической нейропатической боли. Наконец, в Европейском патенте №ЕР 1908464 (CNRS) описываются гуанабенз и хлоргуанабенз и их применение при лечении заболеваний, связанных с удлинением полиглутаминовьгх участков в белках, в частности болезни Хантингтона.
Недавно сообщалось, что гуанабенз обладает терапевтическим потенциалом в ряде других областей. Так, отмечено, что гуанабенз имеет антиприонную активность (D. Tribouillard-Tanvier et al., 2008, PLoS One 3, e1981). Сообщалось, что его активность в смысле защиты от неправильного сворачивания полипептидной цепи белка на удивление оказалась гораздо шире и включает ослабление накопления мутантного хантингтина в экспериментах с клетками (WO 2008/041133) и защиту от летальных эффектов экспрессии склонного к неправильному сворачиванию инсулина при мутации Akita в эндоплазматическом ретикулуме бета-клеток поджелудочной железы линий Min6 и INS-1 (P. Tsaytler, Н.P. Harding, D. Ron and A. Bertolotti, Science, 332, 1 April 2011, 91-94).
Также показано, что гуанабенз дозозависимым образом способствует выживанию клеток HeLa, подвергнутых потенциально цитотоксическому стрессу эндоплазматического ретикулума, вызванного ингибитором N-гликозилирования туникамицином (P. Tsaytler, Н.P. Harding, D. Ron and A. Bertolotti, Science, 332, 1 April 2011, 91-94). Количественное определение жизнеспособности клеток показало, что гуанабенз приводил к удваиванию числа выживающих клеток при стрессе эндоплазматического ретикулума при средней эффективной концентрации ~0,4 мкМ. Ни агонист α2-адренергических рецепторов клонидин, ни антагонист α2-адренергических рецепторов эфароксан не защищали клетки от цитотоксического стресса эндоплазматического ретикулума, причем эфароксан не влиял на защитный эффект гуанабенза (P. Tsaytler, Н.P. Harding, D. Ron and A. Bertolotti, Science, 332, 1 April 201 1, 91-94). Эти наблюдения говорят о том, что механизм спасения клеток от летального стресса эндоплазматического ретикулума под действием гуанабенза не зависит от α2-адренергических рецепторов. Гуанабенз защищает клетки от потенциально летального накопления неправильно свернутых белков путем связывания с регуляторной субъединицей фосфатазы 1, PPP1R15A (GADD34), в результате чего избирательно прекращается обусловленное указанным стрессом дефосфорилирование α-субъединицы фактора инициации трансляции 2 (eIF2α). Под действием гуанабенза в подвергнутых стрессу клетках устанавливается такой уровень трансляции, с которым могут справиться имеющиеся шапероны, и тем самым восстанавливается белковый гомеостаз. Сообщалось, что гуанабенз не связывается с конститутивной субъединицей фосфатазы PPP1R15B (CReP) и таким образом не подавляет трансляцию в клетках, не испытывающих стресс (Р. Tsaytler, Н.P. Harding, D. Ron and A. Bertolotti, Science, 332, 1 April 2011, 91-94).
Невозможность поддерживать стабильность молекул белков (протеостаз) в эндоплазматическом ретикулуме путем клеточного ответа на неправильно свернутые белки (Unfolded Protein Response, UPR) считается фактором развития многих патологических состояний. Так, описанные в настоящем документе соединения, которые ингибируют фосфатазу eIF2 в ходе тонкой регуляции синтеза белков, могут принести пользу в лечении большого числа заболеваний, обусловленных стрессом, связанным с неправильным сворачиванием белков, в частности с накоплением неправильно свернутых белков.
В данном изобретении предлагаются новые соединения на основе структуры гуанабенза, которые могут иметь терапевтическое применение при лечении расстройств, связанных со стрессом, обусловленным неправильным сворачиванием белков, и в частности с накоплением неправильно свернутых белков.
Сущность изобретения
В первом своем аспекте данное изобретение относится к соединениям, описываемым формулой (I), или к их фармацевтически приемлемым солям.
где R1 представляет собой алкил, Cl, F или Br;
R2 представляет собой Н или F;
R3 выбирают из Н и алкила;
R4 выбирают из Н и C(O)R6;
R5 представляет собой Н;
или R4 и R5 соединены, образуя гетероциклическую группировку, которая необязательно является замещенной одной иди более группами R10;
R6 выбирают из R7, OR7 и NR8R9;
R7, R8 и R9 независимо друг от друга выбирают каждый из алкила, циклоалкила, аралкила, циклоалкенила, гетероциклила и арила, каждый из которых необязательно является замещенным одной или более группами R10;
каждая группа R10 независимо от других выбирается из галогена и групп ОН, CN, СОО-алкила, аралкила, SO2-алкила, SO2-арила, СООН, СО-алкила, СО-арила, NH2, NH-алкила, N(алкил)2, CF3, алкила и алкокси-группы;
X и Z независимо друг от друга каждый представляет собой CR11, a Y выбирают из CR11 и N;
R11 представляет собой Н или F;
для применения при лечении расстройств, связанных со стрессом, обусловленным неправильным сворачиванием белков, и, в частности, с накоплением неправильно свернутых белков.
Ранее проведенные исследования показали, что для того, чтобы обсуждаемые соединения проявляли полезную фармакологическую активность, арильная группа должна быть по меньшей мере двухзамещенной (см., например, D. Tribouillard-Tanvier et al, PLoS One 3, e1981 (2008) и EP 1908464 A, CNRS). Однако в противоположность ранее проведенным исследованиям заявитель обнаружил, что однозамещенные арильные производные тоже обладают желаемой активностью.
Кроме того, соединения, описываемые формулой (I), приведенной выше, предпочтительно не проявляют активности в отношении адренергических α2А-рецепторов по сравнению с ранее известными соединениями, например гуанабензом (фиг. 4). Это отсутствие активности в отношении α2 адренергических рецепторов приводит к тому, что соединения по настоящему изобретению полезны при лечении расстройств, связанных со стрессом, обусловленным неправильным сворачиванием белков, и, в частности, с накоплением неправильно свернутых белков, например болезни Шарко-Мари-Тута (СМТ), заболеваний сетчатки (предпочтительно пигментного ретинита, RP), болезни Альцгеймера (AD), болезни Паркинсона (PD), бокового амиотрофического склероза (ALS), болезни Хантингтона (HD), таупатий, прионных заболеваний, диабета (предпочтительно диабета типа 2) и рака. Отсутствие активности в отношении адренергических α2 рецепторов означает, что соединения, описываемые формулой (I), можно вводить пациентам в дозировке, подходящей для лечения упомянутых выше заболеваний, без какого-либо существенного влияния на кровяное давление.
Во втором своем аспекте данное изобретение относится к соединениям, описываемым формулой (II), или к их фармацевтически приемлемым солям,
где R1 представляет собой алкил, Cl, F или Br;
R2 представляет собой Н или F;
R3 выбирают из Н и алкила;
R4 выбирают из Н и С(O)R6;
R5 представляет собой Н;
или R4 и R5 соединены, образуя гетероциклическую группировку, которая необязательно является замещенной одной иди более группами R10;
R6 выбирают из R7, OR7 и NR8R9;
R7, R8 и R9 независимо друг от друга выбирают каждый из алкила, циклоалкила, аралкила, циклоалкенила, гетероциклической группы, арила и гетероарила, каждый из которых необязательно является замещенным одной или более группами R10;
каждая группа R10 независимо от других выбирается из галогена и групп ОН, CN, СОО-алкила, аралкила, SO2-алкила, SO2-арила, СООН, СО-алкила, СО-арила, NH2, NH-алкила, N(алкил)2, CF3, алкила и алкокси-группы;
X и Z независимо друг от друга каждый представляет собой CR11, a Y представляет собой N;
R11 представляет собой Н или F.
В третьем своем аспекте данное изобретение относится к соединениям, описываемым формулой (III), или к их фармацевтически приемлемым солям,
где R1 представляет собой алкил, Cl, F или Br;
R2 представляет собой Н или F;
R3 выбирают из Н и алкила;
R4 представляет собой C(O)R6;
R5 представляет собой Н;
или R4 и R5 соединены, образуя гетероциклическую группировку, которая необязательно является замещенной одной иди более группами R10;
R6 выбирают из R7, OR7 и NR8R9;
R7, R8 и R9 независимо друг от друга выбирают каждый из алкила, циклоалкила, аралкила, циклоалкенила, гетероциклической группы, арила и гетероарила, каждый из которых необязательно является замещенным одной или более группами R10;
каждая группа R10 независимо от других выбирается из галогена и групп ОН, CN, СОО-алкила, аралкила, SO2-алкила, SO2-арила, СООН, СО-алкила, СО-арила, NH2, NH-алкила, N(алкил)2, CF3, алкила и алкокси-группы;
X и Z независимо друг от друга каждый представляет собой CR11, a Y выбирают из CR11 и N; и
R11 представляет собой H или F.
В четвертом своем аспекте данное изобретение относится к соединениям, описываемым формулой (IV), или к их фармацевтически приемлемым солям,
где R1 представляет собой алкил или Br;
R2 представляет собой Н;
R3 выбирают из Н и алкила;
R4 выбирают из Н и C(O)R6;
R5 представляет собой Н;
или R4 и R5 соединены, образуя гетероциклическую группировку, которая необязательно является замещенной одной иди более группами R10;
R6 выбирают из R7, OR7 и NR8R9;
R7, R8 и R9 независимо друг от друга выбирают каждый из алкила, циклоалкила, аралкила, циклоалкенила, гетероциклила и арила, каждый из которых необязательно является замещенным одной или более группами R10;
каждая группа R10 независимо от других выбирается из галогена и групп ОН, CN, СОО-алкила, аралкила, SO2-алкила, SO2-арила, СООН, СО-алкила, СО-арила, NH2, NH-алкила, N(алкил)2, CF3, алкила и алкокси-группы;
X и Z независимо друг от друга каждый представляет собой СН, a Y представляет собой CR11;
R11 представляет собой Н или F.
В другом своем аспекте данное изобретение относится к фармацевтическим композициям, содержащим соединения, описываемые формулой (II), (III) или (IV), как описано выше, смешанные с подходящими фармацевтически приемлемыми разбавителями, носителями или эксципиентами.
Осуществление изобретения
Термин «алкил» в настоящем документе включает насыщенные алкильные группы с неразветвленной или с разветвленной цепью, которые могут быть замещенными (моно- или полизамещенными) либо незамещенными. Предпочтительно алкильные группы в контексте данного изобретения содержат 1-20 атомов углерода (C1-20-алкилы), более предпочтительно 1-15 атомов углерода (С1-15-алкилы), еще более предпочтительно 1-12 атомов углерода (С1-12-алкилы), еще более предпочтительно 1-6 атомов углерода (С1-6-алкилы), более предпочтительно 1-3 атомов углерода (С1-3-алкилы). Особенно предпочтительные по данному изобретению алкильные группы включают, например, метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил, пентил и гексил. Подходящие заместители включают, например, одну или более групп R10. Предпочтительно алкильная группа по данному изобретению является незамещенной.
Термин «циклоалкил» в настоящем документе относится к циклическим алкильным группам, которые могут быть замещенными (моно- или полизамещенными) либо незамещенными. Предпочтительно циклоалкильные группы в контексте данного изобретения содержат 3-12 атомов углерода (С3-12-циклоалкилы). Подходящие заместители включают, например, одну или более групп R10.
Термин «алкенил» в настоящем документе относится к группам, содержащим одну или более двойных связей между атомами углерода, причем эти группы могут быть разветвленными или неразветвленными, замещенными (моно- или полизамещенными) либо незамещенными. Предпочтительно алкенильные группы в контексте данного изобретения содержат 2-20 атомов углерода (С2-20-алкенилы), более предпочтительно 2-15 атомов углерода (С2-15-алкенилы), еще более предпочтительно 2-12 атомов углерода (С2-12-алкенилы) или предпочтительно 2-6 атомов углерода (С2-6-алкенилы), более предпочтительно 2-3 атома углерода (С2-3-алкенилы). Подходящие заместители включают, например, одну или более групп R10, определенных выше. Термин «циклический алкенил» трактуется соответственно.
Термин «арил» в настоящем документе относится к ароматическим группам, содержащим 6-12 атомов углерода (С6-12-арилы), которые могут быть замещенными (моно- или полизамещенными) либо незамещенными. Типичные примеры арилов по данному изобретению включают фенил и нафтил и др. Подходящие заместители включают, например, одну или более групп R10.
Термин «гетероцикл» в настоящем документе (где он называется также гетероциклилом и гетероциклической группой) относится к замещенным (моно- или полизамещенным) либо незамещенным, насыщенным, ненасыщенным либо частично ненасыщенным циклическим группам, содержащим один или более гетероатомов, выбираемых из N, О и S, причем эти гетероциклические группы необязательно содержат также одну или более групп СО. Подходящие заместители включают, например, одну или более групп R10. Термин «гетероцикл» охватывает гетероарильные группы и гетероциклоалкильные группы, описанные ниже.
Термин «гетероарил» в настоящем документе относится к ароматическим группам, содержащим 2-12 атомов углерода (С2-12-группы), которые могут быть замещенными (моно- или полизамещенными) либо незамещенными и содержат один или более гетероатомов. Предпочтительно гетероарильные группы по данному изобретению содержат 4-12 атомов углерода (ароматические С4-12-группы) и один или более гетероатомов, выбираемых из N, О и S. Подходящие гетероарильные группы включают пиррол, пиразол, пиримидин, пиразин, пиридин, хинолин, тиофен, 1,2,3-триазол, 1,2,4-триазол, тиазол, оксазол, изотиазол, изооксазол, имидазол, фуран и т.п. Опять-таки подходящие заместители включают, например, одну или более групп R10.
Термин «гетероциклоалкил» в настоящем документе относится к замещенным (моно- или полизамещенным) либо незамещенным циклическим алифатическим группам, содержащим один или более гетероатомов. Предпочтительные гетероциклоалкильные группы включают пиперидинил, пирролидинил, пиперазинил, тиоморфолинил и морфолинил. Более предпочтительно гетероциклоалкильные группы выбирают из N-пиперидинила, N-пирролидинила, N-пиперазинила, N-тиоморфолинила и N-морфолинила. Подходящие заместители включают, например, одну или более групп R10.
Термин «аралкил» в настоящем документе включает (но не ограничивается перечисленным здесь) группы, обладающие как арильными, так и алкильными функциональными элементами. Так, к примеру, этот термин включает группы, в которых один из атомов водорода алкильной группы замещен арильной группой, например фенильной группой, в которой необязательно имеются один или более заместителей, например галоген, алкил, алкоксильная группа, гидроксильная группа и т.п. Типичные аралкильные группы по данному изобретению включают бензил, фенэтил и т.п.
В одном из предпочтительных воплощений данного изобретения R1 представляет собой Cl, Br, Me или F, более предпочтительно О.
В одном из предпочтительных воплощений данного изобретения R2 представляет собой Н.
В одном из предпочтительных воплощений данного изобретения Y представляет собой CR11.
В другом предпочтительном воплощении данного изобретения Y представляет собой N.
В одном из предпочтительных воплощений данного изобретения R3 и R4 оба представляют собой Н.
В одном из предпочтительных воплощений данного изобретения R3 представляет собой Н и R4 представляет собой C(O)R6.
В одном из предпочтительных воплощений данного изобретения R6 представляет собой алкильную или алкоксильную группу, более предпочтительно метил (Me) или ОМе.
В одном из предпочтительных воплощений данного изобретения R4 и R5 соединены, образуя гетероциклическую группу, необязательно замещенную одной или более группами R10.
В одном из предпочтительных воплощений данного изобретения указанное соединение является соединением, описываемым формулой (Ia), или какой-либо его фармацевтически приемлемой солью,
где R1, R2, R3 и R10 определены выше.
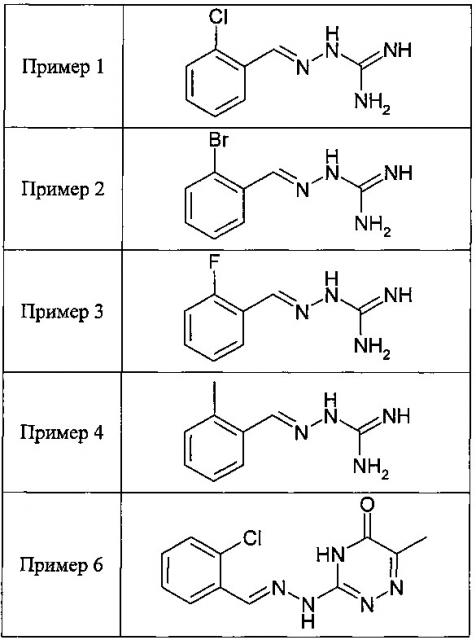
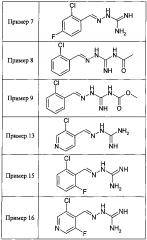
В одном особенно предпочтительном воплощении данного изобретения соединение, описываемое формулой (I), выбирают из следующих:
и их фармацевтически приемлемых солей.
В одном очень предпочтительном воплощении данного изобретения соединение, описываемое формулой (I), выбирают из соединений, представленных в этой таблице как Примеры 1, 3, 6 и 15.
Еще более предпочтительно, чтобы соединение, описываемое формулой (I), выбирали из Примеров 1 и 15, более предпочтительны Примера 1, то есть являлось 1-[(Е)-[(2-хлорфенил)метилиден]амино]-гуанилином.
Соединения
В одном из своих аспектов данное изобретение относится к соединениям, описываемым формулами (II), (III) или (IV), или к их фармацевтически приемлемым солям, определенным выше. Предпочтительные аспекты данного изобретения применимы mutatis mutandis (с необходимыми изменениями). Особенно предпочтительные соединения по этому аспекту данного изобретения включают описанные здесь соединения, обозначенные как Примеры 7, 8, 9,13 и 16.
Терапевтические применения
Заявитель показал, что соединения, описываемые формулой (I), можно применять терапевтически при лечении расстройств, связанных с накоплением неправильно свернутых белков. В частности, было показано, что соединения, описываемые формулой (I), защищают от цитотоксического стресса эндоплазматического ретикулума и возрастных расстройств.
Другой аспект данного изобретения относится к применению соединений, описываемых формулой (I) и определенных выше, при получении медикаментов для лечения расстройств, связанных со стрессом, обусловленным неправильным сворачиванием белков, и, в частности, с накоплением неправильно свернутых белков.
Словосочетание «получение медикамента» в настоящем документе включает применение одного или более из описанных выше соединений непосредственно в качестве медикамента, а также их использование для скрининга других активных агентов или на любой стадии изготовления такого медикамента.
Еще один аспект данного изобретения относится к способу лечения расстройств, связанных со стрессом, обусловленным неправильным сворачиванием белков, и, в частности, с накоплением неправильно свернутых белков, у нуждающихся в этом индивидов, причем указанный способ включает введение указанному индивиду терапевтически эффективного количества соединения, описываемого формулой (I) и определенного выше.
Термин «способ» в настоящем документе относится к видам, средствам, методам и методикам действия, предназначенным для осуществления поставленной задачи, включая (но не ограничиваясь перечисленным здесь) такие виды, средства, методы и методики действия, которые либо известны практикующим специалистам в областях химии, фармакологии, биологии, биохимии и медицины, либо с легкостью разрабатываются из известных в этих областях видов, средств, методов и методик действия.
Термин «лечение» в настоящем документе включает нейтрализацию, существенное подавление, замедление или обращение прогрессирования заболевания или расстройства, существенное ослабление клинических симптомов заболевания или расстройства или существенное предотвращение возникновения клинических симптомов заболевания или расстройства.
Термин «терапевтически эффективное количество» в настоящем документе относится к такому количеству вводимого индивиду соединения, которое обеспечивает ослабление в некоторой степени одного или симптомов заболевания или расстройства, подлежащих лечению.
Клеточный ответ на неправильно свернутые белки (Unfolded Protein Response, UPR) является компонентом защитной системы клетки, которая приспосабливает сворачивание белков в эндоплазматическом ретикулуме к изменяющимся условиям. UPR активируется при накоплении несвернутых или неправильно свернутых белков в просвете эндоплазматического ретикулума. При этом UPR решает две задачи: (i) восстановление нормального функционирования клетки путем приостановления трансляции (синтеза белков) и (ii) активация сигнальных механизмов, ведущих к увеличению образования молекул-шаперонов, участвующих в сворачивании белков. Если эти цели не достигаются в пределах некоторого промежутка времени или приостановка трансляции продолжается, UPR нацеливается на апоптоз.
Вышележащими (upstream) компонентами клеточного ответа на неправильно свернутые белки являются находящиеся в эндоплазматическом ретикулуме трансмембранные белки IRE1, ATF6 и PERK, которые реагируют (т.е.активируются) при дефектах фолдинга для того, чтобы согласованным образом воздействовать на транскрипцию и трансляцию и восстановить протеостаз. Активированные IRE1 и ATF6 вызывают усиление транскрипции генов, продукты которых участвуют в сворачивании белков в эндоплазматическом ретикулуме, например генов, кодирующих шапероны BiP и GRP94. Активированный белок PERK вызывает ослабление синтеза белков в целом, фосфорилируя субъединицу фактора инициации трансляции 2 (eIF2α) по остатку серина в положении 51 и в то же время способствуя трансляции фактора транскрипции ATF4. Последний регулирует экспрессию другого фактора транскрипции - CHOP, который в свою очередь способствует экспрессии PPP1R15A/GADD34. Белок PPP1R15A, являющийся эффектором петли отрицательной обратной связи, прекращающей действие сигнального механизма UPR, приводит в действие каталитическую субъединицу фосфатазы 1 (РР1с), в результате чего eIF2α дефосфорилируется, так что синтез белков восстанавливается. Сбой механизма UPR вносит вклад во многие патологические состояния, которые могли бы быть купированы путем адекватной стимуляции этой адаптивной клеточной реакции. Избирательные ингибиторы индуцируемой стрессом эндоплазматического ретикулума фосфатазы PPP1R15A-PP1, дефосфорилирующей eIF2α, задерживают это дефосфорилирование и, следовательно, синтез белков именно и только в клетках, испытывающих указанный стресс, не влияя на синтез белка в клетках, не испытывающих такой стресс. Это продлевает полезные эффекты UPR. Временное ослабление синтеза белков полезно для клеток, испытывающих стресс, потому что при сокращении потока новосинтезированньгх белковых молекул увеличивается доступность шаперонов, что защищает от стресса, обусловленного неправильным сворачиванием белков (P. Tsaytler, Н.P. Harding, D. Ron and A. Bertolotti, Science, 332,1 April 2011, 91-94). Неизбирательные ингибиторы фосфатазы 2, дефосфорилирующей eIF2α, могут иметь нежелательные эффекты, поскольку непрерывное подавление трансляции губительно для клетки. В самом деле, у мышей ликвидация генетическими методами и PPP1R15A, и PPP1R15B приводит к гибели на ранних стадиях эмбрионального развития, что свидетельствует о губительности для организма в целом ингибирования обеих фосфатаз, дефосфорилирующих eIF2α, - PPP1R15A-PP1 и PPP1R15B-PP1. Напротив, ликвидация генетическими методами только PPP1R15A не имела вредных последствий в экспериментах на мышах (Harding et al., 2009, Proc. Natl. Acad. Sci. USA, 106, 1832-1837). Кроме того, можно ожидать, что специфичные ингибиторы PPP1R15A никак не влияют на клетки, не испытывающие стресс, связанный с неправильным сворачиванием белков, так как PPP1R15A не экспрессируется в отсутствие такого стресса. Таким образом, можно рассчитывать, что избирательные ингибиторы PPP1R15A безопасны. Неизбирательные ингибиторы обеих фосфатаз, дефосфорилирующих eIF2α, также могут оказаться полезными для лечения заболеваний, связанных с неправильным сворачиванием белков, если их использовать в дозах, вызывающих лишь частичное ингибирование указанных фосфатаз.
Защита клеток от стресса эндоплазматического ретикулума может быть определена количественно соответствующими аналитическими методами; например, ее можно определять, используя клетки HeLa, в которых стресс эндоплазматического ретикулума вызывают путем прибавления среды, содержащей туникамицин, представляющий собой смесь гомологичных нуклеозидных антибиотиков, ингибирующих ферменты трансферазы семейства UDP-HexNAc: полипренол-Р HexNAc-1-P и используемых для индукции ответа на несвернутые белки. Спустя некоторое время определяют жизнеспособность клеток в присутствии и в отсутствии соединений-ингибиторов, измеряя восстановление WST-8 в формазан с помощью стандартного аналитического набора для определения жизнеспособности клеток (например, Cell Viability Counting Kit-8 производства Dojindo). Защиту клеток от стресса эндоплазматического ретикулума выражают как увеличение (в процентах) числа жизнеспособных клеток (по сравнению с контролем) после стресса эндоплазматического ретикулума. Более подробно пригодные для такого определения аналитические методы представлены в разделе «Примеры».
В одном из предпочтительных воплощений данного изобретения соединение, описываемое формулой (I), способно продлевать защитный эффект клеточного ответа на белки ненативной конформации (UPR) по сравнению с контролем (т.е. при отсутствии ингибирующего соединения) по меньшей мере на 20%, более предпочтительно по меньшей мере на 30%, еще более предпочтительно по меньшей мере на 40%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, еще более предпочтительно по меньшей мере на 90%.
Заявителем было показано, что соединения, описываемые формулой (I), являются ингибиторами действия PPP1R15A-PP1, вызывающими защитный эффект. Предпочтительно указанные соединения обладают защитным эффектом, характеризующимся ЕС50 менее чем около 5 мкМ, более предпочтительно менее чем около 2 мкМ, еще более предпочтительно менее чем около 1 мкМ. Указанное соединение предпочтительно не имеет α2-адренергической активности. Таким образом, в одном из предпочтительных воплощений данного изобретения соединение, описываемое формулой (I), не проявляет никакой активности в функциональном тесте на α2-адренергическую активность.
Заявителем также было показано, что некоторые соединения, описываемые формулой (I), избирательно ингибируют PPP1R15A-PP1, тем самым продлевая защитный эффект клеточного ответа на неправильно свернутые белки (UPR) и спасая клетки от стресса, обусловленного неправильным сворачиванием белков. Таким образом, описанные в данном изобретении ингибиторы PPP1R15A-PP1 могут иметь терапевтические применения при лечении различных заболеваний, связанных со стрессом, обусловленным неправильным сворачиванием белков, и, в частности, с накоплением неправильно свернутых белков.
В одном из воплощений данного изобретения соединения, описываемые формулой (I), способны ингибировать ферменты PPP1R15A и PPP1R15B.
В одном из предпочтительных воплощений данного изобретения соединения, описываемые формулой (I), способны избирательно ингибировать PPP1R15A по сравнению с PPP1R15B.
В одном из предпочтительных воплощений данного изобретения соединения, описываемые формулой (I), предназначены для применения при лечении нейродегенеративных заболеваний, а именно тех, в механизме развития которых участвует накопление неправильно свернутых белков (Brown et al., 2012, Frontiers in Physiology, 3, Article 263).
В одном из особенно предпочтительных воплощений данного изобретения соединения, описываемые формулой (I), предназначены для применения при лечении заболеваний, выбираемых из болезни Шарко-Мари-Тута, тяжелого синдрома Дежерина-Сотта (Voermans et al., 2012, J. Peripher New Syst., 17(2), 223-5), заболеваний сетчатки (например, но не ограничиваясь перечисленным здесь, пигментного ретинита, цилиопатий сетчатки, макулярной дегенерации сетчатки, диабетической ретинопатии), болезни Альцгеймера, болезни Паркинсона, бокового амиотриофического склероза, болезни Хантингтона, таупатий, прионных заболеваний, диабета типа 2 и/или типа 1, рака, например, но не ограничиваясь только ею, множественной миеломы.
В одном из своих воплощений данное изобретение относится к соединениям, описываемым формулой (I) и определенным выше, предназначенным для применения при лечении расстройств, связанных с механизмом фосфорилирования eIF2α, в развитии которых участвует накопление неправильно свернутых белков. Предпочтительно такое расстройство связано с ферментом PPP1R15A. Примеры таких расстройств включают заболевания, обусловленные неправильным сворачиванием белков, например (не ограничиваясь перечисленным здесь) болезнь Шарко-Мари-Тута, тяжелый синдром Дежерина-Сотта и пигментный ретинит.
В другом своем воплощении данное изобретение относится к соединениям, описываемым формулой (I) и определенным выше, предназначенным для применения при лечении расстройств, обусловленных или сопровождающихся, или связанных с фосфорилированием eIF2α и/или активностью фермента PPP1R15A.
В другом своем воплощении данное изобретение относится к соединениям, описываемым формулой (I) и определенным выше, предназначенным для применения при лечении расстройств клеточного ответа на неправильно свернутые белки (UPR), например (не ограничиваясь только этим) при старении (Naidoo et al., 2008, J Neurosci, 28, 6539-48).
Выражение «заболевание или расстройство, связанное с PPP1R15A» в настоящем документе относится к заболеваниям или расстройствам, характеризующимся аномальной активностью фермента PPP1R15A, в механизме развития которых участвует накопление неправильно свернутых белков. Термин «аномальная активность» относится к ситуациям, когда (i) PPP1R15A экспрессируется в клетках, в которых в норме нет экспрессии этого белка; (ii) имеет место усиленная экспрессия PPP1R15A или (iii) усилена активность PPP1R15A.
В другом своем воплощении данное изобретение относится к способу лечения млекопитающих, страдающих от патологического состояния, облегчаемого ингибированием PPP1R15A, в механизме развития которого участвует накопление неправильно свернутых белков, причем этот способ включает введение в организм указанного млекопитающего терапевтически эффективного количества соединения, описываемого формулой (I) и определенного выше.
В другом своем воплощении данное изобретение относится к ингибиторам PPP1R15A, описываемым формулой (I), или их фармацевтически приемлемым солям для применения при лечении расстройств, связанных со стрессом, обусловленным неправильным сворачиванием белков, и, в частности, с накоплением неправильно свернутых белков, и/или расстройств механизма клеточного ответа на неправильно свернутые белки (UPR), причем указанные соединения-ингибиторы не обладают активностью агонистов α2-адренергических рецепторов или обладают такой активностью в меньшей степени, чем гуанабенз.
В другом своем воплощении данное изобретение относится к ингибиторам PPP1R15A, описываемым формулой (I), или их фармацевтически приемлемым солям для применения при лечении расстройств, связанных со стрессом, обусловленным неправильным сворачиванием белков, и, в частности, с накоплением неправильно свернутых белков, и/или расстройств механизма клеточного ответа на неправильно свернутые белки (UPR), причем указанные соединения не ингибируют трансляцию в клетках, не испытающих стресс эндоплазматического ретикулума, в которых экспрессируется фермент PPP1R15B.
В другом своем воплощении данное изобретение относится к способу лечения расстройств, характеризующихся ответной активностью на стресс эндоплазматического ретикулума с накоплением неправильно свернутых белков, причем этот способ включает введение пациенту терапевтически эффективного количества по меньшей мере одного соединения, описываемого формулой (I), которое модулирует ответ на указанный стресс.
В другом своем воплощении данное изобретение относится к ингибиторам PPP1R15A, описываемым формулой (I), или их фармацевтически приемлемым солям для применения при лечении расстройств, связанных со стрессом, обусловленным неправильным сворачиванием белков, и, в частности, с накоплением неправильно свернутых белков, и/или расстройств механизма клеточного ответа на неправильно свернутые белки (UPR), причем указанные соединения действуют избирательно на холофосфатазу PPP1R15A-PP1 и не действуют на холофосфатазу PPP1R15B-PP1 или же эта активность понижена, а отношение (активность в отношении холофосфатазы PPP1R15A-РР1/активность в отношении PPP1R15B-PP1) для указанных соединений по меньшей мере равно такому отношению для гуанабенза или превышает его.
В другом своем воплощении данное изобретение относится к ингибиторам PPP1R15A, описываемым формулой (I), или их фармацевтически приемлемым солям для применения при лечении расстройств, связанных со стрессом, обусловленным неправильным сворачиванием белков, и, в частности, с накоплением неправильно свернутых белков, и/или расстройств механизма клеточного ответа на неправильно свернутые белки (UPR), причем
- указанные соединения обладают активностью в отношении холофосфотазы PPP1R15A-PP1 и не обладают активностью или обладают сниженной активностью в отношении холофосфотазы PPP1R15B-PP1; и
- отношение (активность в отношении холофосфотазы PPP1R15A-РР1/активность в отношении PPP1R15B-PP1) для указанных соединений по меньшей мере равно таковому отношению для гуанабенза или превышает его; и
- указанные соединения не обладают активностью агонистов α2-адренергических рецепторов или обладают такой активностью в меньшей степени, чем гуанабенз.
В настоящем документе заболевания или расстройства, отличающиеся наличием активного ответа на стресс эндоплазматического ретикулума, и/или заболевания или расстройства, связанные со стрессом, обусловленным неправильным сворачиванием белков, и, в частности, с накоплением неправильно свернутых белков, и/или расстройства клеточного ответа на неправильно свернутые белки (UPR) выбирают из болезни Шарко-Мари-Тута, тяжелого синдрома Дежерина-Сотта (Voermans et al., 2012, J. Peripher. New Syst, 17(2), 223-5), заболеваний сетчатки (например, но не ограничиваясь перечисленным здесь, пигментного ретинита, цилиопатий сетчатки, макулярной дегенерации сетчатки, диабетической ретинопатии), болезни Альцгеймера, болезни Паркинсона, бокового амиотриофического склероза, болезни Хантингтона, диабета (например, диабета типа 2, но не только его) и рака, такого как, множественная миелома, не ограниченного этим примером.
Болезнь Шарко-Мари-Тута
В одно