Способ идентификации корицы цейлонской, китайской, индонезийской и вьетнамской
Иллюстрации
Показать всеИзобретение относится к области аналитической химии, а именно к способам идентификации корицы цейлонской, китайской, индонезийской и вьетнамской. Для этого образцы корицы анализируют методом изотопной масс-спектрометрии, при этом определяют изотопный состав углерода (δ13С), азота (δ15N) и кислорода (δ18О). Полученные значения изотопного состава углерода, азота и кислорода подставляют в предварительно рассчитанные с использованием дискриминантного анализа функции F1-F4, характеризующие вид корицы: идентификацию корицы проводят выбирая максимальное значение дискриминантной функции.
F1 «Цейлонская» = -2263,68-126,18×δl3C+2,23×δl5N+33,42×δ18O;
F2 «Китайская» = -1978,64-104,82×δ13C-7,49×δl5N+48,25×δl8O;
F3 «Вьетнамская» = -2150,03-112,69×δ13С-14,01×δl5N+45,44×δ18O;
F4 «Индонезийская» = -2182,14-118,27×δ13C-10,14×δl5N+40,47×δ18O.
Изобретение позволяет идентифицировать четыре вида корицы при существенном сокращении продолжительности анализа со степенью достоверности 95%. 5 табл., 1 пр.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к области аналитической химии, а именно к способам идентификации корицы цейлонской, китайской, индонезийской и вьетнамской с использованием метода изотопной масс-спектрометрии легких элементов, и может применяться в практике аналитических лабораторий и лабораторий пищевой промышленности.
Уровень техники
Изобретение относится к области аналитической химии, а именно к способам идентификации корицы цейлонской, китайской, индонезийской и вьетнамской на основе определения изотопного состава углерода, азота и кислорода специи с последующим применением дискриминантного анализа.
Существует несколько видов корицы. Наиболее известными являются цейлонская, китайская, вьетнамская и индонезийская корицы. Цейлонская корица считается «настоящей» (Bruneton, J. Pharmacognosy, phytochemistry, medicinal plants / J. Bruneton // Paris, Lavoisier. 1995. P. 451-453), все остальные виды корицы классифицируются как кассия. Кассия считается заменителем цейлонской корицы более низкого качества, стоимость ее значительно ниже и в продаже кассию часто выдают за «настоящую» корицу. Поэтому идентификация вида корицы является важной и актуальной задачей.
Известен способ, позволяющий идентифицировать корицу цейлонскую и корицу китайскую по компонентам эфирного масла методом газовой хроматографии (Evdokimova O.V., Neneleva E.V., Tarrab I., Glazkova I.Y. Comparison of Lipophilic Substances of the Bark of Chinese (Cinnamomum cassia (L.) C. Presl.) and Ceylon Cinnamon (Cinnamomum zeylanicum Blume) // World Applied Sciences Journal. 2013. Vol. 27. Issue 1. P. 70-73), заключающийся в извлечении из исходного сырья методом паровой дистилляции эфирного масла и последующим разделением гексановых экстрактов на газовом хроматографе с пламенно-ионизационным детектором. Идентификацию компонентов проводят путем сопоставления времени удерживания стандартных образцов и компонентов анализируемой пробы. Идентификацию корицы осуществляют по наличию в хроматографическом профиле α-пинена, β-пинена, n-цимола, лимонена, камфоры, эвгенола и β-линоленовой кислоты, характерных для корицы цейлонской и отсутствующих в хроматографическом профиле корицы китайской.
Недостатком данного метода является длительная (трехчасовая) пробоподготовка, связанная с выделением эфирного масла, а также необходимость наличия стандартных образцов для идентификации соединений.
Известен способ, позволяющий различить корицу цейлонскую и корицу китайскую по липофильным и фенольным соединениям, выделенным из эфирного масла методом тонкослойной хроматографии (Ненелева Е.В. Сравнительное фармакогностическое изучение рода Cinnamomum L. как источника лекарственных средств. [Текст]: дис. канд. фарм. наук: 14.04.02: защищена 04.04.17 / Ненелева Елена Викторовна. - Санкт-Петербург, 2017. - 163 с.). Сущность метода заключается в том, что из молотой корицы гидродистилляцией получают эфирное масло, упаривают досуха на водяной бане, растворяют в толуоле и вместе со стандартным раствором наносят на хроматографическую пластинку, высушивают и просматривают в УФ-свете при 365 нм. Идентификацию корицы осуществляют по величинам Rf в сравнении со стандартным образцом, а также по характеру свечения и окраске пятен веществ на хроматограмме.
Недостатком данного способа также является длительная пробоподготовка, связанная с получением эфирного масла из исходного сырья.
Известен способ, позволяющий различить корицу цейлонскую, китайскую, вьетнамскую и индонезийскую по содержанию кумарина (Yan-Hong Wang, Bharathi Avula, N.P. Dhammika Nanayakkara, Jianping Zhao, and Ikhlas A. Khan Cassia Cinnamon as a Source of Coumarin in Cinnamon-Flavored Food and Food Supplements in the United States // Journal of Agricultural and Food Chemistry. 2013. Vol. 61. Issue 18. P. 4470-4476), заключающийся в определении содержания кумарина в метанольных экстрактах корицы с применением метода высокоэффективной жидкостной хроматографии с ультрафиолетовым и масс-спектрометрическим детектированием. Авторами показано, что содержание кумарина в цейлонской корице варьируется от 0,005 до 0,025 мг/г, в китайской корице - от 0,085 до 0,261 мг/г, в индонезийской и вьетнамской корице - от 1,06 до 9,30 мг/г.
Недостатком данного способа является отсутствие четко выделенных диапазонов содержания кумарина для индонезийской и вьетнамской корицы, что не позволяет отличить указанные виды друг от друга.
Наиболее близким к заявленному изобретению является способ, позволяющий различить корицу цейлонскую и кассию по изотопному составу водорода и углерода коричного альдегида, выделенного из эфирного масла корицы и кассии (Sewenig S., Hener U., Mosandl A. Online determination of 2H/1H and 13C/12C isotope ratios of cinnamaldehyde from different sources using gas chromatography isotope ratio mass spectrometry // European Food Res. Technol. 2003. Vol. 217. Issue 5. P. 444-448), который заключается в том, что методом паровой дистилляции из корицы получают эфирное масло и анализируют с использованием газового хроматографа, соединенного через интерфейс сжигания и пиролиза с изотопным масс-спектрометром. Рассчитывают изотопный состав углерода и водорода коричного альдегида и по установленным диапазонам определяют принадлежность исследуемого образца к корице цейлонской или кассии.
Основным недостатком данного способа является то, что предложенный авторами метод не позволяет разделить кассию на китайскую, вьетнамскую и индонезийскую, а также требует достаточно длительного времени на выделение эфирных масел. Сущность изобретения
Задачей данного изобретения является разработка относительно простого и надежного способа, позволяющего идентифицировать корицу при существенном сокращении продолжительности анализа и повышении достоверности определения.
Техническим результатом изобретения является способ идентификации корицы цейлонской, китайской, индонезийской и вьетнамской, отличающийся тем, что методом изотопной масс-спектрометрии определяют изотопный состав углерода (δ13С), азота (δ15N) и кислорода (δ18О) образцов корицы, подставляют полученные значения в предварительно рассчитанные с использованием дискриминантного анализа функции F1-F4:
F1 «Цейлонская» = -2263,68-126,18×δ13C+2,23×δ15N+33,42×δ18O,
F2 «Китайская» = -1978,64-104,82×δ13C-7,49×δ15N+48,25×δl8O,
F3 «Вьетнамская» = -2150,03-112,69×δ13C-14,01×δ15N+45,44×δ18O,
F4 «Индонезийская» = -2182,14-118,27×δ13C-10,14×δ15N+40,47×δ18O,
характеризующие вид корицы, и проводят идентификацию, выбирая максимальное значение дискриминантной функции.
Предлагаемый способ отличается от известных отсутствием стадии пробоподготовки, что значительно сокращает время анализа. Кроме того, разработанный с использованием дискриминантного анализа способ позволяет различать четыре вида корицы: цейлонскую, китайскую, вьетнамскую и индонезийскую, со степенью достоверности 95%.
Заявленный способ осуществляют следующим образом. В оловянные капсулы помещают измельченные образцы корицы массой 0,1 мг для определения изотопного состава углерода и 0,5 мг для определения изотопного состава азота, затем капсулы сворачивают и анализируют на изотопном масс-спектрометре Delta V Advantage, соединенном с элементным анализатором Flash 2000 посредством интерфейсного блока ConFlo 4 (производство Thermo Scientific, Германия). Температура окислительного реактора составляет 1020°С, восстановительного реактора - 650°С.
Для определения изотопного состава кислорода измельченные образцы корицы массой 0,2 мг заворачивают в серебряные капсулы и анализируют на изотопном масс-спектрометре Delta V Advantage, соединенном с пиролизатором ТС/ЕА FINNIGAN посредством интерфейсного блока ConFlo 4 (производство Thermo Scientific, Германия). Температура реактора пиролизатора составляет 1350°С.
Каждый образец анализируют не менее трех раз.
Проверку правильности измерений осуществляют по международным стандартам масла NBS 22 (δ13CVPDB = -29,7‰), мочевины Urea (δ15NAIR = -0,73‰) и бензойной кислоты IAEA-601 (δ18O = 23,3‰).
Изотопный состав углерода, азота и кислорода образцов корицы рассчитывают по формуле:
где A - элемент (углерод, азот, кислород);
Rобр и Rст - отношения распространенностей изотопов 13С/12С, l5N/14N, 18О/16О в анализируемом образце и стандарте соответственно.
Результаты изотопного анализа образцов корицы δ13С, δ15N, δ18О подставляют в предварительно полученные дискриминантные функции:
F1 = -2263,68-126,18×δ13C+2,23×δ15N+33,42×δ18O,
F2 = -1978,64-104,82×δ13C-7,49×δ15N+48,25×δl8O,
F3 = -2150,03-112,69×δ13C-14,01×δ15N+45,44×δ18O,
F4 = -2182,14-118,27×δ13C-10,14×δ15N+40,47×δ18O,
где F1 - «Цейлонская», F2 - «Китайская», F3 - «Вьетнамская», F4 - «Индонезийская» корицы.
Рассчитывают значения F1-F4 и по максимальному значению дискриминантной функции осуществляют идентификацию корицы (по принадлежности к одной из групп).
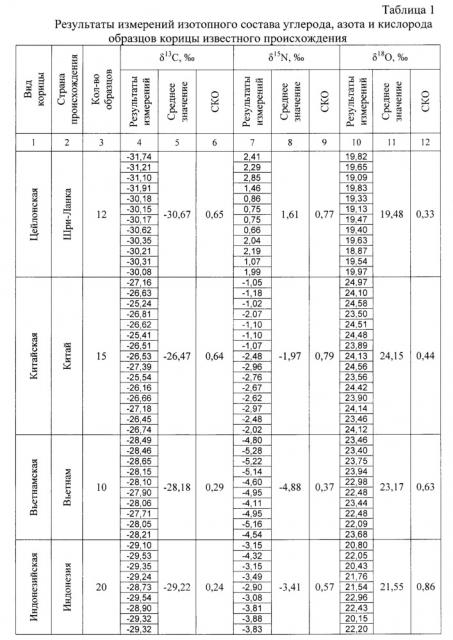
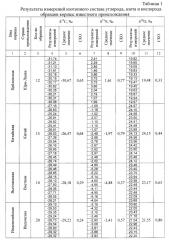
Для получения дискриминантных функций проводили изотопный анализ 57 образцов корицы известного происхождения (имеющих на упаковке маркировку с указанием страны происхождения), приобретенных в специализированных магазинах: 12 образцов цейлонской, 15 китайской, 10 вьетнамской и 20 индонезийской корицы.
Каждый образец анализировали не менее трех раз. Изотопный состав углерода, азота и кислорода образцов корицы рассчитывали по формуле 1.
Полученные результаты измерений изотопного состава образцов корицы представлены в таблице 1.
Используя полученные значения изотопного состава углерода, азота и кислорода образцов корицы известного происхождения, с помощью программного обеспечения STATISTICA 8.0 проводили дискриминантный анализ.
Затем с использованием теста на равенство средних в группах осуществляли выбор наиболее информативных переменных. Результаты теста представлены в таблице 2.
Индивидуальный вклад каждой переменной δ13С, δ15N, δ18O в общую дискриминацию различных видов корицы показывает значение F-критерия. Чем выше значение F-критерия, тем больше индивидуальный вклад соответствующей переменной в степень дискриминации. Значения F-критерия, представленные в таблице 2, показывают, что изотопный состав азота вносит наибольший вклад в общую дискриминацию, изотопный состав кислорода - наименьший. При этом все полученные значения F-критерия выше критического, что свидетельствует о статистической значимости всех переменных.
*Примечание: критическое значение F-критерия при α = 0,05 составляет 3,51
Влияние переменных δ13C, δ15N и δ18O на степень дискриминации описывается значением лямбды Уилкса: значения, близкие к 0, свидетельствуют о хорошей дискриминации, а значения, близкие к 1, свидетельствуют о плохой дискриминации. Как следует из данных, представленных в таблице 2, все значения показателя лямбда Уилкса близки к нулю, что подтверждает высокую степень дискриминации.
Следовательно, все переменные статистически значимые и вносят весомый вклад в процесс дискриминации.
Коэффициенты дискриминантных функций представлены в таблице 3.
Используя данные таблицы 3, составляют дискриминантные функции для каждой группы, которые имеют следующий вид:
F1 = -2263,68-126,18×δ13C+2,23×δ15N+33,42×δ18O,
F2 = -1978,64-104,82×δ13C-7,49×δ15N+48,25×δl8O,
F3 = -2150,03-112,69×δ13C-14,01×δ15N+45,44×δ18O,
F4 = -2182,14-118,27×δ13C-10,14×δ15N+40,47×δ18O,
где F1 - «Цейлонская», F2 - «Китайская», F3 - «Вьетнамская», F4 - «Индонезийская» корицы.
Принадлежность к той или иной группе определяется максимальным значением дискриминантной функции.
Качество дискриминации проверяют с использованием классификационной матрицы, представленной в таблице 4.
Полученная матрица классификации показывает, что все образцы, принадлежащие группам «Цейлонская» и «Китайская», распределены правильно. Один образец из группы «Вьетнамская» и два образца из группы «Индонезийская» классифицированы неверно. Достоверность классификации составляет 95%.
Примеры
Для подтверждения работоспособности заявленного способа использовали 4 образца корицы:
образец №1 - корица производства компании «Kotanyi», Польша. На упаковке указана страна происхождения Индонезия;
образец №2 - корица производства «RATHNA PRODUCERS CINNAMON EXPORTS PVT LTD», Шри-Ланка. На упаковке указана страна происхождения Шри-Ланка;
образец №3 - корица производства компании «Penzeys Spices», Китай. На упаковке указана страна происхождения Китай;
образец №4 - корица производства компании «KING ARTHUR FLOUR», Вьетнам. На упаковке указана страна происхождения Вьетнам.
В оловянные капсулы помещали измельченные образцы корицы №1-4 массой 0,1 мг для определения изотопного состава углерода и 0,5 мг для определения изотопного состава азота, затем капсулы сворачивали и анализировали на изотопном масс-спектрометре Delta V Advantage, соединенном с элементным анализатором Flash 2000 посредством интерфейсного блока ConFlo 4 (производство Thermo Scientific, Германия). Температура окислительного реактора составляла 1020°С, восстановительного реактора - 650°С.
Для определения изотопного состава кислорода измельченные образцы корицы №1-4 массой 0,2 мг заворачивали в серебряные капсулы и анализировали на изотопном масс-спектрометре Delta V Advantage, соединенном с пиролизатором ТС/ЕА FINNIGAN посредством интерфейсного блока ConFlo 4 (производство Thermo Scientific, Германия). Температура реактора пиролизатора составляла 1350°С.
Каждый образец анализировали не менее трех раз.
Результаты изотопного анализа δ13С, δ15N, δ18O образцов корицы №1-4 подставляли в предварительно рассчитанные дискриминантные функции F1-F4. Результаты классификации представлены в таблице 5. Максимальное значение дискриминантной функции (в таблице выделено жирным шрифтом) указывает на групповую принадлежность.
Из данных, представленных в таблице 5, следует, что в результате классификации образец №1 отнесен к корице индонезийской, образец №2 - к корице цейлонской, образец №3 - к корице китайской, а образец №4 - к корице вьетнамской, что соответствует информации, заявленной производителем.
Таким образом, разработанный способ позволяет идентифицировать корицу цейлонскую, китайскую, индонезийскую и вьетнамскую методом изотопной масс-спектрометрии легких элементов с последующим применением дискриминантного анализа с достоверностью 95%. Предложенный способ позволяет исключить стадию пробоподготовки и сократить время анализа до 20 минут.
Способ идентификации корицы цейлонской, китайской, индонезийской и вьетнамской, отличающийся тем, что методом изотопной масс-спектрометрии определяют изотопный состав углерода (δ13С), азота (δ15N) и кислорода (δ18О) образцов корицы, подставляют полученные значения в предварительно рассчитанные с использованием дискриминантного анализа функции F1-F4:
F1 «Цейлонская» = -2263,68-126,18×δ13C+2,23×δ15N+33,42×δ18O,
F2 «Китайская» = -1978,64-104,82×δl3C-7,49×δ15N+48,25×δ18O,
F3 «Вьетнамская» = -2150,03-112,69×δ13С-14,01×δ15N+45,44×δ18O,
F4 «Индонезийская» = -2182,14-118,27×δ13C-10,14×δ15N+40,47×δ18O,
характеризующие вид корицы, и проводят идентификацию, выбирая максимальное значение дискриминантной функции.