Бисфенольные производные флуорена, обладающие антимикоплазменной активностью, и способ их получения
Иллюстрации
Показать всеИзобретение относится к бисфенольным производным флуорена указанной ниже общей формулы 1, обладающим антимикоплазменной активностью, в которой L=OC(O), R1-R4 могут быть одинаковыми или различными и каждый независимо представляет Н, СООН, C(O)NHR5, R5 - фенил, замещенный метилом (за исключением случаев, когда R1=R2=R3=R4=H и R1=R2=R3=R4=C(O)OH). Изобретение относится также к способу получения указанных соединений и применению соединений общей формулы 1, в которой L=OC(O), R1-R4 могут быть одинаковыми или различными и каждый независимо представляет Н, СООН, C(O)NHR5, R5 - фенил, замещенный метилом, в качестве веществ, способных подавлять рост патогенных микоплазм путем воздействия на новые, ранее не использовавшиеся в клинической практике, архитектурные гистоноподобные HU-белки. 3 н. и 4 з.п. ф-лы, 4 ил., 2 табл., 5 пр.
Реферат
Область техники
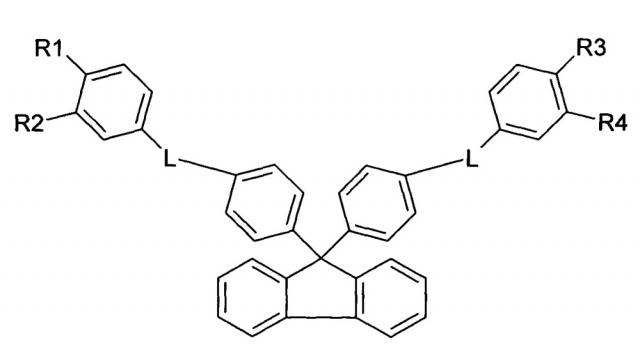
Изобретение относится к области фармакологии, медицины и ветеринарии и касается соединений общей формулы 1, содержащих несколько функциональных групп, связанных с ароматическими кольцами, и флуореновый фрагмент, которые обнаруживают бактерицидную активность по отношению к микоплазмам:
где L=OC(O); R1-R4 могут быть одинаковыми или различными и каждый независимо представляет Н, СООН, C(O)NHR5, R5 - фенил, замещенный метилом; исключая случаи, когда R1=R2=R3=R4=H и R1=R2=R3=R4=C(O)OH.
Уровень техники
Микоплазма (класс Mollicutes) представляет собой особый вид бактерий, у которых отсутствует жесткая клеточная стенка (Коротяев А.И., Бабичев С.А. Медицинская микробиология, иммунология и вирусология. СпецЛит. СПб., 2002, 470-591). Это самые маленькие из известных микроорганизмов (размер 300 нм), которые не видны в световом микроскопе. Микоплазмы относятся к грамположительным бактериям, но имеют редуцированный геном и ограниченные биосинтетические возможности, которые компенсируются паразитическим образом жизни, характеризующимся получением питательных веществ от организма хозяина (Chernova О.А., Medvedeva E.S., Mouzykantov А.А., Baranova N.B., Chernov V.M. Mycoplasmas and their antibioticresistance: the problems and prospectsin controlling infections. Acta Naturae, 2016, 8 (2), 24-34). Микоплазмы паразитируют в млекопитающих, рептилиях, рыбах, насекомых, артроподах, растениях, вызывая инфекционные заболевания у своих хозяев.
Для человека патогенны Mycoplasma genitalium, которая вызывает воспалительные процессы в мочеполовой системе мужчин и женщин, приводящие к бесплодию даже при бессимптомном носительстве (ВОЗ, 1994), а также Mycoplasma hominis, которая паразитирует на клетках слизистой оболочки, выстилающей желудочно-кишечный тракт, и Mycoplasma pneumoniae, которая поражает дыхательный эпителий. Паразитический образ жизни в клетках высших эукариот выработал у микоплазмы способность преодолевать защитные системы организма-хозяина, поэтому контроль микоплазменных инфекций представляет серьезную проблему (Борхсениус С.Н., Чернова О.А., Чернов В.М. Микоплазмы. Молекулярная и клеточная биология, взаимодействие с иммунной системой млекопитающих, патогенность, диагностика. Наука СПб., 2002). Находящиеся внутри клетки организма-хозяина микоплазмы защищены от действия многих лекарственных препаратов и поэтому устойчивы к действию большинства известных антибиотиков. Пенициллины, цефалоспорины, аминогликозиды не действуют на микоплазмы из-за отсутствия клеточной стенки, тетрациклины, макролиды (тилозин, тиамулин) и азалиды являются бактериостатиками и только препятствуют их размножению, рифампицины и сульфаниламиды недостаточно специфичны, фторхинолоны не проникают в уреаплазму из-за липофильности ее оболочки (Chernova О.A., etall, Mycoplasmas and Their Antibiotic Resistance: The Problems and Prospectsin Controlling Infections., ACTANATURAE, 2016, 8 (2), 24-34).
Низкая антимикоплазменная активность известных антибиотиков требует увеличения их дозировки и/или совместного применения в виде нескольких курсов в комплексе с сосудистыми, ферментными и антигистаминными препаратами, а также физиотерапевтическими процедурами. Но даже в этом случае трудно добиться полного уничтожения паразитов (Ильин И.И. и др. Размышления о лечении урогенитального хламидиоза. Вестник дерматол. и венер., 1994, 1, 30-33). Так, в случае инфекционных заболеваний, вызванных Mycoplasma genitalium, при использовании стандартных методов терапии полное излечение наблюдается лишь в 23-30% случаев, а в 15% - лечение не дает никакого результата (Козлова В.И. и Пухнер А.Ф. Вирусные, хламидийные и микоплазменные заболевания гениталий. М.: Авицена, 1995, с. 229-236 и 287-289, патент RU 2137483). Кроме того, повышенные дозы антибиотиков негативно воздействуют на нормальную микрофлору желудочно-кишечного тракта, что увеличивает риск развития дисбактериозов и сопутствующих им грибковых заболеваний и иммунных расстройств.
Проблема микоплазменных инфекций также актуальна в ветеринарии. У ряда домашних животных, например, у собак часто диагностируются урогенитальные заболевания, вызванные различными микоплазмами, причем передаваться возбудитель может как контактным, так и воздушно-капельным путем. А поскольку домашние животные находятся в тесном контакте с человеком, то существует опасность заражения людей в случае адаптации паразита к новому хозяину.
Микоплазменные инфекции также представляют серьезную проблему для агропромышленного комплекса. Например, Mycoplasma gallisepticum вызывает высококонтагиозные респираторные заболевания у сельскохозяйственной птицы, эпидемии которых причиняют серьезный экономический ущерб птицеводству (Бессарабов Б.Ф. и др. Респираторный микоплазмоз у кур: лекция МГ АБВМ и Б им. К.И. Скрябина. - М.: 1998; Коромыслов Н.И. Микоплазмозы в патологии животных. - М.: Агропромиздат, 1987). Медикаментозное лечение микоплазмоза птиц малоэффективно (Фармакологические препараты в ветеринарной медицине. - М.: Аквариум. - 2002, 734-735). Применяемые для антибиотикотерапии микоплазмоза птицы фторхинолоны вызывают развитие резистентности, которая только частично преодолевается при комбинированном использовании препаратов разных групп (Медведева Е.С. и др. Экстраклеточные везикулы микоплазм и формирование устойчивости бактерий к фторхинолонам. Доклады Академии Наук, Биохимия, Биофизика, Молекулярная биология, 2014, 454(6), 725-728). Поэтому единственным надежным способом предотвращения эпидемий микоплазмоза остается забой больной и находящейся с ней в контакте птицы.
В связи со всем вышеперечисленным разрабатываются превентивные способы борьбы с микоплазмозом птицы, например, путем использования профилактической вакцинации с помощью живой или инактивированной вакцины, к которым относятся вакцина инактивированная эмульсионная «АВИВАК-РМ» или живая рекомбинантная вакцина против оспы птиц и микоплазмоза птиц «Вектормун FP-MG».
Доступные вакцины имеют высокую стоимость и низкий уровень поствакцинального иммунитета.
Таким образом, получение новых синтетических препаратов, способных подавлять рост микоплазмы, весьма актуально для медицины и ветеринарии.
Анализ доступных литературных источников показал, что ранее были известны соединения, содержащие флуореновые фрагменты с п-гидроксифенильными заместителями в положении 9, которые обладали бактерицидной активностью по отношению к Bacillus subtilis, Pseudomonas aeruginosa, Staphylococcus aureus, (Ghaemy M., Aghakhani В., Taghavi M., Nasab SMA., Mohseni M. Synthesis and characterization of new imidazole and fluorene-bisphenolbased polyamides: Thermal, photophysical and antibacterial properties. Reactiveand Functional Polymers, 2013, 73 (3), 555-563), однако механизм антибактериального действия определен не был. Позднее у 9-замещенных производных флуорена была обнаружена антибактериальная активность по отношению к Mycobacterium tuberculosis, которая, как предположили авторы работы (Design, synthesis and evaluation of new GEQ derivatives as inhibitors of Inh Aenzyme and Mycobacterium tuberculosis growth. CholletA., MoriG., MenendezC., RodriguezF., FabingI., PascaM.R., MadackiJ., J., ConstantP., ., ., LherbetC., BaltasM. EurJMedChem., 2015, 101, 218-35), была связана с ингибированием фермента enoyl-ACPreductase (InhA).
Вышеперечисленные 9-замещенные производные флуорена только отчасти могут служить прототипами для настоящего изобретения, так как помимо значительных отличий в химической структуре они принципиально отличаются от патентуемых соединений как по механизму действия и клеточной мишени, так и по спектру антибактериальной активности.
Раскрытие изобретения
Техническим результатом данного изобретения является моделирование структуры молекулы и разработка методов синтеза новых смоделированных соединений, способных подавлять рост патогенных микоплазм путем воздействия на новые, ранее не использовавшиеся в клинической практике архитектурные гистоноподобные HU-белки, используемые в качестве белковой мишени.
Для достижения технического результата предложены бисфенольные производные флуорена общей формулы 1, обладающие антимикоплазменной активностью
где L=OC(O); R1-R4 могут быть одинаковыми или различными и каждый независимо представляет Н, СООН, C(O)NHR5, R5 - фенил, замещенный метилом; исключая случаи, когда R1=R2=R3=R4=H и R1=R2=R3=R4=C(O)OH.
Кроме того, L=OC(O); R1=R3=C(O)NHR5 и R2=R4=C(O)OH, или R1=R4=C(O)NHR5 и R2=R3=C(O)OH, или R2=R4=C(O)NHR5 и R1=R3=C(O)OH; R5=м-MePh.
Кроме того, L=OC(O), R1=R3=H, R2=R4=C(O)OH.
Для достижения технического результата предложен способ получения соединений общей формулы 1, заключающийся в окислении 9Н-флуорена, конденсации 9Н-флуорен-9-она с фенолом, О-ацилировании бисфенольного производного 9Н-флуорен-9-она, гидролизе или раскрытии циклического ангидрида ароматическим амином.
Кроме того, для получения соединения общей формулы 1, где L=OC(O); R1=R3=C(O)NHR5 и R2=R4=C(O)OH, или R1=R4=C(O)NHR5 и R2=R3=C(O)OH, или R2=R4=C(O)NHR5 и R1=R3=C(O)OH; R5=м-MePh, на последней стадии раскрытие циклического ангидрида осуществляют взаимодействием с м-толуидином.
Кроме того, для получения соединения общей формулы 1, где L=OC(O), R1=R3=H, R2=R4=C(O)OH, О-ацилирование бисфенольного производного 9Н-флуорен-9-она проводят взаимодействием с дихлорангидридом изофталевой кислоты и последующим гидролизом хлорангидрида нагреванием его водного раствора.
Применение бисфенольных производных флуорена общей формулы 1, где L=OC(O); R1-R4 могут быть одинаковыми или различными и каждый независимо представляет Н, СООН, C(O)NHR5, R5 - фенил, замещенный метилом, в качестве веществ, способных подавлять рост патогенных микоплазм путем воздействия на новые, ранее не использовавшиеся в клинической практике архитектурные гистоноподобные HU-белки.
В качестве белковой мишени были выбраны архитектурные гистоноподобные HU-белки присутствующие во всех бактериях, но отсутствующие у высших эукариот (Berger, М., A.Farcas, et al. Coordination of genomic structure and transcription by the main bacterial nucleoid-associated protein HU.EMBORep, 2010, 11(1), 59-64).
Для получения низкомолекулярных ингибиторов ДНК-связывающей активности HU белков, обладающих антимикоплазменной активностью, была использована пространственная структура HU белка микоплазмы Spiroplasma Melliferum, имеющая наилучшее разрешение по сравнению с доступными структурами аналогов (Воуkо K.М., Rakitina T.V., Korzhenevskiy D.A., Vlaskina A.V., Agapova Y.K., Kamashev D.E., Kleymenov S.Y. & Popov V.O. Structural basis of the high thermal stability of the histone-like HU protein from the mollicute Spiroplasma melliferum KC3. Sci Rep, 2016, 6, 36366.doi:10.1038/srep36366).
Для подготовки структуры к проведению молекулярного докинга использовали программы Modeller (Sali A. and Blundell T.L. Comparative protein modelling by satisfaction of spatial restraints. J MolBiol, 1993, 234(3), 779-815) и Mutate (Строганов О.В., Чилов Г.Г., Новиков Ф.Н. et al. Программа Mutate, 2011. Свидетельство о государственной регистрации программы для ЭВМ 2011615051).
Молекулярный докинг проводили с помощью программы Lead Finder (Stroganov O.V., Novikov F.N., Stroylov V.S., et al. Lead finder: an approach to improve accuracy of protein-ligand docking, binding energy estimation, and virtual screening. J Chemlnf Model, 2008, 48(12), 2371-85), используя виртуальную библиотеку соединений компании Vitas М laboratories (http://www.vitasmlab.com/). Структурную фильтрацию результатов проводили с помощью программы dock_filter (Novikov F.N., Stroylov V.S., Stroganov O.V., et al. Improving performance of docking-based virtual screening by structural filtration. JMolModel, 2010, 16(7), 1223-30), а визуализацию результатов моделирования - в программе VMD (HumphreyW., DalkeA., and K. Schulten. VMD: visualmoleculardynamics. JMolGraph, 1996, 14(1), 33-8).
Таким образом, технический результат достигался за счет того, что химическая структура патентуемых соединений, представляющих собой бисфенольные производные флуорена, обеспечивала их способность прочно связываться с HU белком, препятствуя тем самым образованию комплекса HU белок - ДНК, что вызывало нарушение протекания ДНК-зависимых процессов, включая транскрипцию и, как следствие, приводило к угнетению синтеза белков и к гибели микоплазмы.
Действие полученных соединений специфически направлено на белковый аппарат, обеспечивающий архитектуру бактериального генома, который в случае представителей класса Mollicute представлен исключительно гистоноподобными HU белками. Это обеспечивает избирательную активность бисфенольных производных флуорена в первую очередь в отношении паразитических микоплазм, тогда как их воздействие на более сложно-организованные бактерии, включая нормальную микробиоту желудочно-кишечного тракта, в значительной степени ослаблено, что существенно снижает риск развития дисбактериозов и сопутствующих им грибковых заболеваний и иммунных нарушений.
Краткое описание чертежей
На фиг. 1 показана общая формула 1 бисфенольных производных флуорена, включая их соли с фармакологически приемлемыми основаниями и/или гидраты, где L=OC(O); R1-R4 могут быть одинаковыми или различными и каждый независимо представляет Н, СООН, C(O)NHR5, R5 - фенил, замещенный метилом.
На фиг. 2 показано соединение общей формулы 1, где L=OC(O); R1=R3=C(O)NHR5 и R2=R4=C(O)OH или R1=R4=C(O)NHR5 и R2=R3=C(O)OH или R2=R4=C(O)NHR5 и R1=R3=C(O)OH; R5=м-MePh. Название соединения - 4,5'-(4,4'-(9H-флуорен-9,9-диил)бис(4,1-фенилен))бис(окси)-бис(оксометилен)бис(2-(м-толилкарбамоил)-бензойная кислота) - смесь региоизомеров.
На фиг. 3 показано соединение общей формулы 1, где L=OC(O), R1=R2=R3=R4=C(O)OH. Название соединения - 4,4'-(4,4'-(9H-флуорен-9,9-диил)бис(4,1-фенилен))бис(окси)-бис(оксиметилен)дифталевая кислота.
На фиг. 4 показано соединение общей формулы 1, где L=OC(O), R1=R3=H, R2=R4=C(O)OH. Название соединения - 3,3'-(4,4'-(9H-флуорен-9,9-диил)бис(4,1-фенилен))бис(окси)-бис(оксиметилен)дибензойная кислота.
Осуществление изобретения
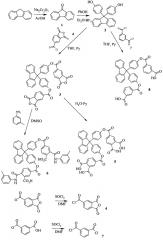
Синтез новых бисфенольных производных 9-флуорена общей формулы 1, показанных на фиг. 2-4, осуществлялся по схеме 1.
Исходные реагенты, используемые для синтеза, являются коммерчески доступными, промежуточные соединения были получены известными в литературе способами.
Структуры предпочтительных соединений, представленные на фиг 2-4, синтезированных в соответствии со схемой 1, подтверждались данными химического и спектрального анализа, а также другими физико-химическими характеристиками:
1. Синтез 4,5'-(4,4'-(9H-флуорен-9,9-диил)бис(4,1-фенилен))бис(окси)-бис(оксометилен)бис(2-(м-толилкарбамоил)бензойной кислоты - смесь региоизомеров: светло-желтое кристаллическое вещество, выход 59%. Элементный анализ C57H40N2O10. Вычислено С 75.00, Н 4.39, N 3.07, найдено С 75.21, Н 4.35, N 3.04;
2. Синтез 4,4'-(4,4'-(9H-флуорен-9,9-диил)бис(4,1-фенилен))бис(окси)-бис(оксиметилен)дифталевой кислоты: бежевое кристаллическое вещество, выход 60%. Элементный анализ С43Н26O12. Вычислено С 70.30, Н 3.54, найдено С 70.33, Н 3.52;
3. Синтез 4,4'-(4,4'-(9H-флуорен-9,9-диил)бис(4,1-фенилен))бис(окси)-бис(оксиметилен)дибензойной кислоты: белое кристаллическое вещество, выход 50%. Элементный анализ С41Н26O8. Вычислено С 19.81, Н 4.02, найдено С 19.79, Н 4.04.
Ниже постадийно описаны методики синтеза соединений, показанных на фиг. 2-4.
Пример 1. 9H-флуорен-9-он (1). 10.0 г (0.06 моль) 9H-флуорена растворяют в 100 мл уксусной кислоты, затем нагревают до 80°С, и в течение 1.5 ч порциями прибавляют 18.0 г (0.06 моль) дигидрата бихромата натрия, поддерживая при этом температуру 85-95°С. По окончании прибавления бихромата реакционную массу выдерживают 2 часа при той же температуре, затем нагревают до кипения и кипятят в течение 30 минут, массу охлаждают и при пониженном давлении отгоняют 60-70 мл уксусной кислоты, остаток выливают в 400 мл воды. Полученный осадок отфильтровывают, обильно промывают водой и сушат в вакуум-эксикаторе над NaOH. После этого продукт очищают методом флэш-хроматографии (силикагель 60 mesh, элюент - бензол), получая 8.7 г (80%) 9H-флуорен-9-она в виде желтых кристаллов с т. пл. 60-62°С.
4,4'-(9H-флуорен-9,9-диил)дифенол (2). В 50 мл четыреххлористого углерода растворяют 5.0 г (0.028 моль) 9H-флуорен-9-она и 7.8 г (0.084 моль) фенола, затем прибавляют 10.8 мл (11.9 г, 0.084 моль) эфирата трехфтористого бора и выдерживают реакционную массу 72 часа при комнатной температуре. По окончании выдержки реакционную массу промывают 100 мл воды, органический слой высушивают над б/в MgSO4, затем упаривают растворитель при пониженном давлении, остаток подвергают флеш-хроматографии (силикагель 60 mesh, элюент - гексан/этилацетат 2:1). Полученную после упаривания массу обрабатывают 30 мл смеси бензол/гексан 1:1. Полученный белый осадок отфильтровывают, промывают 20 мл смеси бензол/гексан 2:1, затем еще 20 мл гексана. Полученный продукт сушат в вакуум-эксикаторе над парафиновой стружкой, получая 8.0 г (81%) 4,4'-(9Н-флуорен-9,9-диил)дифенола (2) в виде белого порошка с т. пл. 232-233°С. Лит. т. пл. 224°C (Morgan P.W. Aromatic Polyesterswith Lange Cross-Plsnsr Sustituentis. Macromolecules, 1970, 3(5), 536-544).
4,4'-(9H-флуорен-9,9-диил)бис(4,1-фенилен) бис(1,3-диоксо-1,3-дигидроизобензофуран-5-карбоксилат) (3). В предварительно продутую аргоном колбу, содержащую раствор 6.0 г (0.028 моль) соединения 4 в 15 мл абсолютированного ТГФ, при интенсивном перемешивании по каплям прибавляют раствор 5.0 г (0.014 моль) соединение 2 и 3.4 мл (3.3 г, 0.042 моль) пиридина в 25 мл абсолютированного ТГФ, поддерживая температуру 0°С. По окончании прибавления реакционную массу выдерживают еще 3 ч при 0°С и 24 ч при комнатной температуре. По окончании выдержки выпавший осадок отфильтровывают, промывают небольшим количеством абсолютированного ТГФ, фильтрат упаривают при пониженном давлении, получая 9.8 г (99%) соединения (3) в виде порошка кремового цвета.
Элементный анализ С43Н22O10. Вычислено С 73.92, Н 3.17; Найдено С 73.68, Н 3.36.
ИК-спектр (KBr): 3 065 см-1 (С аром-Н), 1863 и 1782 см-1 (С=О), 1742 см-1 (С=O), 1502 см-1.
Спектр 1Н ЯМР (CDCl3), δ: 8.78 (с, 2Н), 8.68 (д, 2Н), 8.15 (д, 2Н), 7.80 (д, 2Н), 7.41 (м, 4Н), 7.33 (м, 6Н), 7.14 (д, 4Н).
1,3-диоксо-1,3-дигидро-изобензофуран-5-карбонил хлорид (4). Растворяют 5.0 г (0.026 моль) тримеллитового ангидрида в 3.1 мл (5.0 г, 0.0425 моль) тионилхлорида, добавляют несколько капель ДМФА, нагревают до кипения и кипятят при интенсивном перемешивании в течение 2.5 ч, затем охлаждают и отгоняют оставшийся тионилхлорид при пониженном давлении, остаток обрабатывают гексаном, получают 3.8 г (70%) соединения 4 в виде бежевого порошка с т. пл. 65-66°С. Лит. т. пл. 69°C (UlrichH., RichterR. 4-Isocyanatophthalic anhydride. Noveldifunctionalmonomer. J. Org. Chem., 1973, 38 (14), 2557-2558. DOI: 10.1021/jo00954a034).
4,4'-(4,4'-(9Н-флуорен-9,9-дии л)бис(4,1-фенилен))бис(окси)-бис(оксиметилен)дифталевая кислота (5) (фиг. 3). 200 мг соединения 3 перемешивают в смеси 5 мл воды и 0.5 мл пиридина в течение 0.5 ч, затем реакционную массу подкисляют 1 М соляной кислотой до рН 5, выпавший осадок отфильтровывают и промывают водой. Получают 120 мг (60%) соединения (5).
Пример 2. 4,5'-(4,4'-(9H-флуорен-9,9-диил)бис(4,1-фенилен))бис(окси)-бис(оксометилен)бис(2-(м-толилкарбамоил)-бензойная кислота) - смесь региоизомеров (6) (фиг. 2).
К раствору 200 мг (0.29 ммоль) соединения 3 в 1 мл ДМСО прибавляют 31 мг (0.30 ммоль) м-толуидина. Реакционную массу перемешивают в течение 1 ч и выливают в 5 мл воды. Выпавший осадок отфильтровывают и промывают водой. Получают 135 мг (59%) соединения (6).
Пример 3. 3,3'-(4,4'-(9Н-флуорен-9,9-диил)бис(4,1-фенилен))бис(окси)бис-(оксометилен)дибензойная кислота (8) (фиг. 4).
В предварительно продутую аргоном колбу, охлаждаемую ледяной баней, содержащую раствор 3.0 г (0.018 моль) дихлорангидрида изофталевой кислоты 7 в 25 мл абсолютного ТГФ, при интенсивном перемешивании по каплям прибавляют раствор 3.2 г (0.009 моль) соединения 2 и 2.2 мл (2.1 г, 0.026 моль) пиридина в 30 мл абсолютного ТГФ, поддерживая температуру 5-10°С. По окончании прибавления реакционную массу выдерживают еще 2 ч при комнатной температуре. Реакционную массу концентрируют в вакууме, к остатку добавляют 50 мл воды и выдерживают при 85-90°С 1 ч, получившуюся суспензию отфильтровывают, осадок промывают водой и затем кипятят с 50 мл метанола. Охлаждают, отфильтровывают осадок и промывают метанолом. Получают 2.9 г (50%) соединения (8) в виде порошка белого цвета. Спектр 1НЯМР (ДМСО-d6), δ: 8.60 (с, 2Н), 8.36-8.25 (м, 4Н), 7.98 (д, J=7.5 Гц, 2Н), 7.83-7.71 (м, 2Н), 7.54 (д, J=7.2 Гц, 2Н), 7.47-7.35 (м, 4Н), 7.25 (с, 8Н).
Дихлорангидрид изофталевой кислоты (7). Смесь 5.0 г (0.030 моль) изофталевой кислоты в 3.1 мл (5.0 г, 0.043 моль) тионилхлорида с несколькими каплями ДМФА кипятят при интенсивном перемешивании в течение 2.5 ч. Реакционную массу охлаждают и отгоняют избыток тионилхлорида при пониженном давлении, остаток используют в дальнейших превращениях, считая его как 95%-ный дихлорангидрид изофталевой кислоты.
Пример 4. Определение способности соединений ингибировать ДНК-связывающую активность микоплазменных HU белков. Влияние соединений, показанных на фиг. 2-4, на формирование комплексов HU белков S.melliferum (HUSpm) и M.gallisepticum (HUMgal) с модельной ДНК (синтетическими олигонуклеотидными дуплексами) тестировали с помощью метода торможения в геле (Electromobility shift assay, EMSA), традиционно используемого для исследования ДНК-связывающей способности белков. Данный метод основан на том, что белок, связываясь с олигонуклеотидом, тормозит его миграцию сквозь полиакриламидный гель в процессе электрофореза в нативных условиях (GarnerM. M., and Revzin A. AgelelectrophoresismethodforquantiryingthebindingofproteinstospeciIlcDNAregions: applicationtocomponentsoftheEscherichiacolilactoseoperonregulatorysystem. Nucleic Acids Res, 1981, 9, 3047-60).
В качестве контроля служил образец олигонуклеотида без добавления белка. Присутствие ингибитора препятствует образованию комплекса, а используя флуресцентно-меченый олигонуклеотидный дуплекс можно определить зависимость уменьшения количества ДНК, находящейся в комплексе, от концентрации ингибитора. При проведении EMSA использовали рекомбинантные белки HUSpm и HUMgal, полученные, как описано в работах (K. Boyko et al. Expression, purification, crystallization and preliminary X-ray crystallographic analysis of histone-like HU-protein from Spiroplasma melliferum KC3, ActaCryst. F (Structural Biology Communications) 2015, 71(1), 24-27 и Николаева А.Ю. и др. Выделение, очистка, кристаллизация и предварительное рентгеновское исследование кристаллов HU-белка из M.GALLISEPTICUM. Кристаллография, 2015, 60(6), 922-925) и олигонуклеотидные дуплексы, полученные на основе 5'- Су3-меченого олигонуклеотида длиной 24 п.о. CrD24: 5'-Су3-AGTGCAGTTGAGTCCTTGCTACGACGG-3'. Для получения дуплекса CrD отжигали путем инкубации при 90°С в течение 5 мин с последующим охлаждением в течение 1 часа с полностью комплементарным олигонуклеотидом CrJ24 (правильный дуплекс) или с укороченным олигонуклеотидом длиной 14 п.о. CrJ14: 5'-GACTCAACTGCАСТ-3' (дуплекс с выступающим 3'-концом длиной 10 п.о., overhang). Различные дуплексы использовали потому, что HU белки образуют более прочные комплексы с двухцепочечной ДНК, содержащей одноцепочечные разрывы, вставки или липкие концы, которые делают ДНК более гибкой. Отжиг дуплекса и реакцию образования комплекса проводили в буфере, содержащем 25 мМ Трис-HCl рН 8,0, 10% глицерин и 150 мМ NaCl. Для получения комплекса 0,4 пмоль дуплекса смешивали с 1 пмоль белка в присутствии различных концентраций соединений фиг. 2-4 или 10% (об./об.) диметилсульфоксида (ДМСО) в качестве контроля, т.к. все разведения соединений фиг. 2-4 готовили в ДМСО. Реакцию проводили в объеме 10 мкл при комнатной температуре в течение 5 мин. Затем образцы наносили на 12% полиакриламидный гель, в качестве буфера использовали 100 мМ Трис-боратр Н 8,3. Электрофорез проводили при 300 В и 10°С в течение 2 часов. Гели сканировали при помощи лазерного флюоресцентного анализатора Pharos FX MolecularImager (Bio-RadLaboratories), оцифровку изображений проводили в программе QuantityOne - 4.6.9 (Basic) (Bio-RadLaboratories). Построение кривых ингибирования и определение коэффициента 50% ингибирования (IC50) - концентрации ингибиторов, ингибирующих образование комплекса на 50%, производили при помощи программы Graph Pad Prism (Graph Pad Software, Inc.). Эксперименты повторяли по 2 раза с каждой парой олигонуклеотидных дуплексов. Так как использование разных дуплексов не влияло на ингибирующую активность соединений, результаты были объединены.
Пример 5. Определение способности соединений подавлять рост микоплазмы в культуре. Определение минимальной ингибирующей концентрации (МИК) соединений, показанных на фиг. 2-4, препятствующей росту микоплазмы в культуре, проводили методом микроразведений в жидкой среде (Tanner А.С., Wu С.С., Adaptation of the Sensititrebrothmicrodilution techniquetoantimicrobialsusceptibilitytestingofMycoplasmagallisepticum, Avian Dis. 36 (1992) 714-717). Штаммы S. MelliferumКС3 (паразитирующей на пчелах) и М. gallisepticumS6 (вызывающей респираторные заболевания домашней птицы) были получены из коллекции ФГБУН Института цитологии РАН. Культуры микоплазм культивировали, как описано в работе (Vanyushkina А.А., Fisunov G.Y., Gorbachev A.Y., Kamashev D.E., Govorun V.M. Metabolomic analysis of three Mollicutespecies. PLoS One, 2014, 9(3): e89312. doi: 10.1371/journal.pone.0089312). Перед добавлением ингибиторов культуры, находящиеся в поздне-логарифмической фазе роста, в 10 раз разводили содержащей глюкозу средой Mycoplasma Experience (ME) рН 7,6 и высевали в 96-луночные планшеты по 100 мкл клеточной суспензии в каждую лунку. В лунки добавляли последовательные двукратные разведения ингибиторов в диапазоне концентраций от 0.25 до 256 мкМ или 1% ДМСО (контроль) и инкубировали планшеты при 30°С до визуального изменения цвета культуры в контрольных лунках (обычно около 17 часов). При росте культуры в среде, содержащей глюкозу, в результате ферментации последней происходит закисление среды. Это приводит к изменению цвета среды, содержащей индикатор рН - феноловый красный, с красного на желтый, тогда как при полном ингибировании роста микоплазмы цвет среды не меняется. За МИК принимают минимальную концентрацию антибиотика, которая препятствует изменению цвета среды по сравнению с контролем.
Эксперименты проводили 2-3 раза, по три технических повтора в каждом.
1. Бисфенольные производные флуорена общей формулы 1, обладающие антимикоплазменной активностью,
где L=OC(O); R1-R4 могут быть одинаковыми или различными и каждый независимо представляет Н, СООН, C(O)NHR5, R5 - фенил, замещенный метилом; исключая случаи, когда R1=R2=R3=R4=H и R1=R2=R3=R4=C(O)OH.
2. Соединение по п.1, отличающееся тем, что L=OC(O); R1=R3=C(O)NHR5 и R2=R4=C(O)OH, или R1=R4=C(O)NHR5 и R2=R3=C(O)OH, или R2=R4=C(O)NHR5 и R1=R3=C(O)OH; R5=м-MePh.
3. Соединение по п.1, отличающееся тем, что L=OC(O), R1=R3=H, R2=R4=C(O)OH.
4. Способ получения соединений общей формулы 1 по п.1, заключающийся в окислении 9Н-флуорена, конденсации 9Н-флуорен-9-она с фенолом, О-ацилировании бисфенольного производного 9Н-флуорен-9-она, гидролизе или раскрытии циклического ангидрида ароматическим амином.
5. Способ по п.4 получения соединения общей формулы 1 по п.2, отличающийся тем, что на последней стадии раскрытие циклического ангидрида осуществляют взаимодействием с м-толуидином.
6. Способ по п.4 получения соединения общей формулы 1 по п.3, отличающийся тем, что О-ацилирование бисфенольного производного 9Н-флуорен-9-она проводят взаимодействием с дихлорангидридом изофталевой кислоты и последующим гидролизом хлорангидрида нагреванием его водного раствора.
7. Применение бисфенольных производных флуорена общей формулы 1, где L=OC(O); R1-R4 могут быть одинаковыми или различными и каждый независимо представляет Н, СООН, C(O)NHR5, R5 - фенил, замещенный метилом, в качестве веществ, способных подавлять рост патогенных микоплазм путем воздействия на новые, ранее не использовавшиеся в клинической практике, архитектурные гистоноподобные HU-белки.