Ингибитор ассоциированного с функцией лимфоцитов антигена-1 (lfa-1), способы его получения и его полиморф
Иллюстрации
Показать всеИзобретение относится к способу получения и очистки соединения формулы I или его соли, которое является эффективным ингибитором для лечения опосредованных ассоциированного с функцией лимфоцитов антигеном-1 (LFA-1) заболеваний, включающему стадии: а) проведения гидролиза соединения формулы АА: где R представляет собой углеродсодержащий фрагмент, с основанием в двухфазной среде; и b) выделения указанного соединения формулы I или его соли, причем указанный способ дополнительно включает очистку указанного соединения формулы I путем перекристаллизации с помощью водного раствора ацетона. Технический результат - получение соединения формулы I с оптической чистотой около 98%. 12 з.п. ф-лы, 10 ил., 1 табл., 11 пр.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка испрашивает приоритет на основании предварительной заявки на патент США №61/675663, поданной 25 июля 2012 г., предварительной заявки на патент США №61/680099, поданной 6 августа 2012 г. и предварительной заявки на патент США №61/729294, поданной 21 ноября 2012 г., полное содержание которых включено в настоящее описание посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
[0002] Было обнаружено, что соединение формулы I:
является эффективным ингибитором взаимодействий ассоциированного с функцией лимфоцитов антигена-1 (LFA-1) с семейством молекул межклеточной адгезии (ICAM) и обладает желаемыми фармакокинетическими свойствами, включая быстрый системный клиренс. Тем не менее, целесообразны усовершенствованные способы получения для обеспечения соединения формулы I с повышенной чистотой и/или со сниженным количеством используемых исходных веществ.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0003] Признаки, обеспечивающие новизну изобретения, изложены в прилагаемой формуле изобретения. Лучшее понимание признаков и преимуществ настоящего изобретения будет получено путем ссылки на последующее подробное описание с представленными в нем иллюстративными варианты реализации, в которых используются принципы настоящего изобретения, и прилагаемые графические материалы, на которых:
[0004] ФИГ. 1 представляет собой принципиальную схему, демонстрирующую соотношение между различными формами соединения формулы I.
[0005] ФИГ. 2 представляет собой принципиальную схему, демонстрирующую взаимные превращения между формами I, III и VI соединения формулы I.
[0006] ФИГ. 3 представляет собой диаграмму состояния трехфазной системы соединения формулы I в системе водного раствора ацетона.
[0007] ФИГ. 4 представляет собой графическое отображение дифрактограммы рентгеновской порошковой дифракции кристаллической формы II.
[0008] ФИГ. 5 представляет собой графическое отображение оптической микрофотографии кристаллической формы II.
[0009] ФИГ. 6 представляет собой графическое отображение спектра 1Н ЯМР кристаллической формы II.
[0010] ФИГ. 7 представляет собой графическое отображение термограммы дифференциальной сканирующей калориметрии (ДСК) кристаллической формы II.
[0011] ФИГ. 8 представляет собой графическое отображение термограммы термогравиметрического анализа (ТГА) кристаллической формы II.
[0012] ФИГ. 9 представляет собой графическое отображение кривой гравиметрической сорбции влаги для кристаллической формы II.
[0013] На ФИГ. 10 приведены сводные характеристики форм соединения формулы I.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0014] В первом аспекте настоящего изобретения предложены способы получения соединения формулы I:
или его соли. Согласно настоящему изобретению, такие способы включают стадии проведения гидролиза сложноэфирного предшественника с основанием в двухфазной среде, где указанная сложноэфирная группа предшественника представляет собой углеродсодержащий фрагмент или силилсодержащий фрагмент; и b) выделения соединения формулы I или его соли. В различных вариантах реализации настоящего изобретения указанная двухфазная среда включает водный раствор ацетона, такой как 30%-й водный раствор ацетона. В различных вариантах реализации настоящего изобретения указанная двухфазная среда меняется со временем, таким образом, что в ходе реакции реакционная смесь, являющаяся двухфазной в начале реакции, становится менее двухфазной или однофазной.
[0015] В различных вариантах реализации настоящего изобретения основание для проведения гидролиза представляет собой гидроксид натрия, например, в количестве, находящемся в диапазоне от примерно 1,0 до примерно 1,5 эквивалента, предпочтительно примерно 1,2 эквивалента.
[0016] В различных вариантах реализации настоящего изобретения указанный сложноэфирный предшественник включает сложноэфирную группу R, которая представляет собой замещенную или незамещенную группу, выбранную из низшей алкильной, низшей алкенильной, низшей алкинильной, цикло(низшей)алкильной, цикло(низшей)алкенильной, арильной, аралкильной, гетероциклильной и гетероарильной групп. Предпочтительно сложноэфирная группа R представляет собой бензильную группу.
[0017] В различных вариантах реализации настоящего изобретения предложены способы получения соединения формулы I, в которых требуется применение катализатора межфазного переноса для проведения катализируемого основанием гидролиза. В различных вариантах реализации настоящего изобретения катализатор межфазного переноса, представляет собой соль четвертичного аммония, такую как тетрабутиламмония гидроксид. Такие катализаторы межфазного переноса могут присутствовать в количестве, находящемся 6 диапазоне от примерно 0,01 эквивалента до примерно 0,5 эквивалента.
[0018] Во втором аспекте настоящего изобретения предложены композиции, которые представляют собой реакционные смеси, соответствующие способам получения соединения формулы I, описанным выше.
[0019] В третьем аспекте настоящего изобретения предложены способы очистки соединения формулы I посредством перекристаллизации. В различных вариантах реализации настоящего изобретения перекристаллизацию проводят с помощью водного раствора ацетона. Соответственно, предложены способы, включающие: а) получение неочищенного соединения формулы I или его соли и перекристаллизацию указанного неочищенного соединения с помощью водного раствора ацетона; и b) выделение соединения формулы I или его соли путем удаления водного раствора ацетона. Предпочтительно указанный водный раствор ацетона представляет собой примерно 30%-ный водный раствор ацетона. В различных вариантах реализации настоящего изобретения указанный водный раствор ацетона используют в количестве, составляющем примерно 7 объемов. Предпочтительно указанный способ осуществляют в течение периода времени, составляющего от примерно 1 часа до примерно 48 часов.
[0020] В четвертом аспекте настоящего изобретения предложены композиции, представляющие собой смеси после рекристаллизации, соответствующие способам очистки соединения формулы I, описанным выше.
[0021] В пятом аспекте настоящего изобретения предложено соединение формулы I, синтезированное согласно способам, описанным в настоящем документе, или перекристаллизованное согласно способам, описанным в настоящем документе, или и то, и другое. Предпочтительно указанное соединение по существу не содержит метилэтилкетона, В различных вариантах реализации настоящего изобретения соединение формулы I имеет энантиомерный избыток более чем примерно 96% после выделения его из реакционной смеси катализируемого основанием гидролиза и до перекристаллизации. В различных вариантах реализации настоящего изобретения соединение формулы I, синтезированное и/или перекристаллизованное согласно способам, предложенным в настоящем изобретении, имеет энантиомерный избыток более чем примерно 98%.
[0022] В шестом аспекте настоящего изобретения предложено соединение формулы I, где, указанное соединение представляет собой полиморфную форму II, описанную в настоящем документе. В различных вариантах реализации настоящего изобретения полиморфная форма II указанного соединения присутствует в твердой композиции с фармацевтически приемлемым носителем. В различных вариантах реализации настоящего изобретения указанная композиция содержит по меньшей мере примерно 50% по массе формы II или, в качестве альтернативы, менее чем примерно 5% по массе формы II. В различных вариантах реализации настоящего изобретения указанная твердая композиция дополнительно содержит одну или большее количество твердых форм, выбранных из группы, состоящей из аморфной формы, формы I, формы III, формы IV, формы V и формы VI.
ВКЛЮЧЕНИЕ ПОСРЕДСТВОМ ССЫЛКИ
[0023] Все публикации, патенты и заявки на патент, указанные в настоящем описании, включены в настоящее описание посредством ссылки в той же степени, как если бы в отношении каждой отельной публикации, патента или заявки на патент было бы конкретно и отдельно указано, что они включены посредством ссылки.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0024] Несмотря не то, что в настоящем описании представлены и описаны избранные варианты реализации настоящего изобретения, специалисту в данной области очевидно, что такие варианты реализации представлены только в качестве примера. Специалист в данной области может, без отклонения от настоящего изобретения, представить многочисленные вариации, изменения и замещения. Следует понимать, что при реализации изобретения на практике могут быть использованы различные альтернативы вариантов реализации настоящего изобретения, описанных в настоящем документе. Предполагается, что объем настоящего изобретения определен прилагаемой формулой изобретения и что данная формула изобретения охватывает способы и структуры, находящиеся в пределах объема пунктов формулы и их эквиваленты.
[0025] Определения
[0026] Если не указано иное, все технические и научные термины, используемые здесь, имеют такое же значение, как обычно понимается специалистом в области, к которой это изобретение принадлежит.
[0027] В описании и формуле изобретения термины в единственном числе, как в определенной, так и в неопределенной форме, включают данные термины в форме множественного числа, если из контекста явно не следует иное.
[0028] В настоящем описании термин «фармацевтически приемлемая соль» обозначает соли, которые являются подходящими для применения в фармации, предпочтительно для применения в тканях людей и низших животных без ненадлежащего раздражения, аллергических реакций и т.п. Фармацевтически приемлемые соли аминов, карбоновых кислот и других типов соединений хорошо известны в данной области техники. Например, С.М. Бердж (S.М. Berge) и др. подробно описывают фармацевтически приемлемые соли в. источнике J Pharmaceutical Sciences, 66: 1-19 (1977), включенном в настоящее описание посредством ссылки. Соли могут быть получены in situ в процессе конечного выделения и очистки соединений согласно настоящему изобретению или отдельно путем взаимодействия функциональной группы свободного основания или свободной кислоты с подходящим реагентом, как в общем описано ниже. Например, функциональная группа свободное основания может быть подвергнута взаимодействию с подходящей кислотой. Кроме того, если соединения согласно настоящему изобретению содержат кислотный фрагмент, подходящие фармацевтически приемлемые соли могут включать соли металлов, такие как соли щелочных металлов, например натриевые или калиевые соли, и соли щелочноземельных металлов, например кальциевые или магниевые соли. Примерами фармацевтически приемлемых нетоксичных кислотно-аддитивных солей являются соли по аминогруппе, образованные с неорганическими кислотами, такими как соляная кислота, бром истово дородная кислота, фосфорная кислота, серная кислота и хлорная кислота, или с органическими кислотами, такими как уксусная кислота, щавелевая кислота, малеиновая кислота, винная кислота, лимонная кислота, янтарная кислота или малоновая кислота, или с помощью других методов, применяемых в данной области, таких как ионный обмен. Другие фармацевтически приемлемые соли включают адипатные, альгинатные, аскорбатные, аспартатные, бензоатные, бисульфатные, боратные, бутиратные, камфоратные, камфорсульфонатные, цитратные, циклопентанпропионатные, диглюконатные, додецилсульфатные, формиатные, фумаратные, глюкогептонатные, глицерофосфатные, глюконатные, гемисульфатные, гептаноатные, гексаноатные, гидроиодидные, 2-гидрокси-этансульфонатные, лактобионатные, лактатные, лауратные, лаурилсульфатные, малатные, малеатные, малонатные, метансульфонатные, никотинатные, нитратные, олеатные, оксалатные, пальмитатные, пектинатные, персульфатные, 3-фенилпропионатные, фосфатные, пикратные, пивалатные, пропионатные, стеаратные, сукцинатные, сульфатные, тартратные; тиоцианатные, n-толуолсульфонатные, ундеканоатные, валератные соли и т.п. Примеры солей щелочных или щелочноземельных металлов включают соли натрия, лития, кадия; кальция, магния и т.п. Другие фармацевтически приемлемые соли включают, когда это уместно, нетоксичные аммонийные, четвертичные аммонийные и аминные катионы, образованные путем непосредственного взаимодействия с карбоновой кислотой лекарственного средства или посредством применения противоионов, таких как галогенид, гидроксид, карбоксилат, сульфат, фосфат, нитрат, сульфонат и арилсульфонат.
[0029] Термин «фармацевтически приемлемый носитель» или «фармацевтически приемлемое вспомогательное вещество» включает любые и все растворители, дисперсионные среды, покрытия, антибактериальные и противогрибковые агенты, изотонические и задерживающие всасывание агенты и тому подобное. Применение таких сред и агентов для фармацевтически активных веществ хорошо известно в данной области техники. За исключением тех случаев, когда обычные среды или агенты несовместимы с активным ингредиентом, в терапевтических композициях согласно настоящему изобретению предполагается их использование. В композиции также могут быть включены дополнительные активные ингредиенты.
[0030] Термин «пролекарство», как считается, обозначает соединение, которое в физиологических условиях или путем сольволиза может превращаться в биологически активное соединение, описанное в настоящем документе. Таким образом, термин «пролекарство» обозначает предшественник биологически активного соединения, который является фармацевтически приемлемым. Пролекарство может быть неактивным при введении субъекту, то есть быть в форме сложного эфира, но превращается in vivo в активное соединение, например, путем гидролиза с получением свободной карбоновой кислоты. Соединение, представляющее собой пролекарство, имеет преимущества в отношении растворимости, совместимости с тканями или отсроченного высвобождения в организме млекопитающего (см., например, Bundgard, Н., Design of Prodrugs (1985), pp.7-9, 21-24, (Elsevier, Амстердам). Обсуждение пролекарств приведено в Higuchi, Т., et al., "Pro-drugs as Novel Delivery Systems," A.C.S. Symposium Series, Vol.14 и в Bioreversible Carriers in. Drug Design, ed. Edward B. Roche, American Pharmaceutical Association and Pergamon Press, 1987, причем оба из указанных источников полностью включены в настоящее описание посредством ссылки. Также подразумевается, что термин "пролекарство" включает любые ковалентно связанные носители, которые высвобождают активное соединение in vivo, когда такое пролекарство ввели млекопитающему. Пролекарства активного соединения, описанного в настоящем документе, могут быть получены путем модификации функциональных групп, присутствующих в активном соединении, таким образом, что модификации расщепляются либо путем обычной манипуляции, либо in vivo, с получением родительского активного соединения. Пролекарства включают соединения, в которых гидрокси-, амино- или меркаптогруппа связана с любой группой, которая, когда пролекарство активного соединения ввели млекопитающему, расщепляется с образованием свободной гидрокси-, свободной амино- или свободной меркаптогруппы, соответственно. Примеры пролекарств включают, но не ограничиваются ими, ацетатные, формиатные и бензоатные производные спирта или ацетамидные, формамидные и бензамидные производные функциональной аминогруппы в активном соединении и т.п.
[0031] Термин «субъект» обозначает животное, такое как млекопитающее, например человека. Способы, описанные в настоящем документе, могут быть подходящими как для лечения людей, так и для применения в ветеринарных целях. В некоторых вариантах реализации настоящего изобретения пациент представляет собой млекопитающее, а в некоторых вариантах реализации пациент является человеком. В различных вариантах реализации настоящего изобретения пациент представляет собой животное, не являющееся человеком, такое как собака, кошка, кролик, мышь, крыса, корова, лошадь, свинья или курица.
[0032] Если не указано иное, подразумевается, что структуры, изображенные в настоящем документе, также включают соединения, которые отличаются только присутствием одного или более изотопно обогащенных атомов. Например, соединения, имеющие структуры, где водород заменен на дейтерий или тритий или углерод заменен на 13С- или 14С-обогащенный углерод, находятся в рамках объема настоящего изобретения.
[0033] Соединения согласно настоящему изобретению могут также содержать неестественные пропорции атомных изотопов при одном или нескольких атомах, которые, составляют такие соединения. Например, соединения могут быть помечены радиоактивными изотопами, такими как, например, тритий (3Н), иод-125 (125I) или углерод-14 (14С). Все изотопные варианты соединений согласно настоящему изобретению, вне зависимости от того, являются ли они радиоактивными или нет, включены в объем настоящего изобретения.
[0034] В тех случаях, когда для указания характеристик физических свойств, таких как молекулярная масса, или химических свойств, таких как химические формулы, используются диапазоны, подразумевается, что они включают все комбинации и подкомбинации диапазонов и конкретные их варианты. Термин «примерно» в отношении числа или числового диапазона означает, что данное число или числовой диапазон являются приблизительными в пределах экспериментальной изменчивости (или в пределах статистической ошибки эксперимента), и, таким образом, указанное число или числовой диапазон могут варьироваться в диапазоне, например, от 1% до 15% от заявленного числа или числового диапазона. Термин «содержащий» (и родственные термины, такие как «содержит», или «имеющий», или «включающий») включает варианты реализации; например, вариант реализации любого состава вещества, композиции, способа или процесса или тому подобного, при котором они «состоят из» или «по существу состоят из» описанных признаков.
[0035] Используемые в настоящем описании сокращения имеют их обычное для химической и биологической области значение.
[0036] Соединение формулы I
[0037] Было обнаружено, что соединение формулы I:
является эффективным ингибитором взаимодействий ассоциированного с функцией лимфоцитов антигена-1 (LFA-1) с молекулой межклеточной адгезии-1 (ICAM-1). Данное соединение является представителем класса прямых конкурентных ингибиторов LFA-1, которые непосредственно связываются с сайтом связывания ICAM на LFA-1 и, таким образом, препятствует связыванию ICAM. Прямые конкурентные ингибиторы LFA-1 могут обеспечить возможность более эффективного модулирования воспалительной и/или иммунологической реакции по сравнению реакцией, которую обеспечивают аллостерические ингибиторы, поскольку прямые конкурентные ингибиторы более эффективно перекрывают сайт связывания. Также в настоящее изобретение включены фармацевтически приемлемые, соли соединений формулы I. Дополнительная информация, относящаяся к соединению формулы I, может быть найдена в патенте США 8080562, патентной публикации США 2009/0298869, патентной публикации США 2011/0092707, патенте США 8084047, патентной публикации США 2010/0092542 и патентной публикации США 2006/0281739, причем полное содержание каждого из указанных источников включено в настоящее описание посредством ссылки.
[0038] Для разработки подходящих для клинического применения лекарственных средств лекарственные средства-кандидаты должны быть в достаточной степени химически чистыми, для введения субъекту и иметь приемлемую физическую форму, для того чтобы их можно было бы приготовить в виде в фармацевтически приемлемых лекарственных форм. Один из предпочтительных путей достижения более высокой чистоты, воспроизводимости физической формы и стабильности является идентификация одной или более подходящих кристаллических форм. Способность существовать в различных кристаллических формах известна как полиморфизм, и, как известно, имеет место для многих органических молекул. Эти различные кристаллические формы известны как «полиморфные модификации» или «полиморфы». Несмотря на то, что полиморфные модификации имеют одинаковый химический состав, они отличаются по упаковке, геометрическому расположению и другим описательным свойствам кристаллического твердого состояния. Как таковые, эти модификации могут иметь различные физические свойства в твердом состоянии, которые влияют, например, на растворимость, скорость растворения, биодоступность, химическую и физическую стабильность, текучесть, податливость (fractability) и сжимаемость соединения, а также безопасность и эффективность лекарственных продуктов, полученных на основе данных соединений. В процессе получения полиморфа также может быть осуществлена дальнейшая очистка с точки зрения общей физической чистоты или оптической чистоты.
[0039] Был обнаружен ряд различных форм, в том числе кристаллических форм, соединения формулы I, в том числе кристаллические формы А-Е и аморфная форма. Несмотря на то, что для органических соединений кристаллизацию проводят часто, невозможно предсказать заранее, какие условия будут обеспечивать подходящие условия, позволяющие получить, определенную кристаллическую форму. Кроме того, невозможно предсказать, какая, конкретная кристаллическая форма обеспечит необходимую совокупность физических свойств, неограничивающие примеры которых описаны выше, с получением желаемой лекарственной формы данного лекарственного средства в результате ее приготовления. Дополнительная информация, относящаяся к кристаллическим формам А-Е и аморфной форме соединения формулы I, может быть найдена в патенте США 8080562, патентной публикации США 2009/0298869, патентной публикации США 2011/0092707, патенте США 8084047, патентной публикации США 2010/0092542 и патентной публикации США 2006/0281739, причем полное содержание каждого из указанных источников включено в настоящее описание посредством ссылки.
[0040] Способы получения соединения формулы I
[0041] В одном из вариантов реализации настоящего изобретения соединение формулы I синтезируют, как показано на следующих схемах 1-7. В качестве конечного продукта этого; синтеза получают соединение формулы I в виде аморфного твердого вещества или в виде кристаллической формы, такой как формы А-Е, или его фармацевтически приемлемой соли, прямо или косвенно. Варианты этого общего пути синтеза могут обеспечить повышенные выходы, улучшенную стоимость продуктов и/или повышенную хиральную чистоту.
[0042] Защитные группы для амино- и карбоксильных групп известны в данной области техники. Например, см. Greene, Protective Groups in Organic Synthesis, Wiley Interscience, 1981 и последующие издания.
[0043] В различных вариантах реализации настоящего изобретения на последующих схемах HATU используют в качестве реагента в реакциях по образованию амидной связи. В качестве альтернативы, HATU не используют. В различных вариантах реализации настоящего изобретения по меньшей мере одну реакцию по образованию амидной связи осуществляют с использованием в качестве реагента тионихлорида вместо HATU. В различных вариантах реализации настоящего изобретения все реакции по образованию амидной связи осуществляют с использованием в качестве реагента тионилхлорида с получением хлоридов кислот.
[0044] Схема 1
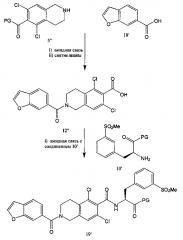
[0045] Согласно первой из альтернативных защитных стратегий, получают соединение 5', защищенные соединения, показанные на схеме 1. Данный синтез начинается с восстановительного аминирования 3,5-дихлорбензальдегида, соединения 1'. Циклизация соединения 2' позволяет получить соединение 3'. Защита свободной аминогруппы соединения 3' с получением защищенного соединения позволяет получить соединение 4' Функциональную группу карбоновой кислоты вводят путем обработки соединения 4' диоксидом углерода с получением соединения 5'. В различных вариантах реализации настоящего изобретения защитная группа соединения 4' представляет собой бензофуранилкарбонильный фрагмент, полученный из соединения 18'.
[0046] В различных вариантах реализации настоящего изобретения при масштабировании реакции до масштаба в несколько килограмм или большего масштаба обработку соединения 4' сильным основанием (таким как н-бутиллитий (nBuLi) для получения соединений лития или диизопропиламид лития (LDA) для получения соединений лития) осуществляют в проточном режиме, а не путем реакции в периодическом режиме ввиду нестабильности соединений лития не при низких температурах. Скорости потока и время удерживания могут быть откорректированы для получения максимального выхода.
[0047] Схема 1В
[0048] В различных вариантах реализации настоящего изобретения для получения соединения 5' в качестве исходного вещества используют 6-гидрокси-1,2,3,4-тетрагидроизохинолин (соединение 3''). Данное исходное вещество хлорируют (х2) например, N-хлорсукцинимидом. В различных вариантах реализации настоящего изобретения хлорирование осуществляют в присутствии сульфоновой кислоты. В различных вариантах реализации настоящего изобретения сульфоновая кислота выбрана из n-толуолсульфоновой кислоты и метансульфоновой кислоты. После защиты аминогруппы вводят функциональную группу к гидроксигруппе, например, в виде сложного эфира трифлата, который карбонилируют с получением аминозащищенного метилового сложного эфира. Гидролиз данного метилового сложного эфира позволяет получить аминозащищенную карбоновую кислоту.
[0049] Схема 2
[0050] В различных вариантах реализации настоящего изобретения бромфенилаланин используют в качестве исходного вещества для части конечной молекулы, как показано на схеме 2. Данное исходное вещество защищают аминозащитной группой с обеспечением возможности введения метилсульфоновой функциональной группы в соединение 8'. Защитные группы перегруппировывали путем введения ортогональной защитной группы, защищающей карбоксильный фрагмент, с последующим снятием защиты с аминогруппы с получением соединения 10'. В различных вариантах реализации настоящего изобретения дорогие или малораспространенные основания заменяют карбонатным основанием, таким как карбонат калия или карбонат кальция, в качестве реагентов.
[0051] Схема 2А
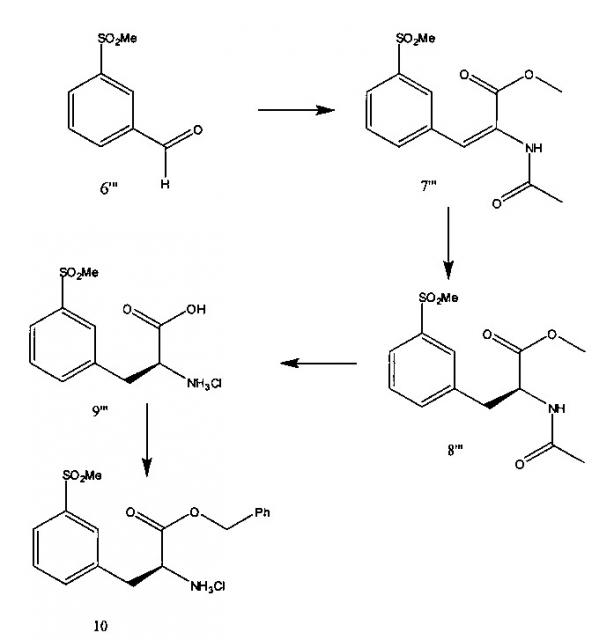
[0052] В различных вариантах реализации настоящего изобретения 3-метилсульфонилбензальденид превращают в 3-метилсульфонилфенилаланиновое производное и вводят функциональную группу с получением соединения 10, как показано выше.
[0053] Схема 3
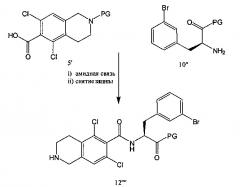
[0054] Соединения 5' и 10' соединяли посредством образования амидной связи с последующим снятием защиты с оставшейся аминогруппы в присутствии карбоксизащитной группы с получением соединения 12' или его соли, такой как соли HCL.
[0055] Схема 3А
[0056] В качестве альтернативы схеме 3, соединение 10'' подвергают реакции сочетания с соединением 5' с получением бромсодержащего соединения 12'''' с последующим введением на следующей стадии метилсульфоновой функциональной группы на место брома с получением соединения 19'. В качестве альтернативы, вместо брома, соединение 10'' включает X, где X представляет собой любой галогенид (Cl, I, Br, F) или уходящую группу, такую как OTs, OTf или тому подобные.
[0057] Схема 4
[0058] Бензофуранилкарбонильный фрагмент соединения формулы I может быть получен с использованием различных альтернативных схем. В одном из вариантов реализации настоящего изобретения бензофуранилкарбонильный фрагмент получают путем защиты гидроксильной группы соединения 13', восстановления карбонила соединения 13' с получением бензофуранильного фрагмента и последующего карбоксилирования с получением соединения 18'.
[0059] Схема 4А
[0060] В одном из вариантов реализации настоящего изобретения соединение 18' получают из 6-гидроксибензофурана через сложный эфир трифлата и 6-карбоксиметиловый сложный эфир в качестве промежуточных веществ, как показано в примере Пример 4А.
[0061] Схема 5
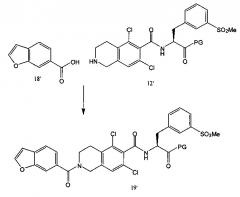
[0062] Бензофуранкарбоновую кислоту 18' подвергают реакции сочетания с соединением 12' (или его солью) путем образования амидной связи с получением защищенного соединения 19', как показано на схеме 5. Образование амидной связи известно в данной области техники.
[0063] Схема 5А
[0064] В качестве альтернативы схемам 3-5, соединения 18' и 5'' могут быть подвергнуты реакции сочетания с образованием амидной связи с последующим снятием защиты с оставшейся карбоксильной группы с получением соединения 12''. Образование амидной связи между соединениями 12'' и 10' позволяет получить соединение 19' с защищенной карбоксильной группой.
[0065] Схема 5В
[0066] В качестве альтернативе схемам 1-5, соединения 12'' и 10'' могут быть подвергнуты реакции сочетания с образованием амидной связи с последующим введением метилсульфоновой функциональной группы вместо брома при превращении соединения 19'' в соединение 19' (аналогично схеме 2). В качестве альтернативы, вместо брома, соединение 10'' включает X, где X представляет собой любой галогенид (Cl, I, Br, F) или уходящую группу, такую как OTs, OTf или тому подобное. Соединение 12'' может быть также получено согласно следующей схеме:
[0067] Схема 6
[0068] Конечное снятие защиты с соединения 19' с получением соединения формулы I или его соли осуществляют множеством способов. В различных вариантах реализации настоящего изобретения полученное в результате соединение формулы I имеет более высокую оптическую чистоту, и/или более высокую общую чистоту, и/или более высокий общий выход.
[0069] Согласно одному из подходов, сложноэфирную защитную группу удаляют путем катализируемого кислотой гидролиза. Например, защитную группу в виде метилового эфира удаляют путем катализируемого кислотой гидролиза. В качестве альтернативы, защитную группу в виде бензилового эфира удаляют кислотой, например HCl в диоксане. Растворитель для катализируемого кислотой гидролиза может быть представлять собой любой доступный в промышленности растворитель, такой как апротонный растворитель, протонный растворитель, полярный растворитель, неполярный растворитель, ионный растворитель иди, сжатый газ, такой как сверхкритический диоксид углерода. В различных вариантах реализации настоящего изобретения растворитель представляет собой апротонный растворитель, такой как диоксан, или тетрагидрофуран, или ацетон. Вариативно растворитель может быть выбран из гексана, бензола, толуола, 1,4-диоксана, хлороформа, диэтилового, эфира, дихлорметана, тетрагидрофурана, этилацетата, ацетона, диметилформамида, ацетонитрила, диметилсульфоксида, н-бутанола, изопропанола, н-пропанола, этанола, метанола, воды, муравьиной кислоты, уксусной кислоты, трифторуксусной кислоты и их комбинаций, таких как водный раствор ацетона. Кислота может представлять собой любую, кислоту, используемую для реакций гидролиза. В различных вариантах реализации настоящего изобретения кислота представляет собой минеральную кислоту. В различных вариантах реализации настоящего изобретения кислота выбрана из хлористого водорода, серной кислоты, фосфорной кислоты и сульфоновых кислот. В различных вариантах реализации настоящего изобретения кислота представляет собой трифторуксусную кислоту, В одном из вариантов реализации настоящего изобретения сложный эфир может быть удален путем нуклеофильного замещения, например, с использованием иодида натрия в диметилсульфоксиде.
[0070] Согласно одному из подходов, защитную группу в виде бензилового эфира удаляют при помощи палладия на угле. Например, бензиловый эфир соединения 19' удаляют путем гидрогенолиза с использованием 10% палладия на угле, с использованием муравьиной кислоты и триэтиламина в смеси метанол : ТГФ 5:1 с получением соединения формулы I.
[0071] В различных вариантах реализации настоящего изобретения соединение 19' представляет собой соединение формулы АА. Общая стратегия превращения соединения формулы АА обеспечивается основным гидролизом сложного эфира с получением соединения формулы I.
Соединение формулы АА может быть подвергнуто реакции с основанием в растворителе для осуществления катализируемого основанием омыления соединения формулы АА с получением соединения формулы I.
[0072] Растворитель для омыления может представлять собой любой доступный в промышленности растворитель, такой как апротонный растворитель, протонный растворитель, полярный растворитель, неполярный растворитель, ионной растворитель или сжатый газ, такой как сверхкритический диоксид углерода. В различных вариантах реализации настоящего изобретения растворитель представляет собой апротонный растворитель, такой как диоксан или тетрагидрофуран или ацетон. Вариативно растворитель может быть выбран из гексана, бензола, толуола, 1,4-диоксана, хлороформа, диэтилового эфира, дихлорметана, тетрагидрофурана, этилацетата, ацетона, диметилформамида, ацетонитрила, диметилсульфоксида, н-бутанола, изопропанола, н-пропанола, этанола, метанола, воды и их комбинаций. В предпочтительном варианте реализации настоящего изобретения растворитель представляет собой водный раствор ацетона. Основание может представлять собой любое основание, используемое для реакций омыления. В различных вариантах реализации настоящего изобретения основание представляет собой гидроксид, такой как гидроксид калия, или гидроксид натрия, или гидроксид лития.
[0073] В различных вариантах реализации настоящего изобретения группа R представляет собой любой углеродсодержащий фрагмент. Такие соединения могут быть подходящими для применения в качестве синтетических промежуточных веществ для получения соединений формулы I, или в виде пролекарств соединения формулы I. В группе, где R представляет собой любой углеродсодержащий фрагмент, R может быть выбран из низшего алкила, низшего алкенила, низшего алкинила, цикло(низшего)алкила, цикло(низшего)алкенила, арила, аралкила, гетероциклила и гетероарила, любой из которых может быть замещенным или незамещенным. В различных вариантах реализации настоящего изобретения низшая алкильная группа представляет собой метил, этил, пропил, изопропил, бутил, пентил, изобутил, трет-бутил или гексил. В различных вариантах реализации настоящего изобретения группа R соединения формулы АА представляет собой бензильную группу. В различных вариантах реализации соединений формулы АА углеродсодержащий фрагмент R не включает бензильную группу.
[0074] В различных вариантах реализации настоящего изобретения группа R представляет собой силилсодержащий фрагмент, такой что соединение формулы АА представляет собой силиловый эфир.
[0075] В одном из вариантов реализации настоящего изобретения сложноэфирную защитную группу удаляют путем катализируемого основанием гидролиза в гомогенной реакции, такой как реакция в растворе. Например, защитную группу в виде бензилового эфира удаляют q помощью NaOH в водном диоксане. В одном из вариантов реализации настоящего изобретения защитную группу в виде бензилового эфира удаляют с помощью NaOH в водном растворе ацетона. В различных вариантах реализации гомогенной жидкостной реакции концентрация NaOH может находиться в диапазоне от примерно 0,1 н. до примерно 2 н., в частности может составлять примерно 0,5 н., 0,6 н., 0,7 н., 0,8 н., 0,9 н., 1,0 н., 1,1 н., 1,2 н., 1,3 н., 1,4 н. или 1,5 н., где все указанные концентрации следует понимать как «примерные»
[0076] В одном варианте реализации настоящего изобретения сложноэфирную защитную, группу удаляют из соединения 19' или соединения формулы АА путем катализируемого основанием гидролиза в гет