Проекция магнитного резонанса для построения четырехмерной визуализации
Иллюстрации
Показать всеИспользование: для проекционной визуализации методом ядерного магнитного резонанса (MR). Сущность изобретения заключается в том, что проекционная визуализации методом ядерного магнитного резонанса (MR) может использоваться для генерирования информации о четырехмерной (4D) визуализации, представляющей физиологический цикл субъекта, например, включающего в себя генерирование двух или более двумерных (2D) изображений, причем 2D-изображения содержат проекционные изображения, представляющие разные проекционные углы, и 2D-изображения генерируют с использованием информации о визуализации, полученной посредством визуализации методом ядерного магнитного резонанса (MR), назначение конкретных 2D-изображений бинам по меньшей мере частично с использованием информации, указывающей временные положения в физиологическом цикле, соответствующие конкретным 2D-изображениям, построение трехмерных (3D) изображений с использованием сгруппированных по бинам 2D-изображений и построение информации о 4D- визуализации, содержащее объединение 3D-изображений. Технический результат: обеспечение возможности предсказания последующего положения целевой области для адаптации лучевой терапии. 3 н. и, 20 з.п. ф-лы, 16 ил.
Реферат
ПРИТЯЗАНИЕ НА ПРИОРИТЕТ
Данная заявка на патент претендует на привилегии приоритета предварительной заявки на патент № 62/090 115 Lachaine et al., озаглавленной «MAGNETIC RESONANCE PROJECTION IMAGING», поданной 10 декабря 2014 г. (дело патентного поверенного № 4186.006PRV), которая настоящим документом включена по ссылке во всей своей полноте.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Лучевая терапия или «радиотерапия» может использоваться для лечения рака или других болезней в ткани млекопитающих (например, человека и животного). Один такой метод радиотерапии упоминается как «гамма-нож», посредством которого пациент облучается с использованием нескольких гамма-лучей малой интенсивности, которые сходятся с высокой интенсивностью и высокой точностью на целевой области (например, опухоли). В другом примере, обеспечивается радиотерапия с использованием линейного ускорителя («linac»), посредством чего целевая область облучается частицами с высокой энергией (например, электронами, протонами, ионами, протонами высокой энергии и т.п.). Расположение и доза пучка излучения точно контролируется для обеспечения предписанной дозы облучения целевой области. Пучок для облучения также, как правило, контролируется с целью уменьшения или минимизации поражения окружающей здоровой ткани, такой, которая может упоминаться как «орган(-ы) риска» (OAR). Облучение может упоминаться как «предписанное», так как, как правило, врач назначает заданную дозу облучения для доставки на целевую область, такую как опухоль.
Как правило, ионизирующее излучение в виде коллимированного пучка направляется от внешнего источника излучения на пациента. Модуляция пучка излучения может обеспечиваться одним или более аттенюаторами или коллиматорами (например, многолепестковым коллиматором). Интенсивность и форма пучка излучения может регулироваться коллимированием, избегая поражения здоровой ткани (например, OAR) рядом с целевой тканью, приводя проецируемый пучок в соответствии с профилем целевой ткани.
Процедура планирования лечения может включать в себя использование трехмерного изображения пациента для идентификации целевой области (например, опухоли) и так, чтобы идентифицировать критические органы около опухоли. Создание плана лечения может представлять собой длительный процесс, где планировщик пытается соблюсти различные требования или ограничения лечения (например, требования гистограммы доза-объем (DVH) или другие ограничения), например, принимая во внимание важность (например, определение веса) соответствующих ограничений, чтобы получить план лечения, который является клинически приемлемым. Эта задача может представлять собой длительный процесс проб и ошибок, который усложняется различными органами риска (OAR), так как когда увеличивается количество OAR (например, около тринадцати для лечения головы и шеи), также увеличивается сложность процесса. OAR вдали от опухоли можно легче уберечь от облучения, но может быть труднее уберечь от облучения во время лечения OAR, которые находятся вблизи или перекрывают целевую опухоль.
Как правило, для каждого пациента первоначальный план лечения может создаваться «автономным» образом. План лечения может разрабатываться задолго до доставки лучевой терапии, например, используя один или более медицинских методов визуализации. Информация о визуализации может включать в себя, например, изображения рентгеновских лучей, компьютерной томографии (CT), ядерного магнитного резонанса (MR), позитронно-эмиссионной томографии (PET), однофотонной эмиссионной компьютерной томографии (SPECT) или ультразвука. Медицинский работник, такой как врач, может использовать информацию о трехмерной визуализации, указывающую анатомию пациента, для идентификации одной или более целевых опухолей вместе с органами риска около опухоли. Медицинский работник может выделить целевую опухоль, которая должна принять предписанную дозу облучения, используя ручной метод, и медицинский работник может аналогично выделить близлежащую ткань, такую как органы, с риском поражения от лечения облучением.
Альтернативно или дополнительно, автоматизированное инструментальное средство (например, ABAS, производимое компанией Elekta AB, Швеция) может использоваться для оказания содействия при идентификации или выделении целевой опухоли и органов риска. План лечения лучевой терапией («план лечения») затем может создаваться с использованием метода оптимизации на основе клинических и дозиметрических требований и ограничений (например, максимальные, минимальные и средние дозы облучения для опухоли и критических органов).
Процедура планирования лечения может включать в себя использование трехмерного изображения пациента для идентификации целевой области (например, опухоли) и для идентификации критических органов около опухоли. Создание плана лечения может представлять собой длительный процесс, где планировщик пытается соблюсти различные требования или ограничения лечения (например, требования гистограммы доза-объем (DVH)), принимая во внимание их индивидуальную важность (например, определение веса), чтобы получить план лечения, который клинически является приемлемым. Эта задача может представлять собой длительный процесс проб и ошибок, который усложняется различными органами риска (OAR), так как когда увеличивается количество OAR (например, до тринадцати для лечения головы и шеи), также увеличивается сложность процесса. OAR вдали от опухоли можно легко уберечь от облучения, тогда как может быть трудным уберечь OAR, которые находятся вблизи или перекрывают целевую опухоль.
План лечения затем может исполняться позже расположением пациента и доставкой предписанной лучевой терапии. План лечения лучевой терапией может включать в себя «фракционирование» дозы, посредством чего обеспечивается последовательность доставок лучевой терапии в течение заданного периода времени (например, 45 фракций или некоторое другое общее число фракций), например, каждая доставка терапии включает в себя заданную фракцию общей предписанной дозы. Во время лечения является важным положение пациента или положение целевой области относительно пучка для лечения, так как такое расположение, частично, определяет, облучается ли целевая область или здоровая ткань.
ОБЗОР
В одном подходе, визуализация методом ядерного магнитного резонанса (MR) может объединяться с системой лучевой терапии, например, для обеспечения информации о визуализации для адаптации или наведения лучевой терапии. Пример такой объединенной системы обычно может упоминаться как «MRI-linac», содержащий систему MR-визуализации вместе с линейным ускорителем в качестве источника энергии для лучевой терапии. В одном проиллюстративном примере получение изображения может выполняться как раз перед инициированием доставки заданной фракции лучевой терапии. Такая визуализация может обеспечивать информацию, полезную для идентификации положения целевой области или для идентификации движения целевой области. Такая одновременная визуализация может упоминаться в общем случае как «режим реального времени», но обычно существует запаздывание или временная задержка между получением изображения и доставкой лучевой терапии.
Изобретатели настоящего изобретения выяснили, помимо всего прочего, что существует проблема при использовании 3D MR-визуализации для планирования или адаптации лучевой терапии. Например, на реконструкцию объемной области изображения может оказываться неблагоприятное воздействие, когда на целевую область воздействует дыхание или другое движение, так как продолжительность визуализации («время визуализации») обычно достаточно длительное для воздействия таким движением. Кроме того, запаздывание получения или большая продолжительность получения может вызывать проблемы, так как целевая область может деформироваться или существенно перемещаться между получением 3D MR-изображения и последующей доставкой лучевой терапии.
В одном подходе, например, когда движение целевой области является периодическим, может использоваться метод четырехмерной MR-визуализации, например, перед лечением облучением. Например, получение изображения может синхронизироваться с физиологическим циклом, например, считыванием информации о заменителе. Примеры заменителей включают в себя сигнал, считываемый с использованием пояса для измерения дыхания, или одномерный (1D) эхо-сигнал навигатора, указываемый MR-визуализацией. Элементы MR-визуализации, такие как полученные срезы визуализации, могут группироваться в бины, используя информацию, указывающую фазу или амплитуду физиологического цикла или заменителя, коррелированного с таким циклом. Однако такой подход также может иметь ограничения. Например, общедоступные методы 4D-визуализации на основе срезов (такие как MR-визуализация без проекции) не включают в себя использование анатомического ориентира, такого как местоположение диафрагмы, для группировки или биннинга полученных 3D-изображений в отношении физиологического цикла. Вместо этого, обычно доступные методы 4D-визуализации получают изображения последовательно, а полученные изображения содержат разные участки анатомии и не имеют общих анатомических признаков на каждом изображении. В противоположность этому, подход проекционной визуализации может включать в себя выбор или генерирование проекционных изображений, имеющих общий анатомический признак в каждом изображении, поэтому общий признак может использоваться для облегчения биннинга. Даже если присутствует другой ракурс признака в каждом из проекционных изображений (например, разные виды признака), такое отслеживание признака для биннинга все же может использоваться в подходе проекционной визуализации. Таким образом, в отличие от общедоступных методов 4D MR-визуализации заменитель (такой как внешний заменитель) не требуется.
Общепринятые протоколы 4D MR-визуализации также включают в себя относительно продолжительные времена получения и могут быть недопустимыми по времени, например, в применениях, где должна выполняться визуализация с обновлением перед каждой фракцией лечения лучевой терапией. Также, методы 4D MR-визуализации необязательно могут представлять или предсказывать анатомическое состояние визуализируемого субъекта во время последующей доставки лучевой терапии. Например, может иметь место дрейф базовой линии, деформации или изменения частоты или фазы физиологического цикла между моментом времени, при котором получается информация 4D MR-визуализации, и последующей доставкой лучевой терапии.
В другом подходе, информация о визуализации, указывающая внутрифракционное движение целевой области или других участков визуализируемого субъекта, может включать в себя визуализацию только участка визуализируемого субъекта без необходимости визуализации полного объема, например, получением двумерных (2D) срезов визуализации, например, через целевую область по разным направлениям (например, включая получение последовательности ортогональных срезов). Такие срезы могут использоваться для того, чтобы способствовать локализации целевой области или другой анатомии, как правило, для доставки лучевой терапии. Такой локализации может способствовать, частично, использование одного или более из методов сегментирования изображения или регистрации изображений. Однако такой подход также может иметь ограничения. Например, последовательности импульсов MR-визуализации, используемые для получения 2D-срезов, могут отличаться от тех, которые используются для получения межфракционной объемного «опорной» 3D- или 4D-визуализации перед лечением. Такие разные последовательности импульсов могут делать проблемным регистрацию между 2D-срезами и ранее полученным объемным опорным изображением. Другим ограничением является то, что теряется информация вне среза, например, в примере, где присутствует многочисленные органы риска (OAR), или, если должны быть выполнены ретроспективные вычисления дозы посредством получения информации о визуализации во время лечения. Еще другим ограничением использования 2D-срезов визуализации является то, что может быть трудным выставление срезов с движением цели, особенно, если движение изменяется между физиологическими циклами, например, между дыхательными циклами. Малые цели, такие как опухоли, могут деформироваться или могут исчезать полностью из конкретного полученного среза визуализации.
Изобретатели настоящего изобретения нашли решение для вышеупомянутых ограничений. Такое решение может включать в себя использование подхода проекционной MR-визуализации. Такой подход проекционной визуализации может использоваться в пределах фракции. Альтернативно или дополнительно, проекционная MR-визуализация может использоваться аналогично для моделирования визуализации, подлежащей использованию для планирования лечения, или визуализации перед лечением (например, «опорной»), выполняемой между фракциями для сдвига пациента или адаптации плана лечения перед доставкой лечения. Использование проекционной MR-визуализации для моделирования визуализации, опорной визуализации перед лечением и последующей визуализации в пределах фракции может обеспечивать согласованность и легкость регистрации или другой обработки. Проекционная MR-визуализация также может обеспечивать информацию о визуализации таким образом, который более точно коррелирует с методами портальной визуализации со стороны пучка (BEV) или с рентгеновскими методами, но без подвергания визуализируемого субъекта ионизирующему облучению во время визуализации. Получение проекционных 2D MR-изображений может существенно уменьшить время ожидания получения визуализации по сравнению с другими подходами, такими как полнообъемная 3D MR-визуализация, а проекционные 2D-изображения могут объединяться так, чтобы получать информацию об объемной визуализации, используя, например, томографирование или методы пространства Фурье (k-пространства). Информация из полученных проекционных 2D MR-изображений или из 3D- или 4D-визуализаций, построенных из проекционных 2D MR-изображений, может сравниваться с информацией об опорной визуализации, например, для локализации целевой области или анатомических ориентиров, или для предсказания последующего положения целевой области. Таким образом, информация, указывающая целевую область, может использоваться для адаптации лучевой терапии.
Согласно различным примерам аппарат и методы, описанные в данном документе, могут использоваться для управления доставкой лучевой терапии к субъекту с использованием методов проекционной визуализации. Например, опорная визуализация может быть принята такой, что включает информацию о визуализации, полученной раннее в отношении планирования лечения лучевой терапией. Проекционное двумерное (2D) изображение может генерироваться с использованием информации о визуализации, полученной посредством визуализации методом ядерного магнитного резонанса (MR), причем проекционное 2D-изображение соответствует заданному проекционному направлению, заданное проекционное направление включает в себя траекторию, пересекающую по меньшей мере часть визуализируемого субъекта. Может определяться изменение между сгенерированным проекционным 2D-изображением и информацией об опорной визуализации. Доставка лучевой терапии может управляться по меньшей мере частично (например, адаптивным образом) с использованием определенного изменения между полученным проекционным 2D-изображением и информацией об опорной визуализации.
Изобретатели настоящего изобретения также выяснили, что информация об опорной визуализации может быть получена с использованием методов проекционной визуализации, например, для использования при пространственной регистрации получаемых позже проекционных изображений с ранее полученной информацией о визуализации. Согласно различным примерам аппарат и методы, описанные в данном документе, могут использоваться для генерирования информации о четырехмерной (4D) и другой визуализации, например, во время одного или более из получения опорных изображений перед лучевой терапией (например, опорная визуализации) или позже, например, перед или во время доставки лучевой терапии (например, внутрифракционная визуализация). Генерирование информации о 4D-визуализации может включать в себя генерирование двух или более двумерных (2D) изображений, причем 2D-изображения содержат проекционные изображения, представляющие разные проекционные углы, где 2D-изображения генерируются с использованием информации о визуализации, полученной посредством визуализации методом ядерного магнитного резонанса (MR). Конкретные 2D-изображения могут назначаться бинам, по меньшей мере частично используя информацию, указывающую временные положения внутри физиологического цикла, соответствующие конкретным 2D-изображениям. Трехмерные (3D) изображения могут составляться с использованием 2D-изображений в бинах. Группа из 3D-изображений может объединяться, чтобы получать информацию о 4D-визуализации.
Этот обзор предназначен для предоставления обзора объекта изобретения по настоящей заявке на патент. Он не предназначен для предоставления всеобъемлющего или исчерпывающего объяснения изобретения. Подробное описание включено для того, чтобы предоставить дополнительную информацию о настоящей заявке на патент.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
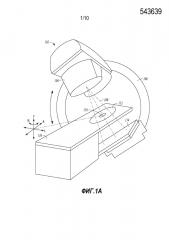
Фиг.1A иллюстрирует в общих чертах пример системы лучевой терапии, которая может включать в себя блок вывода лучевой терапии, выполненный с возможностью обеспечения пучка для терапии.
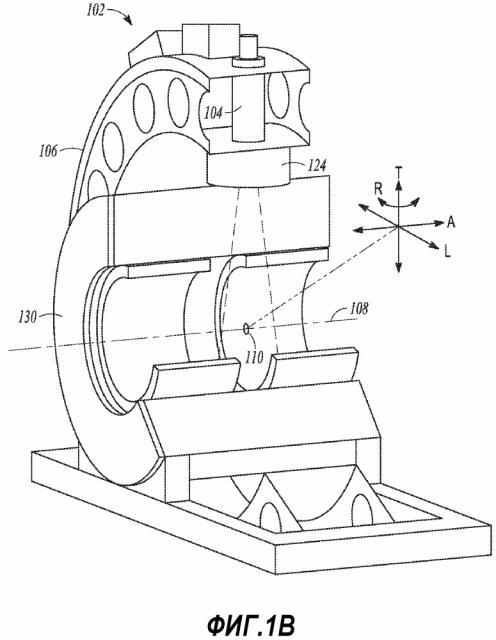
Фиг.1B иллюстрирует в общих чертах вид с частичным разрезом примера системы, которая включает в себя объединенную систему лучевой терапии и систему визуализации методом ядерного магнитного резонанса (MR).
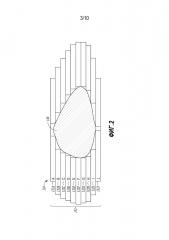
Фиг.2 иллюстрирует в общих чертах пример конфигурации коллиматора, такую, которая может использоваться, частично, для придания формы или коллимирования пучка для лучевой терапии.
Фиг.3 иллюстрирует в общих чертах пример системы лучевой терапии, такой, которая может включать в себя устройство лучевой терапии и устройство получения изображения.
Фиг.4 иллюстрирует в общих чертах пример системы, которая может использоваться для одного или более из получения изображения, сегментирования изображения, предсказания цели, управления терапией или регулировки терапии.
Фиг.5 иллюстрирует в общих чертах пример системы, которая, например, может включать в себя контроллер лучевой терапии, имеющий блок ввода визуализации, генератор лучевой терапии и блок вывода лучевой терапии.
Фиг.6 иллюстрирует в общих чертах метод, такой как способ, который может включать в себя использование MR-визуализации для возбуждения области визуализируемого субъекта, причем область определяет срез визуализации, и получение значения пикселя, соответствующего одномерной проекционной линии через срез.
Фиг.7A иллюстрирует в общих чертах метод, такой как способ, который может включать в себя возбуждение области визуализируемого субъекта с использованием последовательности возбуждения двумерной (2D) MR-визуализации.
Фиг.7B иллюстрирует в общих чертах другой метод, такой как способ, который может включать в себя возбуждение области визуализируемого субъекта с использованием последовательности возбуждения двумерной (2D) MR-визуализации.
Фиг.8A и 8B иллюстрируют в общих чертах метод, такой как способ, который может включать в себя генерирование проекционных двумерных (2D) MR-изображений, представляющих разные проекционные углы, и использование таких проекционных 2D-изображения для составления трехмерных (3D) изображений.
Фиг.9 иллюстрирует в общих чертах метод, такой как способ, который может включать в себя генерирование проекционного двумерного (2D) изображения с использованием MR-визуализации и определение изменения между сгенерированным проекционным 2D-изображением и информацией об опорной визуализации.
Фиг.10A иллюстрирует в общих чертах пространственное расположение ориентации пучка для лучевой терапии относительно одного или более проекционных направлений, которые, например, могут включать в себя два проекционных направления, ориентированные ортогонально друг к другу.
Фиг.10B иллюстрирует в общих чертах пространственное расположение проекционных направлений MR-визуализации, например, соответствующих проекционным углам, охватывающим дугу или окружность вокруг заданной области, такой как изоцентр лечения лучевой терапией.
Фиг.10C иллюстрирует, в общих чертах, пространственное расположение проекционного направления MR-визуализации, такого как ориентированного под заданным углом относительно направления пучка для лучевой терапии.
Фиг.10D иллюстрирует в общих чертах пространственное расположение проекционных направлений MR-визуализации, которые могут задаваться для получения проекционных MR-изображений, подобно стереоскопической рентгеновской визуализации.
На чертежах, которые необязательно выполнены в масштабе, подобные позиции могут описывать подобные компоненты на разных видах. Подобные позиции, имеющие разные буквенные подстрочные индексы, могут представлять разные экземпляры подобных компонентов. Чертежи иллюстрируют в общих чертах и в качестве примера, но не в качестве ограничения, различные варианты осуществления, описанные в настоящем документе.
ПОДРОБНОЕ ОПИСАНИЕ
Фиг.1A иллюстрирует в общих чертах пример системы 102 лучевой терапии, которая может включать в себя блок 104 вывода лучевой терапии, выполненный с возможностью обеспечения пучка 108 для терапии. Блок 104 вывода лучевой терапии может включать в себя один или более аттенюаторов или коллиматоров, такой как многолепестковый коллиматор (MLC), описанный в иллюстративном примере на фиг.2. Ссылаясь снова на фиг.1A, пациент может располагаться в области 112, например, на платформе 116 (например, на столе или кушетке) для приема предписанной дозы лучевой терапии согласно плану лечения лучевой терапией.
Блок 104 вывода лучевой терапии может располагаться на гентри 106 или другой механической опоре, например, для вращения блока 104 вывода терапии вокруг оси («A»). Одно или более из платформы 116 или блока 104 вывода лучевой терапии может перемещаться в другие местоположения, например, может перемещаться в поперечном направлении («T») или в боковом направлении («L»). Возможны другие степени свободы, такие как поворот вокруг одной или более других осей, такой как поворот вокруг поперечной оси (указан как «R»).
Система координат (включающая оси A, T и L), показанная на фиг.1A, может иметь начало отсчета, расположенное в изоцентре 110. Изоцентр может определяться как местоположение, где пучок 108 для лучевой терапии пересекает начало отсчета оси координат, например, для доставки предписанной дозы облучения в местоположение на или внутри пациента. Например, изоцентр 110 может определяться как местоположение, где пучок 108 для лучевой терапии пересекает пациента для различных угловых положений блока 104 вывода лучевой терапии, располагаемого посредством гентри 106, вокруг оси A.
В одном примере, детектор 114 может располагаться внутри поля пучка 108 для терапии, например, может включать в себя детектор с плоской панелью (например, детектор прямого отсчета или сцинтилляционный детектор). Детектор 114 может быть установлен на гентри 106 напротив блока 104 вывода лучевой терапии, так чтобы поддерживать выставление с пучком 108 для терапии во время вращения гентри 106. Таким образом, детектор 114 может использоваться для мониторинга пучка 108 для терапии, или детектор 114 может использоваться для визуализации, например, портальной визуализация проекции пучка 108 через область 112. Область 112 может определять плоскость, а проекция пучка 108 для терапии в области 112 может упоминаться как «проекция со стороны пучка» области 112.
В иллюстративном примере, может автоматически располагаться одно или более из платформы 116, блока 104 вывода терапии или гентри 106, и блок 104 вывода терапии может устанавливать пучок 108 для терапии в соответствии с заданной дозой для конкретного случая доставки терапии. Последовательность доставок терапии может задаваться в соответствии с планом лечения лучевой терапией, например, используя одну или более разных ориентаций или местоположение гентри 106, платформы 116 или блока 104 вывода терапии. Доставки терапии могут происходить последовательно, но могут пересекаться в требуемой целевой области на или внутри пациента, например, в изоцентре 110. Предписанная суммарная доза лучевой терапии, таким образом, может доставляться на целевую область, в тоже время уменьшается или исключается поражение ткани около целевой области, такой как один или более органов риска.
Как упомянуто в отношении других примеров в данном документе, система 102 лучевой терапии может включать в себя или может быть связана с системой получения изображения, так чтобы обеспечивать одно или более из визуализации методом ядерного магнитного резонанса (MR) или рентгеновской визуализации, например, может включать в себя визуализацию методом компьютерной томографии (CT). В одном примере, информация о MR-визуализации или другая информация о визуализации может использоваться для создания информации о визуализации или визуализаций, эквивалентных CT-визуализации без необходимости в фактической CT-визуализации. Такая визуализация может упоминаться как «псевдо-CT» визуализация.
Фиг.1B иллюстрирует в общих чертах вид с частичным разрезом примера системы, которая включает в себя объединенную систему 102 лучевой терапии и систему 130 визуализации методом ядерного магнитного резонанса (MR). Система 130 MR-визуализации может быть выполнена с возможностью образования «отверстия» вокруг оси («A»), и система лучевой терапии может включать в себя блок 104 вывода лучевой терапии, например, для обеспечения пучка 108 для лучевой терапии, направленного на изоцентр 110 в отверстии вдоль оси A. Блок 104 вывода лучевой терапии может включать в себя коллиматор 124, например, для одного или более из управления или придания формы пучку 108 для лучевой терапии для направления пучка 108 на целевую область внутри пациента. Пациент может поддерживаться платформой, такой как платформа, располагаемая вдоль одной или более из осевого направления A, бокового направления L или поперечного направления T. Одна или более частей системы 102 лучевой терапии могут устанавливаться на гентри 106, например, для вращения блока 104 вывода лучевой терапии вокруг оси A.
Фиг.1A и 1B иллюстрируют, в общих чертах, примеры, включающие в себя конфигурацию, в которой блок вывода терапии может вращаться вокруг центральной оси (например, оси «A»). Могут использоваться другие конфигурации блока вывода лучевой терапии. Например, блок вывода лучевой терапии может быть установлен на роботизированной руке или манипуляторе, так чтобы иметь многочисленные степени свободы. В еще другом примере блок вывода терапии может быть стационарным, например, расположенным в области, отделенной в боковом направлении от пациента, а платформа, поддерживающая пациента, может использоваться для выставления изоцентра лучевой терапии с заданной целевой областью внутри пациента.
Фиг.2 иллюстрирует, в общих чертах, пример конфигурации 132 многолепесткового коллиматора (MLC), который может использоваться частично для придания формы или коллимирования пучка для лучевой терапии. На фиг.2, лепестки 132A-132J могут автоматически располагаться так, чтобы определять апертуру, аппроксимирующую сечение или проекцию опухоли 140. Лепестки 132A-132J могут быть выполнены из материала, предусмотренного для ослабления или блокирования пучка для облучения в областях, кроме апертуры, в соответствии с планом лечения облучением. Например, лепестки 132A-132J могут включать в себя металлические пластины, например, содержащие вольфрам, причем продольная ось пластин ориентирована параллельно направлению пучка, а их концы ориентированы ортогонально направлению пучка (как показано на плоскости иллюстрации фиг.2).
«Состояние» MLC 132 может адаптивно регулироваться в ходе лучевой терапии, чтобы устанавливать пучок для терапии, который лучше аппроксимирует форму или местоположение опухоли 140 или другой целевой области, по сравнению с использованием статической конфигурации коллиматора или по сравнению с использованием конфигурации MLC 132, определяемой исключительно для использования метода «автономного» планирования терапии. Метод лучевой терапии, включающий в себя использование MLC 132 для получения заданного распределения дозы облучения на опухоль или на заданные области в опухоли, может упоминаться как лучевая терапия с модулированной интенсивностью (IMRT). Как описано в отношении других примеров в данном документе, визуализация может выполняться для локализации целевой области или для определения или предсказания ракурса целевой области из точки обзора пучка для лучевой терапии, чтобы адаптивно управлять терапией.
Фиг.3 иллюстрирует в общих чертах пример системы 300 лучевой терапии, которая, например, может включать в себя устройство 330 лучевой терапии и устройство получения изображения. Система 300 лучевой терапии может включать в себя модуль 312 обучения, модуль 314 предсказания, базу 322 данных обучения, базу 324 данных тестирования, устройство 330 лучевой терапии и устройство 350 получения изображения. Система 300 лучевой терапии также может быть подсоединена к системе 342 планирования лечения (TPS) и онкологической информационной системе (OIS) 344, которая может предоставлять информацию о пациенте. Кроме того, система 300 лучевой терапии может включать в себя устройство отображения и пользовательский интерфейс.
Фиг.4 иллюстрирует в общих чертах пример системы 400, которая может использоваться для одного или более из получения изображения, сегментирования изображения, предсказания цели, управления терапией или регулировки терапии. Согласно некоторым вариантам осуществления, система 400 может представлять собой одно или более высокопроизводительных вычислительных устройств, способных идентифицировать, анализировать, поддерживать, генерировать или предоставлять большие количества данных, совместимых с описанными вариантами осуществления. Система 400 может быть автономной, или она может быть частью подсистемы, которая, в свою очередь, может быть частью большей системы. Например, система 400 может представлять распределенные высокопроизводительные серверы, которые расположены удаленно и выполняют связь по сети, такой как Интернет, или сеть связи с выделенными каналами, такая как локальная сеть (LAN) или глобальная сеть (WAN). В некоторых вариантах осуществления, система 400 может включать в себя встроенную систему, формирующий изображения сканер (например, сканер на основе ядерного магнитного резонанса (MR) или другой сканер, такой как сканер компьютерной томографии (CT)), и/или устройство отображения с сенсорным экраном на связи с одним или более удаленно расположенными высокопроизводительными вычислительными устройствами.
В одном варианте осуществления, система 400 может включать в себя один или более процессоров 414, одну или более памятей 410 и один или более интерфейсов 415 связи. Процессорами 414 могут быть процессорная схема, включающая в себя один или более устройств обработки общего назначения, таких как микропроцессор, блок центральной обработки (CPU), блок обработки графики (GPU) или т.п. Более конкретно, процессором 414 может быть микропроцессор со сложным набором команд (CISC), микропроцессор с сокращенным набором команд (RISC), микропроцессор со сверхдлинным командным словом (VLIW), процессор, реализующий другие наборы команд, или процессоры, реализующие комбинацию наборов команд.
Процессором 414 также может быть одно или более устройств обработки специального назначения, таких как специализированная интегральная схема (ASIC), программируемая вентильная матрица (FPGA), процессор цифровой обработки сигналов (DSP), система на кристалле (SoC) или т.п. Как понятно для специалиста в данной области техники, в некоторых вариантах осуществления процессором 414 может быть процессор специального назначения, а не процессор общего назначения. Процессор 414 может включать в себя одно или более известных устройств обработки, таких как микропроцессор из семейства Pentium™ или Xeon™, производимый компанией Intel™, из семейства Turion™, производимый компанией AMD™, или любой из различных процессоров, производимых другими изготовителя, такими как Oracle™ (например, процессор с архитектурой SPARC™). Процессор 414 также может включать в себя блоки обработки графики, производимые компанией Nvidia™. Раскрытые варианты осуществления не ограничиваются каким-либо типом процессора(-ов), сконфигурированного(-ых) иным образом для удовлетворения вычислительных требований идентификации, анализа, поддержки, генерирования и/или предоставления больших количеств данных визуализации или любых других типов данных, совместимых с раскрытыми вариантами осуществления.
Память 410 может включать в себя одно или более запоминающих устройств, выполненных с возможностью хранения исполняемых компьютером инструкций, используемых процессором 414 для выполнения функций, относящихся к раскрытым вариантам осуществления. Например, память 410 может хранить инструкции исполняемого компьютером программного обеспечения для программного обеспечения 411 планирования лечения, программное обеспечение 412 операционной системы и программное обеспечение 413 обучения/предсказания. Процессор 414 может быть связан с возможностью выполнения связи с памятью/запоминающим устройством 410 и процессор 414 может быть выполнен с возможностью исполнения исполняемых компьютером инструкций, хранимых на нем для выполнения одной или более операций, совместимых с раскрытыми вариантами осуществления. Например, процессор 414 может исполнять программное обеспечение 413 обучения/предсказания для реализации функциональных возможностей модуля 312 обучения и модуля 314 предсказания. Кроме того, процессорное устройство 414 может исполнять программное обеспечение 411 планирования лечения (например, такое как Monaco©, предоставляемое компанией Elekta), которое может выполнять сопряжение с программным обеспечением 413 обучения/предсказания.
Раскрытые варианты осуществления не ограничиваются отдельными программами или компьютерами, выполненными с возможностью выполнения специализированных задач. Например, память 410 может включать в себя единственную программу, которая выполняет функции системы 400, или многочисленные программы (например, программное обеспечение 411 планирования лечения и/или программное обеспечение 413 обучения/планирования). Кроме того, процессор 414 может исполнять одну или более программ, расположенных удаленно от системы 400, таких как программы, хранимые в базе 420 данных, причем такие удаленные программы могут включать в себя программное обеспечение онкологической информационной системы или программное обеспечение планирования лечения. Память 410 также может хранить данные изображения или данные/информацию любого другого типа в любом формате, которые система может использовать для выполнения операций, совместимых с раскрытыми вариантами осуществления.
Интерфейсом 415 связи может быть одно или более устройств, выполненных с возможностью приема и/или передачи данных системой 400. Интерфейс 415 связи может включать в себя одно или более устройств цифровой и/или аналоговой связи, которые позволяют системе 400 выполнять связь с другими машинами и устройствами, такими как удаленно расположенные компоненты системы 400, базы 420 данных или базы 430 данных больницы. Например, процессор 414 может быть связан с возможностью выполнения связи с базой(-ами) 420 данных или базой(-ами) 430 данных больницы посредством интерфейса 415 связи. Например, интерфейсом 415 связи может быть компьютерная сеть, такая как Интернет, или сеть связи с выделенными каналами, такая как LAN или WAN. Альтернативно, интерфейсом 415 связи может быть линия спутниковой связи или линия цифровой или аналоговой связи любого вида, которая позволяет процессору 414 посылать/принимать данные на/от любой базы (баз) 420, 430 данных.
База(-ы) 420 данных и база(-ы) 430 данных больницы могут вк