Солевая форма ингибитора гистон-метилтрансферазы ezh2 человека
Иллюстрации
Показать всеИзобретение относится к гидробромиду N-((4,6-диметил-2-оксо-1,2-дигидропиридин-3-ил)метил)-5-(этил(тетрагидро-2H-пиран-4-ил)амино)-4-метил-4'-(морфолинометил)-[1,1'-бифенил]-3-карбоксамида, а также его полиморфной форме. Технический результат: получен гидробромид N-((4,6-диметил-2-оксо-1,2-дигидропиридин-3-ил)метил)-5-(этил(тетрагидро-2H-пиран-4-ил)амино)-4-метил-4'-(морфолинометил)-[1,1'-бифенил]-3-карбоксамида, который обладает наибольшей кристалличностью и наименьшей гигроскопичностью, а кроме того, является высокоустойчивым и противодействует генерированию примесей. 13 н. и 20 з.п. ф-лы, 6 табл., 21 ил.
Реферат
РОДСТВЕННАЯ ЗАЯВКА
Настоящая заявка испрашивает приоритет на основании заявки на патент США №61/624215, поданной 13 апреля 2012 г., полное содержание которой полностью включено в данное описание путем ссылки.
УРОВЕНЬ ТЕХНИКИ
По оценкам, в 2012 г. более чем у 1,6 миллиона людей будет диагностирован рак. Например, самым распространенным типом рака у женщин является рак молочной железы, и это заболевание ответственно за один из самых высоких показателей смертности из всех форм рака, поражающих женщин. Современное лечение рака молочной железы ограничивается тотальной или частичной мастэктомией, лучевой терапией или химиотерапией. Почти 230000 случаев рака в 2012 г. будут относиться к раку молочной железы, что, по оценкам, приведет к 40000 смертельных исходов. См. Siegel et al., Ca Cancer J Clin 2012; 62: 10-29.
Ряд случаев смерти от рака вызван гематологическими видами рака, включая лейкозы, миеломы и лимфомы. В 2012 г. почти 80000 случаев рака будут представлять собой лимфомы, которые, по оценкам, приведут к 20000 случаев смерти.
Лучевая терапия, химиотерапия и хирургическое вмешательство являются первичными способами лечения рака. Однако эти способы лечения наиболее успешны только при выявлении рака на ранней стадии. После достижения раком инвазивных/метастатических стадий, линии внедряющихся клеток или метастазирующих клеток могут избежать выявления, приводя, таким образом, к рецидивам, что требует лечения, которое является высокотоксичным. В этот момент и раковые клетки, и непораженные клетки пациента подвергаются токсичной терапии, приводящей, наряду с другими осложнениями, к ослаблению иммунной системы.
В связи с этим, в данной области сохраняется потребность в новых способах лечения рака, такого как рак молочной железы или лимфомы, у пациента.
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
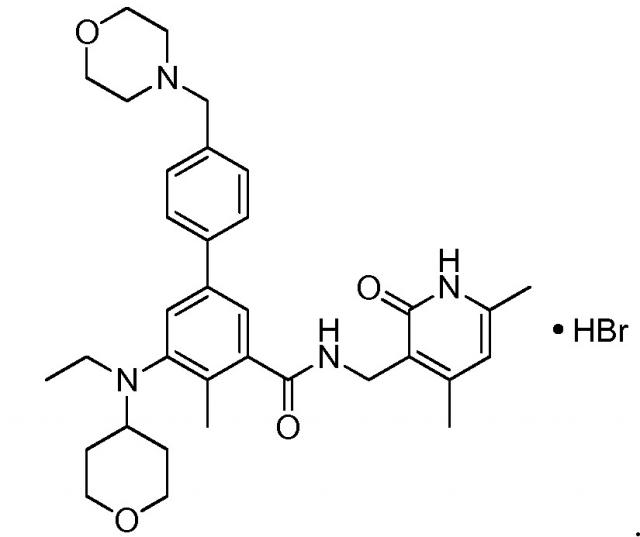
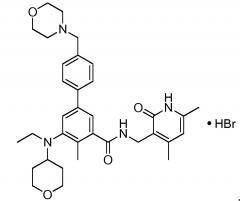
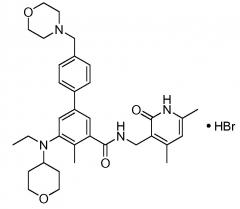
Соответственно, настоящее изобретение относится к гидробромиду N-((4,6-диметил-2-оксо-1,2-дигидропиридин-3-ил)метил)-5-(этил(тетрагидро-2H-пиран-4-ил)амино)-4-метил-4'-(морфолинометил)-[1,1'-бифенил]-3-карбоксамида:
Изобретение также относится к определенной полиморфной форме гидробромида N-((4,6-диметил-2-оксо-1,2-дигидропиридин-3-ил)метил)-5-(этил(тетрагидро-2H-пиран-4-ил)амино)-4-метил-4'-(морфолинометил)-[1,1'-бифенил]-3-карбоксамида («полиморф A», или «полиморф A гидробромида N-((4,6-диметил-2-оксо-1,2-дигидропиридин-3-ил)метил)-5-(этил(тетрагидро-2H-пиран-4-ил)амино)-4-метил-4'-(морфолинометил)-[1,1'-бифенил]-3-карбоксамида»). Как указано в настоящей заявке, представленный здесь гидробромид, а также полиморф A проявляют физические свойства, которые можно использовать для получения новых фармакологических свойств, и которые можно использовать в лекарственном веществе и разработке лекарственного продукта.
В одном варианте осуществления гидробромид является кристаллическим. В другом варианте осуществления гидробромид по существу не содержит примеси. В другом варианте осуществления гидробромид представляет собой кристаллическое твердое вещество, по существу не содержащее аморфный гидробромид N-((4,6-диметил-2-оксо-1,2-дигидропиридин-3-ил)метил)-5-(этил(тетрагидро-2H-пиран-4-ил)амино)-4-метил-4'-(морфолинометил)-[1,1'-бифенил]-3-карбоксамида.
В другом аспекте изобретение относится к фармацевтической композиции, содержащей описанный выше гидробромид и фармацевтически приемлемый носитель или разбавитель.
В одном аспекте описанный выше гидробромид получают, используя способ, включающий объединение N-((4,6-диметил-2-оксо- 1,2-дигидропиридин-3-ил)метил)-5-(этил(тетрагидро-2H-пиран-4-ил)амино)-4-метил-4'-(морфолинометил)-[1,1'-бифенил]-3-карбоксамида с бромистоводородной кислотой.
Полиморф A N-((4,6-диметил-2-оксо-1,2-дигидропиридин-3-ил)метил)-5-(этил(тетрагидро-2H-пиран-4-ил)амино)-4-метил-4'-(морфолинометил)-[1,1'-бифенил]-3-карбоксамида можно определить в соответствии с его профилем порошковой рентгеновской дифракции. Соответственно, в одном варианте осуществления полиморф характеризуется картиной порошковой рентгеновской дифракции, имеющей один или несколько характерных пиков, выраженных в градусах 2-тета, примерно при 3,9+/-0,3 градуса, примерно 17,5+/-0,3 градуса и примерно 22,0+/-0,3 градуса 2-тета. В другом варианте осуществления полиморф характеризуется картиной порошковой рентгеновской дифракции, имеющей характерные пики, выраженные в градусах 2-тета, примерно при 3,9+/-0,3 градуса, примерно 17,5+/-0,3 градуса и примерно 22,0+/-0,3 градуса 2-тета. В еще одном варианте осуществления полиморф характеризуется картиной порошковой рентгеновской дифракции, имеющей характерные пики, выраженные в градусах 2-тета, примерно при 3,9+/-0,3 градуса, 10,1+/-0,3 градуса, 14,3+/-0,3 градуса, 17,5+/-0,3 градуса, 18,7+/-0,3 градуса, 20,6+/-0,3 градуса, 20,9+/-0,3 градуса, 21,8+/-0,3 градуса, 22,0+/-0,3 градуса, 23,3+/-0,3 градуса и 23,6+/-0,3 градуса 2-тета. В еще одном варианте осуществления полиморф характеризуется картиной порошковой рентгеновской дифракции по существу в соответствии с фиг. 1. В другом варианте осуществления полиморф характеризуется картиной порошковой рентгеновской дифракции по существу в соответствии с таблицей 1.
Полиморф A можно также определить в соответствии с его термограммой, полученной дифференциальной сканирующей калориметрией. В одном варианте осуществления полиморф характеризуется термограммой, полученной дифференциальной сканирующей калориметрией, имеющую характерный пик, выраженный в единицах °C при температуре 255+/-5°C. В одном варианте осуществления полиморф характеризуется термограммой, полученной дифференциальной сканирующей калориметрией, по существу в соответствии с фиг. 3.
В одном аспекте полиморф A получают, используя способ, включающий объединение N-((4,6-диметил-2-оксо-1,2-дигидропиридин-3-ил)метил)-5-(этил(тетрагидро-2H-пиран-4-ил)амино)-4-метил-4'-(морфолинометил)-[1,1'-бифенил]-3-карбоксамида с бромистоводородной кислотой.
В другом аспекте изобретение относится к способу перекристаллизации полиморфа A, который включает следующие стадии: (a) растворение полиморфа A в первом растворителе и (b) добавление второго растворителя с тем, чтобы указанный полиморф перекристаллизовался. В одном варианте осуществления первый растворитель представляет собой этанол, и второй растворитель представляет собой MTBE (простой метил-трет-бутиловый эфир). В другом варианте осуществления способ включает (a) растворение полиморфа A в этаноле, (b) нагревание смеси, (c) добавление MTBE к смеси, образуя осадок, содержащий указанный полиморф и фильтрацию осадка с тем, чтобы указанный полиморф перекристаллизовался.
В еще одном аспекте настоящее изобретение относится к фармацевтической композиции, содержащей полиморф A и фармацевтически приемлемый носитель или разбавитель.
Изобретение также относится к способу лечения рака, включающему введение нуждающемуся в нем индивиду терапевтически эффективного количества описанного выше гидробромида соединения, полиморфа A или фармацевтической композиции, содержащей любое из этих соединений. Можно лечить разнообразные виды рака, включая неходжкинскую лимфому или рак молочной железы.
В другом аспекте изобретение относится к способу ингибирования активности гистон-метилтрансферазы EZH2 у нуждающегося в нем индивида, включающему введение индивиду эффективного количества описанного выше гидробромида соединения, полиморфа A или фармацевтической композиции, содержащей любое из этих соединений.
В еще одном аспекте настоящее изобретение относится к способу ингибирования активности гистон-метилтрансферазы EZH2 in vitro, включающему введение описанного выше гидробромида соединения или полиморфа A.
Изобретение также относится к применению описанного выше гидробромида соединения, полиморфа A или фармацевтической композиции, содержащей любое из этих соединений, для получения лекарственного препарата для лечения рака у нуждающегося в лечении индивида.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг. 1 изображен профиль порошковой рентгеновской дифракции полиморфа A (моногидробромида).
На фиг. 2 изображен профиль порошковой рентгеновской дифракции дигидробромида соединения I.
На фиг. 3 изображена полученная дифференциальной сканирующей калориметрией термограмма полиморфа A.
На фиг. 4 изображена динамическая сорбция пара полиморфа A, которая демонстрирует низкую гигроскопичность данного соединения.
На фиг. 5 изображен анализ с использованием ВЭЖХ полиморфа A в течение трех дней при повышенной температуре. Полиморф A в течение этого времени продуцировал минимальное количество примесей.
На фиг. 6 изображена динамическая сорбция пара натриевой соли соединения I, которая демонстрирует значительную гигроскопичность данного соединения.
На фиг. 7 изображена динамическая сорбция пара гемисульфата соединения I, которая демонстрирует, что данное соединение имеет умеренно высокую гигроскопичность.
На фиг. 8 показаны данные дифференциальной сканирующей калориметрии моногидрохлорида соединения I, которые указывают на то, что данное соединение является слабо кристаллическим.
На фиг. 9 изображен профиль порошковой рентгеновской дифракции синтетического промежуточного соединения 5.
На фиг. 10 изображен профиль порошковой рентгеновской дифракции полиморфа B.
На фиг. 11 изображен профиль порошковой рентгеновской дифракции моногидробромида соединения I.
На фиг. 12-14 показаны результаты исследований in vivo гидробромида соединения I в линии клеток лимфомы человека.
На фиг. 15-16 показан противораковый эффект гидробромида соединения I на модели ксенотрансплантата лимфомы мыши.
На фиг. 17 изображен профиль порошковой рентгеновской дифракции синтетического промежуточного соединения 2.
На фиг. 18A и B изображен (A) профиль порошковой рентгеновской дифракции тригидрохлорида соединения I и (B) динамическая сорбция пара моногидрохлорида соединения I, которая демонстрирует значительную гигроскопичность данного соединения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Форма соли HBr и полиморфная форма A
Настоящее изобретение относится к гидробромиду N-((4,6-диметил-2-оксо-1,2-дигидропиридин-3-ил)метил)-5-(этил(тетрагидро-2H-пиран-4-ил)амино)-4-метил-4'-(морфолинометил)-[1,1'-бифенил]-3-карбоксамида:
Используемый здесь термин «соединение I» относится к N-((4,6-диметил-2-оксо-1,2-дигидропиридин-3-ил)метил)-5-(этил(тетрагидро-2H-пиран-4-ил)амино)-4-метил-4'-(морфолинометил)-[1,1'-бифенил]-3-карбоксамиду. Гидробромид соединения I можно применять для ингибирования активности гистон-метилтрансферазы EZH2 или у индивида, или in vitro. Гидробромид соединения I можно также применять для лечения рака у нуждающегося в лечении индивида.
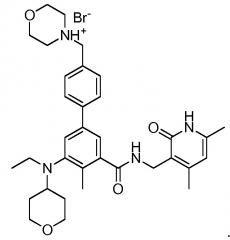
Соединение I может быть протонированным в одном или нескольких его оснόвных участках, таких как морфолиновая, дизамещенная анилиновая и/или пиридоновая части. Соответственно, в определенных вариантах осуществления изобретение относится к моногидробромиду, дигидробромиду или тригидробромиду соединения I. В одном варианте осуществления изобретение относится к моногидробромиду соединения I. Когда соединение представляет собой моногидробромид, то соединение может быть протонированным в любом оснόвном участке. В неограничивающем варианте осуществления соединение I протонировано у атома азота морфолинового заместителя, обеспечивая получение моногидробромида соединения I, имеющего следующую структуру:
Этот конкретный моногидробромид может именоваться «бромидом 4-((3'-(((4,6-диметил-2-оксо-1,2-дигидропиридин-3-ил)метил)карбамоил)-5'-(этил(тетрагидро-2H-пиран-4-ил)амино)-4'-метил-[1,1'-бифенил]-4-ил)метил)морфолин-4-ия». На фиг. 11 изображена кристаллическая структура данной конкретной солевой формы, полученная рентгеновским структурным анализом.
Гидробромид соединения I имеет ряд преимущественных физических свойств относительно его формы свободного основания, а также других солей свободного основания. В частности, гидробромид соединения I имеет низкую гигроскопичность по сравнению с другими солевыми формами соединения I. Для эффективности соединения при лечении в целом требуется, чтобы соединение было минимально гигроскопичным. Лекарственные формы, которые являются высокогигроскопичными, могут быть неустойчивыми, поскольку скорость растворения лекарственной формы может изменяться при его хранении в окружающих условиях с меняющейся влажностью. Гигроскопичность может также воздействовать на крупномасштабное манипулирование и производство соединения, поскольку может быть трудным определение действительной массы гигроскопического активного агента при получении фармацевтической композиции, содержащей этот агент. Гидробромид соединения I имеет низкую гигроскопичность по сравнению с другими солевыми формами соединения I. В связи с этим, он может храниться в течение существенных периодов и не подвергаться повреждающим изменениям, например растворимости, плотности или даже химического состава.
В дополнение к указанным выше преимуществам, гидробромид соединения I может быть получен в высококристаллической форме, которую можно использовать при получении фармацевтических препаративных форм, и он улучшит общее обращение, манипулирование и хранение лекарственного соединения. В предпочтительном варианте осуществления кристаллическая форма гидробромида соединения I представлена в форме, именуемой «полиморф A».
Способность вещества существовать в нескольких кристаллических формах определяется как полиморфизм; различные кристаллические формы конкретного вещества именуются «полиморфами». В целом, на полиморфизм воздействует способность молекулы вещества изменять ее конформацию или образовывать различные межмолекулярные или внутримолекулярные взаимодействия, в частности водородные связи, что отражается в различном расположении атомов в кристаллических решетках различных полиморфов. Напротив, общая внешняя форма вещества известна как «морфология», которая относится к внешней форме кристалла и присутствующим плоскостям без ссылки на внутреннюю структуру. Кристаллы могут проявлять различную морфологию на основании различных условий, таких как, например, скорость роста, перемешивание и присутствие примесей.
Различные полиморфы вещества могут обладать различными энергиями кристаллической решетки и, таким образом, в твердом состоянии они могут демонстрировать различные физические свойства, такие как форма, плотность, температура плавления, цвет, устойчивость, растворимость, скорость растворения и т.д., которые, в свою очередь, могут воздействовать на устойчивость, скорость растворения и/или биодоступность данного полиморфа и его пригодность для применения в качестве фармацевтического средства и в фармацевтических композициях.
Полиморф A является высококристаллическим и проявляет низкую гигроскопичность. Также этот полиморф может быть получен воспроизводимо, и небольшие изменения условий кристаллизации не приводят к получению различных кристаллических форм.
Доступ к различным полиморфам гидробромида соединения I желателен по ряду причин. Одна такая причина состоит в том, что отдельные полиморфы могут после кристаллизации включать различные примеси или химические остатки. Например, примеси можно удалить во время процесса превращения соединения I в полиморф A.
Без связи с теорией, полиморфные формы, проявляющие компактные профили кристаллов, имеют преимущества с точки зрения легкости фильтрации и легкости текучести. Полиморф A демонстрирует компактную форму кристаллов и поэтому обладает данными преимуществами.
В определенных вариантах осуществления полиморф A можно идентифицировать на основании характерных пиков при анализе порошковой рентгеновской дифракции. Порошковая рентгеновская дифракция, также именуемая XRPD, представляет собой научную технологию с использованием дифракции рентгеновских лучей, нейтронов или электронов на порошковых, микрокристаллических или других твердых материалах для структурной характеристики материалов. В одном варианте осуществления полиморф A характеризуется картиной порошковой рентгеновской дифракции, имеющей один или несколько характерных пиков, выраженных в градусах 2-тета, примерно при 3,9+/-0,3 градуса, примерно 17,5+/-0,3 градуса и примерно 22,0+/-0,3 градуса 2-тета. В другом варианте осуществления полиморф характеризуется картиной порошковой рентгеновской дифракции, имеющей характерные пики, выраженные в градусах 2-тета, примерно при 3,9+/-0,3 градуса, примерно 17,5+/-0,3 градуса и примерно 22,0+/-0,3 градуса 2-тета.
В одном варианте осуществления полиморф A характеризуется картиной порошковой рентгеновской дифракции, имеющей по меньшей мере 5 характерных пиков, выраженных в градусах 2-тета, примерно при 3,9+/-0,3 градуса, 10,1+/-0,3 градуса, 14,3+/-0,3 градуса, 17,5+/-0,3 градуса, 18,7+/-0,3 градуса, 20,6+/-0,3 градуса, 20,9+/-0,3 градуса, 21,8+/-0,3 градуса, 22,0+/-0,3 градуса, 23,3+/-0,3 градуса и 23,6+/-0,3 градуса 2-тета. В другом варианте осуществления полиморф A характеризуется картиной порошковой рентгеновской дифракции, имеющей по меньшей мере 6 характерных пиков, выраженных в градусах 2-тета, примерно при 3,9+/-0,3 градуса, 10,1+/-0,3 градуса, 14,3+/-0,3 градуса, 17,5+/-0,3 градуса, 18,7+/-0,3 градуса, 20,6+/-0,3 градуса, 20,9+/-0,3 градуса, 21,8+/-0,3 градуса, 22,0+/-0,3 градуса, 23,3+/-0,3 градуса и 23,6+/-0,3 градуса 2-тета. В еще одном варианте осуществления полиморф A характеризуется картиной порошковой рентгеновской дифракции, имеющей по меньшей мере 7 характерных пиков, выраженных в градусах 2-тета, примерно при 3,9+/-0,3 градуса, 10,1+/-0,3 градуса, 14,3+/-0,3 градуса, 17,5+/-0,3 градуса, 18,7+/-0,3 градуса, 20,6+/-0,3 градуса, 20,9+/-0,3 градуса, 21,8+/-0,3 градуса, 22,0+/-0,3 градуса, 23,3+/-0,3 градуса и 23,6+/-0,3 градуса 2-тета. В другом варианте осуществления полиморф A характеризуется картиной порошковой рентгеновской дифракции, имеющей по меньшей мере 8 характерных пиков, выраженных в градусах 2-тета, примерно при 3,9+/-0,3 градуса, 10,1+/-0,3 градуса, 14,3+/-0,3 градуса, 17,5+/-0,3 градуса, 18,7+/-0,3 градуса, 20,6+/-0,3 градуса, 20,9+/-0,3 градуса, 21,8+/-0,3 градуса, 22,0+/-0,3 градуса, 23,3+/-0,3 градуса и 23,6+/-0,3 градуса 2-тета. В еще одном варианте осуществления полиморф A характеризуется картиной порошковой рентгеновской дифракции, имеющей по меньшей мере 9 характерных пиков, выраженных в градусах 2-тета, примерно при 3,9+/-0,3 градуса, 10,1+/-0,3 градуса, 14,3+/-0,3 градуса, 17,5+/-0,3 градуса, 18,7+/-0,3 градуса, 20,6+/-0,3 градуса, 20,9+/-0,3 градуса, 21,8+/-0,3 градуса, 22,0+/-0,3 градуса, 23,3+/-0,3 градуса и 23,6+/-0,3 градуса 2-тета. В еще одном варианте осуществления полиморф характеризуется картиной порошковой рентгеновской дифракции, имеющей по меньшей мере 10 характерных пиков, выраженных в градусах 2-тета, примерно при 3,9+/-0,3 градуса, 10,1+/-0,3 градуса, 14,3+/-0,3 градуса, 17,5+/-0,3 градуса, 18,7+/-0,3 градуса, 20,6+/-0,3 градуса, 20,9+/-0,3 градуса, 21,8+/-0,3 градуса, 22,0+/-0,3 градуса, 23,3+/-0,3 градуса и 23,6+/-0,3 градуса 2-тета.
В еще одном варианте осуществления полиморф характеризуется картиной порошковой рентгеновской дифракции, имеющей характерные пики, выраженные в градусах 2-тета, примерно при 3,9+/-0,3 градуса, примерно 14,3+/-0,3 градуса, примерно 18,7+/-0,3 градуса, примерно 23,3+/-0,3 градуса и примерно 23,6+/-0,3 градуса 2-тета.
В еще одном варианте осуществления полиморф характеризуется картиной порошковой рентгеновской дифракции, имеющей характерные пики, выраженные в градусах 2-тета, примерно при 3,9+/-0,3 градуса, примерно 10,1+/-0,3 градуса, примерно 14,3+/-0,3 градуса, примерно 17,5+/-0,3 градуса, примерно 18,7+/-0,3 градуса, примерно 20,6+/-0,3 градуса, примерно 20,9+/-0,3 градуса, примерно 21,8+/-0,3 градуса, примерно 22,0+/-0,3 градуса, примерно 23,3+/-0,3 градуса и примерно 23,6+/-0,3 градуса 2-тета. В еще одном варианте осуществления полиморф характеризуется картиной порошковой рентгеновской дифракции, по существу, в соответствии с фиг. 1. В другом варианте осуществления полиморф характеризуется картиной порошковой рентгеновской дифракции, по существу, в соответствии с величинами 2-тета, перечисленными в таблице 1.
Используемый здесь термин «примерно» при ссылке на величины градуса 2-тета относится к указанной величине +/-0,3 градуса 2-тета.
Фармацевтические композиции, содержащие полиморф A, можно идентифицировать сравнением профилей порошковой рентгеновской дифракции композиций с профилем порошковой рентгеновской дифракции полиморфа A. Следует понимать, что фармацевтические композиции, содержащие полиморф A, могут проявлять не идентичные профили порошковой рентгеновской дифракции по сравнению с профилем порошковой рентгеновской дифракции чистого полиморфа A.
В определенных вариантах осуществления полиморф A можно идентифицировать на основании характерного пика, наблюдаемого на термограмме, полученной с помощью дифференциальной сканирующей калориметрии. Дифференциальная сканирующая калориметрия, или DSC, представляет собой термоаналитическую технологию, при которой разность в количестве тепла, требуемого для увеличения температуры образца и эталона, измеряют как функцию температуры. В одном варианте осуществления полиморф A характеризуется термограммой, полученной с использованием дифференциальной сканирующей калориметрии, в единицах °C при температуре примерно 255+/-5°C. В другом варианте осуществления полиморф A характеризуется термограммой, полученной с использованием дифференциальной сканирующей калориметрии, имеющей один эндотермический пик, наблюдаемый в диапазоне температуры 250-255°C. В другом варианте осуществления полиморф A характеризуется термограммой, полученной с использованием дифференциальной сканирующей калориметрии, по существу, в соответствии с фиг. 3.
В определенных вариантах осуществления полиморф A может содержать примеси. Неограничивающие примеры примесей включают нежелательные полиморфные формы или остаточные органические и неорганические молекулы, такие как растворители, вода или соли. В одном варианте осуществления полиморф A, по существу, не содержит примесей. В другом варианте осуществления полиморф A содержит менее чем 10 мас.% общего количества примесей. В другом варианте осуществления полиморф A содержит менее чем 5 мас.% общего количества примесей. В другом варианте осуществления полиморф A содержит менее чем 1 мас.% общего количества примесей. В еще одном варианте осуществления полиморф A содержит менее чем 0,1 мас.% общего количества примесей.
В определенных вариантах осуществления полиморф A представляет собой кристаллическое твердое вещество, по существу, не содержащее аморфный гидробромид соединения I. Используемый здесь термин «по существу, не содержащее аморфный гидробромид соединения I» означает, что соединение не содержит значительное количество аморфного гидробромида соединения I. В определенных вариантах осуществления присутствует по меньшей мере примерно 95 мас.% кристаллического полиморфа A. В еще одних вариантах осуществления изобретения присутствует по меньшей мере примерно 99 мас.% кристаллического полиморфа A.
В другом варианте осуществления полиморф A по существу не содержит полиморфа B.
Соль по изобретению и его кристаллическую форму полиморф A можно обнаружить вместе с другими веществами или их можно выделить. В некоторых вариантах осуществления соль по изобретению или ее кристаллическая форма является по существу выделенной. Под фразой «по существу выделенная» подразумевается, что соль или ее кристаллическая форма, по меньшей мере частично, или по существу отделена от окружающей среды, в которой она была образована или выявлена. Частичное отделение может включать, например, композицию, обогащенную солью по изобретению. Существенное отделение может включать композиции, содержащие по меньшей мере примерно 50%, по меньшей мере примерно 60%, по меньшей мере примерно 70%, по меньшей мере примерно 80%, по меньшей мере примерно 90%, по меньшей мере примерно 95%, по меньшей мере примерно 97% или по меньшей мере примерно 99 мас.% гидробромида соединения I и полиморфа A. Способы выделения соединений и их солей обычно используются в данной области.
И гидробромид соединения I, и полиморф A могут встречаться в виде любого целесообразного таутомера или смеси целесообразных таутомеров. Используемый здесь термин «таутомер» относится к одному из двух или более структурных изомеров, которые существуют в равновесии, и легко превращаются из одной изомерной формы в другую. Примеры включают кето-енольные таутомеры, такие как ацетон/пропен-2-ол, и тому подобные. Гидробромид соединения I и полиморф A могут иметь один или более таутомеров и поэтому включают различные изомеры, т.е. пиридин-2(1H)-он и соответствующий пиридин-2-ол. Все такие изомерные формы этих соединений специально включены в настоящее изобретение.
Получение формы в виде соли HBr и полиморфа A
Гидробромид соединения I, а также полиморф A, можно получить, используя известные технологии. Обычно солевую форму получают объединением в растворе соединения в форме свободного основания и кислоты, содержащей анион желаемой солевой формы, и затем выделением твердого солевого продукта из реакционного раствора (например, кристаллизацией, осаждением, выпариванием и т.д.). Можно использовать другие образующие соль технологии.
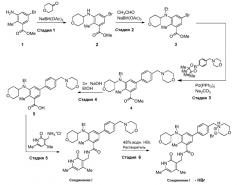
На демонстрируемой ниже схеме 1 представлен конкретный вариант осуществления для получения свободного основания соединения I, а также гидробромида соединения I. Вкратце, метил 3-амино-5-бром-2-метилбензоат (1) взаимодействует с дигидро-2H-пиран-4(3H)-оном в условиях восстановительного аминирования для образования метил 5-бром-2-метил-3-((тетрагидро-2H-пиран-4-ил)амино)бензоата (2) на стадии 1. На стадии 2 снова используют восстановительное аминирование для образования 5-бром-3-(этил(тетрагидро-2H-пиран-4-ил)амино)-2-метилбензоата (3). Затем это соединение взаимодействует в условиях реакции соединения Сузуки на стадии 3 для образования метил 5-(этил(тетрагидро-2H-пиран-4-ил)амино)-4-метил-4'-(морфолинометил)-[1,1'-бифенил]-3-карбоксилата (4), который гидролизуется до соответствующей кислоты (5) на стадии 4. На стадии 5 кислота (5) взаимодействует в условиях реакции соединения амида с гидрохлоридом 3-(аминометил)-4,6-диметил-дигидро-пиридин-2(1H)-она для образования соединения I.
Как показано, соединение I может затем взаимодействовать с водной HBr для образования гидробромида соединения I.
Схема 1
Описанный выше синтез имеет ряд преимуществ. Например, в нем используется ряд промежуточных соединений, которые можно получить в кристаллических формах, которые можно выделить. При использовании кристаллических промежуточных соединений необходимы технологии минимальной очистки (например, хроматография), приводя к общему улучшенному выходу конечного соединения I.
Соответственно, изобретение относится к промежуточному соединению 1 в кристаллической форме. В другом варианте осуществления изобретение относится к промежуточному соединению 2 в кристаллической форме. На фиг. 17 показан профиль порошковой рентгеновской дифракции кристаллического соединения 2. В еще одном варианте осуществления промежуточное соединение 5 является кристаллическим. На фиг. 9 показан профиль порошковой рентгеновской дифракции кристаллического соединения 5. В других вариантах осуществления соединения 2 и/или 5 получают по существу в чистой форме без использования хроматографии. Специалисту в данной области понятно, что кристаллизация промежуточных соединений необязательно протекает без усилий или эффективно.
Изобретение также относится к способу получения N-((4,6-диметил-2-оксо-1,2-дигидропиридин-3-ил)метил)-5-(этил(тетрагидро-2H-пиран-4-ил)амино)-4-метил-4'-(морфолинометил)-[1,1'-бифенил]-3-карбоксамида, включающему взаимодействие 5-(этил(тетрагидро-2H-пиран-4-ил)амино)-4-метил-4'-(морфолинометил)-[1,1'-бифенил]-3-карбоновой кислоты (5) с солью 3-(аминометил)-4,6-диметил-дигидро-пиридин-2(1H)-она. В одном варианте осуществления этого способа (5) представлена в кристаллической форме.
Соединение I может взаимодействовать с водной HBr в присутствии соответствующего растворителя для образования полиморфа A, конкретной кристаллической формы гидробромида. В одном варианте осуществления соединение I взаимодействует с водной HBr в присутствии этанола и этилацетата для образования полиморфа A.
После получения полиморфа он может быть перекристаллизован с использованием того же растворителя (или растворителей), которые использовались для получения полиморфа, или другого растворителя (или растворителей) для получения композиции, которая имеет увеличенную кристалличность. В целом, полиморф A можно перекристаллизовать растворением полиморфа в одном или нескольких растворителях, необязательно, с нагреванием, с последующей необязательной стадией охлаждения, и затем выделением кристаллической структуры посредством, например, стадии фильтрации. После первоначального растворения полиморфа в первом растворителе (или комбинации растворителей), дополнительный, другой растворитель можно добавить в любой точке процесса (до или после нагревания, до или после охлаждения и т.д.) для получения желаемой кристаллической структуры. Например, первый растворитель можно использовать для растворения полиморфного соединения, и затем второй растворитель (например, противорастворитель) можно добавлять для вызова осаждения полиморфа из раствора. В одном варианте осуществления воду добавляют к первому растворителю для содействия растворению полиморфа.
Неограничивающие примеры растворителей, которые можно использовать для перекристаллизации полиморфа A, следующие: метанол, этанол, этилацетат, простой метил-трет-бутиловый эфир, вода, изопропиловый спирт, тетрагидрофуран, ацетон, ацетонитрил, и 2-метилтетрагидрофуран, а также их комбинация. Неограничивающими примерами комбинаций растворителей, которые можно использовать для перекристаллизации полиморфа A, являются (растворитель и противорастворитель, где воду можно добавлять к первому растворителю для содействия растворению полиморфа): метанол/вода и этилацетат, изопропиловый спирт/вода и этилацетат, тетрагидрофуран/вода и этилацетат, ацетон и этилацетат, ацетонитрил/вода и этилацетат, этанол/вода и простой метил-трет-бутиловый эфир, изопропиловый спирт/вода и простой метил-трет-бутиловый эфир, этанол/вода и тетрагидрофуран, изопропиловый спирт/вода и ацетон и этанол/вода и этилацетат. В конкретных вариантах осуществления комбинациями растворителей являются метанол/вода и этилацетат, изопропиловый спирт/вода и этилацетат, этанол/вода и 2-метилтетрагидрофуран и метанол/2-метилтетрагидрофуран.
В одном аспекте полиморф A получают, используя способ, включающий объединение N-((4,6-диметил-2-оксо-1,2-дигидропиридин-3-ил)метил)-5-(этил(тетрагидро-2H-пиран-4-ил)амино)-4-метил-4'-(морфолинометил)-[1,1'-бифенил]-3-карбоксамида с бромистоводородной кислотой.
В другом аспекте изобретение относится к способу перекристаллизации полиморфа A, который включает следующие стадии: (a) растворение полиморфа A в первом растворителе и (b) добавление второго растворителя с тем, чтобы указанный полиморф перекристаллизовался. В одном варианте осуществления первый растворитель представляет собой этанол, а второй растворитель представляет собой MTBE. В другом варианте осуществления способ включает (a) растворение полиморфа A в этаноле, (b) нагревание смеси, (c) добавление MTBE к смеси, образуя осадок, содержащий указанный полиморф, и фильтрацию осадка с тем, чтобы указанный полиморф перекристаллизовался.
Фармацевтические композиции
В другом аспекте изобретение относится к фармацевтической композиции, содержащей гидробромид соединения I и фармацевтически приемлемый носитель или разбавитель. Изобретение также относится к фармацевтической композиции, содержащей полиморф A и фармацевтически приемлемый носитель или разбавитель.
Термин «фармацевтическая композиция» включает препараты, пригодные для введения млекопитающим, например людям. Когда соединения по настоящему изобретению вводятся в виде фармацевтических препаратов млекопитающим, например людям, то их можно вводить в чистом виде или в виде фармацевтической композиции, содержащей, например, от 0,1 до 99,9% (предпочтительнее, от 0,5 до 90%) активного ингредиента в комбинации с фармацевтически приемлемым носителем.
Описанные здесь соединения (т.е. гидробромид соединения I и полиморф A) можно комбинировать с фармацевтически приемлемым носителем в соответствии с обычными технологиями составления фармацевтических композиций. Используемый здесь термин «фармацевтически приемлемый носитель» может включать любой и все растворители, разбавители или другой жидкий носитель, дисперсию или вспомогательные суспендирующие материалы, поверхностно-активные средства, изотонические агенты, загустители или эмульгаторы, консерванты, твердые связывающие агенты, смазывающие вещества и тому подобные, в соответствии с конкретной желаемой лекарственной формой. В руководстве Remington's Pharmaceutical Sciences, Sixteenth Edition, E.W. Martin (Mack Publishing Co., Easton, Pa., 1980) описаны разнообразные носители, используемые при составлении фармацевтических композиций, и известные технологии для их получения. За исключением случаев, когда любая обычная среда носителя несовместима с соединениями по изобретению, например, в связи с оказанием нежелательного биологического эффекта или иным взаимодействием вредным образом с любым(и) другим(и) компонентом(ами) фармацевтической композиции, предусмотрено, что ее использование входит в пределы объема настоящего изобретения. Некоторые примеры материалов, которые могут служить в качестве фармацевтически приемлемых носителей, включают без ограничения сахара, такие как лактоза, глюкоза и сахароза; крахмалы, такие как кукурузный крахмал и картофельный крахмал; целлюлозу и ее производные, такие как карбоксиметилцеллюлоза натрия, этилцеллюлоза и ацетат целлюлозы; порошкообразный трагакант; солод; желатин; тальк; эксципиенты, такие как масло какао и воски для суппозиторий; масла, такие как арахисовое масло, масло хлопковых семян; масло сафлора, кунжутное масло; оливковое масло; кукурузное масло и соевое масло; гликоли, такие как полиэтиленгликоль; сложные эфиры, такие как этилолеат и этиллаурат; агар; забуферивающие агенты, такие как гидроксид магния и гидроксид алюминия; альгиновая кислота; апирогенная вода; изотонический солевой раствор; раствор Рингера; этиловый спирт и фосфатные буферные растворы, а также другие нетоксичные совместимые смазывающие вещества, такие как лаурилсульфат натрия и стеарат магния, а также красящие агенты, высвобождающие агенты, покрывающие агенты, подсластители, ароматизирующие и дезодорирующие агенты, консерванты и антиоксиданты также могут присутствовать в композиции, в соответствии с суждением составителя композиции.
Кроме того, носитель может принимать широкое разнообразие форм, в зависимости от формы желаемого для введения препарата, например, перорального, назального, ректального, вагинального, парентерального (включая внутривенные инъекции или инфузии). При получении композиций для пероральной лекарственной формы можно использовать любую из обычных фармацевтических сред. Обычные фармацевтические среды включают, например, воду, гликоли, масла, спирты, ароматизирующие агенты, консерванты, красящие агенты и тому подобные в случае пероральных жидких препаратов (таких как, например, суспензии, растворы, эмульсии и эликсиры); аэрозоли или носители, такие как крахмалы, сахара, микрокристаллическая целлюлоза, разбавители, гранулирующие агенты, смазывающие вещества, связывающие агенты, разрыхлители и тому подобные, в случае пероральных твердых препаратов (таких как, например, порошки, капсулы и таблетки).
Смачивающие агенты, эмульгаторы и смазывающие вещества, такие как лаурилсульфат натрия и стеарат магния, а также красящие агенты, подсластители, ароматизирующие и дезодорирующие агенты, консерванты и антиоксиданты также могут присутствовать в композициях.
Примеры фармацевтически приемлемых антиоксидантов включают растворимые в воде антиоксиданты, такие как аскорбиновая кислота, цистеин гидрохлорид, бисульфат натрия, метабисульфит натрия, сульфит натрия и тому подобные; растворимые в масле антиоксиданты, такие как аскорбилпальмитат, бутилированный гидроксианизол (BHA), бутилированный гидрокситолуол (BHT), лецитин, пропилгаллат, токоферолы и тому подобные; и хелатиру