Замещенные бензольные соединения
Иллюстрации
Показать всеИзобретение относится к замещенным бензольным соединениям, представленным формулами I, III, VI, VII.
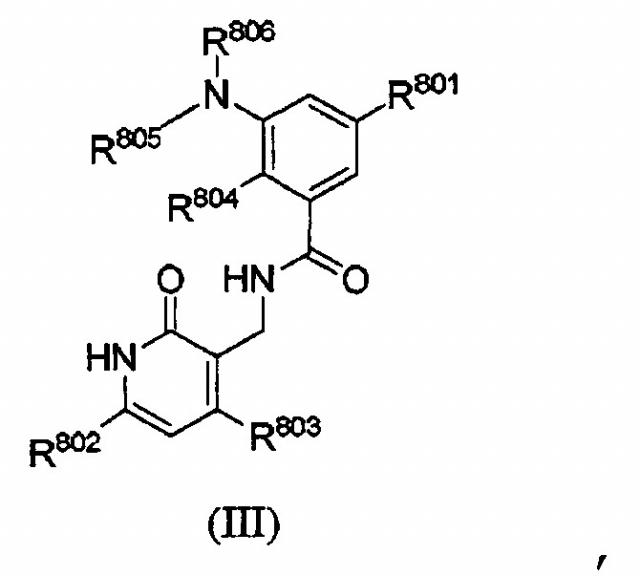
Соединение формулы III:
,
или его фармацевтически приемлемые соли, где R801 представляет собой C1-6 алкил, C2-6 алкинил, гетероциклоалкил, выбранный из морфолина, пирролидина, тетрагидротиофена, пиперидина, пиперазина, оксетана, пирана, тетрагидропирана, азетидина и тетрагидрофурана, фенил или гетероарил, выбранный из пиррола, фурана, тиофена, тиазола, изотиазола, имидазола, триазола, тетразола, пиразола, оксазола, изоксазола, пиридина, пиразина, пиридазина и пиримидина, каждый из которых содержит в качестве заместителя O-C1-6 алкил-Rx, где Rx представляет собой гидроксил или O-C1-3 алкил и Rx необязательно дополнительно замещен O-C1-3 алкилом; каждый из R802 и R803 независимо представляет собой H, галоген, C1-4 алкил или C1-6 алкоксил; каждый из R804 и R805 независимо представляет собой C1-4 алкил; и
R806 представляет собой –Qx-Tx, где Qx представляет собой связь или C1-4 алкильную связующую группу, Tx представляет собой H, тетрагидропиранил, пиперидинил, замещенный 1, 2 или 3 C1-4 алкильными группами, или циклогексил, содержащий в качестве заместителя N(C1-4 алкил)2, где один или оба C1-4 алкила необязательно содержат в качестве заместителя C1-6 алкокси; обладающие способностью ингибировать активность EZH2, а также к фармацевтическим композициям, содержащим указанные соединения, и способам лечения. 9 н. и 46 з.п. ф-лы., 7 табл., 3 пр.
Реферат
РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка испрашивает приоритет на основании предварительных заявок на патент США №№61/714140, поданной 15 октября 2012 г., 61/714145, поданной 15 октября 2012 г., 61/780703, поданной 13 марта 2013 г., и 61/786277, поданной 14 марта 2013 г. Содержание каждой из указанных предварительных заявок включено в настоящую заявку во всей полноте посредством ссылок.
УРОВЕНЬ ТЕХНИКИ
Существует постоянная потребность в новых агентах, действующих в качестве ингибиторов активности EZH2, которые можно применять для лечения расстройств, опосредованных EZH2 (например, рака).
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В одном из аспектов настоящее изобретение относится к замещенным бензольным соединениям нижепредставленных формул или к их фармацевтически приемлемым солям.
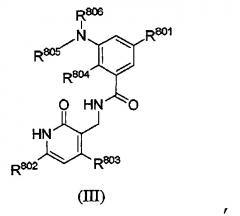
В одном из аспектов настоящее изобретение относится к соединению в соответствии с формулой III:
или к его фармацевтически приемлемой соли или сольвату, где
R801 представляет собой C1-6 алкил, C2-6 алкенил, C2-6 алкинил, C3-8 циклоалкил, 4-7-членный гетероциклоалкил, содержащий 1-3 гетероатома, фенил или 5- или 6-членный гетероарил, каждый из которых содержит в качестве заместителя O-C1-6 алкил-Rx или NH-C1-6 алкил-Rx, где Rx представляет собой гидроксил, О-C1-3 алкил или NH-C1-3 алкил, и Rx необязательно дополнительно замещен O-C1-3 алкилом или NH-C1-3 алкилом, кроме случаев, когда Rx представляет собой гидроксил; и R801 необязательно дополнительно замещен;
каждый из R802 и R803 независимо представляет собой Н, галоген, C1-4 алкил, C1-6 алкоксил или C6-C10 арилокси, каждый из которых необязательно замещен одним или более галогенами;
каждый из R804 и R805 независимо представляет собой C1-4 алкил; и
R806 представляет собой -Qx-Tx, где Qx представляет собой связь или C1-4 алкильную связующую группу, Tx представляет собой Н, необязательно замещенный C1-4 алкил, необязательно замещенный С3-С8 циклоалкил или необязательно замещенный 4-14-членный гетероциклоалкил.
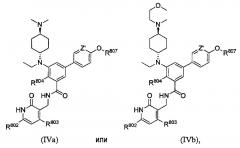
Подмножества соединений формулы III включают соединения формулы IVa или IVb и их фармацевтически приемлемые соли или сольваты:
где Z' представляет собой СН или N, и R807 представляет собой C2-3 алкил-Rx.
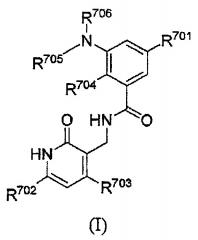
В другом аспекте настоящее изобретение относится к соединению в соответствии с формулой I:
,
или к его фармацевтически приемлемой соли или соль вату, где
R701 представляет собой Н, F, OR707, NHR707, -(С≡С)-(CH2)n7-R708, фенил, 5- или 6-членный гетероарил, C3-8 циклоалкил или 4-7-членный гетероциклоалкил, содержащий 1-3 гетероатома, где каждый из фенила, 5- или 6-членного гетероарила, C3-8 циклоалкила или 4-7-членного гетероциклоалкила независимо необязательно замещен одной или более группами, выбранными из галогена, C1-3 алкила, ОН, O-C1-6 алкила, NH-C1-6 алкила и C1-3 алкила, замещенного C3-8 циклоалкилом или 4-7-членным гетероциклоалкилом, содержащим 1-3 гетероатома, где каждый из O-C1-6 алкила и NH-C1-6 алкила необязательно замещен гидроксилом, O-C1-3 алкилом или NH-C1-3 алкилом, каждый из O-C1-3 алкила и NH-C1-3 алкила необязательно дополнительно замещен O-C1-3 алкилом или NH-C1-3 алкилом;
каждый из R702 и R703 независимо представляет собой Н, галоген, C1-4 алкил, C1-6 алкоксил или С6-С10 арилокси, каждый из которых необязательно замещен одним или более галогенами;
каждый из R704 и R705 независимо представляет собой C1-4 алкил;
R706 представляет собой циклогексил, содержащий в качестве заместителя N(C1-4 алкил)2, где один или оба C1-4 алкила содержат в качестве заместителя C1-6 алкокси; или R706 представляет собой тетрагидропиранил;
R707 представляет собой C1-4 алкил, необязательно замещенный одной или более группами, выбранными из гидроксила, C1-4 алкокси, амино, моно- или ди-C1-4 алкиламино, C3-8 циклоалкила и 4-7-членного гетероциклоалкила, содержащего 1-3 гетероатома, где каждый из C3-8 циклоалкила или 4-7-членного гетероциклоалкила независимо необязательно дополнительно замещен C1-3 алкилом;
R708 представляет собой C1-4 алкил, необязательно замещенный одной или более группами, выбранными из ОН, галогена и C1-4 алкокси, 4-7-членный гетероциклоалкил, содержащий 1-3 гетероатома, или O-C1-6 алкил, где 4-7-членный гетероциклоалкил необязательно дополнительно содержит в качестве заместителя ОН или C1-6 алкил; и
n7 равняется 0, 1 или 2.
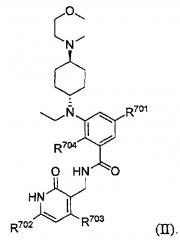
Подмножество соединений формулы I включает соединения формулы II и их фармацевтически приемлемые соли или сольваты:
В другом аспекте настоящее изобретение относится к соединению в соответствии с формулой V:
или к его фармацевтически приемлемой соли или сольвату, где
W1 представляет собой N или СН;
W2 представляет собой N или СН;
R401 представляет собой водород, C1-C6 алкил, C1-C6 галогеналкил;
R402 представляет собой (а) ОН, (b) (CH2)-О-(C1-C6 алкил),
(с) O(C1-C6 алкил), (d) (CH2)j-3-8-членный насыщенный, ненасыщенный или ароматический карбоцикл, (е) (CH2)k-3-8-членный насыщенный, ненасыщенный или ароматический гетероцикл, содержащий один или более гетероатомов, выбранных из группы, состоящей из азота, кислорода и серы, (f) О-(CH2)u-3-8-членный насыщенный, ненасыщенный или ароматический карбоцикл или (g) O-(CH2)v-3-8-членный насыщенный, ненасыщенный или ароматический гетероцикл, содержащий один или более гетероатомов, выбранных из группы, состоящей из азота, кислорода и серы, где (b)-(g) необязательно содержат в качестве заместителя R402a,
R402a представляет собой C1-C6 алкил, C1-C6 галогеналкил, ОН или O(C1-C6 алкил);
t равняется 1, 2 или 3;
u равняется 0, 1, 2 или 3;
v равняется 0, 1, 2 или 3;
j равняется 0, 1, 2 или 3; и
k равняется 0, 1, 2 или 3; при условии, что если R402 представляет собой пиперазинил, W1 и W2 представляют собой N.
В некоторых соединениях формулы V W1 представляет собой N, и W2 представляет собой СН.
В некоторых соединениях формулы V R401 представляет собой C1-C6 алкил. Например, R401 представляет собой метил или изопропил. Например, R401 представляет собой метил.
В некоторых соединениях формулы V R402 представляет собой (CH2)k-4-7-членный насыщенный гетероцикл, содержащий один или более атомов азота или кислорода.
В некоторых соединениях формулы V k равняется 0 или 1. Например, k равняется 0. Например, k равняется 1.
В некоторых соединениях формулы V R402 представляет собой азетидинил, пиперазинил или пиперидинил.
В некоторых соединениях R402 представляет собой (CH2)-азетидинил, (CH2)-пирролидинил, (CH2)-пиперидинил, (CH2)-морфолинил или (CH2)-диазепанил.
В некоторых соединениях формулы V t равняется 1.
В некоторых соединениях формулы V R402a представляет собой ОН, метил или метокси.
В другом аспекте настоящее изобретение относится к соединению в соответствии с формулой VI:
,
или к его фармацевтически приемлемой соли или сольвату, где
n5 равняется 0, 1 или 2;
R501 представляет собой С(Н) или N;
каждый из R502, R503, R504 и R505 независимо представляет собой C1-4 алкил;
R506 представляет собой циклогексил, содержащий в качестве заместителя N(C1-4 алкил) 2, или пиперидин, замещенный 1, 2 или 3 C1-4 алкильными группами;
если R501 представляет собой С(Н), R507 представляет собой морфолин; пиперидин, диазепан, пирролидин, азетидин, O-C1-6 алкил или O-гетероцикл, где гетероцикл представляет собой 4-7-членный гетероцикл, содержащий кислород или азот или и кислород, и азот, и где азот необязательно замещен C1-3 алкилом; где пиперидиновая, диазепановая, пирролидиновая или азетидиновая группы необязательно дополнительно содержат в качестве заместителя ОН, C1-6 алкил или O-C1-3 алкил;
или, если R501 представляет собой С(Н), R507 может представлять собой пиперазин, необязательно дополнительно замещенный C1-6 алкилом, при условии, что R506 представляет собой пиперидин, замещенный 1, 2 или 3 C1-4 алкильными группами;
если R501 представляет собой N, R507 представляет собой морфолин, пиперидин, пиперазин, диазепан, пирролидин, азетидин, O-C1-6 алкил или O-гетероцикл, где гетероцикл представляет собой 4-7-членный гетероцикл, содержащий кислород или азот или и кислород, и азот, и где азот необязательно замещен C1-3 алкилом;
где пиперидиновая, пиперазиновая, диазепановая, пирролидиновая или азетидиновая группы необязательно дополнительно содержат в качестве заместителя ОН, C1-6 алкил или O-C1-3 алкил.
В другом аспекте настоящее изобретение относится к соединению в соответствии с формулой VII:
,
или к его фармацевтически приемлемой соли или сольвату, где
n6 равняется 1 или 2;
каждый из R602, R603, R604 и R605 независимо представляет собой C1-4 алкил;
R606 представляет собой циклогексил, содержащий в качестве заместителя N(C1-4 алкил) 2, или пиперидин, замещенный 1, 2 или 3 C1-4 алкильными группами; и
R607 представляет собой морфолин, пиперидин, пиперазин, пирролидин, диазепан, азетидин или O-C1-6 алкил, где пиперидиновая, диазепановая или азетидиновая группы необязательно дополнительно содержат в качестве заместителя ОН или C1-6 алкил.
В настоящем изобретении также предложены фармацевтические композиции, содержащие один или более фармацевтически приемлемых носителей и одно или более соединений, выбранных из соединений любой из формул, описанных в настоящей заявке.
Другой аспект настоящего изобретения представляет собой способ лечения или предотвращения расстройства, опосредованного EZH2. Указанный способ включает введение субъекту, нуждающемуся в этом, терапевтически эффективного количества одного или более соединений, выбранных из соединений любой из формул, описанных в настоящей заявке. Указанное расстройство, опосредованное EZH2, представляет собой заболевание, расстройство или состояние, по меньшей мере частично опосредованное активностью EZH2. В одном из вариантов реализации расстройство, опосредованное EZH2, относится к повышенной активности EZH2. В одном из вариантов реализации расстройство, опосредованное EZH2, представляет собой раковое заболевание. Раковое заболевание, опосредованное EZH2, может представлять собой лимфому, лейкоз или меланому, например, диффузную крупноклеточную В-клеточную лимфому (ДККЛ), неходжкинскую лимфому (НХЛ), фолликулярную лимфому, хронический миелогенный лейкоз (ХМЛ), острый миелоидный лейкоз, острый лимфоцитарный лейкоз, лейкоз смешанного происхождения или миелодиспластические синдромы (МДС). В одном из вариантов реализации раковое заболевание, опосредованное EZH2, может представлять собой злокачественную рабдоидную опухоль или INI1-дефицитную опухоль. Гистологический диагноз злокачественной рабдоидной опухоли зависит от идентификации характерных рабдоидных клеток (крупных клеток - с эксцентрически расположенными ядрами и избытком эозинофильной цитоплазмы) и иммуноги с то химии с использованием антител к виментину, кератину и мембранному антигену клеток эпителия. В большинстве злокачественных рабдоидных опухолей ген SMARCB1/INI1, расположенный в сегменте хромосомы 22q11.2, инактивируется путем делеций и/или мутаций. В одном из вариантов реализации злокачественные рабдоидные опухоли могут представлять собой INI1-дефицитную опухоль.
Если не указано иное, любое описание способа лечения включает применение соединений для обеспечения лечения или профилактики, представленной в настоящем описании, а также применение соединений для получения лекарственных средств для лечения или предотвращения указанного состояния. Лечение включает лечение людей или животных, отличных от людей, включая модели грызунов и другие модели заболеваний. Способы, описанные в настоящей заявке, могут быть использованы для выявления кандидатов, подходящих для лечения или предотвращения расстройств, опосредованных EZH2. Например, в настоящем изобретении также предложены способы определения ингибитора EZH2 дикого типа, мутантного EZH2 (например, Y641, А677 и/или А687 мутантного EZH2) или их обоих.
Например, способ включает стадию введения субъекту, имеющему раковое заболевание с аномальным метилированием Н3-K27, эффективного количества одного или более соединений формул, описанных в настоящей заявке, где соединение(я) ингибирует(ют) гистонметилтрансферазную активность EZH2, таким образом обеспечивая лечение ракового заболевания. Примеры аномального метилирования Н3-K27 могут включать общее увеличение и/или изменение распределения ди- или триметилирования Н3-K27 в хроматине раковых клеток.
Например, раковое заболевание выбрано из группы, состоящей из раковых заболеваний со сверхэкспрессией EZH2 или других субъединиц PRC2, содержащих мутации с потерей функции в Н3-K27-деметилазах, таких как UTX, или со сверхэкспрессией вспомогательных белков, таких как PHF19/PCL3, способных увеличивать и/или изменять направление действия EZH2 (см. ссылки в Sneeringer et al. Proc Natl Acad. Sci USA 107 (49): 20980-5, 2010).
Например, способ включает стадию введения субъекту, имеющему раковое заболевание со сверхэкспрессией EZH2, терапевтически эффективного количества одного или более соединений формул, описанных в настоящей заявке, где соединение(я) ингибирует(ют) гистонметилтрансферазную активность EZH2, таким образом обеспечивая лечение ракового заболевания.
Например, способ включает стадию введения субъекту, имеющему раковое заболевание с мутацией с потерей функции в Н3-K27-деметилазе UTX, терапевтически эффективного количества одного или более соединений формул, описанных в настоящей заявке, где соединение(я) ингибирует(ют) гистонметилтрансферазную активность EZH2, таким образом обеспечивая лечение ракового заболевания.
Например, способ включает стадию введения субъекту, имеющему раковое заболевание со сверхэкспрессией вспомогательного(ых) компонента(ов) PRC2, такого(их) как PHF19/PCL3, терапевтически эффективного количества одного или более соединений формул, описанных в настоящей заявке, где соединение(я) ингибирует(ют) гистонметилтрансферазную активность EZH2, таким образом обеспечивая лечение ракового заболевания.
В другом аспекте настоящее изобретение относится к способу модулирования активности EZH2 дикого типа, каталитической субъединицы комплекса PRC2, который катализирует моно-, ди- и триметилирование лизина 27 гистона Н3 (Н3-K27). Например, настоящее изобретение относится к способу ингибирования активности EZH2 в клетке. Указанный способ можно осуществлять in vitro или in vivo.
В другом аспекте настоящее изобретение относится к способу ингибирования превращения Н3-K27 в триметилированный Н3-K27 у субъекта. Указанный способ включает введение субъекту терапевтически эффективного количества одного или более соединений формул, описанных в настоящей заявке, для ингибирования гистонметилтрансферазной активности EZH2, что приводит к ингибированию превращения Н3-K27 в триметилированный Н3-K27 у субъекта.
Например, способ включает стадию введения субъекту, имеющему раковое заболевание с экспрессией мутантного EZH2, терапевтически эффективного количества одного или более соединений формул, описанных в настоящей заявке, где соединение(я) ингибирует(ют) гистонметилтрансферазную активность EZH2, таким образом обеспечивая лечение ракового заболевания.
Например, раковое заболевание выбирают из группы, состоящей из фолликулярной лимфомы и диффузной крупноклеточной В-клеточной лимфомы (ДККЛ) В-клеточного подтипа клеток герминативного центра. Например, раковое заболевание представляет собой лимфому, лейкоз или меланому. Предпочтительно, лимфома представляет собой неходжкинскую лимфому (НХЛ), фолликулярную лимфому или диффузную крупноклеточную В-клеточную лимфому. Альтернативно, лейкоз представляет собой хронический миелогенный лейкоз (ХМЛ), острый миелоидный лейкоз, острый лимфоцитарный лейкоз или лейкоз смешанного происхождения.
Например, предраковое состояние представляет собой миелодиспластические синдромы (МДС, ранее известные как предлейкозы).
Например, раковое заболевание представляет собой гематологическое раковое заболевание.
Например, раковое заболевание выбирают из группы, состоящей из рака мозга и центральной нервной системы (ЦНС), рака головы и шеи, рака почек, рака яичников, рака поджелудочной железы, лейкоза, рака легких, лимфомы, миеломы, саркомы, рака молочной железы и рака предстательной железы. Предпочтительно, субъект, нуждающийся в лечении, представляет собой субъекта, у которого ранее был диагностирован, диагностирован или имеется предрасположенность к развитию рака мозга и ЦНС, рака почек, рака яичников, рака поджелудочной железы, лейкоза, лимфомы, миеломы и/или саркомы. Примеры рака мозга и ЦНС включают медуллобластому, олигодендроглиому, атипичную тератоидную/рабдоидную опухоль, карциному хориоидного сплетения, папиллому хориоидного сплетения, эпендимому, глиобластому, менингиому, нейроглиальную опухоль, олигоастроцитому, олигодендроглиому и пинеобластому. Примеры рака яичников включают светлоклеточную аденокарциному яичников, эндометриоидную аденокарциному яичников и серозную аденокарциному яичников. Примеры рака поджелудочной железы включают протоковую аденокарциному поджелудочной железы и эндокринную опухоль поджелудочной железы. Примеры саркомы включают хондросаркому, светлоклеточную саркому мягких тканей, саркому Юинга, желудочно-кишечную стромальную опухоль, остеосаркому, рабдомиосаркому и саркому без дополнительных уточнений (БДУ). Альтернативно, раковые заболевания, подвергающиеся лечению при помощи соединений согласно настоящему изобретению, представляют собой не НХЛ раковые заболевания.
Например, раковое заболевание выбирают из группы, состоящей из медуллобластомы, олигодендроглиомы, светлоклеточной аденокарциномы яичников, эндометриоидной аденокарциномы яичников, серозной аденокарциномы яичников, протоковой аденокарциномы поджелудочной железы, эндокринной опухоли поджелудочной железы, злокачественной рабдоидной опухоли, астроцитомы, атипичной тератоидной/рабдоидной опухоли, карциномы хориоидного сплетения, папилломы хориоидного сплетения, эпендимомы, глиобластомы, менингиомы, нейроглиальной опухоли, олигоастроцитомы, олигодендроглиомы, пинеобластомы, карциносаркомы, хордомы, внегонадной герминогенной опухоли, экстраренальной рабдоидной опухоли, шванномы, плоскоклеточной карциномы кожи, хондросаркомы, светлоклеточной саркомы мягких тканей, саркомы Юинга, желудочно-кишечной стромальной опухоли, остеосаркомы, рабдомиосаркомы и саркомы без дополнительных уточнений (БДУ). Предпочтительно, раковое заболевание представляет собой медуллобластому, светлоклеточную аденокарциному яичников, эндометриоидную аденокарциному яичников, протоковую аденокарциному поджелудочной железы, злокачественную рабдоидную опухоль, атипичную тератоидную/рабдоидную опухоль, карциному хориоидного сплетения, папиллому хориоидного сплетения, глиобластому, менингиому, пинеобластому, карциносаркому, экстраренальную рабдоидную опухоль, шванному, плоскоклеточную карциному кожи, хондросаркому, саркому Юинга, эпителиоидную саркому, ренальную медуллокарциному, диффузную крупноклеточную В-клеточную лимфому, фолликулярную лимфому и/или саркому БДУ. Более предпочтительно, раковое заболевание представляет собой злокачественную рабдоидную опухоль, медуллобластому и/или атипичную тератоидную/рабдоидную опухоль.
Например, способ включает стадию введения субъекту, имеющему раковое заболевание с экспрессией мутантного EZH2, терапевтически эффективного количества одного или более соединений формул, описанных в настоящей заявке, где соединение(я) ингибирует(ют) активность (например, гистонметилтрансферазную активность) мутантного EZH2, EZH2 дикого типа или их обоих, таким образом обеспечивая лечение ракового заболевания.
Например, способ дополнительно включает стадии проведения исследования для детектирования мутантного EZH2 в образце, содержащем раковые клетки, от субъекта, нуждающегося в лечении.
В другом аспекте настоящее изобретение относится к способу выбора терапии для пациента с заболеванием, связанным с метилированием белка, опосредованным EZH2. Способ включает стадии определения наличия мутаций в гене EZH2 субъекта; и выбора терапии для лечения заболевания на основе наличия мутаций в гене EZH2. В одном из вариантов реализации терапия включает введение одного или более соединений согласно настоящему изобретению. В одном из вариантов реализации способ дополнительно включает введение одного или более соединений согласно настоящему изобретению субъекту. В одном из вариантов реализации заболевание представляет собой раковое заболевание, и мутация представляет собой мутацию Y641.
В другом аспекте предложен способ лечения пациента, нуждающегося в лечении, включающий стадии определения наличия мутаций в гене EZH2 и лечения пациента, нуждающегося в лечении, на основе наличия мутаций в гене EZH2, где терапия включает введение соединений согласно настоящему изобретению. В одном из вариантов реализации пациент представляет собой пациента с раковым заболеванием, и мутация представляет собой мутацию Y641.
В другом аспекте настоящее изобретение относится к способу модулирования гистонметилтрансферазной активности EZH2 дикого типа и мутантного EZH2, каталитической субъединицы комплекса PRC2, который катализирует моно-, ди- и триметилирование лизина 27 гистона Н3 (Н3-K27). Например, настоящее изобретение относится к способу ингибирования активности некоторых мутантных форм EZH2 в клетке. Мутантные формы EZH2 включают замещение тирозином 641 (Y641, также Tyr641) остатка другой аминокислоты EZH2 дикого типа. Указанный способ можно проводить in vitro или in vivo.
В другом аспекте настоящее изобретение относится к способу ингибирования превращения Н3-K27 в триметилированный Н3-K27 у субъекта. Способ включает введение субъекту с экспрессией мутантного EZH2 терапевтически эффективного количества одного или более соединений любой из формул, описанных в настоящей заявке, для ингибирования гистонметилтрансферазной активности EZH2, что приводит к ингибированию превращения Н3-K27 в триметилированный Н3-K27 у субъекта. Например, ингибирование гистонметилтрансферазной активности наблюдается в случае EZH2, мутантного по Y641. Например, соединение согласно настоящему изобретению селективно ингибирует гистонметилтрансферазную активность EZH2, мутантного по Y641. Например, EZH2, мутантный по Y641, выбирают из группы, состоящей из Y641C, Y641F, Y641H, Y641N и Y641S.
Способ ингибирования превращения Н3-K27 в триметилированный Н3-K27 у субъекта также может включать проведение исследования для детектирования мутантного EZH2 в образце, полученном от субъекта, перед введением субъекту с экспрессией мутантного EZH2 терапевтически эффективного количества одного или более соединений любой из формул, описанных в настоящей заявке. Например, проведение исследования для детектирования мутантного EZH2 включает повторное секвенирование всего генома или повторное секвенирование целевого участка, позволяющее определить нуклеиновую кислоту, кодирующую мутантный EZH2. Например, проведение исследования для детектирования мутантного EZH2 включает приведение образца в контакт с антителом, которое специфически связывается с полипептидом или его фрагментом, характерным для мутантного EZH2. Например, проведение исследования для детектирования мутантного EZH2 включает приведение образца в очень строгих условиях в контакт с зондом нуклеиновой кислоты, который гибридизуется с образованием нуклеиновой кислоты, кодирующей полипептид или его фрагмент, характерный для мутантного EZH2.
Кроме того, настоящее изобретение также относится к способу определения ингибитора мутантного EZH2, EZH2 дикого типа или их обоих. Способ включает стадии объединения выделенного EZH2 с гистоновым субстратом, донорной метильной группой и исследуемым соединением, где гистоновый субстрат содержит форму Н3-K27, выбранную из группы, состоящей из неметилированного Н3-K27, монометилированного Н3-K27, диметилированного Н3-K27 и любой их комбинации; и проведения исследования для определения метилирования Н3-K27 (например, образование триметилированного Н3-K27) в гистоновом субстрате, что позволяет определить применимость исследуемого соединения в качестве ингибитора EZH2, если метилирование Н3-K27 (например, образование триметилированного Н3-K27) в присутствии исследуемого соединения меньше, чем метилирование Н3-K27 (например, образование триметилированного Н3-K27) при отсутствии исследуемого соединения.
В одном из вариантов реализации проведение исследования для определения метилирования Н3-K27 в гистоновом субстрате включает измерение включения меченых метильных групп.
В одном из вариантов реализации меченые метильные группы представляют собой изотопно меченые метильные группы.
В одном из вариантов реализации проведение исследования для определения метилирования Н3-K27 в гистоновом субстрате включает приведение гистонового субстрата в контакт с антителом, специфически связывающимся с триметилированным Н3-K27.
Также объем настоящего изобретения охватывает способ определения селективного ингибитора мутантного EZH2. Способ включает стадии объединения выделенного мутантного EZH2 с гистоновым субстратом, донорной метильной группой и исследуемым соединением, где гистоновый субстрат содержит форму Н3-K27, выбранную из группы, состоящей из монометилированного Н3-K27, диметилированного Н3-K27 и комбинации монометилированного Н3-K27 и диметилированного Н3-K27, с образованием таким образом исследуемой смеси; объединения выделенного EZH2 дикого типа с гистоновым субстратом, донорной метильной группой и исследуемым соединением, где гистоновый субстрат содержит форму Н3-K27, выбранную из группы, состоящей из монометилированного Н3-K27, диметилированного Н3-K27 и комбинации монометилированного Н3-K27 и диметилированного Н3-K27, с образованием таким образом контрольной смеси; проведения исследования для определения метилирования гистонового субстрата в каждой из исследуемой смеси и контрольной смеси; вычисления отношения (а) триметилирования с мутантным EZH2 и исследуемым соединением (М+) к (b) триметилированию с мутантным EZH2 при отсутствии исследуемого соединения (М-); вычисления отношения (с) триметилирования с EZH2 дикого типа и исследуемым соединением (WT+) к (d) триметилированию с EZH2 дикого типа при отсутствии исследуемого соединения (WT-); сравнения соотношения (а)/(b) и соотношения (c)/(d); и определения применимости исследуемого соединения в качестве ингибитора мутантного EZH2, если соотношение (а)/(b) меньше, чем соотношение (c)/(d).
В настоящем изобретении также предложен способ определения субъекта в качестве кандидата для прохождения лечения с применением одного или более соединений согласно настоящему изобретению. Способ включает стадии проведения исследования для определения мутантного EZH2 в образце, полученном от субъекта; и определения субъекта с экспрессией мутантного EZH2 в качестве кандидата для прохождения лечения с применением одного или более соединений согласно настоящему изобретению, где указанное(ые) соединение(я) ингибирует(ют) гистонметилтрансферазную активность EZH2.
Другой аспект настоящего изобретения представляет собой способ ингибирования превращения Н3-K27 в триметилированный Н3-K27. Способ включает стадию приведения EZH2 дикого типа, мутантного EZH2 или их обоих в контакт с гистоновым субстратом, содержащим Н3-K27 и эффективное количество соединения согласно настоящему изобретению, где указанное соединение ингибирует гистонметилтрансферазы активность EZH2, что обеспечивает ингибирование превращения Н3-K27 в триметилированный Н3-K27.
Кроме того, соединения или способы, описанные в настоящей заявке, могут быть применены в исследованиях (например, изучение эпигенетических ферментов) и других нетерапевтических целях.
В некоторых вариантах реализации предпочтительные соединения, представленные в настоящей заявке, имеют улучшенные фармакологические и/или фармакокинетические свойства, например, более низкие скорости выведения, сниженный риск проявления нежелательных межлекарственных взаимодействий при комбинированной терапии за счет снижения зависящего от времени обратимого ингибирования ферментов цитохрома Р-450.
Если не указано иное, все технические и научные термины, применяемые в настоящей заявке, имеют то же значение, которое обычно понимает специалист в области техники, к которой относится настоящее изобретение. Если в контексте явно не указано иное, в настоящем описании формы единственного числа также включают формы множественного числа. Несмотря на то, что при реализации на практике или при тестировании настоящего изобретения могут быть использованы способы и материалы, схожие или эквивалентные способам и материалам, описанным в настоящей заявке, подходящие способы и материалы описаны ниже. Все публикации, патентные заявки, патенты и другие ссылки, указанные в настоящей заявке, включены посредством ссылки. Ссылки, приведенные в настоящей заявке, не являются уровнем техники по отношению к заявленному изобретению. В случае противоречий, настоящее описание, включая определения, будет иметь решающее значение. Кроме того, материалы, способы и примеры представлены только в иллюстративных целях и не предназначены для ограничения.
Другие признаки и преимущества настоящего изобретения понятны из нижеприведенного подробного описания и формулы изобретения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящем изобретении предложены новые замещенные бензольные соединения, способы получения соединений, фармацевтические композиции, содержащие соединения, и различные способы применения соединений.
В одном из аспектов настоящее изобретение относится к соединению в соответствии с формулой I:
,
или к его фармацевтически приемлемой соли или сольвату, где
R701 представляет собой Н, F, OR707, NHR707, - (С≡С)-(CH2)n7-R708, фенил, 5- или 6-членный гетероарил, C3-8 циклоалкил или 4-7-членный гетероциклоалкил, содержащий 1-3 гетероатома, где каждый из фенила, 5- или 6-членного гетероарила, C3-8 циклоалкила или 4-7-членного гетероциклоалкила независимо необязательно замещен одной или более группами, выбранными из галогена, C1-3 алкила, ОН, O-C1-6 алкила, NH-C1-6 алкила и C1-3 алкила, замещенного C3-8 циклоалкилом или 4-7-членным гетероциклоалкилом, содержащим 1-3 гетероатома, где каждый из O-C1-6 алкила и NH-C1-6 алкила необязательно замещен гидроксилом, O-C1-3 алкилом или NH-C1-3 алкилом, каждый из O-C1-3 алкила и NH-C1-3 алкила необязательно дополнительно замещен O-C1-3 алкилом или NH-C1-3 алкилом;
каждый из R702 и R703 независимо представляет собой Н, галоген, C1-4 алкил, C1-6 алкоксил или C6-C10 арилокси, каждый из которых необязательно замещен одним или более галогенами;
каждый из R704 и R705 независимо представляет собой C1-4 алкил;
R706 представляет собой циклогексил, содержащий в качестве заместителя N(C1-4 алкил)2, где один или оба C1-4 алкила содержат в качестве заместителя C1-6 алкокси; или R706 представляет собой тетрагидропиранил;
R707 представляет собой C1-4 алкил, необязательно замещенный одной или более группами, выбранными из гидроксила, C1-4 алкокси, амино, моно- или ди-C1-4 алкиламино, C3-8 циклоалкила и 4-7-членного гетероциклоалкила, содержащего 1-3 гетероатома, где каждый из C3-8 циклоалкила или 4-7-членного гетероциклоалкила независимо необязательно дополнительно замещен C1-3 алкилом;
R708 представляет собой C1-4 алкил, необязательно замещенный одной или более группами, выбранными из ОН, галогена и C1-4 алкокси, 4-7-членный гетероциклоалкил, содержащий 1-3 гетероатома, или O-C1-6 алкил, где 4-7-членный гетероциклоалкил необязательно дополнительно содержит в качестве заместителя ОН или C1-6 алкил; и
n7 равняется 0, 1 или 2.
Например, R706 представляет собой циклогексил, содержащий в качестве заместителя N(C1-4 алкил)2, где один из C1-4 алкилов является незамещенным, а другой содержит в качестве заместителя метокси.
Например, где R706 представляет собой
Подмножество соединений формулы I включает соединения формулы II и их фармацевтически приемлемые соли:
Соединения формулы I или II могут содержать один или более следующих признаков:
Например, R702 представляет собой метил или изопропил.
Например, R703 представляет собой метил или метоксил.
Например, R704 представляет собой метил.
Например, R701 представляет собой OR707.
Например, R707 представляет собой C1-3 алкил, необязательно содержащий в качестве заместителя ОСН3 или морфолин.
Например, R701 представляет собой Н или F.
Например, R701 представляет собой тетрагидропиранил, необязательно содержащий в качестве заместителя метил, метокси, этил, замещенный морфолином, или -OCH2CH2OCH3.
Например, R701 представляет собой фенил, необязательно содержащий в качестве заместителя метил, метокси, этил, замещенный морфолином, или -OCH2CH2OCH3.
Например, R701 представляет собой 5-членный гетероарил (например, пирролил, фурил, тиофенил, тиазолил, изотиазолил, имидазолил, триазолил, тетразолил, пиразолил, оксазолил или изоксазолил), необязательно содержащий в качестве заместителя метил, метокси, этил, замещенный морфолином, или -OCH2CH2OCH3.
Например, R701 представляет собой 6-членный гетероарил (например, пиридил, пиразинил, пиридазинил или пиримидил), необязательно содержащий в качестве заместителя метил, метокси, этил, замещенный морфолином, или -OCH2CH2OCH3.
Например, R701 представляет собой пиридил, пиримидил, пиразинил, имидазолил или пиразолил, каждый из которых необязательно содержащий в качестве заместителя метил, метокси, этил, замещенный морфолином, или -OCH2CH2OCH3.
Например, R708 представляет собой морфолин, пиперидин, пиперазин, пирролидин, диазепан или азетидин, каждый из которых необязательно содержит в качестве заместителя ОН или C1-6 алкил.
Например, R708 представляет собой морфолин.
Например, R708 представляет собой пиперазин, замещенный C1-6 алкилом.
Например, R708 представляет собой трег-бутил или С(СН3)2ОН.
Например, соединения формулы I или II не включают N-((4,6-диметил-2-оксо-1,2-дигидропиридин-3-ил)метил)-3-(этил(тетрагидро-2Н-пиран-4-ил)амино)-2-метил-5-((1-метилпиперидин-4-ил)этинил)бензамид (т.е. соединение 105).
Например, соединения формулы I или II не включают N-((4,6-диметил-2-оксо-1,2-дигидропиридин-3-ил)метил)-3-(этил(4-((2-метоксиэтил)(метил)амино)циклогексил)амино)-2-метил-5-(3-морфолинопроп-1-ин-1-ил)бензамид или N-((4,6-диметил-2-оксо-1,2-дигидропиридин-3-ил)метил)-3-(этил((1r,4r)-4-((2-метоксиэтил)(метил)амино)циклогексил)амино)-2-метил-5-(3-морфолинопроп-1-ин-1-ил)бензамид (т.е. соединение 2).
Например, соединения формулы I или II включают N-((4,6-диметил-2-оксо-1,2-дигидропиридин-3-ил)метил)-3-(этил(тетрагидро-2Н-пиран-4-ил)амино)-2-метил-5-((1-метилпиперидин-4-ил)этинил)бензамид (т.