Полиморфные формы
Иллюстрации
Показать всеИзобретение относится к новым полиморфным формам 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты. Технический результат: получены новые полиморфные формы 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, которые обладают стабильностью и негигроскопичностью, которые могут использоваться для получения лекарственного средства для лечения состояний, опосредованных активностью 5-HT4. 12 н. и 4 з.п. ф-лы, 3 табл., 11 пр., 14 ил.
Реферат
Область техники, к которой относится настоящее изобретение
[0001] Настоящее изобретение относится к новым кристаллическим формам 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты. Более конкретно, настоящее изобретение относится к полиморфным формам (полиморфной форме I, полиморфной форме II, полиморфной форме III, полиморфной форме IV, полиморфной форме V и полиморфной форме VI) и к способам их получения, к композициям, содержащим такие полиморфы, и к их применению.
Известный уровень техники
[0002] 4-{[4-({[4-(2,2,2-Трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновая кислота раскрыта в PL1 как агонист рецептора 5-HT4, которую можно использовать для лечения или облегчения болезненных состояний, опосредованных активностью рецептора 5-HT4; в частности, агонистом рецептора 5-HT4, такой как гастроэзофагеальная рефлюксная болезнь (GERD), желудочно-кишечные заболевания, нарушения перистальтики желудка, диспепсия неязвенного происхождения, функциональная диспепсия (FD), синдром раздраженного кишечника (IBS), запор, диспепсия, эзофагит, гастроэзофагеальная болезнь, гастрит, тошнота, заболевания центральной нервной системы, болезнь Альцгеймера, когнитивные расстройства, рвота, мигрень, неврологические заболевания, боль, сердечно-сосудистые нарушения, сердечная недостаточность, нарушения сердечного ритма, диабет и синдром апноэ (см. NPL 1-13 и PL 2-7).
[0003] Просто белое твердое вещество было получено известными ранее способами получения 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, раскрытыми в PL 1. Поэтому специалистам не были известны ни кристаллы, ни смеси кристаллических форм.
[0004]
Список цитирования
Патентная литература
[0005] {PL 1} WO2006/090224.
{PL 2} Патент США № 6106864.
{PL 3} WO 00/35298.
PL 4} WO 91/11172.
{PL 5} WO 94/02518.
{PL 6} WO 98/55148.
{PL 7} PCT/JP2012/003288.
Непатентная литература
[0006] {NPL 1} Bockaert J. et al., TiPs 13;141-45, 1992.
{NPL 2} Ford A. P et al., Med. Res. Rev. 13: 633-62, 1993.
{NPL 3} Gullikson G. W. et al., Drug Dev. Res. 26; 405-17, 1992.
{NPL 4} Richard M. Eglen et al., TiPs 16; 391-98, 1995.
{NPL 5} Bockaert J. et al., CNS Drugs 1; 6-15, 1994.
{NPL 6} Romanelli M. N. et al., Arzheim Forsch./Drugs Res., 43; 913-18, 1993.
{NPL 7} Kaumann A. J. et al., Naunyn-Schmiedebergs Arch Pharmacol., 344; 150-59, 1991.
{NPL 8} Remington’s Pharmaceutical Sciences, 19th Edition (Mack Publishing Company, 1995).
{NPL 9} Expert Opinion in Therapeutic Patents, H(6), 981-986, by Liang and Chen (2001).
{NPL 10} Tablets, Vol. 1, by H. Lieberman and L. Lachman (Marcel Dekker, New York, 1980).
{NPL 11} Pharmaceutical Technology On-line, 25(2), 1-14, by Verma et al. (2001).
{NPL 12} J Pharm Sci, 88 (10), 955-958, by Finnin and Morgan (October 1999).
{NPL 13} Evrard, B., et al., Journal of Controlled Release 96 (3), pp. 403-410, 2004.
{NPL 14} Byrn S. R. et al., Solid-State Chemistry of Drugs 2nd ed., pp 3-43 и 461-503, 1999, SSCI, Inc.
Сущность изобретения
Техническая проблема
[0007] Как хорошо известно специалистам в данной области, всегда было желательно найти или получить кристаллы или кристаллические формы для создания лекарственных средств, улучшенных с различных точек зрения, включая составление рецептуры и изготовление лекарственных средств (см. Byrn S. R. et al., Solid-State Chemistry of Drugs 2nd ed., pp 3-43 и 461-503, 1999, SSCI, Inc.).
[0008] Соответственно, были предприняты серьезные попытки обнаружить или получить кристаллы или кристаллическую форму 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты после того, как указанное соединение было раскрыто в 2006 (WO2006/090224) Pfizer Inc. Например, сложные эфиры, такие как этилацетат, спирты, такие как метанол, этанол и изопропиловый спирт, нитрилы, такие как ацетонитрил, простые эфиры, такие как диэтиловый эфир и MTBE (метил трет-бутиловый эфир), кетоны, такие как ацетон и метилэтилкетон, галогенированные углеводороды, такие как дихлорметан и хлороформ, были использованы в качестве растворителей при перекристаллизации, но все они не привели к нужному результату.
[0009] Несмотря на столь большое количество попыток, до сих пор не были идентифицированы фармацевтически приемлемые кристаллические формы указанного соединения.
Как было указано выше, если этилацетат использовали в качестве растворителя при перекристаллизации обычным способом, хорошо известным специалистам в данной области, получали только неудачные результаты. После обширных и тщательных исследований авторам настоящего изобретения удалось найти весьма специфические и уникальные условия получения кристаллической формы, используя этилацетат, что привело к получению долгожданной кристаллической формы (полиморфной формы I) указанного соединения.
[0010] Как раскрыто в рабочем примере настоящего изобретения, белое твердое вещество указанного соединения суспендировали в этилацетате в течение 1 дня при 40°C и 5 дней при комнатной температуре (обычно от 15 до 35°C) с получением полиморфной формы I. Ранее специалисты в данной области никогда не предполагали таких условий кристаллизации.
[0011] Полиморфную форму II получали из полиморфной формы I, полученной в указанных выше специфических условиях. Полиморфная форма I превращается в полиморфную форму II при температуре 110°C или выше, но полученная полиморфная форма II превращается в полиморфную форму I в условиях измерения, таких как поток азота при охлаждении полиморфной формы II до комнатной температуры. Авторы настоящего изобретения также выявили условия получения полиморфной формы II при комнатной температуре в диапазоне от 15 до 35°C.
Кроме того, после получения затравочных кристаллов кристаллической формы, та же самая кристаллическая форма, как правило, моет быть легко получена при синтезе в малых масштабах. При крупномасштабном синтезе существенным является температурный контроль для получения фармацевтически приемлемой кристаллической формы.
[0012] В соответствии с указанным, полиморфная форма I и полиморфная форма II были включены в патентную заявку PCT/JP2012/003288 тех же авторов, что и авторы рассматриваемой заявки, которая никогда не была опубликована для ознакомления.
[0013] Полиморфная форма III была получена из полиморфной формы I в следующих условиях. Полиморфная форма I превращается в полиморфную форму III в условиях высокой относительной влажности, например, 70°C/75% RH. И даже в условиях 25°C/60% RH полиморфная форма I постепенно превращается в полиморфную форму III.
Кроме того, полиморфная форма III также была получена в условиях от 3 до 5% (об./об.) воды в изопропиловом спирте или этаноле с использованием затравки полиморфной формы III.
[0014] Полиморфная форма IV также была получена из полиморфной формы III в следующих условиях. Полиморфная форма III начинает превращаться в полиморфную форму IV при 90°C, а затем полностью превращается в полиморфную форму IV при 100°C.
[0015] Полиморфная форма V также была получена из полиморфной формы I в следующих условиях. Полиморфная форма I превращается в полиморфную форму V в условиях суспензии в воде. Кроме того, полиморфная форма V также была получена в условиях от 10 до 50% (об./об.) воды в тетрагидрофуране.
[0016] Полиморфная форма VI была получена из полиморфной формы I в следующих условиях. Полиморфная форма VI также была получена в условиях от 5 до 10% (об./об.) воды в ацетоне, от 5 до 10% (об./об.) воды в ацетонитриле или 5% (об./об.) воды в тетрагидрофуране.
[0017] Полиморфная форма VI превращается в полиморфную форму III, когда ее высушивают.
[0018] Целью настоящего изобретения является создание фармацевтически приемлемых кристаллических форм 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, которые можно было бы легко, экономично и воспроизводимо получать для применения в фармацевтических композициях, обладающих постоянными эксплуатационными характеристиками, такими как, например, превосходная стабильность и негигроскопичность. Кроме того, целью настоящего изобретения является создание способов получения композиций, в которых содержатся и используются такие полиморфные формы.
Решение проблемы
[0019] Таким образом, в настоящем изобретении предложены:
[1]
Полиморфная форма III 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, которая характеризуется порошковой дифракционной картиной рентгеновских лучей (PXRD), полученной в результате облучения источником Cu-K-альфа, которая включает основные пики при 2-тета 5,5, 10,1, 10,9, 13,9, 15,7, 18,5, 18,9, 20,8, 21,8 и 23,6 (°), где каждый пик имеет предел погрешности +/- 0,2 (°);
[0020] [2]
Полиморфная форма III 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, которая характеризуется инфракрасным спектром (ИК) (диффузное отражение), который демонстрирует полосы поглощения при 4376-4370, 3525-3519, 3462, 2946-2940, 2127, 1713, 1624, 1537, 1508, 1441, 1368, 1287, 1157, 1121, 1103, 1063, 1034, 1013, 916, 870, 816, 781, 746, 733, 654, 619, 590 и 556 см-1, где каждый пик имеет предел погрешности +/- 2 см-1.
[0021] [3]
Полиморфная форма III 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано в п.[1] или [2], которая дополнительно характеризуется данными дифференциальной сканирующей калориметрии (DSC), которые демонстрируют эндотермический пик при 170°C, где указанная температура измерения имеет предел погрешности +/- 1°C;
[0022] [4]
Полиморфная форма IV 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, которая характеризуется картиной порошковой дифракции рентгеновских лучей (PXRD), полученной в результате облучения источником Cu-K-альфа, которая включает основные пики при 2-тета 5,6, 9,8, 10,2, 11,3, 13,6, 13,8, 15,7, 17,0, 18,7, 19,3, 21,3 и 22,8 (°), где каждый пик имеет предел погрешности +/- 0,2 (°);
[0023] [5]
Полиморфная форма V 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, которая характеризуется картиной порошковой дифракции рентгеновских лучей (PXRD), полученной в результате облучения источником Cu-K-альфа, которая включает основные пики при 2-тета 5,2, 10,0, 10,3, 11,6, 15,5, 17,7, 18,6, 19,2, 20,5, 21,7, 22,4 и 24,3 (°), где каждый пик имеет предел погрешности +/- 0,2 (°);
[0024] [6]
Полиморфная форма V 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, которая характеризуется инфракрасным спектром (ИК) (диффузное отражение), который демонстрирует полосы поглощения при 4381-4375, 4130, 2853, 2760, 1701, 1630, 1618, 1541, 1387, 1281, 1186, 1171, 1157, 1123, 1103, 1069, 1032, 1013, 991, 962, 917, 787, 748, 731, 660 и 650 см-1, где каждый пик имеет предел погрешности +/- 2 см-1.
[0025] [7]
Полиморфная форма V 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано в п.[5] или [6], которая дополнительно характеризуется данными дифференциальной сканирующей калориметрии (DSC), которые демонстрируют эндотермический пик при 169°C, где указанная температура измерения имеет предел погрешности +/- 1°C;
[0026] [8]
Полиморфная форма VI 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, которая характеризуется картиной порошковой дифракции рентгеновских лучей (PXRD), полученной в результате облучения источником Cu-K-альфа, которая включает основные пики при 2-тета 10,3, 10,6, 11,4, 12,6, 18,8, 19,2, 19,5, 20,2, 21,2 и 21,7 (°), где каждый пик имеет предел погрешности +/- 0,2 (°);
[0027] [9]
Полиморфная форма VI 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, которая характеризуется инфракрасным спектром (ИК) (диффузное отражение), который демонстрирует полосы поглощения при 4378-4372, 3944, 3467-3461, 3306, 2959, 2884, 2835, 1711, 1537, 970, 920, 883 и 785 см-1, где каждый пик имеет предел погрешности +/- 2 см-1.
[0028] [10]
Полиморфная форма VI 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано п.[8] или [9], которая дополнительно характеризуется данными дифференциальной сканирующей калориметрии (DSC), которые демонстрируют эндотермический пик при 170°C, где указанная температура измерения имеет предел погрешности +/-1°C;
[0029] [11]
Фармацевтическая композиция, включающая полиморфную форму 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано в любом одном из пп.[1]-[10], вместе с одним или более из фармацевтически приемлемых эксципиентов;
[0030] [12]
Полиморфная форма 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано в любом одном из пп.[1]-[10], предназначенная для применения в качестве лекарственного средства;
[0031] [13]
Применение полиморфной формы 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано в любом одном из пп.[1]-[10], или фармацевтической композиции, как описано в п.[11], для получения лекарственного средства для лечения, паллиативного лечения или профилактики болезненных состояний, опосредованных активностью рецепторов 5-HT4;
[0032] [14]
Способ лечения болезненных состояний, опосредованных активностью рецепторов 5-HT4, который включает введение эффективного количества полиморфной формы 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано в любом одном из пп.[1]-[10], или фармацевтической композиции, как раскрыто в п.[11], животному, включая человека, нуждающемуся в таком лечении;
[0033] [15]
Способ получения полиморфной формы III 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано в любом одном из пп.[1]-[3], включающий стадию выдерживания полиморфной формы I в условиях относительной влажности в интервале от 60 до 100% при комнатной температуре от 15 до 35°C или выше;
[0034] [16]
Способ получения полиморфной формы III 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано в любом одном из пп.[1]-[3], включающий стадию выдерживания полиморфной формы I в условиях от 3 до 5% (об./об.) воды в спирте, предпочтительно в этиловом спирте или изопропиловом спирте;
[0035] [17]
Способ получения полиморфной формы IV 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано в п.[4], включающий стадию размещения полиморфной формы III в атмосфере при температуре 90-115°C, предпочтительно от 90°C до 100°C;
[0036] [18]
Способ получения полиморфной формы V 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано в любом одном из пп.[5]-[7], включающий стадию выдерживания полиморфной формы I в условиях образования полиморфной формы V, без образования каких-либо других полиморфных форм, в смеси воды и органического растворителя. Более конкретно, указанный способ можно осуществить способом, описанным, например, в указанном ниже примере 7; и
[0037] [19]
Способ получения полиморфной формы VI 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано в любом одном из пп.[8]-[10], включающий стадию выдерживания полиморфной формы I в условиях образования полиморфной формы VI, без образования какой-либо другой полиморфной формы, в смеси воды и органического растворителя.
Преимущества осуществления настоящего изобретения
[0038] Как указано выше, задачей настоящего изобретения является создание или получение кристаллов или кристаллической формы для создания лекарственного средства, подходящего с различных точек зрения, включая составление рецептуры и изготовление лекарственного средства. Неожиданно было обнаружено, что указанной задачи можно достичь с помощью настоящего изобретения, в котором предложены кристаллические полиморфные формы 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, известные как полиморфная форма I, полиморфная форма II, полиморфная форма III, полиморфная форма IV, полиморфная форма V и полиморфная форма VI.
До сих пор не было найдено фармацевтически приемлемых кристаллических форм указанного соединения, несмотря на многочисленные попытки специалистов в данной области.
[0039] Все полиморфы по настоящему изобретению обладают превосходными и неожиданными преимуществами по сравнению с белым твердым веществом, раскрытым ранее в WO2006/090224. Обнаружено, что полиморфная форма I и полиморфная форма II более стабильны, чем белое твердое вещество, раскрытое ранее в WO2006/090224. Кроме того, с точки зрения гигроскопичности обе формы обладают превосходными и неожиданными преимуществами по сравнению с белым твердым веществом, раскрытым ранее в WO2006/090224.
[0040] Кроме того, полиморфная форма III и полиморфная форма V также обладают более низкой гигроскопичностью по сравнению с белым твердым веществом, раскрытым ранее в WO2006/090224.
Как указано выше, полиморфная форма I обладает хорошей стабильностью в твердом состоянии по сравнению со стабильностью белого твердого вещества, раскрытого ранее в WO2006/090224, но полиморфная форма III обладает более высокой стабильностью в твердом состоянии, чем полиморфная форма I.
Полиморфная форма IV представляет собой хорошее промежуточное соединение для получения полиморфной формы III, поскольку полиморфную форму IV легко превратить в полиморфную форму III, если ее просто охладить. Полиморфная форма VI также представляет собой хорошее промежуточное соединение для получения полиморфной формы III, поскольку полиморфную форму VI легко превратить в полиморфную форму III, если ее просто высушить.
[0041] Кроме того, было обнаружено, что полиморфные формы по настоящему изобретению применимы для крупномасштабного синтеза. Они обладают приемлемыми характеристиками в твердом состоянии для создания твердой лекарственной формы.
Краткое описание рисунков
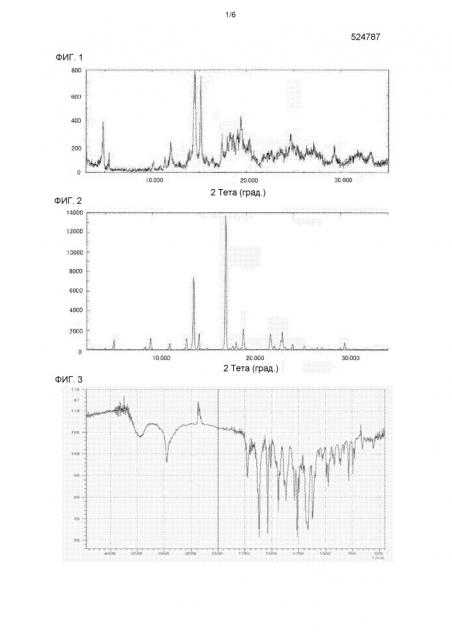
[0042] ФИГ.1 демонстрирует картину PXRD сравнительного продукта, полученного по способу получения 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, описанному в примере 1 WO2006/090224.
[0043] ФИГ.2 демонстрирует картину PXRD полиморфной формы I 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты.
[0044] ФИГ.3 демонстрирует ИК спектр (KBr) полиморфной формы I 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты.
[0045] ФИГ.4 демонстрирует ИК спектр (диффузное отражение) полиморфной формы I 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты.
[0046] ФИГ.5 демонстрирует картину PXRD полиморфной формы II 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты.
[0047] ФИГ.6 демонстрирует ИК спектр (KBr) полиморфной формы II 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты.
[0048] ФИГ.7 демонстрирует картину PXRD полиморфной формы III 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты.
[0049] ФИГ.8 демонстрирует ИК спектр (диффузное отражение) полиморфной формы III 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты.
[0050] ФИГ.9 демонстрирует картину PXRD полиморфной формы IV 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты.
[0051] ФИГ.10 демонстрирует картину PXRD полиморфной формы V 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты.
[0052] ФИГ.11 демонстрирует ИК спектр (диффузное отражение) полиморфной формы V 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты.
[0053] ФИГ.12 демонстрирует картину PXRD полиморфной формы VI 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты.
[0054] ФИГ.13 демонстрирует ИК спектр (диффузное отражение) полиморфной формы VI 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты.
[0055] ФИГ.14 демонстрирует изменение массы в % (увеличение массы в %) полиморфной формы I, полиморфной формы III, полиморфной формы V и белого твердого вещества, раскрытого ранее в WO2006/090224, в каждом из условий RH.
Предпочтительный вариант осуществления настоящего изобретения
[0056] Соответственно, в настоящем изобретении предложена кристаллическая полиморфная форма I 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, которая характеризуется картиной порошковой дифракции рентгеновских лучей (PXRD), полученной в результате облучения источником Cu-K-альфа, которая включает основные пики при 2-тета 5,9, 9,3, 9,8, 11,9, 13,7, 14,3, 15,0, 17,8, 18,2-19,3, 19,7, 22,6, 23,4-24,5 и 24,9 (°), где каждый пик имеет предел погрешности +/- 0,2 (°);
[0057] Полиморфная форма I 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано выше, которая дополнительно характеризуется данными дифференциальной сканирующей калориметрии (DSC), которые демонстрируют эндотермический пик при 169°C, где указанная температура измерения имеет предел погрешности +/- 1°C;
[0058] Полиморфная форма I 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано выше, которая дополнительно характеризуется инфракрасным спектром (ИК) (KBr), который демонстрирует полосы поглощения при 2948, 1723, 1615, 1535, 1506, 1437, 1383, 1366, 1287, 1262, 1245, 1180, 1164, 1120, 1095, 1059, 1032, 992, 974, 935, 918, 869, 858, 828, 784, 746, 732, 654 и 556 (см-1), где каждый пик имеет предел погрешности +/- 2 (см-1);
[0059] Полиморфная форма II 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, которая характеризуется картиной порошковой дифракции рентгеновских лучей (PXRD), полученной в результате облучения источником Cu-K-альфа, которая включает основные пики при 2-тета 5,8, 9,7, 10,5, 11,8, 12,4, 13,5, 14,2, 14,6-14,9, 15,4, 17,8, 18,2, 19,9-20,5, 21,2, 21,8, 23,6, 24,1 и 24,6 (°), где каждый пик имеет предел погрешности +/- 0,2 (°);
[0060] Полиморфная форма II 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано выше, которая дополнительно характеризуется данными дифференциальной сканирующей калориметрии (DSC), которые демонстрируют эндотермический пик примерно при 167-169°C; и
[0061] Полиморфная форма II 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано выше, которая дополнительно характеризуется инфракрасным спектром (ИК) (KBr), который демонстрирует полосы поглощения при 2950, 1724, 1614, 1534, 1507, 1438, 1383, 1366, 1287, 1262, 1245, 1180, 1164, 1121, 1095, 1059, 1031, 992, 974, 935, 918, 869, 857, 828, 784, 746, 732, 654 и 555 (см-1), где каждый пик имеет предел погрешности +/- 2 (см-1).
[0062] Полиморфная форма III 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, которая характеризуется картиной порошковой дифракции рентгеновских лучей (PXRD), полученной в результате облучения источником Cu-K-альфа, которая включает основные пики при 2-тета 5,5, 10,1, 10,9, 13,9, 15,7, 18,5, 18,9, 20,8, 21,8 и 23,6 (°), где каждый пик имеет предел погрешности +/- 0,2 (°);
[0063] Полиморфная форма III 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано выше, которая дополнительно характеризуется данными дифференциальной сканирующей калориметрии (DSC), которые демонстрируют эндотермический пик при 170°C, где указанная температура измерения имеет предел погрешности +/- 1°C;
[0064] Полиморфная форма IV 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, которая характеризуется картиной порошковой дифракции рентгеновских лучей PXRD, полученной в результате облучения источником Cu-K-альфа, которая включает основные пики при 2-тета 5,6, 9,8, 10,2, 11,3, 13,6, 13,8, 15,7, 17,0, 18,7, 19,3, 21,3 и 22,8 (°), где каждый пик имеет предел погрешности +/- 0,2 (°);
[0065] Полиморфная форма V 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, которая характеризуется картиной порошковой дифракции рентгеновских лучей (PXRD), полученной в результате облучения источником Cu-K-альфа, которая включает основные пики при 2-тета 5,2, 10,0, 10,3, 11,6, 15,5, 17,7, 18,6, 19,2, 20,5, 21,7, 22,4 и 24,3 (°), где каждый пик имеет предел погрешности +/- 0,2 (°);
[0066] Полиморфная форма V 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано выше, которая дополнительно характеризуется данными дифференциальной сканирующей калориметрии (DSC), которые демонстрируют эндотермический пик при 169°C, где указанная температура измерения имеет предел погрешности +/- 1°C;
[0067] Полиморфная форма VI 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, которая характеризуется картиной порошковой дифракции рентгеновских лучей (PXRD), полученной в результате облучения источником Cu-K-альфа, которая включает основные пики при 2-тета 10,3, 10,6, 11,4, 12,6, 18,8, 19,2, 19,5, 20,2, 21,2 и 21,7 (°), где каждый пик имеет предел погрешности +/- 0,2 (°);
[0068] Полиморфная форма VI 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты, как описано выше, которая дополнительно характеризуется данными дифференциальной сканирующей калориметрии (DSC), которые демонстрируют эндотермический пик при 170°C, где указанная температура измерения имеет предел погрешности +/- 1°C.
[0069] В качестве следующего аспекта настоящего изобретения предложена полиморфная форма 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты по настоящему изобретению, предназначенная для применения в качестве лекарственного средства.
[0070] В качестве еще одного аспекта настоящего изобретения предложено применение полиморфной формы 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты по настоящему изобретению для получения лекарственного средства для лечения любого заболевания, которое опосредовано антагонистом рецептора 5-HT4, в частности, для лечения, профилактики или паллиативного лечения гастроэзофагеальной рефлюксной болезни (GERD), желудочно-кишечных заболеваний, нарушений перистальтики желудка, диспепсии неязвенного происхождения, функциональной диспепсии (FD), синдрома раздраженного кишечника( IBS), запора, диспепсии, эзофагита, гастроэзофагеальной болезни, гастрита, тошноты, заболеваний центральной нервной системы, болезни Альцгеймера, когнитивных расстройств, рвоты, мигрени, неврологических заболеваний, боли, сердечно-сосудистых нарушений, сердечной недостаточности, нарушений сердечного ритма, диабета и синдрома апноэ.
[0071] В качестве альтернативного аспекта предложен способ лечения любого заболевания, которое опосредовано антагонистом рецептора 5-HT4, в частности, для лечения, профилактики или паллиативного лечения гастроэзофагеальной рефлюксной болезни (GERD), желудочно-кишечных заболеваний, нарушений перистальтики желудка, диспепсии неязвенного происхождения, функциональной диспепсии (FD), синдрома раздраженного кишечника (IBS), запора, диспепсии, эзофагита, гастроэзофагеальной болезни, гастрита, тошноты, заболеваний центральной нервной системы, болезни Альцгеймера, когнитивных расстройств, рвоты, мигрени, неврологических заболеваний, боли, сердечно-сосудистых нарушений, сердечной недостаточности, нарушений сердечного ритма, диабета и синдрома апноэ, включающий введение терапевтически эффективного количества полиморфной формы 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты по настоящему изобретению животному, включая человека, нуждающемуся в таком лечении.
[0072] Полиморфную форму 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты по настоящему изобретению можно использовать для общего лечения болезненных состояний, опосредованных активностью рецептора 5-HT4.
[0073] Полиморфную форму 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты по настоящему изобретению можно также использовать для лечения нарушения или состояния, выбранного из группы, состоящей из гастроэзофагеальной рефлюксной болезни (GERD), желудочно-кишечных заболеваний, нарушений перистальтики желудка, диспепсии неязвенного происхождения, функциональной диспепсии (FD), синдрома раздраженного кишечника (IBS), запора, диспепсии, эзофагита, гастроэзофагеальной болезни, гастрита, тошноты, заболеваний центральной нервной системы, болезни Альцгеймера, когнитивных расстройств, рвоты, мигрени, неврологических заболеваний, боли, сердечно-сосудистых нарушений, сердечной недостаточности, нарушений сердечного ритма, диабета и синдрома апноэ.
[0074] Способы синтеза для получения 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты описаны в WO2006/090224 и в разделе примеры, приводимом ниже.
[0075] Полиморфную форму I 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты можно получить путем кристаллизации из раствора 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты в этилацетате.
[0076] Органические растворители, включая этилацетат, можно использовать для кристаллизации полиморфной формы I. Предпочтительно, примеры растворителей, которые можно смешивать с этилацетатом, включают один или более из растворителей, выбранных из: воды, спиртов, таких как метанол, этанол и пропанол; простых эфиров, таких как диэтиловый эфир, трет-бутилметиловый эфир, диоксан и тетрагидрофуран; углеводородов, таких как гексан, гептан, циклогексан, дихлорметан, хлороформ, бензол, толуол и ксилол; кетонов, таких как ацетон и метилэтилкетон; амидов, таких как диметилформамид и диметилацетамид; и сульфоксидов, таких как диметилсульфоксид.
[0077] В зависимости от концентрации соединения, скорость уменьшения температуры при перекристаллизации обычно ниже, чем 100°C/час при концентрации примерно от 0,1 мг/мл до примерно 200 мг/мл. Для перекристаллизации предпочтительно использовать скорости ниже, чем 50°C/час, более предпочтительно ниже, чем 20°C/час, и наиболее предпочтительно ниже, чем 5°C/час.
[0078] Полиморфную форму II 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты можно получить, размещая полиморфную форму I в условиях при температуре 110°C или выше.
[0079] Полиморфную форму III 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты можно получить путем преобразования полиморфа I в условиях высокой относительной влажности. Относительная влажность может меняться в интервале от 60 до 100% при комнатной температуре в диапазоне от 15 до 35°C или выше.
[0080] Кроме того, полиморфную форму III можно получить путем преобразования полиморфной формы I в смеси воды и изопропилового спирта, необязательно используя затравочные кристаллы полиморфной формы III. Условия от 3 до 5% (об./об.) воды в спирте можно использовать для получения полиморфной формы III без образования каких-либо других полиморфных форм. Примеры предпочтительных спиртов включают, но ими не ограничиваются, этанол, изопропиловый спирт и т.п.
[0081] Полиморфную форму IV 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты можно получить путем преобразования полиморфной формы III при температуре от 90 до 100°C. Полиморф IV является стабильным вплоть до 115°C.
[0082] Полиморфную форму V 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты можно получить путем преобразования полиморфа I в условиях суспензии в воде.
[0083] Кроме того, полиморфную форму V можно получить путем преобразования полиморфа I в смеси воды и органического растворителя. Содержание воды в органическом растворителе зависит от используемого растворителя. Например, в случае тетрагидрофурана, для получения полиморфной формы V можно использовать 10% (об./об.) или выше воды в тетрагидрофуране. В случае изопропилового спирта, для получения полиморфной формы V можно использовать 20% (об./об.) или выше воды в изопропиловом спирте. В случае ацетона или ацетонитрила, для получения полиморфной формы V можно использовать 50% (об./об.) или выше воды в ацетоне или ацетонитриле.
Примеры органических растворителей включают, но ими не ограничиваются, тетрагидрофуран, изопропиловый спирт, этанол, ацетон, ацетонитрил и т.п.
[0084] Полиморфную форму VI 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты можно получить путем преобразования полиморфа I в смеси воды и органического растворителя. Содержание воды в органическом растворителе зависит от используемого растворителя. Например, в случае ацетона, для получения полиморфной формы VI можно использовать от 5 до 10% (об./об.) воды в ацетоне. В случае ацетонитрила, для получения полиморфной формы VI можно использовать от 5 до 10% (об./об.) воды в ацетонитриле. В случае тетрагидрофурана, для получения полиморфной формы VI можно использовать 5% (об./об.) воды в тетрагидрофуране.
Примеры органических растворителей включают, но ими не ограничиваются, тетрагидрофуран, изопропиловый спирт, этанол, ацетонитрил, ацетон и т.п.
[0085] Полиморфную форму 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]-метил}тетрагидро-2H-пиран-4-карбоновой кислоты по настоящему изобретению можно вводить отдельно или в комбинации с одним или более из других лекарственных средств (или в виде любой их комбинации). Обычно их вводят в виде композиции вместе с одним или более из фармацевтически приемлемых эксципиентов. Термин ‘эксципиент’ здесь используют для описания любого ингредиента, отличного от соединения по настоящему изобретению. Выбор эксципиента в значительной степени зависит от таких факторов, как конкретный способ введения, влияние эксципиента на растворимость и стабильность и характер лекарственной формы.
[0086] Таким образом, в следующем аспекте настоящего изобретения предложена фармацевтическая композиция, включающая полиморфную форму 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты и один или более из подходящих эксципиентов. Указанные композиции являются подходящими для лечения болезненных состояний, опосредованных активностью рецептора 5-HT4.
[0087] Термин «полиморфная форма (полиморфные формы)», используемый в описании, включает полиморфную форму I, полиморфную форму II, полиморфную форму III, полиморфную форму IV, полиморфную форму V и/или полиморфную форму VI.
[0088] Массовая степень чистоты полиморфной формы 4-{[4-({[4-(2,2,2-трифторэтокси)-1,2-бензизоксазол-3-ил]окси}метил)пиперидин-1-ил]метил}тетрагидро-2H-пиран-4-карбоновой кислоты по настоящему изобретению не ограничена, но предпочтительно использовать практически чистые полиморфные формы для конкретных вариантов осуществления настоящего изобретения.
[0089] Во избежание недоразумений, если в описании используют выражение ‘практически чистые’, оно означает по меньшей мере 90 масс.% степени чистоты. Более предпочтительно, ‘