Фармацевтический состав, содержащий алимемазина тартрат
Иллюстрации
Показать всеИзобретение относится к области химико-фармацевтической промышленности и медицины. Фармацевтический состав содержит алимемазина тартрат и вспомогательные компоненты. В качестве вспомогательных компонентов выбраны микрокристаллическая целлюлоза, гипромеллоза, кремния диоксид коллоидный и стеарат магния в указанных в формуле изобретения количествах. Фармацевтический состав алимемазина тартрата выполнен в форме таблетки, покрытой пленочной оболочкой. Таблетка по изобретению обеспечивает пролонгированное высвобождение алимемазина тартрата, при этом сохраняя преимущества в виде короткого периода полувыведения; характеризуется удовлетворительной стабильностью, прочностью более чем 70 Н и прочностью на истирание не менее 98,5%. 4 з.п. ф-лы, 4 табл., 5 пр.
Реферат
Изобретение относится к области химико-фармацевтической промышленности и медицины и касается способов получения новых препаративных форм нейролептиков.
В последние десятилетия наблюдается тенденция к увеличению распространенности психогенных заболеваний, таких как невроз и другие заболевания с нерезко выраженными нарушениями психической деятельности, возникновение, течение, компенсация и декомпенсация которых определяются преимущественно психогенными факторами.
Среди препаратов, используемых для лечения подобных заболеваний, показал свою эффективность алимемазина тартрат. Впервые препарат был синтезирован в 1958 г. в лаборатории французской фирмы «Theraplix». Этот препарат быстро стал лидером рынка в своем сегменте, как в Европе, так и в Америке.
Алимемазина тартрат - антипсихотический препарат, который относится к числу производных фенотиазина - 10-(3-диметиламино-2-метилпропил)-фенотиазина гидротартрат, и по химическому строению близок к дипразину и левомепромазину. Препарат оказывает антигистаминное, спазмолитическое, серотонинблокирующее, умеренное альфа-адреноблокирующее, противорвотное, снотворное, седативное и противокашлевое действие [Ибрагимов Д.Ф. «Алимемазин во врачебной практике» // Журн. Неврологии и психиатрии им. С.С. Корсакова, 2008; Т. 108, №9, С. 76-78].
Выпускается и назначается алимемазин тартрат в основном в таблетках, например, под торговым названием Тералиджен® (Teraligen®) (http://www.vidal.ru/poisk_preparatov/teraligen.htm).
Известен патент RU 2384336 на фармацевтический состав, который содержит в качестве активного компонента алимемазин тартрат, а также целевые вспомогательные вещества: лактозу, картофельный крахмал, целлюлозу микрокристаллическую, коллидон, стеарат магния при соответствующем соотношении компонентов. Состав выполнен в форме таблеток, покрытых оболочкой, состоящей из поливинилового спирта, талька, полиэтиленгликоля, титана диоксида, приемлемых красителей. Состав требует приема несколько раз в день.
В настоящее время большую актуальность приобретает вопрос создания пролонгированных лекарственных форм, способных обеспечить длительное действие лекарственного средства с одновременным снижением его суточной дозы.
Известен патент RU 2424807, опубликованный 27.07.2011, раскрывающий фармацевтические композиции с пролонгированным действием, используемые для коррекции психосоматических расстройств. Композиции содержат в качестве активного компонента алимемазин тартрат, а также целевые вспомогательные вещества: лактозу, гидроксипропилметилцеллюлозу, крахмал прежелатинизированный, стеарат магния, кремния диоксид коллоидный при соответствующем соотношении компонентов. Композиция выполнена в форме таблеток, покрытых оболочкой, состоящей из поливинилового спирта, талька, полиэтиленгликоля, титана диоксида, приемлемых красителей. Процесс изготовления таблеток осуществляют методом прямого прессования.
Данное решение может быть указано в качестве ближайшего аналога-прототипа. Недостатком данного технического решения является высокое содержание в препарате лактозы, что может вызвать нежелательные эффекты у пациентов с тяжелыми формами непереносимости лактозы (http://digestive.niddk.nih.gov/ddiseases/pubs/lactoseintolerance/#products).
Задачей настоящего изобретения является разработка нового фармацевтического состава пролонгированного действия, обладающего психосоматическим действием, содержащего алимемазин тартрат.
Техническими результатами настоящего изобретения являются:
- улучшение фармакокинетических параметров заявленной композиции;
- повышение стабильности композиции.
Поставленная задача осуществляется, а технические результаты достигаются разработкой фармацевтического состава пролонгированного действия, содержащего алимемазина тартрат и вспомогательные компоненты. В качестве вспомогательных компонентов выбраны микрокристаллическая целлюлоза, гипромеллоза, кремния диоксид коллоидный и стеарат магния. При этом содержание компонентов следующее (в масс. % от общей массы сухой смеси):
алимемазина тартрат - 10,00-30,00;
целлюлоза микрокристаллическая - 35,00-42,00;
гипромеллоза - 33,50-46,00;
кремния диоксид коллоидный - 1,00-2,00;
магния стеарат - 0,50-2,00.
В предпочтительных вариантах изобретения:
- упомянутый состав не содержит лактозу;
- фармацевтический состав выполнен в форме капсулы или таблетки,
- фармацевтический состав выполнен в форме таблетки, представляющей собой ядро, покрытое оболочкой;
- предпочтительно, фармацевтический состав выполнен в форме таблетки, представляющей собой ядро, покрытое пленочной оболочкой;
- пленочная оболочка составляет 2,50-6,00% от массы ядра.
Наличие пленочной оболочки придает стабильность композиции при хранении и улучшает ее внешний вид.
Пленочная оболочка может включать, без ограничения, поливиниловый спирт, частично гидролизованный поливинилацетат, производные целлюлозы, такие как этилцеллюлоза, гидроксипропилцеллюлоза (ГПЦ), гидроксипропилметилцеллюлоза (ГПМЦ) в качестве пленкообразующих веществ, полиэтиленгликоль, пропиленгликоль, глицерин в качестве пластификаторов, лецитин, полисорбат 80 в качестве поверхностно-активных веществ, стеариновую кислоту, тальк в качестве глидантов, мальтодекстрин, фармацевтически приемлемые красители. Красители могут быть выбраны из любых красителей или пигментов, одобренных для медицинского применения. Например, красители могут представлять собой диоксид титана, алюминиевые лаки, оксиды железа или природные пигменты (см. патент США US 6448323).
Пленочное покрытие может наноситься в количестве 2,50-6,00% от массы ядра таблетки.
В наиболее предпочтительном варианте могут быть получены круглые двояковыпуклые таблетки, покрытые пленочной оболочкой.
Предложенный состав не содержит лактозы, поэтому не будет вызывать нежелательных побочных явлений у пациентов с непереносимостью лактозы.
Лекарственные формы ретард (от лат. retardo - замедлять, tardus - тихий, медленный; синонимы - ретардеты, лекарственные формы ретардированные) - это пролонгированные лекарственные формы, обеспечивающие в организме запас лекарственного вещества и его последующее медленное высвобождение. Данные лекарственные формы применяются преимущественно перорально, однако иногда используются и для ректального введения.
Для выбора составов таблеток с модифицированным высвобождения были протестированы вещества-пролонгаторы и наполнители, использование которых позволяет получать пролонгированный фармацевтический с улучшенными фармакокинетическими свойствами. При этом был подобран состав наполнителя и пролонгирующего компонента, который позволяет получать твердую лекарственную форму на обычной схеме производства без специального технологического оборудования. Определено, что необходимыми характеристиками обладает комбинация гипромеллозы и микрокристаллической целлюлозы.
Авторами изобретения неожиданно обнаружено, что состав алимемазина тартрата согласно настоящему изобретению обладает улучшенными фармакокинетическими параметрами и повышенной стабильностью по сравнению с прототипом.
Показания к применению состава согласно настоящему изобретению: в качестве седативного (успокаивающего), анксиолитического (противотревожного) и снотворного средства, деменция (в том числе деменция в связи с эпилепсией), протекающая с проявлениями психомоторного возбуждения, аффекта, тревоги; органическое тревожное расстройство; шизофрения; расстройства настроения (аффективные расстройства); генерализованное тревожное расстройство; обсессивно-компульсивное расстройство; реакция на тяжелый стресс и нарушения адаптации; диссоциативные (конверсионные) расстройства; соматоформные расстройства; неуточненное расстройство вегетативной (автономной) нервной системы, другие расстройства вегетативной (автономной) нервной системы; нервная анорексия; эмоционально неустойчивое расстройство личности (импульсивный и пограничный типы); истерическое расстройство личности, тревожное (уклоняющееся, избегающее) расстройство личности; стойкое изменение личности после переживания катастрофы; гиперкинетическое расстройство поведения; расстройство поведения, ограниченное рамками семьи; несоциализированное расстройство поведения; беспокойство, возбуждение и другие симптомы и признаки, относящиеся к эмоциональному состоянию; другие невротические расстройства (неврастения, неуточненное невротическое расстройство); бессонница неорганической этиологии; эмоциональные расстройства, начало которых специфично для детского возраста, в качестве противоаллергического средства, зуд независимо от места и этиологии; астма, поллиноз, коклюш (в качестве противоаллергического средства для купирования кашля, одышки и приступов удушья); неуточненная аллергия.
Возможность осуществления изобретения может быть продемонстрирована представленными ниже примерами, которые иллюстрируют, но не ограничивают изобретение.
Пример 1. Получение таблетки пролонгированного действия, покрытой пленочной оболочкой.
В установку для грануляции и сушки технологией псевдоожижения загружают просеянные микрокристаллическую целлюлозу и алимемазина тартрат и запускают процесс гранулирования, используя в качестве увлажнителя воду. Процесс сушки продолжают до достижения показателя «потери в массе при высушивании» значения 3,0±0,5.
По окончании процесса гранулирования полученный сухой гранулят методом рассева калибруют через металлическое сито с диаметром отверстий 0,8 мм (фракцию с размером гранул крупнее 0,8 мм протирают через сито принудительно).
В смеситель барабанного типа загружают просеянную микрокристаллическую целлюлозу, откалиброванный гранулят и просеянную гипромеллозу. Перемешивают в течение 2-4 минут. Затем загружают просеянный кремния диоксид коллоидный, перемешивают в течение 2-3 минут, затем загружают просеянный магния стеарат, перемешивают в течение 1-2 минут.
Таблеточную массу прессуют на ротационном прессе, используя пунсоны круглой формы (глубокая сфера) диаметром 8,0±0,2 мм (для всех дозировок).
На таблетки-ядра наносят готовое пленочное покрытие.
Готовые таблетки после анализа контроля качества расфасовывают в контурную ячейковую упаковку из поливинилхлоридной пленки и алюминиевой фольги с последующим вложением в картонную пачку.
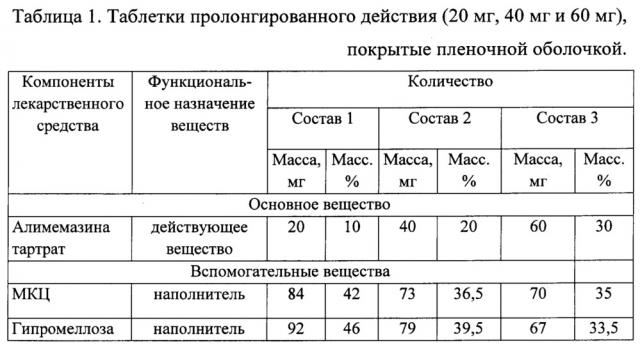
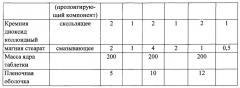
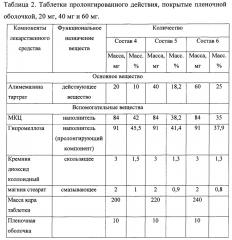
Таблетки пролонгированного действия получали, как описано выше, в соответствии с составами, приведенными в Таблицах 1 и 2.
Ядра таблеток покрывали композициями пленочного покрытия (1), (2) или (3) в количестве 5, 10 и 12 мг на таблетку.
Композиция пленочного покрытия (1).
Готовая смесь порошков для пленочного покрытия: поливиниловый спирт частично гидролизованный, макрогол, тальк, титана диоксид Е171, краситель железа оксид красный Е172, краситель железа оксид желтый Е172.
Композиция пленочного покрытия (2).
Смесь ГПМЦ, макрогола 400, полисорбата 80 и диоксида титана (например, Opadry® "White coating premix", компания Colorcon).
Композиция пленочного покрытия (3).
Смесь ГПМЦ, макрогола 400 и мальтодекстрина (например, Opadry® "Clear coating premix", компания Colorcon).
Пример 2. Исследование фармакокинетики таблетки пролонгированного действия, покрытой пленочной оболочкой.
С целью подтверждения пролонгированного действия предложенной таблетки пролонгированного действия, покрытой пленочной оболочкой, а также улучшенной фармакокинетики было проведено исследование фармакокинетики композиции алимемазина тартрата в дозировке 60 мг по Примеру 1, Таблица 1, в сравнении с препаратом Тералиджен® (таблетки 5 мг, производства «Хаузанг» («ХГ-Фарм»), Вьетнам), а также композицией согласно патенту RU 2424807 в дозировке 60 мг (прототип). Таблетки Тералиджен® 5 мг вводили в суммарной дозе 60 мг.
Цель исследования: определение фармакокинетики алимемазина в плазме крови кроликов после однократного введения трех таблетированных форм алимемазина (Таблетка пролонгированного действия, покрытая пленочной оболочкой, по Примеру 1, Таблица 1, ретард-форма согласно прототипу и таблетки Тералиджен®, 5 мг, «ХГ-Фарм»).
Материалы и методы.
Исследование проведено на 10 кроликах-самцах массой 2,4±0,52 кг, содержащихся в стандартных условиях вивария. Животным однократно через зонд вводили 1 таблетку пролонгированного действия, покрытую пленочной оболочкой, согласно изобретению или 1 ретард-таблетку пролонгированного действия, покрытую пленочной оболочкой, согласно прототипу, или 12 таблеток Тералиджен® «ХГ-Фарм». Образцы крови отбирали из краевой ушной вены через дискретные интервалы времени (0; 1,0; 2,0;.3,0; 4,0; 6,0; 8,0; 12,0; 24,0 и 36,0 часа).
Количественное определение алимемазина в плазме крови кроликов проводили методом ВЭЖХ с пределом детектирования 25 нг/мл.
Полученные экспериментальные данные предварительно были подвергнуты статистической обработки с помощью программы Statistica 6.0.
Рассчитывали основные фармакокинетические параметры.
Результаты.
Сравнительный анализ основных фармакокинетических параметров алимемазина показал, что время достижения максимальных концентраций алимемазина (tmax) для заявленных таблеток пролонгированного действия, покрытых пленочной оболочкой, составило 6,8±0,28 ч, по прототипу - 4,18±0,72 ч, а из таблеток Тералиджен® «ХГ-Фарм» - 2,70±0,38 ч (см. Таблицу 2). Между величинами tmax для заявленных таблеток пролонгированного действия, покрытых пленочной оболочкой, и таблеток ретард согласно прототипу установлены достоверные различия (р<0.05).
Период полувыведения для пролонгированной лекарственной формы составил 10,84±2,80 ч, по прототипу - 10,76±2,78 ч, для сравнительных таблеток Тералиджен® «ХГ-Фарм» - 10,29±1,46 ч.
Относительная биодоступность алимемазина из таблеток пролонгированного действия, покрытых пленочной оболочкой, по изобретению по отношению к обычным таблеткам Терапиджена® в среднем составляет 87,6%.
Таким образом, исследования показывают улучшенные фармакокинетические параметры новой таблетки пролонгированного действия, покрытой пленочной оболочкой (время достижения максимально концентрации), по сравнению с прототипом. Препарат по изобретению высвобождает действующее вещество в соответствии с заданными характеристиками в желудочно-кишечном тракте, при этом сохраняя преимущества в виде короткого периода полувыведения.
Пример 3. Исследование общетоксического действия состава в форме таблетки пролонгированного действия, покрытой пленочной оболочкой.
Цель исследования: определение переносимых, токсических и летальных доз и причин наступления гибели животных, оценка степени повреждающего действия препарата при его длительном введении на мелких лабораторных животных, выявление наиболее чувствительных органов и систем организма и исследование степени обратимости вызываемых повреждений
Изучение острой токсичности.
Материалы и методы.
Изучение острой токсичности заявленной таблетки пролонгированного действия, покрытой пленочной оболочкой, при однократном внутрижелудочном введении проведено на 20 белых нелинейных мышах-самцах весом 18-20 г, содержащихся в стандартных условиях вивария со свободным доступом к воде и корму. Испытывали дозы препарата 180, 250, 320 и 390 мг (по алимемазину)/кг массы тела. На протяжении 14 дней оценивали общее состояние животных. О токсичности препаратов судили по гибели животных и общей картине интоксикации. Статистический анализ выполнялся с помощью программного обеспечения Статистика 6.0.
Параметры острой токсичности дали следующие результаты:
DL50=313 (301-326) мг/кг, DL16=243 мг/кг, DL84=403 мг/кг.
Таким образом, исследованный препарат по параметрам острой токсичности по классификации Hodge и Sterner (1943) может быть отнесен к умеренно токсичным соединениям.
Субхроническую токсичность препарата исследовали на 25 белых нелинейных крысах-самцах весом 172-216 г, содержащихся в стандартных условиях вивария со свободным доступом к воде и корму. Животным опытных групп в течение 30 дней ежедневно один раз в день вводили исследуемый препарат внутрижелудочно в дозах 6 и 60 мг (по алимемазина тартрату)/кг массы тела в виде взвеси в 2% крахмальном геле, что соответственно, равно и в 10 раз превышает терапевтическую дозу для человека с учетом межвидового пересчета. После окончания эксперимента всех животных умерщвляли для проведения дальнейшего патоморфологического исследования внутренних органов и тканей.
Местно-раздражающее действие оценивали при макроскопическом и микроскопическом исследовании мест введения препаратов - желудочно-кишечного тракта.
Статистическое сравнение опытных и контрольных групп проводили по t-критерию Стьюдента.
Результаты.
В группах животных, получавших внутрижелудочно суспензии исследуемого препарата в дозе 60 мг/кг, наблюдалась тенденция к снижению скорости прироста массы тела, незначительное, но достоверное увеличение активности трансаминаз крови и снижение спонтанной двигательной активности животных. Изученный препарат в дозах 6 и 60 мг/кг не вызывал отклонений биохимических и гематологических показателей. Не наблюдалось изменения суточного диуреза для групп животных, получавших опытный препарат, по отношению к группе контрольных животных, получавших внутрижелудочно 2% крахмальный гель в аналогичном объеме.
Патоморфологическое и микроскопическое исследование внутренних органов свидетельствуют об отсутствии в испытанных дозах выраженных признаков токсического действия препарата на внутренние органы, однако указывают на возможное проявление его местнораздражающего действия на слизистую оболочку желудка после 30 дней внутрижелудочного введения в дозе, в 10 раз превышающей терапевтическую с учетом межвидового пересчета доз.
Заявленный препарат не проявляет мутагенных свойств в опытах на дрозофилах, не обладает аллергенностью, не обладает репродуктивной токсичностью.
Пример 4. Определение стабильности таблеток пролонгированного действия, покрытых пленочной оболочкой, методом ускоренного старения.
Исследование стабильности проводят в сравнении с композицией согласно прототипу (патенту RU 2424807).
Цель исследования: определение стабильности пролонгированной лекарственной формы по Примеру 1.
Исследование проведено в ИЦ ПАО «Валента Фарм».
Таблетки, полученные в соответствии с Примеру 1 по настоящему изобретению и в соответствии с прототипом, упаковывают в блистеры из алюминиевой фольги ('Alu-Alu') и помещают в климатическую камеру в условия ускоренных испытаний. Содержание действующего вещества алимемазина тартрата определяют методом ВЭЖХ с использованием стандартов.
Метод «ускоренного старения» заключается в выдерживании испытуемого лекарственного средства при температурах и влажности, превышающих температуру и влажность его хранения в процессе обращения. При повышенных температурах, как правило, ускоряются протекающие в лекарственных средствах физико-химические процессы, приводящие со временем к нежелательным изменениям качества. Таким образом, при повышенной температуре промежуток времени, в течение которого контролируемые показатели качества лекарственного средства сохраняются в допустимых пределах (экспериментальный срок годности), искусственно сокращается в сравнении со сроком годности при температуре хранения. Это позволяет значительно сократить время, необходимое для установления срока годности.
По результатам, полученным в процессе «ускоренного старения» лекарственного средства, можно решить также обратную задачу, т.е. установить температуру хранения, обеспечивающую какой-либо заданный срок годности.
Срок годности (С) при температуре хранения (tхр), связан с экспериментальным сроком годности (СЭ) при повышенной температуре экспериментального хранения (tэ) следующей зависимостью:
C=K⋅CЭ,
где K - коэффициент соответствия рассчитывается как .
Температурный коэффициент скорости химической реакции (А) принят равным 2,5. Приведенная зависимость основана на правиле Вант-Гоффа о 2-4-кратном росте скоростей химических реакций при увеличении температуры на 10°С.
В соответствии с фармакопейной статьей ОФС.1.1.0009.15 значение коэффициента соответствия (K) в зависимости от выбранного температурного интервала (tэ-tхр), равного 30°С, составляет 15,6. Срок экспериментального хранения при выбранном сроке годности 3 года составляет 71 сутки.
Статистическую обработку параметров и оформление результатов исследования проводят в соответствии с Правилами надлежащей клинической практики Евразийского экономического союза с помощью статистического пакета SPSS Statistics 19.0.
Показано, что пролонгированная лекарственная форма согласно изобретению обладает статистически достоверно увеличенной стабильностью при хранении по сравнению с прототипом.
Установлено, что после 71 суток хранения в условиях метода ускоренного старения таблетки пролонгированного действия по настоящему изобретению обладают статистически достоверно увеличенной стабильностью и остаются химически чистыми. Таблетки, полученные в соответствии с прототипом, остаются химически чистыми в течение менее 10 суток, далее содержание действующего вещества алимемазина тартрата уменьшается более чем на 3%. То есть таблетки по настоящему изобретению являются значительно более стабильными по сравнению с прототипом.
Пример 5. Определение механической прочности и истираемости таблеток пролонгированного действия, покрытых пленочной оболочкой.
Определение и нормирование механической прочности таблеток необходимо как в условиях промышленного производства (например, процесс покрытия таблеток и фасовка), так и для обеспечения потребительских свойств препарата (сохранение целостности таблетки при извлечении из упаковки) в соответствии со статьей ОФС.1.4.2.0011.15.
Оборудование представляет собой два расположенных друг против друга зажима, один из которых может перемещаться по направлению к другому. Плоскости поверхностей зажимов перпендикулярны направлению движения. Допускается использование прибора, в котором оба зажима могут перемещаться с постоянной скоростью по направлению друг к другу. Сдавливающие поверхности зажимов должны быть плоскими и превосходить по размеру зону контакта с таблеткой. Прибор должен обеспечивать прекращение сдавливания при любом нарушении целостности таблеток. Прибор калибруют с использованием системы, обеспечивающей точность 1 Н (ньютон).
Таблетку помещают между зажимами ребром по отношению к движущейся части прибора. Таблетку, поставленную на ребро, сжимают до разрушения. Измерения проводят для десяти таблеток. Перед каждым измерением тщательно удаляют все фрагменты предыдущей таблетки.
Истираемость выражают потерей в массе, вычисленной в процентах от исходной массы испытуемых таблеток.
Прибор состоит из барабана со съемной крышкой, диаметром около 200 мм и глубиной около 38 мм, изготовленного из прозрачного синтетического полимера; внутренние поверхности барабана должны быть отполированы и не должны электризоваться. По внутреннему периметру стенки барабана расположены 12 лопастей (35×35 мм) под углом 20° к касательной барабана, которые при его вращении приводят в движение таблетки. Барабан крепится к горизонтальной оси устройства, обеспечивающего вращение барабана со скоростью 20 об/мин. Прибор должен автоматически выключаться по истечении заданного времени испытания.
Десять таблеток, обеспыленных и взвешенных с точностью до 0,001 г, помещают в барабан, привинчивают крышку и включают устройство на 5 мин, что соответствует 100 оборотам барабана. По истечении установленного времени таблетки извлекают из барабана, обеспыливают и снова взвешивают с точностью до 0,001 г. Потеря в массе не должна превышать 3%.
Если после испытания обнаруживают треснутые, расколотые или разбитые таблетки, результат испытания на истираемость признают неудовлетворительным.
Потеря в массе в каждом из дополнительных испытаний или средняя потеря в массе, вычисленная по результатам 3 испытаний, не должна превышать нормированное значение.
По результатам эксперимента полученные согласно заявленному изобретению таблетки пролонгированного действия, покрытые пленочной оболочкой, обладают высокой прочностью более чем 70 Н и прочностью на истираемость не меньше 98,5%.
1. Фармацевтический состав, содержащий алимемазина тартрат и вспомогательные компоненты, выполненный в форме таблетки, покрытой пленочной оболочкой, отличающийся тем, что в качестве вспомогательных компонентов выбраны микрокристаллическая целлюлоза, гипромеллоза, кремния диоксид коллоидный и стеарат магния при следующем содержании компонентов в мас.%:
| алимемазина тартрат | 10,00-30,00 |
| целлюлоза микрокристаллическая | 35,00-42,00 |
| гипромеллоза | 33,50-46,00 |
| кремния диоксид коллоидный | 1,00-2,00 |
| магния стеарат | 0,50-2,00 |
2. Фармацевтический состав по п. 1, отличающийся тем, что упомянутый состав не содержит лактозу.
3. Фармацевтический состав по п. 1, отличающийся тем, что упомянутый состав выполнен в форме капсулы или таблетки.
4. Фармацевтический состав по п. 2, отличающийся тем, что фармацевтический состав выполнен в форме таблетки, представляющей собой ядро, покрытое оболочкой.
5. Фармацевтический состав по п. 4, отличающийся тем, что пленочная оболочка составляет 2,50-6,00% от массы ядра.