Новые растительные цис-регуляторные элементы для разработки патоген-чувствительных химерных промоторов
Иллюстрации
Показать всеИзобретение относится к области биотехнологии, а именно к изолированным цис-регуляторным элементам для придания промотору индуцируемости патогеном, химерному промотору, обладающему индуцируемостью патогеном, рекомбинантному гену для экспрессии в растительной клетке после контакта с патогеном, экспрессирующим вектору для повышения устойчивости растения к патогенам, где патоген представляет собой грибок или оомицет. Также изобретение представляет собой прокариотическую или эукариотическую клетку для получения растения с повышенной устойчивостью к патогенам, трансгенное растение для снижения риска заражения патогеном, семя растения для культивирования растения со сниженным риском заражения, ткань растения для in vitro культивирования, часть растения для снижения риска заражения патогеном, способ создания трансгенного растения, способ патоген-индуцируемой экспрессии эндогенного гена в растительной клетке под контролем нативного промотора, растительную клетку и растение, способные к патоген-индуцируемой экспрессии эндогенного гена. Изобретение обеспечивает технологию создания трансгенного растения, в частности, стойкого к действию патогена, где патоген представляет собой грибок или оомицет. 14 н. и 3 з.п. ф-лы, 16 ил., 3 табл.
Реферат
Данное изобретение касается цис-регуляторных элементов и созданных из них химерных промоторов с активностью в растениях, индуцируемой патогенами или элиситорами. Кроме того, изобретение касается клетки-хозяина, трансгенной растительной клетки, трансгенной растительной ткани, а также трансгенного растения и его семян. Также данное изобретение относится к технологии создания трансгенного растения, в частности, стойкого к действию патогена.
Заболевания растений, вызываемые грибками, вирусами, нематодами и бактериями, приводят к большим потерям урожая во всем мире, ухудшают качество продукции и требуют использования дорогостоящих химических средств защиты растений, так как природные механизмы защиты растений, с помощью которых они способны защититься от большей части потенциальных возбудителей болезней или замедлить и ограничить их распространение, зачастую недостаточны. Для создания растений, резистентных к действию вышеназванных патогенов, можно использовать методы генной инженерии. Такие растения обладают повышенной стойкостью, так как они способны вырабатывать протеины (эффекторы), вызывающие сильную реакцию сопротивления, или молекулы, являющиеся токсичными для патогенов или подавляющие их рост и вирулентность; причем выработка происходит именно в месте заражения (контакта патогена и растения).
Эффекторами, вызывающими сильную реакцию сопротивления растения, являются, например, протеины самоактивирующихся генов устойчивости (R-генов) или гены авирулентности, которые вызывают активацию эндогенных генов устойчивости растения. К сильным реакциям сопротивления относятся гиперинтенсивная реакция (HR), контролируемая смерть клеток ткани хозяина в месте контакта, укрепление стенки клетки благодаря лигнификации и образованию каллуса, образование фитоалексинов и выработка PR-протеинов (патогенез-зависимых). Так как для этих реакций требуется большое количество энергии, и они могут привести к отмиранию (некрозу) клеток растения, их активация должно строго контролироваться. Это относится и к экспрессии токсичных для патогенов протеинов или пептидов, если конститутивная экспрессия таких протеинов или пептидов оказывает отрицательное действие на растение или его агрономические свойства, например, урожайность. В рамках трансгенных технологий обеспечить контроль можно путем использования промоторов с нужными свойствами.
Например, добиться индуцированной патогенами экспрессии таких трансгенов, как эффекторы, можно путем использования различных известных природных промоторов, индуцируемых патогенами, например, промотора PR1 (Rushton et al., 1996). В частности, разработка микроматричной технологии привела к идентификации большого количества индуцируемых патогенами промоторов (WO 03/00898, WO 02/50293 или JP 2003284566).
Однако, подобные природные индуцируемые патогенами промоторы могут демонстрировать крайне неспецифические действия, так как они могут активировать многочисленными разнообразными стимулами. Это связано с модульной структурой промотора, состоящего из нескольких разных цис-регуляторных элементов, которые объединяются самые разные сигналы в сложный экспрессионный профиль. Следовательно, природные индуцируемые патогенами промоторы отличаются и нежелательными действиями, например, в определенных тканях или сильной фоновой активностью.
Например, индуцируемые патогенами промоторы дефензинов из пшеницы являются активными во время развития и всхожести семян (Kovalchuk et al., 2010). Уже упомянутый промотор PR1 индуцируется не только патогенами, но и старением (Morris et al. 2000)
Другие исследования показали, что природный, индуцируемый ржавчиной промотор Fis1 из льна после трансформации не годился для особого регулирования экспрессии самоактивирующихся форм гена устойчивости к ржавчине L6 в Linum usitatissimum, при котором помимо стойкости к ржавчине не возникали бы отрицательные с агрономической точки зрения свойства, например, карликовость (Howies et al., 2005). Одним из способов повышения требуемой специфичности промотора является идентификация цис-регуляторных элементов, ответственных за нужную индукцию, и создание химерных промоторов из таких цис-регуляторных элементов (Venter, 2007). Напротив, мотивы, отвечающие за другие стимулы, удаляются. Промоторы многих индуцируемых патогенами генов изучены подробнее, причем были идентифицированы многие цис-регуляторные элементы, которые могут влиять на патоген-специфическую индукцию (Strittmatter et al., 1996; Eulgem et al., 2000; Kirsch et al., 2000, 2001; Himmelbach et al., 2010). Другими примерами являются цис-регуляторные элементы D-бокс, S-бокс или W-бокс (WO 00/29592), идентифицированные путем пошаговой мутации природных индуцируемых патогенами промоторов, или участки сканирования линкером LS10 и LS7 (Lebel et al., 1998). В частности, хорошо изучен W-бокс, причем его сердцевинную последовательность TTGAC(C/T) можно использовать для поиска дополнительных вариантов W-бокса в природных патоген-индуцируемых промоторах.
Кроме того, идентифицировать новые цис-регуляторные элементы можно методами биоинформатики с помощью таких программ, как MEME (Bailey and Elkan, 1994; Humphry et al., 2010) или BEST (Che et al., 2005). Одно из преимуществ при этом состоит в том, что цис-регуляторный элемент идентифицируется не как короткая отдельная последовательность, а как точно заданный мотив последовательности, с помощью которого собирается информация сразу о нескольких вариантах цис-регуляторного элемента, то есть о нескольких вариантах точки связывания транскрипционного фактора. В любом случае, такие биоинформационные подходы отличаются высокой вероятностью определения ложно-положительных последовательностей, поэтому их можно использовать только для предварительного отбора потенциальных последовательностей и мотивов. При этом абсолютно необходимо подтверждение и проверка пригодности использования в качестве цис-регуляторного элемента в целом и в качестве цис-регуляторного элемента, обеспечивающего индуцируемость патогеном, в частности. Кроме того, такие методики экспериментального анализа достаточно затратны.
Дальнейшее повышение специфичности промотора возможно путем сочетания различных цис-регуляторных элементов (Rushton et al., 2002). При этом к повышению активности (синергии) приводит не само сочетание, напротив, синергетический эффект возникает только при определенных сочетаниях, предсказать которые невозможно и нужно определять эмпирическим путем в каждом конкретном случае. Например, известны химерные промоторы с сочетаниями цис-регуляторных элементов D-бокс и S-бокс (WO 00/29592). Сила промотора и фоновая активность зависят от количества повторений элементов.
Еще одна проблема при разработке патоген-индуцируемых химерных промоторов заключается в их свойствах в различных видах растений. Хотя почти во всех исследованных видах растений удалось выявить индуцируемость патогеном, связанную с известными патоген-индуцируемыми химерными промоторами, они все же демонстрируют фоновую активность даже при отсутствии поражения патогеном. Фоновая активность колеблется в зависимости от вида растения, в котором используются химерные промоторы. То же относится к интенсивности индукции (частное от активности промотора в инфицированной и не инфицированной ткани) и к абсолютной активности промоторов (их силе). Например, из-за слишком высокой фоновой активности в не инфицированной ткани можно выявить лишь незначительную индуцируемость патогенов в инфицированной ткани.
В соответствии с современным уровнем знаний за вышеописанные колебания фоновой активности, интенсивности индукции, силы промотора, кинетики индукции и пространственного расширения активации промотора отвечают используемые цис-регуляторные элементы промотора (Rushton et al., 2002, Venter, 2007). Даже если известные химерные промоторы превосходят природные, все равно необходимо оптимизировать их, в частности, с точки зрения цис-регуляторных элементов и (или) их сочетаний. До сих пор недостаточно хорошо охарактеризованных цис-регуляторных элементов и подходящих сочетаний таких элементов, с помощью которых можно было бы конструировать химерные промоторы, которые обеспечивают точно заданную и контролируемую патоген-индуцированную экспрессию требуемых трансгенов сами по себе, а также в различных видах растений, причем экспрессия должна происходить только в результате заражения патогеном и практически исключительно в месте заражения (Gurr & Rushton, 2005). В этой связи задача настоящего изобретения заключается в создании таких новых цис-регуляторных элементов, обеспечивающих индуцируемость патогеном, и их сочетаний.
Ниже приводится более подробное описание некоторых терминов, используемых в данной заявке.
Под "элиситором" в данном изобретении понимается индуктор или медиатор, способствующий мерам защиты от растительных патогенов, например, синтезу фитоалексинов. Элиситоры могут быть либо эндогенного или экзогенного происхождения. Предпочтительно, чтобы (экзогенный) элиситор происходил из патогена и распознавался растением. К ним также относятся ПАМП (патоген-ассоциированные молекулярные паттерны), например, флагеллин, РЕР25 и хитин. Элиситоры можно использовать, чтобы имитировать заражение или контакт с патогеном, при котором элиситор вносится искусственно, в отсутствие патогена. В связи с данным изобретением элиситоры используются, в частности, для проверки индуцируемости промоторов.
"Одиночная последовательность" - последовательность нуклеотидов или оснований (пар оснований), причем каждая позиция в одиночной последовательности определяется только одним четко заданным основанием (а, с, g или t). Одиночная последовательность изолируется из природного промотора и является результатом биоинформационного анализа. Она состоит из сердцевинной последовательности и боковых частей последовательности. Понятие "одиночная последовательность" означает также молекулу нуклеиновой кислоты, последовательность нуклеотидов или (пар) оснований соответствует одиночной последовательности.
"Сердцевинная последовательность" - это последовательность нуклеотидов или (пар) оснований в определенным участке цис-регуляторного элемента, причем данный участок отвечает за функциональность цис-регуляторного элемента. Сердцевинная последовательность является частью одиночной. Понятие "сердцевинная последовательность" означает также молекулу нуклеиновой кислоты, последовательность нуклеотидов или (пар) оснований соответствует сердцевинной последовательности.
"Промотор" - не транслированная последовательность ДНК, обычно ориентированная против направления кодирующего участка, содержащая точку связи с РНК-полимеразой и инициирующая транскрипцию ДНК. Кроме того, в промоторе часто есть другие элементы, являющиеся регулятора экспрессии гена (например, цис-регуляторные элементы).
"Минимальный промотор" - промотор, имеющий только базовые элементы, необходимые для инициации транскрипции (например, ТАТА-бокс и (или) инициатор). "Химерным промотором" называется промотор, не встречающийся в природе и состоящий из нескольких элементов. Он состоит из минимального промотора и по направлению вверх по меньшей мере один цис-регуляторный элемент, который представляет собой точку связи для транс-активных факторов (trans-acting factors, например, факторов транскрипции). Химерный промотор создается в соответствии с требованиями и индуцируется или тормозится различными факторами. Выбор цис-регуляторного элемента или сочетаний таких элементов имеет решающее значение, например, для специфичности или уровня активности промотора. Цис-регуляторный элемент в химерном промоторе либо гетерологичен используемому минимальному промотору, т.е. элемент и используемый минимальный промотор происходят из разных организмов или видов (например, как показано на рис. 15А-С), либо гомологичен ему, т.е. элемент и используемый минимальный промотор встречаются в одном природном промоторе, однако цис-регуляторный элемент сам по себе или как дополнительный элемент в химерном промоторе и природный промотор локализованы в разном генетическом окружении. Под химерным промотором также понимается (природный) промотор, который был изменен мультимеризацией по меньшей мере одного цис-регуляторного элемента (например, как показано на рис. 15D).
"Комплементарная" последовательность нуклеотидов относительно двуспиральной ДНК означает, что во второй цепочке ДНК, комплементарной первой цепочке, в соответствии с правилами сочетания оснований и с учетом ориентации есть нуклеотидные основания, соответствующие основаниям первой цепочки (пример: 5'-gcat-3' комплементарен 5'-atgc-3').
"Патоген" - организм, который при взаимодействии с растением приводит к возникновению симптомов заболевания одного или нескольких органов этого растения. К таким патогенам относятся например, животные, грибковые, бактериальные или вирусные организмы и оомицеты.
Под "заражением патогеном" понимается самый ранний момент времени, в который обмен веществ патогена подготавливается к проникновению в ткани растения-хозяина. Например, у грибов или оомицетов к этому относится прорастание гифы или образование специальных структур, например, гифы для пенетрации и апрессории.
Под "патоген-/элиситор-индуцируемостью" в контексте изобретения понимается особое свойство промотора, который после заражения патогеном или применения элиситора приводит к усиленной по меньшей мере в два раза транскрипции оперативно связанного гена. Кроме того, под "патоген-/элиситор-индуцируемостью" в контексте изобретения понимается свойство генов, которые после заражения патогеном или применения элиситора транскрибируются с по меньшей мере двойным усилением.
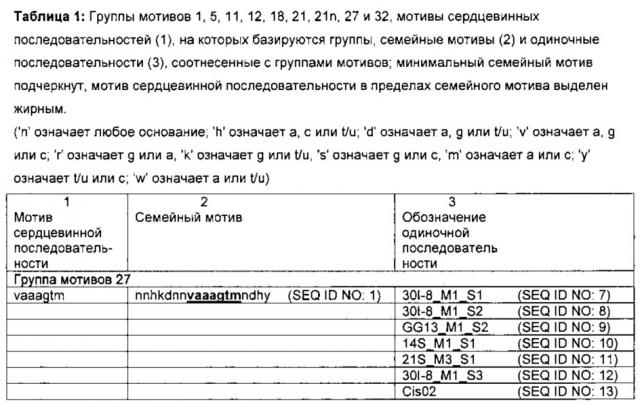
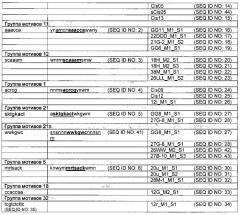
Согласно изобретению поставленная задача решается путем создания новых цис-регуляторных элементов, способствующих индуцируемости патогеном и (или) элиситором. Они значительно отличаются от уже известных элементов, в частности, в пределах сердцевинной последовательности, и не представляют собой их вариации. Таким образом, цис-регуляторные элементы согласно изобретению должны представлять собой точки распознавания и (или) связи для новых факторов транскрипции, следовательно, индуцируемость патогеном и (или) элиситором является новой характеристикой. Цис-регуляторные элементы согласно изобретению были идентифицированы биоинформационными методами в промоторах патоген- или РАМР- (элиситор)-индуцированных генов Arabidopsis thaliana. В результате различных этапов анализа изолированные одиночные последовательности цис-регуляторных элементов удалось соотнести с восемью группами мотивов (группы 1, 5, 11, 12, 18, 21, 27 и 32). Кроме того, несколько изолированных одиночных последовательностей удалось соотнести с группой мотивов 21n. К одной группе мотивов относятся те одиночные последовательности, которые при сравнении идентифицированных мотивов обнаруживают высокую степень консервативности. Таким образом, все одиночные последовательности одной группы мотивов совпадают в одном характерном мотиве сердцевинной последовательности. Следовательно, поставленная задача решается с помощью изолированного цис-регуляторного элемента, включающего молекулу нуклеиновой кислоты, нуклеотидная последовательность которой соответствует одному из мотивов сердцевинной последовательности из:
a) vaaagtm,
b) aaacca,
c) scaaam,
d) acrcg,
e) sktgkact,
f) mrtsack,
g) ccaccaa,
h) tcgtctcttc или
i) wwkgwc
Менее консервативные позиции основании в характерных мотивах сердцевинной последовательности а) - i): Υ' означает гуанин (g) или аденин (а), то есть пуриновое основание, 'k' означает гуанин (g) или тимин (t)урацил (u), 's' означает гуанин (g) или цитозин (с), 'm' означает аденин (а) или цитозин (с) и 'w' означает аденин (а) или тимин (t)/урацил (u). Определенный мотив сердцевинной последовательности воспроизводит по меньшей мере одну частичную последовательность сердцевинной последовательности каждой одиночной последовательности группы мотивов, относящейся к мотиву сердцевинной последовательности, причем эта частичная последовательность может составлять минимум 30% общей сердцевинной последовательности одной одиночной последовательности. В группах мотивов сердцевинной последовательности g) и h) мотив сердцевинной последовательности соответствует всей сердцевинной последовательности одиночных последовательностей. Изобретение также включает изолированный цис-регуляторный элемент, включающий молекулу нуклеиновой кислоты, нуклеотидная последовательность которой соответствует одному мотиву сердцевинной последовательности, комплементарному а) - i). Характерный мотив сердцевинной последовательности определенной группы мотивов может также неоднократно встречаться в сердцевинной последовательности определенной одиночной последовательности, причем мотивы сердцевинной последовательности могут перекрываться в ней и (или) обладать разной ориентацией. Например, сердцевинная последовательность Cis09 из группы мотивов 1, с одной стороны, имеет частичную последовательность, соответствующую мотиву сердцевинной последовательности acrcg, с другой стороны, - перекрывающуюся на два основания частичную последовательность, которая соответствует комплементарному мотиву сердцевинной последовательности acrcg, и именно cgygt. Другим примером является сердцевинная последовательность 21G-2_M1_S2 из группы мотивов 11, где сердцевинная последовательность имеет две частичные последовательности, которые перекрываются одним основанием и соответствуют комплементарному мотиву сердцевинной последовательности ааасса, а именно tggttt.
Для групп мотивов 1, 5, 11, 12, 21, 21 η и 27 на основании экспериментальных данных о функциональности удалось определить семейный мотив, включающий характерный мотив сердцевинной последовательности. Семейный мотив является производным отличительным признаком фактора транскрипции или семейства факторов транскрипции. Преимущество семейного мотива состоит в том, что он объединяет возможные варианты области распознавания/связывания. Предпочтительно, чтобы семейный мотив определенной группы мотивов объединял все сердцевинные последовательности одиночных последовательностей этой группы. С этой целью для части одиночных последовательностей учитывалась комплементарная цепочка цис-регуляторного элемента; в дальнейшем такие комплементарные последовательности идентифицированных цис-регуляторных последовательностей обозначаются '(inv) ', если это необходимо для понимания. Определенный таким образом семейный мотив имеет длину минимум 15 нуклеотидов, предпочтительно минимум 13 нуклеотидов, особенно предпочтительно минимум 11 нуклеотидов. Кроме соответственного мотива сердцевинной последовательности семейный мотив имеет боковые части, которые при использовании изобретенного цис-регуляторного элемента в химерном промоторе оказывают значительное количественное воздействие на его свойства, например, фоновую активность и силу экспрессии. При увеличении расстояния между определенным основанием боковых частей и сердцевинной последовательностью в одиночной последовательности количественное воздействие ослабевает. Для определения семейного мотива можно дополнительно учитывать и другие высококонсервативные отдельные основания, выходящие за пределы сердцевинных последовательностей одиночных последовательностей и расширяющиеся семейный мотив. Семейные мотивы групп мотивов 1, 5,11, 12, 21, 21 η и 27 перечислены в столбце 2 таблицы 1. Таким образом, изобретение включает и изолированный цис-регуляторный элемент, включающий молекулу нуклеиновой кислоты, нуклеотидная последовательность которой
a) соответствует семейному мотиву согласно SEQ ID NO: 1, включающему мотив сердцевинной последовательности vaaagtm,
b) соответствует семейному мотиву согласно SEQ ID NO: 2, включающему мотив сердцевинной последовательности ааасса,
c) соответствует семейному мотиву согласно SEQ ID NO: 3, включающему мотив сердцевинной последовательности scaaam,
d) соответствует семейному мотиву согласно SEQ ID NO: 4, включающему мотив сердцевинной последовательности acrcg,
e) соответствует семейному мотиву согласно SEQ ID NO: 5, включающему мотив сердцевинной последовательности sktgkact,
f) соответствует семейному мотиву согласно SEQ ID NO: 6, включающему мотив сердцевинной последовательности mrtsack,
g) соответствует семейному мотиву согласно SEQ ID NO: 41, включающему мотив сердцевинной последовательности wwkgwc,
или нуклеотидная последовательность которой соответствует определенному семейному мотиву, комплементарному а) - д).
Кроме того, семейный мотив может быть и короче. В самой короткой форме он определяется как минимальный семейный мотив, который после упорядочения одиночных последовательностей в соответствии с общим мотивом сердцевинной последовательности включает только те позиции оснований, который встречаются в сердцевинных последовательностях всех одиночных последовательностей одной группы мотивов. В некоторых случаях минимальный семейный мотив соответствует мотиву сердцевинной последовательности. В столбце 2 таблицы 1 (заголовок "Семейный мотив") подчеркнуты минимальные семейные мотивы групп мотивов 1, 5, 11, 12, 21, 21n и 27.
Изобретение также касается всех идентифицированных и изолированных одиночных последовательностей цис-регуляторных элементов согласно изобретению и их сердцевинных последовательностей (таблицы 1 и 2). Таким образом, задача решается за счет изолированного цис-регуляторного элемента, включающего
a) молекулу нуклеиновой кислоты с последовательностью нуклеотидов согласно SEQ ID NO: 7, SEQ ID NO: 8, SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 11, SEQ ID NO: 12, SEQ ID NO: 13, SEQ ID NO: 14, SEQ ID NO: 15, SEQ ID NO: 16, SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19, SEQ ID NO: 20, SEQ ID NO: 21, SEQ ID NO: 22, SEQ ID NO: 23, SEQ ID NO: 24, SEQ ID NO: 25, SEQ ID NO: 26, SEQ ID NO: 27, SEQ ID NO: 28, SEQ ID NO: 29, SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34, SEQ ID NO: 42, SEQ ID NO: 43 или SEQ ID NO: 44,
b) молекулу нуклеиновой кислоты с последовательностью нуклеотидов согласно сердцевинной последовательности из SEQ ID NO: 7, SEQ ID NO: 8, SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 11, SEQ ID NO: 12, SEQ ID NO: 13, SEQ ID NO: 14, SEQ ID NO: 15, SEQ ID NO: 16, SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19, SEQ ID NO: 20, SEQ ID NO: 21, SEQ ID NO: 22, SEQ ID NO: 23, SEQ ID NO: 24, SEQ ID NO: 25, SEQ ID NO: 26, SEQ ID NO: 27, SEQ ID NO: 28, SEQ ID NO: 29, SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34, SEQ ID NO: 42, SEQ ID NO: 43 или SEQ ID NO: 44, или
с) молекулу нуклеиновой кислоты с последовательностью нуклеотидов, комплементарной одной из последовательностей нуклеотидов из а) или b). Цис-регуляторный элемент, включающий молекулу нуклеиновой кислоты с последовательностью нуклеотидов согласно SEQ ID NO: 24, SEQ ID NO: 25 или SEQ ID NO: 26 относится к группе мотивов 1, элемент с последовательностью нуклеотидов согласно SEQ ID NO: 30, SEQ ID NO: 31 или SEQ ID NO: 32 к группе мотивов 5, элемент с последовательностью нуклеотидов согласно SEQ ID NO: 16, SEQ ID NO: 17, SEQ ID NO: 18 или SEQ ID NO: 19 к группе мотивов 11, элемент с последовательностью нуклеотидов согласно SEQ ID NO: 20, SEQ ID NO: 21, SEQ ID NO: 22 или SEQ ID NO: 23 к группе мотивов 12, элемент с последовательностью нуклеотидов согласно SEQ ID NO: 33 к группе мотивов 18, элемент с последовательностью нуклеотидов согласно SEQ ID NO: 27 или SEQ ID NO: 28 к группе мотивов 21, элемент с последовательностью нуклеотидов согласно SEQ ID NO: 27, SEQ ID NO: 28, SEQ ID NO: 42 или SEQ ID NO: 43 к группе мотивов 21n, элемент с последовательностью нуклеотидов согласно SEQ ID NO: 7, SEQ ID NO: 8, SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 11, SEQ ID NO: 12, SEQ ID NO: 13, SEQ ID NO: 14, SEQ ID NO: 44 или SEQ ID NO: 15 к группе мотивов 27 и элемент с последовательностью нуклеотидов согласно SEQ ID NO: 34 - к группе мотивов 32.
Изобретенный цис-регуляторный элемент может иметь длину менее 50 нуклеотидов, предпочтительно менее 40 нуклеотидов и особенно предпочтительно менее 30 нуклеотидов. Сердцевинная последовательность изобретенного цис-регуляторного элемента может иметь длину менее 20 нуклеотидов, предпочтительно менее 15 нуклеотидов, особенно предпочтительно менее 10 нуклеотидов, однако она не должна быть короче 6 нуклеотидов.
Некоторые одиночные последовательности цис-регуляторных элементов согласно изобретению могут помимо идентифицированной новой сердцевинной последовательности содержать и сердцевинную последовательность известного цис-регуляторного элемента, способствующего патоген-/элиситор-индуцируемости, что при определенных обстоятельствах может влиять и на специфичность новой идентифицированной сердцевинной последовательности и (или) идентифицированной одиночной последовательности. Одним из примеров является цис-регуляторный элемент Cis05 (SEQ ID NO: 14), которые помимо идентифицированной сердцевинной последовательности между позициями нуклеотидов 14 и 20 содержит также сердцевинную последовательность W-бокса между позициями нуклеотидов 29 и 35. Для этой цели были проведены подробные анализы мутаций (см. рис. 5А, 5В и 11). Цис-регуляторный элемент согласно изобретению можно использовать в химерном промоторе, причем данный элемент придает химерному промотору специфическую патоген- и (или) элиситор-индуцируемость. Таким образом, данное изобретение включает химерный промотор, который подходит для того, чтобы под действием заражения патогеном или обработки патогенным элиситором воздействовать на экспрессию оперативно связанной молекулы нужной нуклеиновой кислоты, например, гетерологической последовательности ДНК, в растительной клетке, и который состоит из минимального промотора и по меньшей мере одного цис-регуляторного элемента согласно изобретению. Один изобретенный цис-регуляторный элемент в таком химерном промоторе уже может содействовать значительной патоген- и (или) элиситор- индуцируемости. Таким образом, этого цис-регуляторного элемента уже достаточно для конструирования патоген-/элиситор-реактивного химерного промотора в сочетании с минимальным промотором.
Предпочтительно, чтобы это был такой химерный промотор, содержащий только один или несколько цис-регуляторных элементов согласно изобретению, который реагировал бы только на патоген и (или) элиситор, то есть этот промотор не должен индуцироваться (или должен индуцироваться лишь в небольшой степени) другими стимулами, например, абиотическим стрессом. Индукция такого химерного промотора, включающего один или несколько цис-регуляторных элементов согласно изобретению, после контакта с патогеном/элиситором минимум в 2 раза, предпочтительно в 10 раз, особенно предпочтительно минимум в 25 раз сильнее индукции без контакта с патогеном/элиситором (фоновая активность).
В предпочтительном варианте индуцированная экспрессия ограничивается местом заражения, то есть в аналогичной или меньшей степени по сравнению с контролируемой экспрессией природных PR-генов. Особенно предпочтительно, чтобы контролируемая активация транскрипции химерным промотором согласно изобретению происходила только в тех клетках, которые контактируют с патогеном или патогенным элиситором. Однако в результате взаимодействия клеток транскрипция может активироваться и в тех клетках, которые окружают место или места заражения. Однако химерные промоторы согласно данному изобретению не ограничиваются исключительно патоген-реактивными. При сочетании с другими регуляторными элементами индуцированную экспрессию можно задать более точно, например, путем комбинирования с цис-регуляторным элементом, который способствует, например, определенной специфичности ткани, индуцируемости при хранении, холоде или высокой температуре, а также специфической активности на определенных этапах развития. Химерные промоторы согласно изобретению могут включать и по меньшей мере одну комбинацию из минимум двух цис-регуляторных элементов, причем данная (минимум одна) комбинация включает по меньшей мере один цис-регуляторный элемент согласно изобретению. Другими цис-регуляторными элементами в комбинации для создания химерного промотора могут быть и известные элементы, способствующие патоген-/элиситор-индукции, например, W-бокс, S-бокс или D-бокс (см. WO 00/29592).
Кроме того, изобретение включает химерный промотор, который содержит один или несколько мономеров и (или) один или несколько мультимеров цис-регуляторных элементов согласно изобретению. Предпочтительными формами являются димеры и тетрамеры Мономеры сами по себе или отдельные мономеры в мультимере могут иметь разные ориентации, т.е. они могут быть расположены, например, комплементарно. Мультимерные цис-регуляторные элементы согласно изобретению могут быть функционально связаны, то есть в мультимерной форме они демонстрируют синергетическое или антагонистическое действие, например, на связывающую способность фактора транскрипции, который, в том числе, распознает характерный мотив сердцевинной последовательности определенной группы мотивов. Изобретение также включает химерный промотор, который подходит для того, чтобы под действием заражения патогеном или обработки патогенным элиситором воздействовать на экспрессию оперативно связанной молекулы нужной нуклеиновой кислоты в растительной клетке, и который состоит из минимального промотора и по меньшей мере двух цис-регуляторных элементов согласно изобретению, причем минимум два цис-регуляторных элемента согласно изобретению могут быть функционально связаны в гомо- и (или) гетеромерной форме. Индукция химерного промотора, включающего минимум один мультимер цис-регуляторных элементов согласно изобретению, после контакта с патогеном/элиситором минимум в 2 раза, предпочтительно в 10 раз, особенно предпочтительно минимум в 25 раз сильнее индукции без контакта с патогеном/элиситором (фоновая активность).
В предпочтительном варианте химерных промоторов согласно изобретению расстояние от минимального промотора до первого в направлении вверх цис-регуляторного элемента согласно изобретению составляет от 0 до 300 пар оснований, предпочтительно от 0 до 70 пар, особенно предпочтительно менее 10 пар. Дополнительно или альтернативно расстояние между двумя одинаковыми мономерами цис-регуляторных элементов согласно изобретению в мультимерной форме составляет от 0 до 10 пар оснований. Предпочтительно, чтобы два отдельных мультимера в химерном промоторе согласно изобретению разделялись примерно 0-50 парами оснований.
Специфические комбинации цис-регуляторных элементов согласно изобретению с другими цис-регуляторными элементами согласно изобретению или с другими известными регуляторными элементами или фрагментами, например, S-боксом, D-боксом или Gst1 по результатам экспериментальных анализов неожиданно продемонстрировали воздействие на свойства промоторов, например, на невысокую фоновую активность или особо специфическую либо особо сильную индуцируемость (до 183-кратной 2xCis13-2xCis05). При этом некоторые комбинации демонстрируют синергетическое действие на определенное свойство промотора, например, на фактор индукции (см. например 2xCis13-2xC¡s05 в петрушке, рис. 12 и 13), а другие - антагонистическое действие на фактор индукции, но особенно низкую фоновую активность (например, 4xCis05-2xD в сахарной свекле). Кроме того, изобретение включает все возможные сочетания цис-регуляторных элементов согласно изобретению между собой и с известными цис-регуляторными элементами, оказывающие предпочтительное синергетическое или антагонистическое действие на индуцируемость промотора. Предпочтительными комбинациями являются те, которые можно выбрать из следующей группы: 4х sCis05, 4х 20u_M1_S1, 4х 27G-8_M1_S1, 4х 38M_M1_S1, 4х 18H_M2_S3, 4х 18H_M2_S1, 4х GG13_M1_S2, 4х 21S_M3_S1, 4х 30I-8_M1_S2, 2х Cis02 - 2х Cis02, 2х Cis02 - 2х Cis05, 2х Cis02 - 2х Cis12, 2х Cis02 - 2х C¡s13, 2х Cis02 - 2х D, 2х Cis02 - 2х S, 2х Cis02 - Gst1, 2х Cis02 - 2х 30I-8_M1_S2, 2х Cis05 - 2х Cis02, 2х Cis05 - 2х Cis05, 2х Cis05 - 2х Cis12, 2х C¡s05 - 2х Cis13, 2х Cis05 -2х D, 2х Cis05 - 2х S, 2х C¡s05 - Gst1, 2x Cis05 - 2x 30I-8_M1_S2, 2x Cis12 - 2x Cis02, 2x C¡s12-2x C¡s05, 2x Cis12-2x Cis12, 2x C¡s12-2x Cis13, 2x Cis12-2x D, 2x Cis12-2x S, 2x Cis12 - Gst1, 2x Cis12 - 2x 30I-8_M1_S2, 2x Cis13 - 2x Cis02, 2x Cis13 - 2x Cis05, 2x Cis13-2x Cis12, 2x Cis13-2x Cis13, 2x Cis13-2x D, 2x Cis13-2xS, 2x C¡s13-Gst1, 2x C¡s13 - 2x 30I-8_M1_S2, 2x D - 2x Cis02, 2x D - 2x C¡s05, 2x D - 2x Cis12, 2x D -2x Cis13, 2x D - 2x 30I-8_M1_S2, 2x S - 2x Cis02, 2x S - 2x Cis05, 2x S - 2x Cis12, 2x S -2x Cis13, 2x S - 2x 30I-8_M1_S2, Gst1 - 2x Cis02, Gst1 - 2x Cis05, Gst1 - 2x Cis12, Gst1 -2x Cis13, Gst1 - 2x 30I-8_M1_S2, 2x 30I-8_M1_S2 - 2x Cis02, 2x 30I-8_M1_S2 - 2x C¡s05, 2x 30I-8_M1_S2 - 2x Cis12, 2x 30I-8_M1_S2 - 2x Cis13, 2x 30I-8_M1_S2 - 2x D, 2x 30I-8_M1_S2 - 2x S, 2x 30I-8_M1_S2 - Gst1 и 2x 30I-8_M1_S2 - 2x 30I-8_M1_S2. Особенно предпочтительные комбинации с неожиданным воздействием на фактор индукции и активность приведены в таблице 3.
Данное изобретение также относится к химерным промоторам, которые включают по меньшей мере одну из вышеназванных комбинаций цис-регуляторных элементов.
В предпочтительном варианте химерных промоторов согласно изобретению минимальный промотор происходит, например, из промотора CaMV35S, для однодольных растений, например, из промотора пшеницы TaPal (SEQ ID NO: 39), промотора кукурузы ZmUbiquitin (SEQ ID NO: 40) или промотора риса OsGnsI (SEQ ID NO: 38), для двудольных растений из известных минимальных промоторов (WO 07/147395). Кроме того, для конструирования химерного промотора согласно изобретению можно использовать и минимальные промоторы из других источников.
В любом случае, химерный промотор согласно изобретению соответствует основным требованиям, которые предъявляются к строгому регулированию экспрессии трансгена в генной инженерии, например, при создании растения, резистентного к определенному патогену/заболеванию. Трансген - это оперативно связанная с химерным промотором молекула нуклеиновой кислоты, например, гетерологическая последовательность ДНК, кодирующая для гена резистентности (R-гена) автоактивируемый ген резистентности, ген авирулентности, другой эффектор, протеин, токсичный по отношению к по меньшей мере одному патогену, компонент передачи сигнала, протеин, участвующий в синтезе фитоалексинов, двуцепочечную РНК для образования направленной против патогена siPHK или антимикробный пептид. Кроме того, многочисленные опыты с петрушкой (Petroselinum erispum), Arabidopsis thaliana, пшеницей (Triticum sp.) и сахарной свеклой (Beta vulgaris) показали, что химерный промотор согласно изобретению функционирует с разными видами растений (см., например, 4xCis05 в петрушке, сахарной свекле и пшенице).
Определение семейного мотива для каждой группы мотивов 1, 5, 11, 12, 21, 21n и 27 открывает перед специалистом новые возможности конструирования химерных промоторов согласно данному изобретению. Наблюдаемая активность разных членов групп мотивов 27 и 12 (рис. 8) показывает, что боковые участки последовательности можно использовать для точной настройки нужных уровней экспрессии. Это относится и к настройке уровней экспрессии в зависимости от вида растения. Семейный мотив воспроизводит возможности варьирования отдельных оснований в боковых областях, показывая специалисту, насколько можно модифицировать эти области. Кроме того, на основании семейного мотива специалист получает информацию о том, насколько консервативны отдельные позиции оснований в пределах этого мотива. При этом следует исходить из того, что модификация сильно консервативного основания влияет на конечные свойства химерного промотора сильнее, чем слабо консервативное основание.
Кроме того, изобретение касается рекомбинантного гена, включающего химерный промотор согласно изобретению. Предпочтительно, чтобы рекомбинантный ген был таким, чтобы химерный промотор был оперативно связан с молекулой нуклеиновой кислоты, например, с гетерологической последовательностью ДНК. Такая гетерологическая последовательность ДНК кодирует, в частности, (поли)пептид, цитотоксичный протеин (например, Bt-токсин, авирулентный протеин или такие энзимы, как глюкозооксидазы, вырабатывающие реактивные формы кислорода) антитело, антисмысловую РНК, смысловую РНК, фактор транскрипции, протеазу, нуклеазу, липазу, ингибитор энзимов или измеримый маркер (например, люциферазу, GFP или β-галактосидазу). Последние маркеры, а также маркеры, известные на данный момент можно использовать в тестах, чтобы определить патогенную специфичность химерного промотора согласно изобретению или идентифицировать эффекторы, способствующие индукции химерного промотора или тормозящие ее. Химерные промоторы согласно изобретению можно также использовать в технологиях подавления экспрессии генов на базе PHKi, причем оперативно связанная молекула нуклеиновой кислоты кодирует, например, антисмысловую РНК, смысловую РНК или двуцепочечную РНК (dsPHK). Молекула РНК может представлять собой короткую нуклеотидную последовательность (минимум 10 нуклеотидов, предпочтительно минимум 14 нуклеотидов, в некоторых вариантах до 100 нукл