Композиции для лечения гипертензии и/или фиброза
Иллюстрации
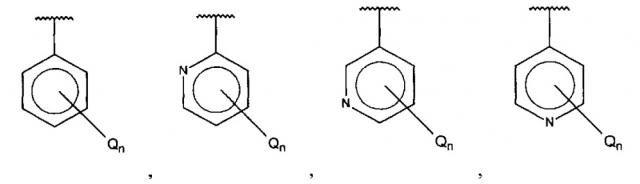
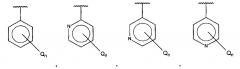
Показать всеИзобретение относится к соединению формулы (1) или его фармацевтически приемлемой соли, где А выбран из группы, состоящей из фенила или пиридина, замещенных Qn, или конденсированных кольцевых структур, приведенных ниже; Q независимо выбран из галогена, алкила, гидрокси, амино и замещенного амино; n равняется 0, 1, 2, 3, 4 или 5; R1, R3 и R4 независимо представляют собой С, СН, CH2, О, N, NH или S, и R2 представляет собой С, СН, СН2, N, NH, C-CF3, CH-CF3 или С=O; причем, если n равняется 1, Q не может представлять собой гидрокси; замещенный амино имеет формулу -NHW, где W выбран из -CN, -SO2(X)aY и -CO(X)aY, а равняется 0 или 1, X выбран из -NH- и -О-, и Y выбран из -Н, -СН3, -СН2СН3, -СН2ОН и -СН2СН2ОН, и где связи между R1 и R2, R2 и R3, R3 и R4 независимо представляют собой двойные или одинарные связи. Также изобретение относится к фармацевтической композиции, обладающей эффектами, снижающими артериальное давление, и/или противофиброзными эффектами, содержащей эффективное количество соединения или его фармацевтически приемлемой соли формулы (1) и фармацевтически приемлемое вспомогательное средство. Соединения по изобретению предназначены для лечения гипертензии, предгипертензии и фиброза. 11 н. и 7 з.п. ф-лы, 22 пр., 21 ил.
,
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к новым соединениям и их применению при профилактическом и/или терапевтическом лечении сердечно-сосудистых заболеваний, и, в частности, лечении предгипертензии, гипертензии и/или фиброзных состояний.
Настоящее изобретение было разработано преимущественно для профилактического и/или терапевтического лечения сердечно-сосудистого заболевания и будет описано далее в данном документе со ссылкой на настоящую заявку. Однако следует принимать во внимание, что настоящее изобретение не ограничено данной конкретной областью применения.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Любое обсуждение уровня техники по всему настоящему описанию никоим образом не должно рассматриваться как допущение того, что такой уровень техники широко известен или образует часть общеизвестных знаний в данной области.
Гипертензия (высокое артериальное давление) поражает 26% взрослого населения по всему миру с частотой встречаемости 30-33% в западных странах. Ожидается, что частота встречаемости гипертензии в мире достигнет 29% к 2025 году вследствие вестернизации Индии и Китая. Современные исследования указывают на то, что менее чем 20% пациентов с гипертензией достигают рекомендованного целевого значения артериального давления (BP) и что для достижения этих целей >75% пациентов нуждаются в терапии с использованием нескольких антигипертензивных средств. Предгипертензия (немного повышенное артериальное давление) поражает 31% взрослых в США и без лечения может развиться в гипертензию.
Все доступные в настоящее время методы терапии имеют побочные эффекты:
• ингибиторы ангиотензинпревращающего фермента (ACEI) - кашель, ангионевротический отек, гиперкалиемия;
• блокаторы рецепторов ангиотензина (ARB) - ангионевротический отек, гиперкалиемия;
• блокаторы кальциевых каналов (ССВ) - гиперемия, отек ноги/лодыжки, запор;
• тиазидные диуретики - впервые выявленный диабет, подагра, гипонатриемия;
• бета (β)-блокаторы - впервые выявленный диабет, неспособность к физическим нагрузкам, брадикардия, скрытая гипогликемия у больных диабетом, и
• антагонисты альдостерона - гинекомастия, меноррагия, гиперкалиемия.
Необходимость применения комбинированной терапии повышает вероятность того, что пациенты будут испытывать побочные эффекты и, как следствие, не достигнут целевого значения BP.
Гипертензия и предгипертензия представляют собой основной фактор развития повреждения сердца, почек и кровеносных сосудов, приводя к замещению нормальной функциональной ткани рубцовой тканью или фиброзом. Некоторые из существующих антигипертензивных средств - ингибиторы АСЕ, ингибиторы ренина ARB и антагонисты альдостерона, способны замедлять прогрессирование замещения функциональной ткани фиброзом, однако ни для одного из них не было показано обращение существующего фиброза и восстановление нормального строения ткани. Таким образом, существует потребность в средствах, которые эффективны в существенном снижении значения BP и, таким образом, позволяют более значительной части пациентов достигнуть целевого значения BP при терапии одним средством, и/или обратить существующий фиброз, и/или восстановить нормальное строение ткани.
Целью настоящего изобретения является преодоление или устранение по меньшей мере одного из недостатков уровня техники или предоставление полезной альтернативы.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Авторы настоящего изобретения неожиданно обнаружили, что некоторые новые терфенильные соединения обладают эффектами, снижающими артериальное давление, и/или противофиброзными эффектами. Эти эффекты можно наблюдать в исследованиях с внутривенным и/или пероральным введением дозы.
Согласно одному аспекту настоящее изобретение предусматривает соединение формулы
,
где
А выбран из группы, состоящей из
и ,
Q независимо выбран из галогена, алкила, гидрокси, амино и замещенного амино;
n равняется 0, 1, 2, 3, 4 или 5;
R1, R3 и R4 независимо представляют собой C, CH, CH2, О, N, NH или S, и
R2 представляет собой C, СН, CH2, N, NH, C-CF3, CH-CF3 или C=O,
или его стереоизомер или фармацевтически приемлемую соль,
где, если n равняется 1, Q не может представлять собой гидрокси.
В одном варианте осуществления Q представляет собой галоген, выбранный из группы, состоящей из F, Cl, Br и I.
В одном варианте осуществления Q представляет собой замещенный амино формулы -NHW, и где
W выбран из -CN, -SO2(X)aY и -CO(X)aY,
а равняется 0 или 1,
X выбран из -NH- и -O-, и
Y выбран из -H, -CH3, -CH2CH3, -CH2OH и -CH2CH2OH.
В одном варианте осуществления Q представляет собой замещенный амино, выбранный из группы, состоящей из -NHSO2CH3, -NHCOH, -NHCONHCH3, -NHCONHCH2CH3, -NHSO2NHCH3, -NHSO2NHCH2CH3, -NHCOCH3, -NHCOOCH3, -NHCOOCH2CH2OH, -NHCONH2 и -NHCN.
В одном варианте осуществления Q представляет собой алкил, выбранный из группы, состоящей из метила, этила, пропила, бутила и пентила.
В одном варианте осуществления A выбран из:
и .
В одном варианте осуществления A представляет собой
,
где
X, Y или Z представляют собой C или N, где только один из X, Y или Z может представлять собой N,
R5-R9 независимо выбраны из водорода, галогена, алкила, гидрокси, амино и замещенного амино, при условии, что если один из R5-R9 представляет собой галоген, то по меньшей мере один из оставшихся R5-R9 не может представлять собой водород.
В одном варианте осуществления A представляет собой
,
где
X, Y или Z представляют собой C или N, где только один из X, Y или Z может представлять собой N,
R5-R9 независимо выбраны из водорода, галогена, алкила, гидрокси, амино и замещенного амино, при условии, что если один из R5-R9 представляет собой галоген, то по меньшей мере один из оставшихся R5-R9 должен представлять собой галоген, алкил, гидрокси, амино или замещенный амино.
В одном варианте осуществления A представляет собой
,
где
X, Y или Z представляют собой C или N, где только один из X, Y или Z может представлять собой N,
R5-R9 независимо выбраны из водорода, галогена, алкила, гидрокси, амино и замещенного амино, при условии, что если один из R5-R9 представляет собой галоген, то по меньшей мере один из оставшихся R5-R9 должен представлять собой алкил, гидрокси, амино или замещенный амино.
В одном варианте осуществления A представляет собой
,
где
X, Y или Z представляют собой C или N, где только один из X, Y или Z может представлять собой N,
R5-R9 независимо выбраны из водорода, галогена, алкила, гидрокси, амино и замещенного амино, при условии, что если один из R5-R9 представляет собой алкил, то по меньшей мере один из оставшихся R5-R9 не может представлять собой водород.
В одном варианте осуществления A представляет собой
,
где
X, Y или Z представляют собой C или N, где только один из X, Y или Z может представлять собой N,
R5-R9 независимо выбраны из водорода, галогена, алкила, гидрокси, амино и замещенного амино, при условии, что если один из R5-R9 представляет собой алкил, то по меньшей мере один из оставшихся R5-R9 должен представлять собой галоген, алкил, гидрокси, амино или замещенный амино.
В одном варианте осуществления A представляет собой
,
где
X, Y или Z представляют собой C или N, где только один из X, Y или Z может представлять собой N,
R5-R9 независимо выбраны из водорода, галогена, алкила, гидрокси, амино и замещенного амино, при условии, что если один из R5-R9 представляет собой алкил, то по меньшей мере один из оставшихся R5-R9 должен представлять собой галоген, гидрокси, амино или замещенный амино.
В одном варианте осуществления A представляет собой
,
где
X, Y или Z представляют собой C или N, где только один из X, Y или Z может представлять собой N,
R5-R9 независимо выбраны из водорода, галогена, алкила, гидрокси, амино и замещенного амино, при условии, что если один из R5-R9 представляет собой гидрокси, то по меньшей мере один из оставшихся R5-R9 не может представлять собой водород.
В одном варианте осуществления A представляет собой
,
где
X, Y или Z представляют собой C или N, где только один из X, Y или Z может представлять собой N,
R5-R9 независимо выбраны из водорода, галогена, алкила, гидрокси, амино и замещенного амино, при условии, что если один из R5-R9 представляет собой гидрокси, то по меньшей мере один из оставшихся R5-R9 должен представлять собой галоген, гидрокси, амино или замещенный амино.
В одном варианте осуществления A представляет собой
,
где
X, Y или Z представляют собой C или N, где только один из X, Y или Z может представлять собой N,
R5-R9 независимо выбраны из водорода, галогена, алкила, гидрокси, амино и замещенного амино, при условии, что если один из R5-R9 представляет собой гидрокси, то по меньшей мере один из оставшихся R5-R9 должен представлять собой галоген, амино или замещенный амино.
В одном варианте осуществления A представляет собой , Q представляет собой замещенный амино, и n равняется 1.
В одном варианте осуществления A представляет собой , Q представляет собой замещенный амино, и n равняется 2.
В одном варианте осуществления A представляет собой , Q представляет собой амино, и n равняется 1.
В одном варианте осуществления A представляет собой , Q представляет собой амино, и n равняется 2.
В одном варианте осуществления A представляет собой , Q представляет собой гидрокси, и n равняется 2.
В одном варианте осуществления A представляет собой .
В одном варианте осуществления A представляет собой .
В одном варианте осуществления A представляет собой .
В одном варианте осуществления A представляет собой .
В одном варианте осуществления A представляет собой .
В одном варианте осуществления A представляет собой .
В одном варианте осуществления A представляет собой , X и Y представляют собой C, Z представляет собой N, и один из R5-R9 представляет собой амино.
В одном варианте осуществления A представляет собой , все из X, Y и Z представляют собой C, один из R5-R9 представляет собой гидрокси, и по меньшей мере один из оставшихся R5-R9 представляет собой галоген.
В одном варианте осуществления A представляет собой , все из Z, Y и Z представляют собой C, два из R5-R9 представляют собой гидрокси, и по меньшей мере один из оставшихся R5-R9 представляет собой галоген.
В одном варианте осуществления A представляет собой , все из Z, Y и Z представляют собой C, два из R5-R9 представляют собой гидрокси, и по меньшей мере один из оставшихся R5-R9 представляет собой алкил.
В одном варианте осуществления A представляет собой , все из Z, Y и Z представляют собой C, один из R5-R9 представляет собой алкил, и по меньшей мере один из оставшихся R5-R9 представляет собой гидрокси.
В одном варианте осуществления A представляет собой , все из Z, Y и Z представляют собой C, один из R5-R9 представляет собой галоген, и по меньшей мере один из оставшихся R5-R9 представляет собой гидрокси.
В одном варианте осуществления A представляет собой , все из Z, Y и Z представляют собой C, два из R5-R9 представляют собой галоген, и по меньшей мере один из оставшихся R5-R9 представляет собой гидрокси.
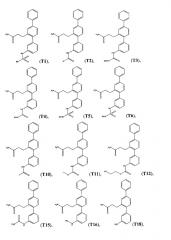
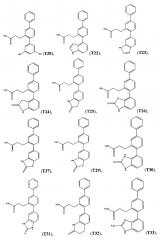
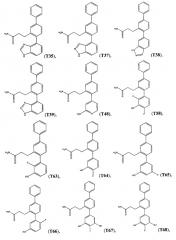
В одном варианте осуществления соединение выбрано из группы, состоящей из:
и .
Согласно другому аспекту настоящее изобретение относится к фармацевтической композиции, содержащей соединение по настоящему изобретению и фармацевтически приемлемое вспомогательное вещество.
Согласно другому аспекту настоящее изобретение относится к способу терапевтического лечения гипертензии или предгипертензии у субъекта, включающему введение субъекту соединения согласно настоящему изобретению.
Согласно другому аспекту настоящее изобретение относится к способу терапевтического лечения фиброза у субъекта, включающему введение субъекту соединения согласно настоящему изобретению.
Согласно другому аспекту настоящее изобретение относится к способу профилактического лечения фиброза у субъекта, включающему введение субъекту соединения согласно настоящему изобретению.
Согласно другому аспекту настоящее изобретение относится к способу терапевтического лечения гипертензии и фиброза у субъекта, включающему введение субъекту соединения согласно настоящему изобретению.
Согласно другому аспекту настоящее изобретение относится к способу терапевтического лечения предгипертензии и фиброза у субъекта, включающему введение субъекту соединения согласно настоящему изобретению.
В одном варианте осуществления фиброз представляет собой фиброз миокарда или фиброз почки.
В другом варианте осуществления фиброз представляет собой фиброз миокарда и фиброз почки.
Согласно другому аспекту настоящее изобретение относится к соединению по настоящему изобретению для применения в терапевтическом лечении гипертензии или предгипертензии.
Согласно другому аспекту настоящее изобретение относится к соединению по настоящему изобретению для применения в терапевтическом лечении фиброза.
Согласно другому аспекту настоящее изобретение относится к соединению по настоящему изобретению для применения в профилактическом лечении фиброза.
Согласно другому аспекту настоящее изобретение относится к соединению по настоящему изобретению для применения в терапевтическом лечении гипертензии и фиброза.
Согласно другому аспекту настоящее изобретение относится к соединению по настоящему изобретению для применения в терапевтическом лечении предгипертензии и фиброза.
Согласно другому аспекту настоящее изобретение относится к применению соединения по настоящему изобретению для изготовления лекарственного препарата для терапевтического лечения гипертензии или предгипертензии.
Согласно другому аспекту настоящее изобретение относится к применению соединения по настоящему изобретению для изготовления лекарственного препарата для терапевтического лечения фиброза.
Согласно другому аспекту настоящее изобретение относится к применению соединения по настоящему изобретению для изготовления лекарственного препарата для профилактического лечения фиброза.
Согласно другому аспекту настоящее изобретение относится к применению соединения по настоящему изобретению для изготовления лекарственного препарата для терапевтического лечения гипертензии и фиброза.
Согласно другому аспекту настоящее изобретение относится к применению соединения по настоящему изобретению для изготовления лекарственного препарата для терапевтического лечения предгипертензии и фиброза.
Если контекст явно не требует иного, по всему описанию и формуле изобретения слова "содержит", "содержащий" и тому подобное должны быть истолкованы во включающем смысле в противоположность исключающему или исчерпывающему смыслу; то есть в смысле "включая без ограничения".
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фигура 1: Синтез 3-формилбифенил-4-ил-трифторметансульфоната.
Фигура 2: Синтез T1, Т2, Т10 и Т18.
Фигура 3: Синтез диэтил(карбоилметил)фосфоната.
Фигура 4: Синтез Т20.
Фигура 5: Синтез Т70.
Фигура 6: Синтез Т48.
Фигура 7: Синтез 3-(3-амино-3-оксопропил)бифенил-4-ил-трифторметансульфоната.
Фигура 8: Синтез Т25.
Фигура 9: Синтез индолонпинаколового эфира бороновой кислоты.
Фигура 10: Синтез Т31.
Фигура 11: Нормализованный относительно исходного уровня клеточный индекс для различных соединений в трех концентрациях, 62,5 мкМ (белые столбики), 125 мкМ (заштрихованные столбики) и 250 мкМ (столбики со сплошной заливкой) на гладкомышечных клетках сосудов крысы А10, определенный при помощи инструмента xCELLigence RTCA.
Фигура 12: Нормализованный относительно исходного уровня клеточный индекс для различных соединений в трех концентрациях, 62,5 мкМ (белые столбики), 125 мкМ (заштрихованные столбики) и 250 мкМ (столбики со сплошной заливкой) на эндотелиальных клетках бычьей аорты, определенный при помощи инструмента xCELLigence RTCA.
Фигура 13: Значения систолического (заштрихованные столбики) и диастолического (белые столбики) артериального давления в контрольных образцах и у обработанных крыс со спонтанной гипертензией (SHR) на 2,2% солевой диете через 4 недели после терапии. T1, Т2, Т20, Т31 и Т48 вводили при 500 пкмоль/кг/мин. в раствор для питья (5% этанола) в течение 4 недель, Т70 вводили при 100 пкмоль/кг/мин. в раствор для питья. * p<0,05, ** p<0,01, *** p<0,005 и **** p<0,0005 - систолическое артериальное давление при лечении по сравнению со систолическим артериальным давлением в контроле; # p<0,05, ## p<0,025 и ### p<0,005 - диастолическое артериальное давление при лечении по сравнению с диастолическим артериальным давлением в контроле.
Фигура 14: Связь между нормализованным относительно исходного уровня клеточным индексом для гладкомышечных клеток сосудов А10 и систолическим артериальным давлением для различных соединений.
Фигура 15: Связь между нормализованным относительно исходного уровня клеточным индексом для эндотелиальных клеток бычьей аорты и систолическим артериальным давлением для различных соединений.
Фигура 16: Фиброз миокарда, определенный количественно при помощи компьютеризированной гистоморфометрии на гистологических срезах, окрашенных с помощью трехцветной окраски по Массону, у SHR на 2,2% солевой диете через 14 недель и спустя 4 недели после обработки лекарственным средством, добавляемым в питьевой раствор, или для контроля, получавшего носитель. * p<0,005, ** p<0,001 и *** p<0,0005 по сравнению с 18-недельным контролем, обработанным носителем. # p<0,05, ## p<0,01, ### p<0,005 и #### p<0,0005 по сравнению с 14-недельным контролем. Последнее сравнение указывает на способность обращать существующую патологию.
Фигура 17: Интерстициальный фиброз в почке, определенный количественно при помощи компьютеризированной гистоморфометрии на гистологических срезах, окрашенных с помощью трехцветной окраски по Массону, у SHR на 2,2% солевой диете через 14 недель и спустя 4 недели после обработки лекарственным средством, добавляемым в питьевой раствор, или для контроля, получавшего носитель. * p<0,005, ** p<0,001 и *** p<0,0005 по сравнению с 18-недельным контролем, обработанным носителем. # p<0,05 по сравнению с 14-недельным контролем.
Последнее сравнение указывает на способность обращения существующей патологии.
Фигура 18: Связь между нормализованным относительно исходного уровня клеточным индексом для эндотелиальных клеток бычьей аорты и фиброзом миокарда для различных соединений.
Фигура 19: Связь между нормализованным относительно исходного уровня клеточным индексом для эндотелиальных клеток бычьей аорты и интерстициальным фиброзом почки для различных соединений.
Фигура 20: Микрофотографии сердца контрольных крыс (А) и крыс, обработанных в течение четырех недель при 500 пкмоль/кг/мин. Т1 (В), Т2 (С), Т20 (D) или Т31 (Е).
Фигура 21: Микрофотографии почки контрольных крыс (А) и крыс, обработанных в течение четырех недель при 500 пкмоль/кг/мин. Т1 (В), Т2 (С), Т20 (D) или Т31 (Е).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к некоторым новым терфенильным соединениям, которые характеризуются эффектами, снижающими артериальное давление, и/или противофиброзными эффектами при исследовании с пероральным введением дозы на экспериментальной животной модели. Что касается противофиброзной активности, соединения по настоящему изобретению являются эффективными в предотвращении фиброза, замедлении прогрессирования развившегося фиброза и/или снижении степени (обращении) развившегося фиброза. Это важное заключение в отношении диапазона и тяжести состояний, которые можно лечить с помощью соединений по настоящему изобретению.
Соединения по настоящему изобретению представлены формулой:
,
где
А выбран из группы, состоящей из
и ,
Q независимо выбран из галогена, алкила, гидрокси, амино и замещенного амино;
n равняется 0, 1, 2, 3, 4 или 5;
R1, R3 и R4 независимо представляют собой C, СН, CH2, О, N, NH или S, и
R2 представляет собой C, СН, CH2, N, NH, C-CF3, CH-CF3 или C=O,
или их стереоизомером или фармацевтически приемлемой солью,
где, если n равняется 1, Q не может представлять собой гидрокси.
Следующие соединения являются конкретными, но не ограничивающими примерами соединений по настоящему изобретению:
и .
Применяемое в данном документе выражение "галоген" означает -F, -О, -Br или -I; выражение "гидрокси" означает -OH; выражение "амино" означает -NH2, и выражение "замещенный амино" включает -NHW, где W выбран из -CN, -SO2(X)aY и -CO(X)aY, а равняется 0 или 1, X выбран из -NH- и -O-, и Y выбран из -H, -CH3, -CH2CH3, -CH2OH и -CH2CH2OH.
Применяемые в данном документе аббревиатуры Me, Et, Ph, Ms представляют собой метил, этил, фенил и метансульфонил, соответственно. Более полный перечень аббревиатур, используемых специалистами в области органической химии в данной области техники, представлен в первом выпуске каждого тома Journal of Organic Chemistry; этот перечень обычно представлен в таблице под названием Стандартный перечень аббревиатур. Аббревиатуры, содержащиеся в упомянутом перечне, и все аббревиатуры, используемые специалистами в области органической химии в данной области техники, включены в данный документ с помощью ссылки.
Соединения по настоящему изобретению могут существовать в определенных геометрических или стереоизомерных формах. Настоящее изобретение предполагает все подобные соединения, включая цис- и транс-изомеры, (R)- и (S)-энантиомеры, диастереомеры, (D)-изомеры, (L)-изомеры, их рацемические смеси и другие их смеси, как попадающие в объем настоящего изобретения. Все подобные изомеры, а также их смеси предназначены для включения в настоящее изобретение.
Если, например, необходим определенный энантиомер соединения по настоящему изобретению, его можно получить путем асимметричного синтеза или путем получения производного с хиральным вспомогательным веществом, где разделяют полученную диастереомерную смесь и отщепляют вспомогательную группу с получением необходимых чистых энантиомеров. В качестве альтернативы, диастереомерные соли могут быть образованы с помощью подходящей оптически активной кислоты или основания с последующим разделением образованных таким образом диастереомеров фракционной кристаллизацией или хроматографическими средствами, хорошо известными из уровня техники, и последующим восстановлением чистых энантиомеров.
В целом, соединения по настоящему изобретению могут быть получены с помощью способов, проиллюстрированных на общих схемах реакций, как, например, описано ниже, или путем их модификаций с использованием легко доступных исходных веществ, реагентов и общепринятых методик синтеза. В данных реакциях также можно воспользоваться вариантами, которые сами по себе известны, но не упомянуты в данном документе.
Настоящее изобретение также предусматривает фармацевтически приемлемые соли соединений. Выражение "фармацевтически приемлемая соль" включает соли присоединения как кислоты, так и основания, и относится к солям, которые сохраняют биологическую эффективность и свойства свободных оснований или кислот и которые не являются биологически или иным образом нежелательными. Фармацевтически приемлемые соли образуются с неорганическими или органическими кислотами или основаниям и могут быть получены in situ во время окончательного выделения и очистки соединений или путем отдельной реакции очищенного соединения в форме его свободного основания или кислоты с соответствующей органической или неорганической кислотой или основанием и выделения образованной таким образом соли.
Выражение "фиброз", применяемое в контексте настоящего изобретения, включает без ограничения фиброз миокарда и/или фиброз почки.
В дополнение к лечению развившегося фиброза соединения по настоящему изобретению могут использоваться профилактически у субъекта с риском развития фиброза. В качестве примера субъектов в категории риска развития фиброза выступают имеющие гипертензию, диабет, миокардит, ишемическую болезнь сердца, синдром Конна, феохромоцитому, генетическую предрасположенность и высокосолевой рацион, и/или получающие лекарственные средства, используемые при химиотерапии рака (такие как даунорубицин). Выражение "профилактический", применяемое в контексте настоящего изобретения, предназначено inter alia для охвата способов лечения, используемых для предупреждения или замедления развития фиброза у находящихся в группе риска. Субъекты, которым может быть предоставлено профилактическое лечение, уже могут иметь признаки ранних нарушений сердца на эхокардиографии.
Выражение "гипертензия", применяемое в контексте настоящего изобретения, указывает на значение артериального давления у взрослого выше приблизительно 139 мм рт.ст. для систолического и/или выше приблизительно 89 мм рт.ст. для диастолического.
Выражение "предгипертензия", применяемое в контексте настоящего изобретения, указывает на значение артериального давления у взрослого в диапазоне приблизительно 120-139 мм рт.ст. для систолического и/или приблизительно 80-89 мм рт.ст. для диастолического.
Настоящее изобретение также предусматривает фармацевтические композиции, которые включают соединения по настоящему изобретению в сочетании с приемлемыми фармацевтическими вспомогательными веществами. Выражение "фармацевтически приемлемое вспомогательное вещество", применяемое в контексте настоящего изобретения, означает любой фармацевтически приемлемый неактивный компонент композиции. Как хорошо известно из уровня техники, вспомогательные вещества включают разбавители, буферы, связующие вещества, смазывающие вещества, разрыхлители, красители, антиоксиданты/консерванты, регуляторы pH и т.д. Вспомогательные вещества выбирают, исходя из желаемых физических аспектов конечной формы: например, получение таблетки с желаемой твердостью и хрупкостью, являющейся быстро диспергируемой и легко проглатываемой и т.д. Требуемая скорость высвобождения активного вещества из композиции после ее приема также играет определенную роль в выборе вспомогательных веществ. Фармацевтические композиции могут включать в себя любой тип лекарственной формы, такой как таблетки, капсулы, порошки, жидкие составы, замедленного или длительного высвобождения, пластыри, средства для вдыхания через нос, назальные спреи и тому подобное. Физическая форма и содержание предусмотренных фармацевтических композиций представляют собой традиционные препараты, которые могут быть составлены специалистом в области фармацевтических составов и основаны на хорошо установленных принципах и композициях, описанных, например, в Remington: The Science and Practice of Pharmacy, 19th Edition, 1995; British Pharmacopoeia 2000, а также аналогичных текстах и руководствах по составам.
Например, если соединения или композиции подлежат введению перорально, их можно составить в виде таблеток, капсул, гранул, порошков или сиропов; или для парентерального введения их можно составить в виде инъекций (внутривенных, внутримышечных или подкожных), препаратов для капельного вливания или суппозиториев. Для применения через слизистую оболочку глаза их можно составить в виде глазных капель или глазных мазей. Эти составы можно получить с помощью обычных средств, и, если необходимо, активный ингредиент можно смешивать с любой традиционной добавкой, такой как вспомогательное вещество, связующее вещество, разрыхляющее средство, смазывающее вещество, модификатор лекарственных средств, солюбилизирующее средство, суспендирующее вспомогательное средство, эмульгирующее средство или покрывающее средство.
Когда соединение(-ия) по настоящему изобретению вводят в виде фармацевтических препаратов человеку и животным, их можно принимать per se или в виде фармацевтической композиции, содержащей, например, от 0,1 до 99,5% (более предпочтительно от 0,5 до 90%) активного ингредиента в комбинации с фармацевтически приемлемым носителем.
Дозировку соединения и частоту введения, которые следует использовать, также может легко определить практикующий врач для получения требуемого ответа.
Несмотря на то, что дозировка будет варьироваться в зависимости от симптомов, возраста и массы тела пациента, природы и тяжести расстройства, подлежащего лечению или профилактике, пути введения и формы лекарственного средства, в целом суточная доза от 0,0001 мг до 200 мг соединения по настоящему изобретению может быть подходящим эффективным количеством для взрослого пациента-человека, и ее можно вводить в виде одной дозы или в виде раздельных доз.
"Пациент" или "субъект", подлежащий лечению заявленным способом, может означать человека или субъекта, не относящегося к человеку.
"Эффективное количество" заявленного соединения в связи со способом лечения относится к количеству терапевтического средства в препарате, которое при применении в виде части требуемого режима дозирования обеспечивает пользу согласно клинически приемлемым стандартам лечения или профилактики определенного нарушения.
Настоящее изобретение далее будет описано более подробно со ссылкой на конкретные, но не ограничивающие примеры, описывающие конкретные композиции и способы применения. Однако следует понимать, что подробное описание конкретных процедур, композиций и способов включено исключительно для целей иллюстрации настоящего изобретения. В любом случае его не следует понимать в качестве ограничения широкого описания концепции изобретения, как изложено выше.
ПРИМЕРЫ
Пример 1 - Синтез 3-формилбифенил-4-ил-трифторметансульфоната
Синтетический путь, используемый для получения 3-формилбифенил-4-ил-трифторметансульфоната (14), показан на фигуре 1. Вкратце, использовали реакцию перекрестного сочетания Сузуки между 5-бром-2-гидроксибензальдегидом и фенилбороновой кислотой с получением 2-гидрокси-5-фенилбензальдегида (13), который затем вводили в реакцию с N-фенилтрифламидом с получением 3-формилбифенил-4-ил-трифторметасульфоната (14).
Получение 2-гидрокси-5-фенилбензальдегида (13)
5-Бромсалицилальдегид (2,49 г, 12,4 ммоль), фенилбороновую кислоту (1,51 г, 12,4 ммоль), палладия(II) ацетат (14 мг, 0,5 мол. %) и карбонат калия (5,14 г, 37,2 ммоль) перемешивали в дегазированной воде (75 мл) при температуре окружающей среды в течение 2 часов в атмосфере аргона. Реакцию контролировали при помощи TLC (1:1 дихлорметан/пентан). Добавляли воду (75 мл) и подкисляли реакционную смесь (pH 6) с помощью 10% HCl, затем экстрагировали этилацетатом (3х). Объединенные органические экстракты промывали солевым раствором, затем высушивали и концентрировали. Неочищенное вещество пропускали через короткую колонку силикагеля с элюированием смесью 1:1 дихлорметан/пентан, затем перекристаллизовывали из смеси этилацетат/пентан с получением 2-гидрокси-5-фенилбензальдегида (1,89 г, 77%) в виде темно-желтых кристаллов (при необходимости можно растирать в порошок с пентаном вместо перекристаллизации); т.пл. 100-101°C. 1Н ЯМР (400 МГц, CDCl3) δ 10,99 (s, 1Н); 9,97 (s, 1H); 7,78-7,73 (m, 2H); 7,56-7,52 (m, 2H); 7,47-7,41 (m, 2H); 7,37-7,32 (m, 1H); 7,09-7,04 (m, 1H). 13C ЯМР (100 МГц, CDCl3) δ 196,9, 161,2, 139,6, 136,0, 133,6, 132,1, 129,2, 127,6, 126,8, 121,0, 118,4. EIMS: масса/заряд 198 [M]+. HRMS рассчитанное для C13H10O2 198,0675, обнаруженное 198,0677.
Получение 3-формилбифенил-4-ил-трифторметансульфоната (14)
2-Гидрокси-5-фенилбензальдегид (13) (100 мг, 0,50 ммоль), N-фенилтрифлимид (180,0 мг, 0,51 ммоль) и карбонат калия (209 мг, 1,51 ммоль) перемешивали в сухом THF в герметично закрытой пробирке и нагревали при 120°C в течение 6 минут с помощью микроволнового излучения. Удаляли растворитель при пониженном давлении; добавляли воду и дихлорметан и разделяли слои. Водный слой дополнительно экстрагировали дихлорметаном (2х). Объединенные органические экстракты промывали солевым раствором (1х), затем высушивали и концентрировали. Очищали с помощью радиальной хроматографии с элюированием смесью 1:1 дихлорметан/пентан с получением 3-формилбифенил-4-ил-трифторметансульфоната (143 мг, 86%) в виде прозрачного бесцветного масла. 1Н ЯМР (200 МГц, CDCl3) δ 10,32 (s, 1Н); 8,17 (d, 1Н, J=2,4 Гц); 7,89 (dd, 1H, J=8,6, 2,5 Гц); 7,63-7,36 (m, 6Н). 13С ЯМР (125 МГц, CDCL3) δ 186,5, 149,1, 142,3, 138,0, 134,1, 129,2, 129,1, 128,8, 128,6, 127,2, 122,9, 118,7 (q, JCF-=320,9 Гц). 19F ЯМР(188 МГц, CDCl3) δ -73,2. EIMS: масса/заряд 330 [М]+. HRMS рассчитанное для C14H9F3O2S 330,0168, обнаруженное 330,0163.
Пример 2 - Синтез Т1, Т2, Т10 и Т18
Синтетический путь, используемый для получения T1, Т2, Т10 и Т18, показан на фигуре 2. Вкратце, проводили реакцию перекрестного сочетания 3-формилбифенил-4-ил-трифторметансульфоната (14) с 3-нитрофенилбороновой кислотой с получением нитротерфенила (17), который затем вводили в реакцию Хорнера-Уодсворта-Эммонса с диэтил(карбамоилметил)фосфонатом (18) с получением терфенилакриламида (19). С помощью гидрогенолиза соединения 19 одновременно восстанавливали олефиновые группы и нитрогруппы с получением 3-(3-амино-[1,1':4',1''-терфенил]-2'-ил)пропанамида (Т18), который затем использовали для получения 3-(3-(метилсульфонамидо)-[1,1':4',1''-терфенил]-2'-ил)пропанамида (Т1) посредством