Фармацевтическая композиция в гелевой лекарственной форме для местного применения на основе n-(2-адамантил)-гексаметиленимина гидрохлорида
Иллюстрации
Показать всеИзобретение относится к химико-фармацевтической промышленности и представляет собой фармацевтическую композицию с противоболевым и противовоспалительным действием в гелевой лекарственной форме для местного применения, которая содержит 2,00-8,00 мас.% N-(2-адамантил)-гексаметиленимина гидрохлорида (гимантана), 1,00-20,00 мас.% гелеобразующего полимера, 0,05-1,00 мас.% консерванта, 1,00-10,00 мас.% усилителя всасывания и 61,00-95,95 мас.% растворителя. Изобретение позволяет повысить эффективность использования гимантана, расширить арсенал противоболевых и противовоспалительных средств местного применения, используемых в терапии заболеваний опорно-двигательной системы и купирования боли, связанной с травмами различного генеза, а также обеспечивает быструю доставку лекарственного вещества в локальную зону и снижает частоту побочных эффектов. 4 з.п. ф-лы, 4 табл., 7 пр.
Реферат
Изобретение относится к медицине, в частности к фармации, и касается создания гелевых лекарственных форм для местного применения на основе известного вещества N-(2-адамантил)-гексаметиленимина гидрохлорида (гимантана). Техническим результатом настоящего изобретения является повышение эффективности использования гимантана и расширение арсенала противоболевых и противовоспалительных средств местного применения, используемых для терапии заболеваний опорно-двигательной системы и купирования боли, связанной с травмами различного генеза, а также обеспечение быстрой доставки лекарственного вещества в локальную зону и снижение частоты побочных эффектов.
Не менее 1-1,5% населения страдает хроническими воспалительными заболеваниями суставов и позвоночника; более 10% - остеоартрозом и более 10% - хроническими болями, связанными с дорсопатиями. Нестероидные противовоспалительные средства (НПВС) при пероральном приеме эффективны для симптоматической терапии боли и воспаления острых и хронических заболеваний опорно-двигательного аппарата (уровень доказательности А). Однако пероральный прием НПВС сопровождается высоким риском развития серьезных побочных эффектов: поражений желудочно-кишечного тракта (ЖКТ), нарушений агрегации тромбоцитов, функции почек, печени и др. (Каратеев А.Е., Яхно Н.Н., Лазебник Л.Б. и др. Применение нестероидных противовоспалительных препаратов. Клинические рекомендации. М.: ИМА-ПРЕСС, 2009, 168 с.). Монотерапия заболеваний опорно-двигательной системы НПВС местного применения эффективна при доказанном снижении частоты побочных эффектов со стороны ЖКТ (Moore R.A., Tramer M.R., Carroll D. et al. Quantitative systematic review of topically applied non-steroidal anti-inflammatory drugs. BMJ. 1998, Vol.316, №7128, 333-338; Evans J.M., McMahon A.D., McGilchrist M.M., et al. Topical non-steroidal antiinflammatory drugs and admission to hospital for upper gastrointestinal bleeding and perforation: a record linkage case-control study. BMJ. 1995, Vol. 311, №6996, 22-26.). Использование местных противовоспалительных и противоболевых средств приобретает все большую актуальность и в связи с их включением в схемы комплексной терапии болевых синдромов с целью снижения доз и кратности приема препаратов системного действия (Васенина Е.Е., Левин О.С. Точка зрения: местные формы нестероидных противовоспалительных препаратов в лечении болевых синдромов. Consilium Medicum. 2014, №9, 45-50).
Известно, что гимантан является соединением, обладающим противопаркинсоническим действием (Патент РФ №1825499), у которого обнаружена выраженная противоболевая и противовоспалительная активность при отсутствии ульцерогенного побочного эффекта (Патент РФ №2559777). Противовоспалительное действие гимантана показано на моделях экссудативного воспаления у мышей и крыс, нейровоспаления у крыс и на модели индуцированной конканавалином А псевдоаллергической реакции у мышей (Патент РФ №2559777; Непоклонов А.В., Таллерова А.В. Изучение противовоспалительной активности нового противопаркинсонического препарата гимантан. Материалы IV съезда фармакологов России «Инновации в современной фармакологии», Казань, 2012 г., с. 139.). Противоболевое действие гимантана выявлено на моделях висцеральной боли и термической соматической боли у мышей; боли у крыс, вызванной переменным электрическим током, и формалиновой боли у крыс (Патент РФ №2559777; Ivanova Е.А., Kapitsa I.G., Valdman Е.А., Voronina Т.А. Comparison of the analgesic activity of antiparkinsonian aminoadamantane derivatives amantadine and hemantane. Advances in Parkinson's Disease. 2016, №3, 50-60).
Механизм противовоспалительного действия гимантана заключается в его способности снижать повышенный уровень провоспалительных цитокинов и продуктов перекисного окисления липидов у мышей и крыс при экспериментальной патологии (Таллерова А.В., Иванова Е.А., Капица И.Г., Коваленко Л.П., Вальдман Е.А., Воронина Т.А. Влияние противопаркинсонического препарата гимантан на уровень цитокинов в эксперименте. Иммунология. 2013, т. 34, №5, 254-257; Иванова Е.А., Капица И.Г., Золотов Н.Н., Вальдман Е.А., Непоклонов А.В., Колясникова К.Н., Воронина Т.А. Влияние гимантана на уровень продуктов перекисного окисления липидов в головном мозге при экспериментальном паркинсоническом синдроме. Фармакокинетика и фамакодинамика. 2016, №3, 9-12). Механизм анальгетической активности препарата обусловлен блокадой ионного канала глутаматных рецепторов NMDA подтипа (Елшанская М.В., Вальдман Е.А., Соболевский А.И., Ходоров Б.И. Взаимодействие потенциального противопаркинсонического средства производного адамантана с ионными каналами глутаматных рецепторов NMDA подтипа. Экспериментальная и клиническая фармакология. 2001, Т. 64, №1, 18-21.) и его способностью ингибировать обратный захват серотонина (Зимин И.А. Изучение роли серотонинергического компонента в механизме действия противопаркинсонического препарата гимантана. Дисс. канд. мед. наук. М.: 2011; 122 с.).
Сущность изобретения заключается в создании фармацевтической композиции в гелевой лекарственной форме для местного применения на основе N-(2-адамантил)-гексаметиленимина гидрохлорида (гимантана), обладающей противоболевым и противовоспалительным действием и пригодной к использованию для купирования болей в суставах и мышцах, а также для уменьшения выраженности воспаления и отечности в тканях, в следующих соотношениях мас.%:
| N-(2-адамантил)-гексаметиленимина гидрохлорида | 2,00-8,00 |
| Гелеобразующий полимер | 1,00-20,00 |
| Консервант | 0,05-1,00 |
| Усилитель всасывания | 1,00-10,00 |
| Растворитель | 61,00-95,95, |
где в качестве гелеобразующего полимера может выступать как минимум одно вещество из следующей группы полимеров: производные целлюлозы (метилцеллюлоза, карбоксиметилцеллюлоза и ее соли, гидроксипропилметилцеллюлоза (ГПМЦ)), производные акриловой кислоты (карбопол), сополимеры полиоксиэтилена и полиоксипропилена (плюроники);
где в качестве консерванта может выступать как минимум одно вещество из следующей группы: парабены (нипагин, нипазол), кислоты и их соли (бензойная кислота, салициловая кислота);
где в качестве усилителя всасывания может выступать как минимум одно вещество из следующей группы: диметилсульфоксид (ДМСО), моноэтиловый эфир диэтиленгликоля, поверхностно-активные вещества (бензалкония хлорид, лаурилсульфат натрия); где в качестве растворителя может выступать одно вещество из следующей группы: вода очищенная, спирт этиловый.
Особенности изготовления предлагаемой фармацевтической композиции и ее фармакологическая активность иллюстрируются следующими примерами.
Пример 1
Предварительно отвешивали растворителя воды очищенной 30,00 г (60 мас. %) и при нагревании на водяной бане вводили консерванты нипагин 0,075 г (0,15 мас.%) и нипазол 0,025 г (0,05 мас. %) при перемешивании до полного растворения, затем остужали при комнатной температуре. В раствор отвешивали усилителя всасывания моноэтиловый эфир диэтиленгликоля 1,00 г (2,0 мас. %). Затем вводили 2,50 г N-(2-адамантил)-гексаметиленимина гидрохлорида (5,0 мас. %), перемешивали до полного растворения. Вводили гелеобразующего полимера ГПМЦ 1,00 г (2 мас. %), доводили полученную смесь водой очищенной (растворитель) до массы 50,00 г. Перемешивали в течение 15 минут, оставляли до образования геля.
Пример 2
Предварительно отвешивали растворителя воды очищенной 60,00 (60 масс. %) г и при нагревании на водяной бане вводили консерванты нипагин 0,15 (0,15 масс. %) г и нипазол 0,05 г (0,05 масс. %) при перемешивании до полного растворения, затем остужали при комнатной температуре. В раствор отвешивали усилителя всасывания ДМСО 8,00 г (8,0 масс. %). Затем вводили 5,00 г N-(2-адамантил)-гексаметиленимина гидрохлорида, перемешивали до полного растворения (5,0 масс. %). Вводили гелеобразующего полимера ГПМЦ 2,00 г, (2,0 масс. %) доводили полученную смесь водой очищенной до массы 100,00 г. Перемешивали в течение 15 минут, оставляли для набухания ГПМЦ и образования геля.
Пример 3
Предварительно отвешивали растворителя воды очищенной 60,00 (60 масс. %) г и при нагревании на водяной бане вводили консерванты нипагин 0,15 г(0,15 масс. %) и нипазол 0,05 г (0,05 масс. %) при перемешивании до полного растворения, затем остужали при комнатной температуре. В раствор отвешивали усилителя всасывания бензалкония хлорид 10,00 г (10,0 масс. %). Затем вводили 5,00 г N-(2-адамантил)-гексаметиленимина гидрохлорида, перемешивали до полного растворения (5,0 масс. %). Вводили гелеобразующего полимера плюроника полоксомера Р407 17,00 г (17,0 масс. %), доводили полученную смесь водой очищенной до массы 100,00 г. Перемешивали в течение 15 минут, оставляли в холодильнике на 12 часов до образования геля.
Пример 4
Предварительно отвешивали растворителя воды очищенной 60,00 (60 масс. %) г и при нагревании на водяной бане вводили консерванты нипагин 0,15 г (0,15 масс. %) и усилитель всасывания бензалкония хлорид 0,05 г (0,05 масс. %) при перемешивании до полного растворения, затем остужали при комнатной температуре. Лаурилсульфатнатрия 5,0 г (5 масс. %) Затем вводили 5,00 г N-(2-адамантил)-гексаметиленимина гидрохлорида (5,0 масс. %), перемешивали до полного растворения. Вводили гелеобразующего полимера карбопола (974Р) 19,00 г (19,0 масс. %), доводили полученную смесь водой очищенной до массы 100,00 г. Перемешивали в течение 15 минут, оставляли в холодильнике на 12 часов до образования геля.
Для проведения экспериментов, описанных в примерах 5, 6, 7, использовали следующие фармацевтические композиции: фармацевтическую композицию серии 070916, изготовленную по примеру 1; фармацевтическую композицию серии 080916, изготовленную по примеру 2; фармацевтическую композицию серии 090916, изготовленную по примеру 3.
Пример 5
Влияние гелевых лекарственных форм гимантана для местного применения на выраженность болевой реакции в формалиновом тесте у крыс.
Противоболевое действие гелевых лекарственных форм гимантана оценивали в формалиновом тесте, позволяющем выявить выраженность противоболевой активности в отношении двух отличающихся по механизму развития фаз боли: ранней острой и поздней тонической. Острая фаза боли развивается сразу после субплантарного введения раствора формалина и характеризуется воздействием формалина на первичные афференты боли, тоническая фаза боли отставлена во времени и вызвана воспалительной реакцией (Il-Ok Lee, You-Seong Jeong. Effects of different concentrations of formalin on paw edema and pain behaviors in rats. JKoreanMedSci, 2002, 17, P. 81-85).
Эксперимент проводили на аутбредных крысах-самцах массой 240-270 г. Крысы были распределены по четырем группам:
1. Контрольная группа, животным которой на лапу наносили гель-плацебо, не содержащий в своем составе гимантана
2. Группа крыс, которым на лапу наносили 5% гелевую форму гимантана серии 070916
3. Группа крыс, которым на лапу наносили 5% гелевую форму гимантана серии 080916
4. Группа крыс, которым на лапу наносили 5% гелевую форму гимантана серии 090916
5% гели гимантана серий 070916, 080916, 090916 и гель-плацебо наносили на правую заднюю лапу крыс за 1 час до индукции формалиновой боли. Формалиновая боль моделировалась путем субплантарного введения крысам 100 мкл 2% раствора формалина (Воронина Т.А., Гузеватых Л.С. Методические рекомендации по изучению анальгетической активности лекарственных средств. Руководство по проведению доклинических исследований лекарственных средств. Часть первая. М.: Гриф и К, 2012. С. 197-218). Регистрировали изменение поведения животных, по времени соответствующее двум фазам болевой реакции, - ранней острой фазе болевой реакции, которая длится на протяжении первых 5 минут теста, и поздней тонической фазе болевой реакции, которая регистрируется с 20 по 60 минуты опыта (Il-Ok Lee, You-Seong Jeong. Effects of different concentrations of formalin on paw edema and pain behaviors in rats. JKoreanMedSci 2002, 17, P. 81-85). Каждые 5 минут в течение обеих фаз боли в баллах регистрировали 4 типа поведенческих реакций:
0 - отсутствие реакции;
1 - лапа остается на земле, но животное на нее не опирается;
2 - лапа поднята;
3 - лапа облизывается, грызется или встряхивается.
Также для каждой группы подсчитывали сумму баллов в острую и тоническую фазу боли. Критерием анальгетического эффекта считали уменьшение числа болевых реакций в получавших гелевые лекарственные формы гимантана группах крыс относительно контрольной группы.
Статистическая обработка проводилась с помощью программы Statistica 10.0. Так как болевая реакция регистрировалась в баллах, то при статистической обработке данных использовался метод непараметрической статистики - критерий Манна-Уитни. Данные в таблицах представлены как медиана, 25%-75%. Различия между группами считали достоверными при р≤0,05.
Результаты
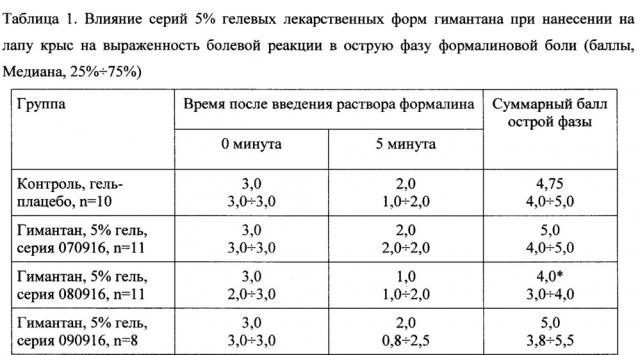
Влияние гелевых лекарственных форм гимантана на острую фазу боли. Во всех экспериментальных группах в момент введения раствора формалина (0 минута) свидетельствующее о боли поведение животных характеризовалось максимальным баллом, который снижался к 5 минуте острой фазы боли. Хотя достоверных различий между группами на 5 минуте после введения альгогена и не наблюдалось, минимальное значение медианы болевой реакции было зарегистрировано в группе крыс, которым на лапу наносили 5% гель гимантана серии 080916. Благодаря этому суммарный балл болевых реакций в группе животных, получавших 5% гель гимантана серии 080916, был на 15,8% достоверно ниже суммарного балла болевых реакций в контрольной группе, что свидетельствует о том, что препарат в этой лекарственной форме оказывает противоболевое действие в отношении острой фазы формалиновой боли (Табл. 1).
5% гели гимантана серий 070916 и 090916 влияния на суммарный балл болевых реакций в острую фазу формалиновой боли не оказывали (Табл. 1).
* - р<0,05, достоверность отличий по сравнению с группой «Контроль, гель-плацебо», критерий Манна-Уитни
Влияние гелевых лекарственных форм гимантана на тоническую фазу боли
Свидетельствующее о боли поведение животных контрольной группы в тоническую фазу формалиновой боли характеризовалось 2 (20, 30-60 минуты опыта) и 3 баллами (25 минута опыта), медиана суммарного балла болевой реакции тонической фазы в контрольной группе составила 20 баллов (Табл. 2).
5% гели гимантана серий 080916 и 090916 достоверно снижали медиану суммарного балла болевой реакции тонической фазы формалиновой боли соответственно на 25% и 30% по сравнению с контрольной группой. При этом гель гимантана серии 080916 достоверно уменьшал выраженность свидетельствующего о боли поведения животных через 45 минут после введения раствора формалина и на уровне статистической тенденции (р≤0,1) - через 35 и 55 минут. Гель гимантана серии 090916 снижал выраженность болевой реакции на уровне статистической тенденции (р≤0,1) на 25, 35 и 45 минутах и достоверно - на 50 минуте эксперимента (Табл. 2).
5% гель гимантана серии 070916 обнаружил наименее выраженное противоболевое действие, снижая медиану суммарного балла болевой реакции тонической фазы формалиновой боли на уровне статистической тенденции (р≤0,1) на 20%. В отдельные временные интервалы тонической фазы формалиновой боли эта лекарственная форма гимантана статистически значимо выраженность болевого поведения животных не уменьшала (Табл. 2).
* - р<0,05 - достоверность отличий по сравнению с группой «Контроль, гель-плацебо», критерий Манна-Уитни
# - р<0,1 - статистическая тенденция по сравнению с группой «Контроль, гель-плацебо», критерий Манна-Уитни
Таким образом, результаты эксперимента по оценке противоболевого действия трех гелевых лекарственных форм гимантана свидетельствуют о том, что все изучаемые лекарственные формы уменьшают выраженность болевой реакции в формалиновом тесте у крыс.5% гели гимантана серий 070916 и 090916 снижают проявления свидетельствующего о боли поведения животных в тоническую фазу формалиновой боли. Противоболевое действие 5% геля гимантана серии 080916 более выражено, так как данная лекарственная форма обладает способностью уменьшать боль как в острую фазу, связанную с влиянием формалина на первичные афференты боли, так и в тоническую фазу формалиновой боли, развивающейся вследствие воспаления. При этом противоболевая активность 5% геля гимантана серии 080916 более выражена и по сравнению с активностью субстанции гимантана при ее внутрибрюшинном введении в дозе 20 мг/кг, так как при введении внутрибрюшинно препарат снижает выраженность только тонической фазы формалиновой боли, не влияя на острую фазу (Ivanova Е.А., Kapitsa I.G., Valdman Е.А., Voronina Т.А. Comparison of the analgesic activity of antiparkinsonian aminoadamantane derivatives amantadine and hemantane. Advances in Parkinson's Disease. 2016. №3. P. 50-60).
Пример 6
Влияние гелевых лекарственных форм гимантана на выраженность экссудативного воспаления в тесте формалинового отека лапы у крыс.
Эксперимент проводили на аутбредных крысах-самцах массой 240-270 г. Крысы были распределены по четырем группам:
1. Контрольная группа, животным которой на лапу наносили гель-плацебо
2. Группа крыс, которым на лапу наносили 5% гелевую форму гимантана серии 070916
3. Группа крыс, которым на лапу наносили 5% гелевую форму гимантана серии 080916
4. Группа крыс, которым на лапу наносили 5% гелевую форму гимантана серии 090916
5% гели гимантана серий 070916, 080916, 090916 и гель-плацебо наносили на правую заднюю лапу крыс за 1 час до субплантарного введения 100 мкл 2% раствора формалина в правую заднюю лапу крыс.
На фоне субплантарного введения раствора формалина у животных развивается отек лапы, выраженность которого максимальна через 4 часа после инъекции (JHBrown, JWKissel, PMLish. Studies on the acute inflammatory response. I. Involvement of the central nervous system in certain models of inflammation. J Pharmacol Exp Ther 1968; 160: 231-42; 10 Lee, G. Crosby. Halothane effect on formalin-induced paw edema and flinching in rats. JKoreanMedSci 1999; 14: 34-8.). Поэтому через 4 часа после индукции воспаления оценивали степень отечности лап животных. Отек лапы регистрировали по разнице диаметра лапы (миллиметры), измеренного штангенциркулем, через 4 часа после индукции воспаления относительно диаметра лапы до индукции воспаления. Противовоспалительный эффект оценивали по уменьшению отека у крыс на фоне изучаемых гелевых лекарственных форм гимантана относительно показателя контрольной группы.
Статистическая обработка проводилась с помощью программы Statistica 10.0. Нормальность распределения проверяли с помощью критерия Шапиро-Уилка с последующей оценкой равенства дисперсий по критерию Левена. Так как распределение в группах было нормальным, и равенство дисперсий Левена соблюдалось, то использовали метод параметрической статистики - t-критерий Стьюдента. Данные в таблицах представлены как среднее ± стандартная ошибка среднего (СОС), стандартное отклонение (СО). Различия между группами считали достоверными при р≤0,05.
Результаты
Субплантарное введение раствора формалина приводило к развитию отека лапы крыс, выраженность которого через 4 часа после инъекции соответствовала увеличению диаметра лапы на 1,83 мм в контрольной группе животных (Табл. 3).
* - р<0,05 - достоверность отличий по сравнению с группой «Контроль, гель-плацебо», t-критерий Стьюдента
# - р=0,112, статистическая тенденция по сравнению с группой «Контроль, гель-плацебо», t-критерий Стьюдента
5% гели гимантана серий 070916 и 080916 достоверно снижали экссудативную реакцию, уменьшая выраженность отека лапы крыс соответственно на 53,0% и 44,3% по сравнению с контрольной группой (Табл. 3). 5% гель гимантана серии 090916 снижал выраженность воспалительной реакции у крыс на уровне статистической тенденции на 30,6% (р=0,112).
Таким образом, все изучаемые гелевые лекарственные формы гимантана серий 070916, 080916, 090916 снижают выраженность воспалительной реакции в тесте формалинового отека у крыс.
Пример 7
Влияние гелевых лекарственных форм гимантана на выраженность экссудативного воспаления в тесте каррагенанового отека лапы у крыс.
Эксперимент проводили на аутбредных крысах-самцах массой 240-270 г. Крысы были распределены по четырем группам:
1. Контрольная группа, животным которой на лапу не наносили гелевые лекарственные формы гимантана.
2. Группа крыс, которым на лапу наносили 5% гелевую форму гимантана серии 070916.
3. Группа крыс, которым на лапу наносили 5% гелевую форму гимантана серии 080916.
5% гели гимантана серий 070916 и 080916 наносили на правую заднюю лапу крыс за 1 час до субплантарного введения 100 мкл 1% раствора каррагенана в правую заднюю лапу крыс. Субплантарное введение 0,1 мл 1% раствора каррагенана (сульфатированного полисахарида из ирландского морского мха) воспроизводит острую воспалительную реакцию - отек лапы (Winter С., Risley Е., Nuss G. Proc. Soc. Exp. Biol. Med., 1962. - Vol. 111. - P. 544). Выраженность отека лапы регистрировали в динамике по разнице диаметра лапы (миллиметры), измеренного штангенциркулем, через 1, 2, 3 и 4 часа после индукции воспаления относительно диаметра лапы до индукции воспаления. Противовоспалительный эффект оценивали по уменьшению отека у крыс на фоне изучаемых гелевых лекарственных форм гимантана относительно соответствующих показателей контрольной группы.
Статистическая обработка проводилась с помощью программы Statistica 10.0. Нормальность распределения проверяли с помощью критерия Шапиро-Уилка с последующей оценкой равенства дисперсий по критерию Левена. Так как распределение в группах отличалось от нормального, и не соблюдалось межгрупповое равенство дисперсий, использовался метод непараметрической статистики - критерий Манна-Уитни. Данные в таблицах представлены как медиана, 25%-75%. Различия между группами считали достоверными при р<0,05.
Результаты
Субплантарное введение 1% раствора каррагенана вызывало развитие острой экссудативной реакции, выраженность которой была максимальна через 2 часа после введения флогогена (Табл. 4).
* - р<0,05 по сравнению с контрольной группой, критерий Манна-Уитни
# - р≤0,1, статистическая тенденция по сравнению с контрольной группой, критерий Манна-Уитни
5% гель гимантана серии 080916 снижал выраженность воспалительной реакции у крыс. Достоверное уменьшение отечности лап животных на фоне изучаемой лекарственной формы наблюдалось через 2 и 4 часа после введения раствора каррагенана. Через 2 часа после введения раствора каррагенана отечность лап крыс была на 27,7% меньше, чем в контрольной группе, а через 4 часа выраженность воспалительной реакции снижалась в 2 раза по сравнению с контрольной группой. Через 1 и 3 часа после индукции воспаления выраженность отека лап животных, получавших 5% гель гимантана серии 080916, снижалась на уровне статистической тенденции (р≤0,1), соответственно, на 24,8% и 10,5% (Табл. 4).
5% гель гимантана серии 070916 проявил способность снижать выраженность воспалительной реакции только через 4 часа после введения раствора каррагенана, достоверно уменьшая отечность лап крыс на 18,2% по сравнению с контрольной группой (Табл. 4).
Таким образом, результаты проведенного эксперимента показали, что 5% гелевые лекарственные формы гимантана серий 070916 и 080916 проявляют противовоспалительную активность в тесте каррагенанового отека лапы у крыс. При этом наиболее выраженный эффект зарегистрирован на фоне 5% геля гимантана серии 080916, снижавшего выраженность отечности на протяжении всего опыта. 5% гель гимантана серии 070916 проявлял противовоспалительную активность только через 4 часа после индукции воспаления.
Список литературы
1. Васенина Е.Е., Левин О.С. Точка зрения: местные формы нестероидных противовоспалительных препаратов в лечении болевых синдромов. Consilium Medicum. 2014, №9, 45-50.
2. Воронина Т.А., Гузеватых Л.С. Методические рекомендации по изучению анальгетической активности лекарственных средств. Руководство по проведению доклинических исследований лекарственных средств. Часть первая. М.: Гриф и К, 2012. С.197-218.
3. Елшанская М.В., Вальдман Е.А., Соболевский А.И., Ходоров Б.И. Взаимодействие потенциального противопаркинсонического средства производного адамантана с ионными каналами глутаматных рецепторов NMDA подтипа. Экспериментальная и клиническая фармакология. 2001, Т.64, №1,18-21.
4. Зимин И.А. Изучение роли серотонинергического компонента в механизме действия противопаркинсонического препарата гимантана. Дисс. канд. мед. наук. М.:2011; 122 с.
5. Иванова Е.А., Капица И.Г., Золотов Н.Н., Вальдман Е.А., Непоклонов А.В., Колясникова К.Н., Воронина Т.А. Влияние гимантана на уровень продуктов перекисного окисления липидов в головном мозге при экспериментальном паркинсоническом синдроме. Фармакокинетика и фамакодинамика. 2016, №3, 9-12.
6. Каратеев А.Е., Яхно Н.Н., Лазебник Л.Б. и др. Применение нестероидных противовоспалительных препаратов. Клинические рекомендации. М.: ИМА-ПРЕСС, 2009, 168 с.
7. Непоклонов А.В., Таллерова А.В. Изучение противовоспалительной активности нового противопаркинсонического препарата гимантан. Материалы IV съезда фармакологов России «Инновации в современной фармакологии», Казань, 2012 г, С. 139.
8. Патент РФ №1825499.
9. Патент РФ №2559777.
10. Таллерова А.В., Иванова Е.А., Капица И.Г., Коваленко Л.П., Вальдман Е.А., Воронина Т.А. Влияние противопаркинсонического препарата гимантан на уровень цитокинов в эксперименте. Иммунология. 2013, Т. 34, №5, 254-257.
11. Evans J.M., McMahon A.D., McGilchrist М.М., et al. Topical non-steroidal antiinflammatory drugs and admission to hospital for upper gastrointestinal bleeding and perforation: a record linkage case-control study. BMJ. 1995, Vol. 311, №6996, 22-26.
12. Il-Ok Lee, You-Seong Jeong. Effects of different concentrations of formalin on paw edema and pain behaviors in rats. JKoreanMedSci 2002, 17, P. 81-85
13. Ivanova E.A., Kapitsa I.G., Valdman E.A., Voronina T.A. Comparison of the analgesic activity of antiparkinsonian aminoadamantane derivatives amantadine and hemantane. Advances in Parkinson's Disease. 2016, №3, 50-60.
14. Moore R.A., Tramer M.R., Carroll D. et al. Quantitative systematic review of topically applied non-steroidal anti-inflammatory drugs. BMJ. 1998, Vol.316, №7128, 333-338.
15. Winter C., Risley E., Nuss G. Proc. Soc. Exp. Biol. Med., 1962. - Vol. 111. - P. 544.
1. Фармацевтическая композиция, выполненная в гелевой лекарственной форме для местного применения, обладающая противоболевым и противовоспалительным действием, на основе N-(2-адамантил)-гексаметиленимина гидрохлорида, также содержащая фармацевтически приемлемые компоненты в следующих соотношениях, мас.%:
| N-(2-адамантил)-гексаметиленимина гидрохлорид | 2,00-8,00 |
| Гелеобразующий полимер | 1,00-20,00 |
| Консервант | 0,05-1,00 |
| Усилитель всасывания | 1,00-10,00 |
| Растворитель | 61,00-95,95 |
2. Фармацевтическая композиция по п. 1, отличающаяся тем, что в качестве гелеобразующего полимера может выступать как минимум одно вещество из следующей группы полимеров: производные целлюлозы (метилцеллюлоза, карбоксиметилцеллюлоза и ее соли, гидроксипропилметилцеллюлоза (ГПМЦ)), производные акриловой кислоты (карбопол), сополимеры полиоксиэтилена и полиоксипропилена (плюроники).
3. Фармацевтическая композиция по п. 1, отличающаяся тем, что в качестве консерванта может выступать как минимум одно вещество из следующей группы: парабены (нипагин, нипазол), кислоты и их соли (бензойная кислота, салициловая кислота).
4. Фармацевтическая композиция по п. 1, отличающаяся тем, что в качестве усилителя всасывания может выступать как минимум одно вещество из следующей группы: диметилсульфоксид (ДМСО), моноэтиловый эфир диэтиленгликоля, поверхностно-активные вещества (бензалкония хлорид, лаурилсульфат натрия).
5. Фармацевтическая композиция по п. 1, отличающаяся тем, что в качестве растворителя может выступать как минимум одно вещество из следующей группы: вода очищенная, спирт этиловый.