Способ получения 6-метиленгидрокортизона или его эфиров из 21-ацетата гидрокортизона
Иллюстрации
Показать всеИзобретение относится к способу получения 6-метиленгидрокортизона (11β,17α,21-тригидрокси-6-метиленпрегн-4-ен-3,20-диона) или его эфиров общей формулы I
в которой R=COCF3 или Н; R1=СОСН3 или Н, из 21-ацетата гидрокортизона формулы II, последовательностью превращений, включающей защиту 11β-гидроксильной группы этерификацией производным трифторуксусной кислоты в среде апротонного растворителя в условиях основного катализа с использованием эффективного количества катализатора с образованием 21-ацетокси-17α-гидрокси-11β-трифторацетилоксипрегн-4-ен-3,20-диона формулы III, енолэтерификацию Δ4-3-кетосистемы полученного соединения действием триалкилортоформиата в присутствии кислого катализатора с образованием 3-алкоксиэфира Δ3,5-3-гидроксипроизводного общей формулы IV, конденсацию его с реагентом, полученным из формальдегида и вторичного амина, в присутствии кислого катализатора с образованием смеси 6α- и 6β-изомеров 6-(N-метил-Т-фенил)-аминометилпроизводного общей формулы V, расщепление полученной смеси стероидных оснований Манниха по связи C-N действием протонной минеральной кислоты в присутствии солей галогеноводородной кислоты и удаление защитных группировок 11β- и 21-гидроксильных групп полностью или частично. Технический результат: разработан простой способ получения соединения общей формулы I из 21-ацетата гидрокортизона с выходом целевых продуктов не менее 80%. 55 з. п. ф-лы, 11 пр.
Реферат
Область техники
Настоящее изобретение относится к области органического синтеза, конкретно касается получения стероидных соединений (кортикостероидов), таких как 6-метиленгидрокортизон или его эфиры, и может быть использовано в химической и фармацевтической отраслях промышленности, а также в промышленной биотехнологии для производства стероидных медицинских препаратов.
Уровень техники
6-Метиленгидрокортизон является промежуточным соединением в синтезе 6α-метилгидрокортизона (CAS №1625-39-4) и 6α-метилпреднизолона (CAS №83-43-2), а также 6-дегидро-6-метилгидрокортизона (CAS №85310-39-0) и 6-дегидро-6-метилпреднизолона (CAS №95810-22-3), из гидрокортизона (CAS №50-23-7) или 21-ацетата гидрокортизона (CAS №50-03-3).
Полученные в соответствии с предлагаемым способом 6-метиленгидрокортизон и его эфиры (11-трифторацетат 6-метиленгидрокортизона, 21-ацетат 6-метилен-гидрокортизона и 11-трифторацетат 21-ацетата 6-метиленгидрокортизона) не только служат исходными субстратами для дальнейшего превращения в 6α-метилгидрокортизон и 6α-метилпреднизолон (химическим и комбинированным химико-биотехнологическим способами соответственно), но также могут быть использованы для получения 6-дегидро-6-метилгидрокортизона и 6-дегидро-6-метилпреднизолона (соответственно химическим и комбинированным химико-биотехнологическим или химическим способами).
Введение метиленовой группы в положение С6 молекулы гидрокортизона или 21-ацетата гидрокортизона является ключевой стадией известных способов получения 6α-метилгидрокортизона - синтетического прекурсора 6α-метилпреднизолона.
Введение С6-метиленовой группы осуществляют различными методами, используя формальдегид или его производные как метиленирующие агенты. Однако все способы предусматривают обязательную предварительную енолизацию α,β-ненасыщенного кетона кольца А, необходимую для поляризации системы двойных связей с образованием нуклеофильного атома углерода С6, с последующим замещением атома водорода при С6 на формильную или метиленовую группу и различаются тем, что в одних случаях образованный промежуточный 3,5-диенол выделяют в виде эфира [D. Burn et al., Tetrahedron, 1965, 21(6), 1619-1624] или 3,5-диенамина [F. Schneider et al., Helv. Chim. Acta, 1973, 56(7), 2396-2404], в других же случаях енолизация проводится in situ без выделения промежуточного продукта [DE 4121484, 1993].
Наиболее привлекательными являются методы так называемой прямой конденсации с формальдегидом или его производными. Это метод прямого γ-метиленирования, предложенный Анненом и соавт. [US 4322349, 1982; Synthesis, 1982, №1, p. 34-40; ЕР 0100874, 1984; ЕР 0149222, 1985], и метод конденсации с реагентом Манниха [R. Bohlmann et al, DE 4121484, 1993].
Метод прямого γ-метиленирования заключается во взаимодействии стероида с производными формальдегида (такими как диметилацеталь, диэтилацеталь формальдегида или метоксиметилацетат) в хлорсодержащих растворителях при температуре кипения в присутствии избытка хлорокиси фосфора и ацетата натрия. Однако этот метод непригоден для метиленирования соединений, содержащих незащищенную 11β-гидроксильную группу. Так, при прямом γ-метиленировании 21-ацетата гидрокортизона выход 6-метиленпроизводного составляет всего лишь 18% [Synthesis, 1982, №1, р. 34-40, Таблица 1, соединение 6n].
Известно также, что енолэтерификация Δ4-3-кетосистемы кольца А стероидов, катализируемая п-толуолсульфокислотой (п-ТСК), в присутствии незащищенной 11β-гидроксильной группы может сопровождаться нежелательной реакцией ее элиминирования с образованием Δ9(11)-связи [Zhao Q. et al. Synth. Commun., 1993, 23(10), 1473-1478]. Поэтому для сохранения 11β-гидроксильной группы необходима ее защита.
Известно, что для защиты 11β-гидроксигруппы ее обычно этерифицируют, превращая в тригалогенацетат (в частности трифторацетат) или триметилсилиловый эфир. Эти защиты считаются наиболее приемлемыми, так как не только легко образуются, но и легко удаляются. Применение для защиты 11β-гидроксигруппы метода этерификации ангидридами низших кислот возможно, однако ограничено из-за проблем, возникающих при их последующем удалении химическими методами сольволиза.
Способы применения трифторацетатной защиты 11β-гидроксильной группы молекулы 21-ацетата гидрокортизона (II) известны. Это способ, описанный в патенте [US 4330541, 1982, пример 1], который заключается в том, что реакцию этерификации 5 г 21-ацетата гидрокортизона проводят в среде пиридина действием трифторуксусного ангидрида при температуре минус 15°С. Далее смесь выливают в водный раствор хлорида натрия, отфильтрованный осадок растворяют в дихлорметане, органический раствор промывают водой, осушают сульфатом натрия и упаривают досуха. Получают 5.1 г (82,4%) остатка, содержащего 11-трифторацетокси-производное (III) 21-ацетата гидрокортизона (II). Однако это соединение не охарактеризовано, так как содержащий его остаток без очистки и выделения кристаллического продукта использован авторами патента на следующей стадии химического синтеза.
Другие патенты [DE 1112511, 1961 (пример 16) и DE 1125422, 1962 (пример 15)] описывают способ получения 11-трифторацетокси-производного (III) из 21-ацетата гидрокортизона (II) действием трифторуксусного ангидрида в среде абсолютного диоксана. После 18 ч выдержки при комнатной температуре реакционную смесь выливают на ледяную воду. Далее продукт экстрагируют, экстракт промывают водой, упаривают досуха в вакууме. После кристаллизации остатка в эфире и хроматографирования на окиси алюминия получают 11-трифторацетокси-производное (III) 21-ацетата гидрокортизона (II), выход которого не указан. Продукт охарактеризован: т.пл. 206-207°С, [α]D +165,7° (хлф); λmax 238-240 mμ. Спектральная характеристика отсутствует.
Получение метилового 3,5-диенолэфира 11-трифторацетокси-производного 21-ацетата гидрокортизона - соединение IVa - в литературных источниках не описано.
Получение этилового 3,5-диенолэфира 11-трифторацетокси-производного 21-ацетата гидрокортизона - соединение IVb - описано в патентах [DE 1112511, 1961 (пример 16) и DE 1125422, 1962 (пример 15)] и заключается в реакции соединения III с этилортоформиатом в среде диоксана в присутствии п-ТСК при комнатной температуре. После окончания реакции смесь выливают в воду и экстрагируют дихлорметаном. Экстракт промывают водой, осушают сульфатом натрия и упаривают досуха. Маслянистый остаток, содержащий соединение IVb, выход которого не указан, охарактеризован: [α]D ±0° (хлф); λmax 240-242 mμ, logε 4,15. Соединение IVb не было выделено авторами в кристаллическом виде. Спектральная характеристика, отсутствует, температура плавления не определена.
6-Аминометильные производные общей формулы V являются новыми соединениями, в литературе не описаны.
6-Метилен-производное 11-трифторацетокси-производного 21-ацетата гидрокортизона - соединение VI - является новым соединением, в литературе не описано.
6-Метилен-производное 11-трифторацетата гидрокортизона - соединение VII - известно. Так, известен способ получения 11-трифторацетата 6-метиленгидрокортизона (VII), описанный в патенте [RU 2337918, 2008, пример 14]. Однако соединение VII получено другим способом из другого соединения, а именно из 11β-трифторацетилокси-17α,20;20,21-бисметилендиокси-6-метиленпрегн-4-ен-3,20-диона удалением бисметиленовой защиты диоксиацетоновой боковой цепи в среде уксусной кислоты при температуре 0-2°С действием концентрированной соляной кислоты (на 5 г стероида используют 20 мл уксусной кислоты и 75 мл соляной кислоты).
Соединение VIII - 21-ацетокси-11β,17α-дигидрокси-6-метиленпрегн-4-ен-3,20-дион (21-ацетат 6-метиленгидрокортизона) - известно.
Известен способ получения 21-ацетата 6-метиленгидрокортизона из 21-ацетокси-11β,17α-дигидрокси-6-гидроксиметил-3-метокси-прегна-3,5-диен-20-она [US 3112305, 1963, пример 43], согласно которому 500 мг указанного исходного соединения нагревают при 80°С в 3 мл 95% водной уксусной кислоты в течение 10 мин., затем осаждают продукт водой и кристаллизуют из смеси ацетон-гексан. Получают 21-ацетат 6-метиленгидрокортизона, выход которого не указан.
Известен способ получения 21-ацетата 6-метиленгидрокортизона [D. Burn, J.P. Yardley, and V. Petrow, Tetrahedron, 1969, Vol. 25. p. I I55-1158], согласно которому к смеси 21-ацетокси-6-формил-3-метокси-3,5-прегнадиен-11β,17α-диол-20-она (3.6 г) и NaOAc (3.6 г) в метаноле (100 мл) добавляют Pt/C (1.25 г) в метаноле (25 мл) и смесь гидрируют до поглощения 180 мл (1 моль-экв.) водорода. Затем катализатор удаляют фильтрацией, растворитель упаривают при пониженном давлении, остаток распределяют между хлороформом и водой. Органическую фазу отделяют и добавляют п-ТСК (0.2 г) в метаноле (10 мл); после выдерживания в течение 15 мин. при комнатной температуре реакционный раствор промывают водным раствором Na2CO3, затем водой, сушат (Na2SO4) и упаривают при пониженном давлении. Кристаллизацией и осаждением из смеси хлороформа и диизопропилового эфира получают 6-метиленпроизводное (1.8 г) с т.пл. 206-207°С (выход 53.4%).
Также известен способ получения 21-ацетата 6-метиленгидрокортизона из 21-ацетата гидрокортизона [DE 4121484, 1993, пример 2], который заключается во введении метиленовой группы в положение С6 молекулы 21-ацетата гидрокортизона. Согласно описанию этого способа 5 г 21-ацетата гидрокортизона (II) суспендируют в смеси 50 мл тетрагидрофурана, 15 мл триэтилортоформиата и 15 мл этанола, добавляют 500 мг тозилата пиридиния и перемешивают в течение 1 ч при температуре 40°С в бане. Затем добавляют 5,5 мл N-метиланилина и 6,5 мл 40% раствора формальдегида и перемешивают не менее часа при температуре 40°С. После этого реакционную массу обрабатывают ледяной водой, содержащей винную кислоту и хлорид натрия, экстрагируют дихлорметаном, промывают раствором бикарбоната натрия и хлорида натрия, осушают сульфатом натрия и упаривают в вакууме досуха. Полученный остаток (5,8 г) хроматографируют на 600 г кизельгеля, элюируя смесью гексан-этилацетат, и получают 2,1 г (40,8%) 6-метилен-производного 21-ацетата гидрокортизона.
Недостатками описанного в [DE 4121484, 1993] процесса являются:
- применение для очистки 21-ацетата 6-метилен-гидрокортизона хроматографии, существенно усложняющей технологический процесс;
- низкий выход продукта 21-ацетата 6-метиленгидрокортизона (40,8%) на стадии метиленирования, который можно объяснить, во-первых, наличием побочных реакций с участием незащищенной гидроксильной группы при С11, и, во-вторых, низкой регионаправленностью реакции расщепления стероидного основания Манниха. Вероятно, что в описанных условиях реакции дезаминирования (расщепление по связи C-N) сопутствует побочный процесс дезаминометилирования (расщепление по связи С-С) с регенерацией 21 -ацетата гидрокортизона. Поэтому хроматографическая очистка продукта становится необходимой.
Способы получения 6-метиленгидрокортизона (I) известны. Так, известен способ получения 6-экзометилен-4-прегнен-11β,17α,21-триол-3,20-диона и его 21-ацетата [US 3090781, 1963 (пример 8); US 3074935, 1963 (пример 8)], согласно которому суспензию 0,26 г 6-экзометилен-17α,20:20,21-бис-метилендиокси-4-прегнен-11β-ол-3-она в 8-кратном количестве 60% водной муравьиной кислоты нагревают на паровой бане в течение 20 мин; полученный раствор охлаждают, выливают в ледяную воду и экстрагируют хлороформом. Органическую фазу промывают водным раствором бикарбоната натрия, сушат и концентрируют в вакууме. После кристаллизации из этилацетата получают 30 мг 6-экзометилен-4-прегнен-11β,17α,21-триол-3,20-диона с т.пл. 203°С. Некристаллизующийся материал (175 мг), полученный после отделения 30 мг 6-метиленгидрокортизона, обрабатывают 1N раствором метоксида натрия в метаноле при комнатной температуре в атмосфере азота для расщепления различных эфиров муравьиной кислоты, реакционную массу нейтрализуют уксусной кислотой, выливают в воду, экстрагируют хлороформом, хлороформную фазу промывают водой, упаривают досуха. 6-Экзометилен-4-прегнен-11β,17α,21-триол-3,20-дион, содержащийся в остатке, подвергают ацетилированию в пиридине действием уксусного ангидрида. Для этого к остатку добавляют 2,1-кратное количество пиридина и 2-кратное количество уксусного ангидрида, смесь выдерживают в течение ночи при комнатной температуре. После выливания реакционной массы на воду, экстракции хлороформом, упаривания досуха и хроматографирования на окиси алюминия получают 42 мг 6-экзометилен-4-прегнен-11β,17α,21-триол-3,20-диона-21-ацетата, т.пл. которого после перекристаллизации из этилацетата составляет 199-204°С. Таким образом, суммарный молярный выход продуктов (6-метиленгидрокортизона (I) и его 21-ацетата (VIII) не превышает 29%.
Наиболее близким по сущности к предложенному способу получения 6-метиленгидрокортизона является способ [RU 2297423, 2007, примеры 3 (вариант 2) и 4], который заключается во введении метиленовой группы в положение С6 молекулы 11β,17α,21-триалканоилокси-прегн-4-ен-3,20-диона. Согласно описанию этого способа (пример 3, вариант 2) к раствору 10 г 11,17,21-триацетата гидрокортизона в 75 мл тетрагидрофурана добавляют 10 мл этанола, 10 мл триэтилортоформиата, 130 мг п-ТСК и нагревают до 40°С. Реакционную массу выдерживают в течение 1 ч и добавляют дополнительно 130 мг п-ТСК. После перемешивания в течение еще 1 ч при температуре 40°С добавляют 4,3 мл N-метиланилина и 3-6 мл водного 37% раствора формальдегида. Реакционную массу выдерживают в течение 2 ч, затем охлаждают до комнатной температуры, добавляют 25 мл концентрированной соляной кислоты и перемешивают 30 мин. Смесь экстрагируют хлористым метиленом, органический слой промывают водой до нейтральной реакции, растворитель упаривают. После кристаллизации получают 9,4 г 11β,17α,21-триацетокси-6-метиленпрегн-4-ен-3,20-диона с выходом 92%. По примеру 4 этого способа в аналогичных условиях из 1 г 21-ацетокси-11β,17α-бис(трифторацетилокси)-прегн-4-ен-3,20-диона получают 0,93 г 6-метилен-производного с выходом 91%.
Основным недостатком указанного способа является необходимость обязательной защиты всех гидроксильных групп, имеющихся в структуре молекулы гидрокортизона с последующим удалением защит. Так, при применении для защиты метода исчерпывающего ацетилирования, несмотря на высокие постадийные выходы при получении 11β,17α,21-триацетокси-6α-метилпрегн-4-ен-3,20-диона и 21-ацетокси-11β,17α-бис(трифторацетилокси)-прегн-4-ен-3,20-диона, эффективное удаление сложноэфирной защиты с регенерацией 11β-гидроксильной группы возможно только с применением биотехнологического метода [RU 2297423, 2007, пример 8], а именно микробиологической трансформацией 11β,17α,21-триацетокси-6-метиленгидрокортизона (вариант 1) или 21-ацетокси-11β,17α-бис(трифторацетилокси)-прегн-4-ен-3,20-диона (вариант 2) клетками бактерий Arthrobacter mediolanus ВКМ-1388, который осуществляется в 2 этапа (энзиматическое удаление защиты 11β-гидроксильной группы и гидролиз защиты 17α-гидроксильной группы действием 10% раствора гидроксида натрия) с общей продолжительностью процесса дезацилирования 72 ч. При этом сложноэфирная защита гидроксильной группы при С21 может частично сниматься на биотехнологическом этапе, а щелочной гидролиз защиты 17α-гидроксильной группы протекает путем ацильной миграции с первоочередным удалением ацетильной защиты гидроксила при С21. Это существенно усложняет способ.
Раскрытие изобретения
Технической задачей в заявленном изобретении является разработка более простого способа получения 6-метиленгидрокортизона или его эфиров из 21-ацетата гидрокортизона при обеспечении выхода целевых продуктов не менее чем 80%.
Упрощение способа обеспечивается 1) за счет проведения последовательных реакций функционализации положения С6 молекулы 11-трифторацетокси-производного 21-ацетата гидрокортизона (III) с образованием 21-ацетокси-11-трифторацетилокси-6-метилен-гидрокортизона (VI) при температуре окружающей среды (т.е. при комнатной температуре) без применения нагрева реакционных масс; 2) за счет проведения непрерывного технологического процесса функционализации положения С6 молекулы 11-трифторацетата 21-ацетата гидрокортизона (III) без выделения интермедиатов IV и V целевого продукта (VI) на ключевых стадиях синтеза и исключения тем самым не только потерь указанных интермедиатов IV и V в маточных растворах, но и механических потерь, которые обычно имеют место на технологических операциях экстракции, фильтрации, сушки и т.п.; 3) за счет достижения практически полной конверсии исходных продуктов и высокой селективности реакций образования интермедиатов IV и V и целевого продукта VI в процессе функционализации положения С6 молекулы 11-трифторацетокси-производного 21-ацетата гидрокортизона (III) и тем самым снижения вероятности протекания побочных реакций; 4) за счет практически полного исключения образования побочных продуктов и осмоления реакционной массы на стадиях удаления защитных группировок. В результате достигается высокий выход конечных продуктов I, VI, VII и VIII (от 82 до 97), считая из 21-ацетата гидрокортизона (II).
Техническая задача решается способом получения 6-метиленгидрокортизона или его эфиров общей формулы (I)
где R=COCF3 или Н, R1=СОСН3 или Н из 21-ацетата гидрокортизона формулы (II),
включающим предварительную защиту 11β-гидроксильной группы молекулы 21-ацетата гидрокортизона методом этерификации ангидридом трифторуксусной кислоты в условиях основного катализа с использованием каталитических количеств катализатора, последующее С6-метиленирование образовавшегося 21-ацетокси-17α-гидрокси-11β-трифторацетилокси-прегн-4-ен-3,20-диона, одновременное, поэтапное или последовательное удаление защиты 11β- и 21- гидроксильных групп методами химического сольволиза, или поэтапную (последовательную) защиту гидроксильных групп 11β,17α,21-тригидрокси-6-метиленпрегн-4-ен-3,20диона с образованием 21-ацетокси-17α-гидрокси-11β-трифторацетилокси-6-метиленпрегн-4-ен-3,20-диона через 21-ацетокси-11β,17α-дигидрокси-6-метиленпрегн-4-ен-3,20-дион.
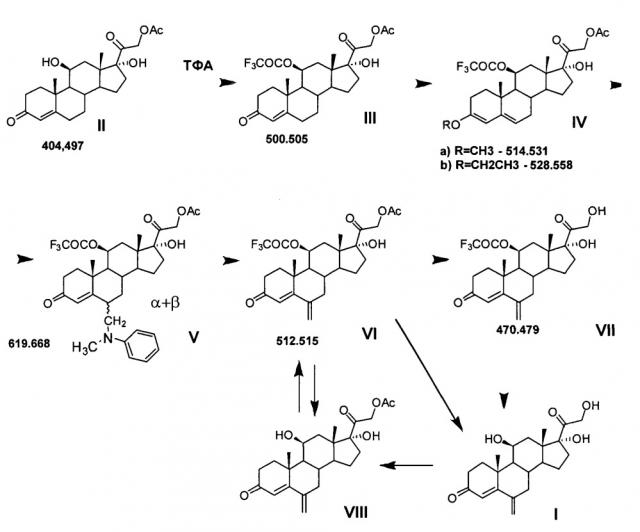
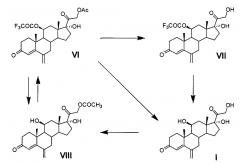
Ниже представлена предлагаемая схема синтеза 6-метиленгидрокортизона (I) или его сложных эфиров (VI, VII и VIII) из 21-ацетата гидрокортизона (II).
Схема включает 4 (для VI) или 5 (для I и VII), или 6 (для VIII) химических реакций, которые могут быть проведены в 2 или 3, или 4 технологических стадии соответственно. Химическая схема синтеза включает: 1) защиту 11β-гидроксильной группы молекулы 21-ацетата гидрокортизона (II) образованием 11β-трифторацетилокси-производного (III); 2) енолизацию α,β-ненасыщенного кетона кольца А соединения III с образованием 3,5-диенолэфира (IV); 3) реакцию трехкомпонентной конденсации по типу реакции Манниха с образованием смеси С6-аминометильных производных (V); 4) расщепление аминометильных производных (V) по связи C-N с образованием С6-метилен-производного (VI); 5) удаление защитных группировок молекулы соединения VI полностью с образованием 6-метиленгидрокортизона (I) или частично по гидроксильной группе С21 с образованием соединения VII, при этом 6-метиленгидрокортизон (I) может быть превращен в его 21-ацетокси-производное (VIII) ацетилированием в условиях основного катализа, из которого далее может быть получено соединение VI. Частичное удаление ацетильной защиты гидроксильной группы при С21 с сохранением трифторацетильной защиты гидроксильной группы при С11 обеспечивает возможность дальнейшей функционализации стероидной молекулы по диоксиацетоновой боковой цепи соединения VII без участия гидроксильной группы при С11.
Сущность заявленного изобретения, касающегося получения 6-метиленгидрокортизона или его эфиров, заключается в том, что с целью повышения выхода и упрощения процесса 21-ацетат гидрокортизона сначала подвергают предварительной защите 11β-гидроксильные группы, затем метиленированию положения С6 с образованием 6-метилен-производного, удалению защитных группировок.
Преимущества заявляемого способа состоят в следующем:
- проведение трифторацетатной защиты 11β-гидроксильной группы 21-ацетата гидрокортизона и селективной деэтерификации побочного продукта реакции этерификации 11,17-бис(трифторацетата) 21-ацетата гидрокортизона с регенерацией 17α-гидроксильной группы осуществляется в одну химическую стадию без выделения целевого продукта;
- проведение конденсации с реагентом Манниха в присутствии свободного гидроксила при С17 в мягких условиях (при комнатной температуре) исключает появление нежелательных продуктов (дегидратации 17α-гидроксигруппы с образованием Δ16-связи и D-гомоаннелирования с образованием 6-членного кольца D), что подтверждается данными ЯМР-спектроскопии;
- региоселективность расщепления стероидного основания Манниха минеральной кислотой исключительно по связи C-N обеспечивается присутствием в реакционной среде соли галогенводородной кислоты и щелочного, или щелочноземельного металла, или аммония;
- отсутствие необходимости использования многократной кристаллизации 11-трифторацетата 21-ацетата 6-метиленгидрокортизона или хроматографирования с целью его очистки, так как содержание основного вещества в продукте составляет 90-95% (ВЭЖХ), что соответствует требованиям, например, каталитической изомеризации 6-экзометиленовой двойной связи в 6,7-эндометиленовую двойную связь или процесса каталитического гидрирования с образованием 11-трифторацетата 21-ацетата 6α-метилгидрокортизона химическим методом;
- отсутствие необходимости использования многократной кристаллизации 6-метиленгидрокортизона или хроматографирования с целью его очистки, так как удаление защитных групп приводит к незначительному появлению побочных соединений; при этом содержание основного вещества в продукте составляет 90-95% (ВЭЖХ), что соответствует требованиям, например, последующего процесса каталитической изомеризации 6-экзометиленовой двойной связи в 6,7-эндометиленовую двойную связь или процесса каталитического гидрирования с образованием 6α-метилгидрокортизона;
- реакции трифторацетилирования, енолэтерификации, конденсации с реагентом Манниха, дезаминирования стероидного основания Манниха проводятся при комнатной температуре;
- значительное сокращение потерь основного продукта на стадиях, что обеспечивается высокой селективностью химических реакций и возможностью совмещения химических стадий в один технологический процесс без выделения интермедиатов, позволяет существенно увеличить достигаемый общий выход 6-метиленгидрокортизона или его эфиров (11-трифторацетата 21-ацетата, или 11-трифторацетата, или 21-ацетата) из 21-ацетата гидрокортизона до 88% и 85,2-97,8% соответственно.
Осуществление изобретения
21-Ацетат гидрокортизона (II), CAS №50-03-3, C12H32O6 (качество USP, или ЕР, или BP), является коммерчески доступным, может быть приобретен, например, у компании Steraloids (USA), или у других производителей. 4-Диметиламинопиридин (≥99.0%), ангидрид трифторуксусной кислоты (≥99.0%), ангидрид уксусной кислоты (≥99.0%), триметилортоформиат (≥99.0%), триэтилортоформиат (≥98.0%), 5-сульфосалициловая кислота (≥99.0%), п-толуолсульфокислота (≥98.0%), N-метиланилин (≥98.0%), циклогексен (≥99.0%), триэтиламин (≥99.0%) являются коммерчески доступными, были приобретены у компании Sigma-Aldrich Со. Другие реагенты, растворители и инертные газы являются коммерчески доступными, были приобретены у российских производителей.
Для выделения продуктов по окончании реакций выливанием реакционных масс в воду, а также для промывки осадков, экстрактов в органических растворителях, использовали питьевую водопроводную воду, если не оговорено особо. Для приготовления водных растворов кислот, хлорида натрия, аммиака и гидроксида натрия использовали дистиллированную воду.
Все процедуры, если не оговорено особо, осуществляли при комнатной температуре или температуре окружающей среды, то есть в диапазоне от 20 до 25°С. Для процессов, требующих более низкие температуры, чем комнатная, охлаждение обеспечивали холодной водопроводной водой (в диапазоне от 10 до 20°С), или смесью колотого льда и холодной воды (в диапазоне от 5 до 10°С), или смесью колотого льда и хлорида кальция (при температуре ниже 5°С). Для обогрева при проведении реакций при температуре выше комнатной и для упаривания растворителей при атмосферном давлении использовали электрический колбонагреватель.
Упаривание растворителей в вакууме осуществляли с использованием ротационного вакуумного испарителя Rotavapor ( Labortechnik AG), при остаточном давлении 0,35±0,05 кгс/см2 (35±5 кПа) и температуре воды в бане в диапазоне от 35-50°С в зависимости от природы упариваемого растворителя.
Высушивание кристаллов продуктов до постоянного веса осуществляли при температуре 35-45°С при атмосферном давлении или с использованием вакуум-сушильного шкафа при остаточном давлении 0,35±0,05 кгс/см2 (35±5 кПа).
Для определения рН промывных вод использовали универсальную индикаторную бумагу с диапазоном значений от 0 до 12 (Лахема, Чехия).
Сухие (безводные) растворители (ацетон, триэтиламин, метанол, этанол) получали общеизвестными методами органической химии.
Колоночную хроматографию осуществляли на колонке (16×650 мм), используя силикагель марки Silica gel 60 (0.040-0.063 мм) (Merck, Germany).
Контроль за ходом реакций осуществляли методом тонкослойной хроматографии (ТСХ), используя пластины Silica gel 60 F254 (Merck, Germany).
Структуру и чистоту всех выделенных соединений подтверждали, по меньшей мере, одним из следующих методов: ТСХ (пластины для ТСХ Silica gel 60 F254 (Merck, Germany)), масс-спектрометрия, элементный анализ, ядерный магнитный резонанс (ЯМР), высокоэффективная жидкостная хроматография (ВЭЖХ).
Температуру плавления выделенных соединений определяли на приборе для определения точки плавления М-565 ( Labortechnik AG).
1Н- и 13С- ЯМР спектры были определены на спектрометре Bruker Avance-400 (Bruker BioSpin GmbH) с рабочей частотой 400 МГц и 100.6 МГц соответственно, используя дейтерированный хлороформ (99,8% D, Sigma-Aldrich), или дейтерированный диметилсульфоксид (99,9% D, Sigma-Aldrich) в качестве растворителя относительно тетраметилсилана (TMS NMR grade ≥99,9%, Sigma-Aldrich) в качестве внутреннего стандарта, в миллионных долях (м.д.).
Элементный анализ был выполнен с использованием анализатора Vario MICRO Cube (Elementar Analysensysteme, GmbH).
ВЭЖХ-анализ проводили на хроматографе Knauer Smartline (Germany), укомплектованном градиентным HPLC-насосом, ячейкой для термостатированной колонки, инжектором, диодно-матричным детектором Smartline 2600, интегратором-компьютером, при температуре 24°С, скорости потока 1 мл/мин и УФ-детектировании при длине волны 254 нм. В качестве неподвижной фазы использовали Kromasil® 100-5С18, в качестве мобильной фазы - 35% (по объему) раствор Н2О в ацетонитриле.
Способ получения 6-метиленгидрокортизона или его эфиров общей формулы (I) осуществляется по вышеприведенной схеме.
21-Ацетат гидрокортизона (21-ацетокси-11β,17α-дигидроксипрегн-4-ен-3,20-дион) формулы (II),
подвергают защите 11β-гидроксильной группы методом этерификации действием ангидрида трифторуксусной кислоты в среде апротонного растворителя в условиях основного катализа в присутствии каталитического количества диметиламинопиридина. Для этого на 1 моль 21-ацетата гидрокортизона (21-ацетокси-11β,17α-дигидроксипрегн-4-ен-3,20-диона) используют 1-1.5 моля ангидрида трифторуксусной кислоты и не более 0.1 моля диметиламинопиридина. Полученный с выходом до 99,95% 21-ацетокси-17α-гидрокси-11β-трифторацетилокси-прегн-4-ен-3,20-дион (III) подвергают енолэтерификации Δ4-3-кетосистемы кольца А действием триалкилортоформиата в присутствии сульфоароматической кислоты (сульфосалициловой или п-ТСК) в качестве кислого катализатора, необходимого для енолизации Δ4-3-кето-группы. Затем полученный 3,5-диенолэфир (IV) подвергают каталитической конденсации с реагентом Манниха, образованным из формальдегида и N-метиланилина in situ, с образованием 6-(N,N-дизамещенного)-аминометилпроизводного (V) с последующим его дезаминированием и превращением в 6-метилен-производное (VI), причем конденсация с реагентом Манниха может быть проведена как с предварительным выделением, так и без выделения 3,5-диенолэфира (IV), а также как с выделением, так и без выделения продукта конденсации (V) из реакционной массы. После этого химическим сольволизом 21-ацетокси-17α-гидрокси-11β-трифторацетилокси-6-метиленпрегн-4-ен-3,20-диона (VI) получают 6-метиленгидрокортизон (I) или его 11β-трифторацетат (VII). При этом удаление защитных групп соединения VI с образованием соединения I может быть реализовано одновременно в условиях основного катализа или поэтапно через образование соединения VII сольволизом в условиях кислого катализа и последующим сольволизом 11-трифторацетоксигруппы соединения VII в условиях основного катализа. Синтез 21-ацетокси-11β,17α-дигидрокси-6-метиленпрегн-4-ен-3,20-диона (VIII) может быть реализован селективным ацетилированием 21-гидроксильной группы соединения I или селективным удалением трифторацетильной группы соединения VI в известных условиях [US 4330541, 1982, пример 1].
Общий достигаемый выход 21-ацетокси-17α-гидрокси-11β-трифторацетилокси-6-метиленпрегн-4-ен-3,20-диона (VI) из 21-ацетата гидрокортизона (II) составляет 97,8%.
Общий достигаемый выход 11-трифторацетата 6-метиленгидрокортизона (VII) из 21-ацетата гидрокортизона (II) составляет 92,7%.
Общий достигаемый выход 6-метиленгидрокортизона (I) из 21-ацетата гидрокортизона (II) составляет 88,3%.
Общий достигаемый выход 21-ацетата 6-метиленгидрокортизона (VIII) из 21-ацетата гидрокортизона (II) составляет 85,2%.
Защиту 11β-гидроксильной группы молекулы 21-ацетата гидрокортизона (II) осуществляют образованием эфира трифторуксусной кислоты в среде органического растворителя в условиях основного катализа. Этот вариант защиты наиболее оптимален, так как реакция этерификации протекает в мягких условиях с практически количественным выходом. Кроме этого, трифторацетатная защитная группа, устойчивая в кислой среде, легко удаляется при необходимости гидролизом в условиях основного катализа. Ацилирование проводят с использованием минимально необходимого количества ангидрида трифторуксусной кислоты в безводных условиях в среде органического апротонного растворителя. Специалисту в области органической химии, а также из уровня техники, известно, что вместо ангидрида трифторуксусной кислоты в этом процессе может быть использован хлорангидрид трифторуксусной кислоты, а в качестве апротонного растворителя при осуществлении изобретения - способа получения 6-метиленгидрокортизона или его эфиров - могут быть использованы любые апротонные (неполярные, малополярные и полярные) растворители, пригодные для проведения реакции и инертные по отношению к ацилирующему реагенту и катализатору, такие как диалкилкетоны (например, ацетон, метилэтилкетон), циклические простые эфиры (например, диоксан, тетрагидрофуран) и другие, известные из уровня техники, обеспечивающие полноту проведения реакции. В качестве основного катализатора могут быть использованы гетероарильные соединения (например, пиридин или его производные), или алкиламины (например, триэтиламин), или другие органические основания, или их смеси, обычно используемые для катализа реакций ацилирования гидроксильных групп, известные из уровня техники. Наиболее оптимальным температурным режимом с технологической точки зрения является проведение процесса этерификации при температуре окружающей среды. Продолжительность процесса устанавливается по результатам контроля содержания исходного продукта в реакционной массе. Минимальное количество катализатора, необходимое для обеспечения полного и быстрого протекания реакции этерификации определяется экспериментально и может варьировать в зависимости от использованного катализатора.
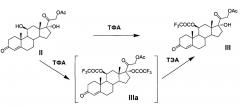
Реакция трифторацетилирования соединения II протекает регионаправленно, этерифицируя предпочтительно вторичную гидроксильную группу при атоме С11 соединения II. Для обеспечения протекания реакции необходимым минимальным количеством ангидрида трифторуксусной кислоты является 1 моль на 1 моль стероида. Для более полного и быстрого протекания реакции используется небольшой избыток ацилирующего агента (~1,2-1,5 моль ТФА на 1 моль стероида). Однако это условие не является обязательным. Применение избыточного количества реагента приводит к частичному трифторацетилированию третичной гидроксильной группы при С17 продукта реакции III с образованием 10-20% примеси 11β,17α-дитрифторацетилокси-производного (IIIa).
Однако в условиях предлагаемого нами способа эфир трифторуксусной кислоты по С17 удаляется легко и селективно с регенерацией 17α-гидроксильной группы и с сохранением трифторацетатной защиты 11β-гидроксильной группы, что достигается обработкой реакционной массы триэтиламином. Выход 21-ацетокси-17α-гидрокси-11β-трифторацетилокси-прегн-4-ен-3,20-диона (III) на стадии составляет от 96 до 99,95%.
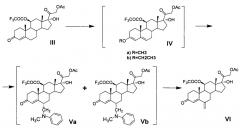
Синтез 21-ацетокси-17α-гидрокси-11β-трифторацетилокси-6-метиленпрегн-4-ен-3,20-диона (VI) из 21-ацетокси-17α-гидрокси-11β-трифторацетилокси-прегн-4-ен-3,20-диона (III) включает три последовательных химических процесса, которые могут быть проведены с выделением любого из интермедиатов общей формулы IV и V или без выделения по следующим вариантам химической схемы синтеза:
Вариант схемы 1: III - IV - V - VI; или
Вариант схемы 2: III - IV - [V] - VI; или
Вариант схемы 3: III - [IV] - V - VI; или
Вариант схемы 4: III - [IV] - [V] - VI.
Наиболее оптимальным и предпочтительным является вариант схемы 4.
Для повышения нуклеофильности атома С6 и тем самым уменьшения вероятности протекания побочных процессов конденсации по другим реакционным центрам (например, по атому С2) на первом этапе синтеза проводится реакция енолизации Δ4-3-кетосистемы кольца А соединения III с образованием 3,5-диенолэфира общей формулы IV. Реакция енолэтерификации Δ4-3-кетосистемы кольца А как с выделением енолэфира IV (варианты 1 и 2), так и без выделения енолэфира IV (варианты 3 и 4) из реакционной массы, может быть проведена с применением или без применения растворителя. Реакцию енолэтерификации Δ4-3-кетосистемы с применением растворителя проводят действием триалкилортоэфира муравьиной кислоты (например, триметилортоформиата или триэтилортоформиата) с использованием минимального количества триалкилортоформиата, необходимого для обеспечения протекания реакции (не менее 1 моля на 1 моль стероида). Для более полного и быстрого протекания реакции (15-30 мин, но не более 2 ч) используется избыток триалкилортоформиата (от 2,5 до 9 моль на 1 моль стероида). Однако это условие не является обязательным. Реакция проводится в безводных условиях в соответствующем протонном растворителе - алифатическом спирте (в метаноле или этаноле) или в апротонном растворителе, выбранном из группы циклических эфиров (например, диоксан или тетрагидрофуран) или ароматических углеводородов группы бензола (например, бензол или толуол). Реакция енолэтерификации Δ4-3-кетосистемы без применения растворителя проводится в среде реагента триалкилортоформиата.
В качестве катализатора енолизации могут быть любые протонные кислоты, обеспечивающие енолизацию Δ4-3-кетосистемы кольца А соединения III с образованием 3,5-диенола, известные из уровня техники специалисту, в частности органические и минеральные кислоты. Минеральные кислоты выбирают из группы растворимых в воде - кислородсодержащих (например, HClO4, H2SO4, HNO3) или бескислородных (например, HCl). Предпочтительно использовать органические кислоты, например сульфоароматические (сульфосалициловую кислоту, п-ТСК или т.п.) как безводные, так и в виде кристаллогидрата. При проведении реакции без выделения енолэфира IV (вариант 3 и 4) из реакционной массы предпочтительно использовать п-ТСК, которая является также катализатором последующей реакции аминометилирования.
В синтезе соединений общей формулы V введение заместителя в положение С6 осуществляют методом трехкомпонентной конденсации по типу реакции Манниха с применением реагента Манниха, образованного in situ взаимодействием формальдегида и N-метиланилина или других вторичных аминов, применимых для целей настоящего изобретения, пригодных для образования 6-(N,N-дизамещенных)-аминометил-соединений и известных из уровня техники, например, N-этиланилин, дифениламин, N-мет