Белки, связывающие рецептор пролактина, и их применение
Иллюстрации
Показать всеНастоящее изобретение относится к иммунологии. Предложено антитело, способное связывать рецептор пролактина (PRLR). Также описаны кодирующая его нуклеиновая кислота, экспрессионный вектор и клетка-хозяин для получения указанного антитела. Кроме того, рассмотрены фармацевтическая композиция, содержащая указанное антитело, и конъюгат антитела с лекарственным средством. Антитело по настоящему изобретению пригодно для обнаружения PRLR и для ингибирования активности PRLR у человека, страдающего нарушением, при котором активность PRLR является вредоносной. 6 н. и 5 з.п. ф-лы, 11 ил., 26 табл., 10 пр.
Реферат
РОДСТВЕННЫЕ ЗАЯВКИ
По настоящему изобретению испрашивается приоритет по временной заявке США № 61/745707, поданной 24 декабря 2012 года, полное содержание которой включено в настоящее описание в качестве ссылки.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка содержит список последовательностей, который предоставлен в электронной форме в формате ASCII и включен в настоящее описание в качестве ссылки в полном объеме. Указанная копия ASCII, созданная 26 февраля 2014 года, названа 117813-10320_SL.txt и имеет размер 210528 байт.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к белкам, связывающим рецептор пролактина (PRLR), и к их применению для предупреждения и/или лечения различных заболеваний, включая злокачественную опухоль.
УРОВЕНЬ ТЕХНИКИ, К КОТОРОМУ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Рецептор пролактина (PRLR) представляет собой трансмембранный рецептор, который взаимодействует с пептидным гормоном пролактином (PRL). PRLR содержит один трансмембранный домен и является гомологичным рецепторам цитокинов, таких как IL2, IL3, IL4, IL6, IL7, эритропоэтин и GM-CSF. PRLR присутствует в молочных железах, яичниках, гипофизе, сердце, легком, тимусе, селезенке, печени, поджелудочной железе, почке, надпочечнике, матке, скелетной мышце, коже и областях центральной нервной системы (Mancini, et al., Endocrinol Metab Clin North Am, 2008, 37(1):67-99). При активации пролактином PRLR димеризуется, что приводит к активации Janus-киназы 2 - тирозинкиназы, которая инициирует каскад JAK-STAT и также приводит к активации митоген-активируемых протеинкиназ и Src-киназы. Гормон роста также связывается с PRLR и активирует рецептор.
PRLR вовлечен в множество биологических функций, включая рост клеток, дифференцировку, развитие, лактацию и репродукцию. кДНК PRLR человека первоначально была выделена из библиотек гепатомы и рака молочной железы (Boutin et al., Molec. Endocr. 3: 1455-1461, 1989). Исходя из нуклеотидной последовательности, был предсказан зрелый белок из 598 аминокислот со значительно более длинным цитоплазматическим доменом, чем в PRLR печени крысы. Ген PRLR располагается в той же хромосомной области, что и ген рецептора гормона роста, который был картирован на 5p13-p14 (Arden, et al., Cytogenet. Cell Gene 53: 161-165, 1990).
Геномная организация гена PRLR человека была определена (Hu, Z.-Z. et al., J. Clin. Endocr. Metab. 84: 1153-1156, 1999). 5-штрих-нетранслируемая область гена PRLR содержит 2 альтернативных первых экзона: E13, человеческий аналог E13 крысы и мыши, и новый тип альтернативного первого экзона человека, названный E1N. 5-штрих-нетранслируемая область также содержит общий некодирующий экзон 2 и часть экзона 3, которая содержит кодон инициации трансляции. Экзоны E13 и E1N находятся в пределах 800 пар оснований друг от друга. Эти 2 экзона экспрессируются в ткани молочной железы человека, клетках рака молочной железы, половых железах и печени. В целом, в большинстве тканей преобладает транскрипт, содержащий E13. Продукт гена PRLR кодируется экзонами 3-10, среди которых экзон 10 кодирует основную часть внутриклеточного домена. Экзоны E13 и E1N транскрибируются с альтернативных промоторов PIII и PN, соответственно. Промотор PIII содержит элементы Sp1 и C/EBP, которые идентичны элементам в промоторе грызунов и на 81% сходны с областью -480/-106 у крысы и мыши. Промотор PN содержит предполагаемые участки связывания для белков семейства ETS и половинный участок для ядерных рецепторов.
PRLR существует в нескольких различных изоформах, которые отличаются длиной их цитоплазматических доменов. В подкожной брюшной жировой ткани и жировой ткани молочной железы было выявлено четыре изоформы мРНК PRLR (L, I, S1a и S1b) (Ling, C. et al., J. Clin. Endocr. Metab. 88: 1804-1808, 2003). Кроме того, с использованием иммуноблоттинга была обнаружена экспрессия как L-PRLR, так и I-PRLR, в подкожной брюшной жировой ткани человека и жировой ткани молочной железы. В недавних сообщениях было сделано предположение, что PRLR экспрессируется и активируется в тканях рака молочной железы и рака предстательной железы человека (Li et al., Cancer Res., 64:4774-4782, 2004; Gill et al., J Clin Pathol., 54:956-960, 2001; Touraine et al., J Clin Endocrinol Metab., 83:667-674, 1998). Сообщалось, что активация Stat5 и экспрессия PRLR ассоциированы с высокой гистологической степенью в 54% образцов рака предстательной железы (Li et al., выше). В других сообщениях утверждалось, что образцы первичного рака молочной железы ответственны за PRL в анализах колониеобразования и что концентрации PRL в плазме коррелируют с риском рака молочной железы (Tworoger et al., Cancer Res., 64:6814-6819, 2004; Tworoger et al., Cancer Res., 66:2476-2482, 2006). В другом сообщении указано, что у мышей с трансгенным PRL развиваются злокачественные карциномы молочной железы или гиперплазия предстательной железы (Wennbo et al., J Clin Invest., 100:2744-2751, 1997; Wennbo et al., Endocrinology, 138:4410-4415, 1997).
Было показано, что моноклональное антитело PRLR уменьшает встречаемость опухолей молочной железы у мышей (Sissom et al., Am. J. Pathol. 133:589-595, 1988). Кроме того, было показано, что антагонист PRL (мутант PRL S179D) ингибирует пролиферацию клеточной линии карциномы предстательной железы человека DU-145 in vitro и индуцируемых DU-145 опухолей in vivo (Xu et al., Cancer Res., 61:6098-6104, 2001).
Таким образом, остается потребность в связывающих PRLR белках, которые можно использовать для терапевтических целей для лечения злокачественной опухоли.
Сущность изобретения
Настоящее изобретение относится к связывающим PRLR белкам и их конъюгатам. Связывающие белки по изобретению включают, но не ограничиваются ими, антитела, антигенсвязывающие фрагменты и другие антигенсвязывающие белки, способные связывать PRLR человека. Кроме того, изобретение относится к способам получения и применения связывающих PRLR белков и их конъюгатов.
В одном аспекте настоящее изобретение относится к связывающему белку, например, антителу или его антигенсвязывающему фрагменту, содержащему антигенсвязывающий домен, причем указанный связывающий белок способен связывать рецептор пролактина (PRLR), указанный антигенсвязывающий домен содержит по меньшей мере одну CDR, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 97, 98, 99, 100, 101, 102, 151 и 152. В одном варианте осуществления, по меньшей мере одна CDR содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 40-42, 46, 47, 49-51, 56-58, 62, 63, 65-67, 71-73, 77, 79-81, 85-87, 92-94, 149 и 150. В другом варианте осуществления, связывающий белок, например антитело или его антигенсвязывающий фрагмент, содержит по меньшей мере 3 CDR. В другом варианте осуществления 3 CDR представляют собой набор CDR вариабельных доменов тяжелой цепи (CDR1, CDR2 и CDR3), выбранный из группы, состоящей из SEQ ID NO: 40, 41 и 42; SEQ ID NO: 46, 47 и 42; SEQ ID NO: 56, 57 и 58; SEQ ID NO: 62, 63 и 58; SEQ ID NO: 71, 72 и 73; SEQ ID NO: 71, 77 и 73; SEQ ID NO: 85, 86 и 87; SEQ ID NO: 149, 150 и 87. Альтернативно или в комбинации, 3 CDR представляют собой набор CDR вариабельных доменов легкой цепи (CDR1, CDR2 и CDR3), выбранный из группы, состоящей из SEQ ID NO: 49, 50 и 51; SEQ ID NO: 65, 66 и 67; SEQ ID NO: 79, 80 и 81; и SEQ ID NO: 92, 93 и 94.
В другом варианте осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, содержит по меньшей мере один набор CDR вариабельных доменов тяжелой цепи и по меньшей мере один набор CDR вариабельных доменов легкой цепи. В некоторых вариантах осуществления по меньшей мере два набора CDR вариабельных доменов выбраны из группы, состоящей из:
(1) либо из наборов CDR вариабельных доменов тяжелой цепи SEQ ID NO: 40, 41 и 42 или SEQ ID NO: 46, 47 и 42, и набора CDR вариабельных доменов легкой цепи SEQ ID NO: 49, 50 и 51;
(2) либо из наборов CDR вариабельных доменов тяжелой цепи SEQ ID NO: 56, 57 и 58 или SEQ ID NO: 62, 63 и 58, и набора CDR вариабельных доменов легкой цепи SEQ ID NO: 65, 66 и 67;
(3) либо из наборов CDR вариабельных доменов тяжелой цепи SEQ ID NO: 71, 72 и 73 или SEQ ID NO: 71, 77 и 73, и набора CDR вариабельных доменов легкой цепи SEQ ID NO: 79, 80 и 81; и
(4) либо из набора CDR вариабельных доменов тяжелой цепи SEQ ID NO: 85, 86 и 87 или SEQ ID NO: 149, 150 и 87, и набора CDR вариабельных доменов легкой цепи SEQ ID NO: 92, 93 и 94.
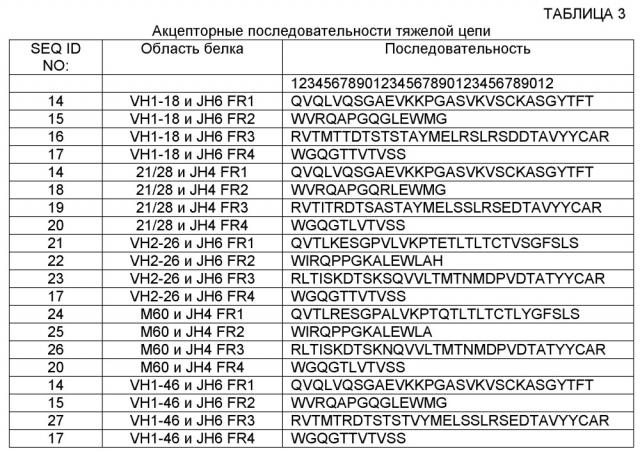
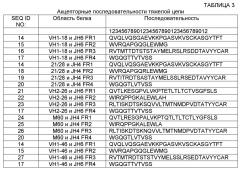
В других вариантах осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, дополнительно содержит акцепторную каркасную область человека. В некоторых вариантах осуществления акцепторная каркасная область человека содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 14-38 или 158. В других вариантах осуществления акцепторная каркасная область человека содержит по меньшей мере одну аминокислотную замену каркасной области, где аминокислотная последовательность каркасной области по меньшей мере на 65% идентична последовательности указанной акцепторной каркасной области человека и содержит по меньшей мере 70 аминокислотных остатков, идентичных указанной акцепторной каркасной области человека. Альтернативно, акцепторная каркасная область человека содержит по меньшей мере одну аминокислотную замену каркасной области в ключевом остатке, причем ключевой остаток выбран из группы, состоящей из:
остатка, соседнего с CDR;
остатка участка гликозилирования;
редкого остатка;
остатка, способного взаимодействовать с PRLR человека;
остатка, способного взаимодействовать с CDR;
канонического остатка;
контактного остатка между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи;
остатка в зоне Vernier; и
остатка в области, которая перекрывается между определенной по Chothia CDR1 вариабельной областью тяжелой цепи и определенной по Kabat каркасной областью первой тяжелой цепи.
В других вариантах осуществления ключевой остаток выбран из группы, состоящей из 2L, 43L, 48L, 58L, 64L, 87L, 27H, 48H, 60H, 63H, 64H, 65H, 67H, 69H, 71H, 73H, 75H, 93H. В другом варианте осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, представляет собой консенсусный вариабельный домен человека.
В одном варианте осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, содержит по меньшей мере один вариабельный домен, имеющий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 39; SEQ ID NO: 43; SEQ ID NO: 44; SEQ ID NO: 45; SEQ ID NO: 55; SEQ ID NO: 59; SEQ ID NO: 60; SEQ ID NO: 61; SEQ ID NO: 70; SEQ ID NO: 74; SEQ ID NO: 75; SEQ ID NO: 76; SEQ ID NO: 84; SEQ ID NO: 88; SEQ ID NO: 89; SEQ ID NO: 90; SEQ ID NO: 121; SEQ ID NO: 122 и SEQ ID NO: 123. В некоторых вариантах осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, содержит два вариабельных домена, где указанные два вариабельных домена имеют аминокислотные последовательности, выбранные из группы, состоящей из:
(1) одной из SEQ ID NO: 39; SEQ ID NO: 43; SEQ ID NO: 44 или SEQ ID NO: 45; и одной из SEQ ID NO: 48, SEQ ID NO: 52, SEQ ID NO: 53 или SEQ ID NO: 54;
(2) одной из SEQ ID NO: 55; SEQ ID NO: 59; SEQ ID NO: 60 или SEQ ID NO: 61; и одной из SEQ ID NO: 64, SEQ ID NO: 68 или SEQ ID NO: 69;
(3) одной из SEQ ID NO: 70; SEQ ID NO: 74; SEQ ID NO: 75 или SEQ ID NO: 76; и одной из SEQ ID NO: 78, SEQ ID NO: 82 или SEQ ID NO: 83; и
(4) одной из SEQ ID NO: 84; SEQ ID NO: 88; SEQ ID NO: 89; SEQ ID NO: 90; SEQ ID NO: 121; SEQ ID NO: 122 или SEQ ID NO: 123; и одной из SEQ ID NO: 91, SEQ ID NO: 95 или SEQ ID NO: 96.
В одном варианте осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, содержит по меньшей мере один вариабельный домен, имеющий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 48; SEQ ID NO: 52; SEQ ID NO: 53; SEQ ID NO: 54; SEQ ID NO: 64; SEQ ID NO: 68; SEQ ID NO: 69; SEQ ID NO: 78; SEQ ID NO: 82; SEQ ID NO: 83; SEQ ID NO: 91; SEQ ID NO: 95 и SEQ ID NO: 96.
В конкретном варианте осуществления связывающий белок содержит последовательность тяжелой цепи и последовательность легкой цепи, выбранную из группы, состоящей из: (a) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 124; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 125; (b) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 124; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 126; (c) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 124; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 127; (d) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 124; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 128; (e) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 129; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 125; (f) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 129; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 126; (g) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 129; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 127; (h) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 129; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 128; (i) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 130; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 125; (j) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 130; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 126; (k) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 130; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 127; (l) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 130; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 128; (m) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 131; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 132; (n) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 131; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 133; (o) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 131; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 134; (p) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 135; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 132; (q) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 135; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 133; (r) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 135; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 134; (s) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 136; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 132; (t) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 136; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 133; (u) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 136; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 134; (v) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 137; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 138; (w) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 137; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 139; (x) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 137; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 140; (y) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 141; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 138; (z) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 141; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 139; (aa) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 141; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 140; (bb) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 142; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 138; (cc) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 142; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 139; (dd) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 142; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 140; (ee) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 143; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 144; (ff) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 143; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 145; (gg) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 143; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 146; (hh) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 147; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 144; (ii) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 147; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 145; (jj) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 147; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 146; (kk) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 148; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 144; (ll) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 148; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 145; (mm) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 148; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 146; (nn) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 153; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 139; (oo) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 154; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 139; и (pp) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 155; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 139.
В одном варианте осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, связывает PRLR. В некоторых вариантах осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, способен модулировать биологическую функцию PRLR. В других вариантах осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, способен нейтрализовать PRLR. В других вариантах осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, имеет константу скорости ассоциации (Kon) с PRLR, выбранную из группы, состоящей из: по меньшей мере приблизительно 102 M-1с-1; по меньшей мере приблизительно 103 M-1с-1; по меньшей мере приблизительно 104 M-1с-1; по меньшей мере приблизительно 105 M-1с-1; и по меньшей мере приблизительно 106 M-1c-1; при измерении с использованием поверхностного плазмонного резонанса. В других вариантах осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, имеет константу скорости диссоциации (Koff) в отношении PRLR, выбранную из группы, состоящей из: не более чем приблизительно 10-3 с-1; не более чем приблизительно 10-4 с-1; не более чем приблизительно 10-5 с-1; и не более чем приблизительно 10-6 с-1, при измерении с помощью поверхностного плазмонного резонанса. В другом варианте осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, имеет константу диссоциации (KD) в отношении PRLR, выбранную из группы, состоящей из: не более чем приблизительно 10-7 M; не более чем приблизительно 10-8 M; не более чем приблизительно 10-9 M; не более чем приблизительно 10-10 M; не более чем приблизительно 10-11 M; не более чем приблизительно 10-12 M; и не более чем 10-13 M.
В другом аспекте изобретение относится к связывающему белку, например, антителу или его антигенсвязывающему фрагменту, способным связывать PRLR, который конкурирует с антителом. В одном варианте осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, конкурирует с антителом, содержащим вариабельный домен тяжелой цепи и вариабельный домен легкой цепи, выбранные из группы, состоящей из:
(1) вариабельной области тяжелой цепи, имеющей аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 39; SEQ ID NO: 43; SEQ ID NO: 44 и SEQ ID NO: 45; и вариабельной области легкой цепи, имеющей аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 48, SEQ ID NO: 52, SEQ ID NO: 53 и SEQ ID NO: 54;
(2) вариабельной области тяжелой цепи, имеющей аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 55; SEQ ID NO: 59; SEQ ID NO: 60 и SEQ ID NO: 61; и вариабельной области легкой цепи, имеющей аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 64, SEQ ID NO: 68 и SEQ ID NO: 69;
(3) вариабельной области тяжелой цепи, имеющей аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 84; SEQ ID NO: 88; SEQ ID NO: 89; SEQ ID NO: 90; SEQ ID NO: 121; SEQ ID NO: 122; и SEQ ID NO: 123; и вариабельной области легкой цепи, имеющей аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 91, SEQ ID NO: 95 и SEQ ID NO: 96;
(4) аминокислотной последовательности вариабельной области тяжелой цепи, указанной в SEQ ID NO: 112, и аминокислотной последовательности вариабельной области легкой цепи, указанной в SEQ ID NO: 103;
(5) аминокислотной последовательности вариабельной области тяжелой цепи, указанной в SEQ ID NO: 113, и аминокислотной последовательности вариабельной области легкой цепи, указанной в SEQ ID NO: 104;
(6) аминокислотной последовательности вариабельной области тяжелой цепи, указанной в SEQ ID NO: 114, и аминокислотной последовательности вариабельной области легкой цепи, указанной в SEQ ID NO: 105;
(7) аминокислотной последовательности вариабельной области тяжелой цепи, указанной в SEQ ID NO: 116, и аминокислотной последовательности вариабельной области легкой цепи, указанной в SEQ ID NO: 107;
(8) аминокислотной последовательности вариабельной области тяжелой цепи, указанной в SEQ ID NO: 117, и аминокислотной последовательности вариабельной области легкой цепи, указанной в SEQ ID NO: 108;
(9) аминокислотной последовательности вариабельной области тяжелой цепи, указанной в SEQ ID NO: 118, и аминокислотной последовательности вариабельной области легкой цепи, указанной в SEQ ID NO: 109;
(10) аминокислотной последовательности вариабельной области тяжелой цепи, указанной в SEQ ID NO: 119, и аминокислотной последовательности вариабельной области легкой цепи, указанной в SEQ ID NO: 110; и
(11) аминокислотной последовательности вариабельной области тяжелой цепи, указанной в SEQ ID NO: 120, и аминокислотной последовательности вариабельной области легкой цепи, указанной в SEQ ID NO: 111.
В другом варианте осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, конкурирует с антителом, содержащим вариабельный домен тяжелой цепи и вариабельный домен легкой цепи, выбранные из группы, состоящей из:
(1) вариабельной области тяжелой цепи, имеющей аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 39; SEQ ID NO: 43; SEQ ID NO: 44 и SEQ ID NO: 45; и вариабельной области легкой цепи, имеющей аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 48, SEQ ID NO: 52, SEQ ID NO: 53 и SEQ ID NO: 54;
(2) вариабельной области тяжелой цепи, имеющей аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 55; SEQ ID NO: 59; SEQ ID NO: 60 и SEQ ID NO: 61; и вариабельной области легкой цепи, имеющей аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 64, SEQ ID NO: 68 и SEQ ID NO: 69;
(3) вариабельной области тяжелой цепи, имеющей аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 84; SEQ ID NO: 88; SEQ ID NO: 89; SEQ ID NO: 90; SEQ ID NO: 121; SEQ ID NO: 122; и SEQ ID NO: 123; и вариабельной области легкой цепи, имеющей аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 91, SEQ ID NO: 95 и SEQ ID NO: 96;
(4) аминокислотной последовательности вариабельной области тяжелой цепи, указанной в SEQ ID NO: 112, и аминокислотной последовательности вариабельной области легкой цепи, указанной в SEQ ID NO: 103;
(5) аминокислотной последовательности вариабельной области тяжелой цепи, указанной в SEQ ID NO: 113, и аминокислотной последовательности вариабельной области легкой цепи, указанной в SEQ ID NO: 104;
(6) аминокислотной последовательности вариабельной области тяжелой цепи, указанной в SEQ ID NO: 114, и аминокислотной последовательности вариабельной области легкой цепи, указанной в SEQ ID NO: 105; и
(7) аминокислотной последовательности вариабельной области тяжелой цепи, указанной в SEQ ID NO: 120, и аминокислотной последовательности вариабельной области легкой цепи, указанной в SEQ ID NO: 111.
В другом варианте осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, конкурирует с антителом, содержащим аминокислотную последовательность вариабельной области тяжелой цепи, указанную в SEQ ID NO: 119, и аминокислотную последовательность вариабельной области легкой цепи, указанную в SEQ ID NO: 110.
В другом варианте осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, конкурирует с антителом, содержащим вариабельный домен тяжелой цепи и вариабельный домен легкой цепи, выбранный из группы, состоящей из:
(1) аминокислотной последовательности вариабельной области тяжелой цепи, указанной в SEQ ID NO: 115, и аминокислотной последовательности вариабельной области легкой цепи, указанной в SEQ ID NO: 106;
(2) аминокислотной последовательности вариабельной области тяжелой цепи, указанной в SEQ ID NO: 116, и аминокислотной последовательности вариабельной области легкой цепи, указанной в SEQ ID NO: 107; и
(3) аминокислотной последовательности вариабельной области тяжелой цепи, указанной в SEQ ID NO: 117, и аминокислотной последовательности вариабельной области легкой цепи, указанной в SEQ ID NO: 108.
В другом варианте осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, конкурирует с антителом, содержащим вариабельную область тяжелой цепи, имеющую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 39; SEQ ID NO: 43; SEQ ID NO: 44 и SEQ ID NO: 45; и вариабельную область легкой цепи, имеющую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 48, SEQ ID NO: 52, SEQ ID NO: 53 и SEQ ID NO: 54. В других вариантах осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, конкурирует с антителом, содержащим вариабельную область тяжелой цепи, имеющую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 84; SEQ ID NO: 88; SEQ ID NO: 89; SEQ ID NO: 90; SEQ ID NO: 121; SEQ ID NO: 122; и SEQ ID NO: 123; и вариабельную область легкой цепи, имеющую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 91, SEQ ID NO: 95 и SEQ ID NO: 96.
В другом аспекте изобретение относится к связывающему белку, способному связывать PRLR, который конкурирует с антителом, содержащим последовательность тяжелой цепи и последовательность легкой цепи, выбранные из группы, состоящей из (a) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 124; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 125; (b) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 124; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 126; (c) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 124; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 127; (d) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 124; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 128; (e) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 129; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 125; (f) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 129; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 126; (g) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 129; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 127; (h) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 129; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 128; (i) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 130; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 125; (j) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 130; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 126; (k) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 130; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 127; (l) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 130; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 128; (m) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 131; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 132; (n) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 131; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 133; (o) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 131; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 134; (p) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 135; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 132; (q) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 135; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 133; (r) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 135; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 134; (s) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 136; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 132; (t) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 136; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 133; (u) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 136; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 134; (v) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 137; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 138; (w) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 137; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 139; (x) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 137; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 140; (y) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 141; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 138; (z) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 141; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 139; (aa) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 141; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 140; (bb) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 142; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 138; (cc) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 142; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 139; (dd) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 142; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 140; (ee) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 143; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 144; (ff) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 143; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 145; (gg) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 143; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 146; (hh) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 147; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 144; (ii) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 147; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 145; (jj) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 147; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 146; (kk) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 148; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 144; (ll) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 148; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 145; (mm) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 148; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 146; (nn) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 153; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 139; (oo) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 154; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 139; и (pp) тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 155; и легкой цепи, имеющей аминокислотную последовательность SEQ ID NO: 139.
В другом аспекте изобретение относится к связывающему белку, например, антителу или его антигенсвязывающему фрагменту, способному связывать PRLR, который связывается с эпитопом в PRLR, содержащим три, четыре, пять, шесть, семь, восемь, девять или все из аминокислотных остатков E8, F10, C12, R25, E43, G44, I76, D91, E92, L93, Y94, V95, D96, Y99, I100, E145, F160, K185, D187, H188, Y190 и W191 SEQ ID NO: 2. В одном варианте осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, способный связывать PRLR, связывается с эпитопом, где эпитоп содержит по меньшей мере пять аминокислотных остатков. В другом варианте осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, способный связывать PRLR, связывается с эпитопом, где эпитоп содержит все из аминокислотных остатков E8, F10, C12, R25, E43, G44, I76, D91, E92, L93, Y94, V95, D96, Y99, I100, E145, F160, K185, D187, H188, Y190 и W191 SEQ ID NO: 2. В конкретном варианте осуществления связывающий белок представляет собой антитело или его антигенсвязывающую часть, выбранные из группы, состоящей из Ab1, Ab6, chAb6 и Ab14-Ab25.
В другом аспекте изобретение относится к связывающему белку, например, к антителу или его антигенсвязывающему фрагменту, способному связывать PRLR, который связывается с эпитопом в PRLR, содержащим три, четыре, пять, шесть, семь, восемь, девять или все из аминокислотных остатков E8, I9, F10, K11, C12, R25, E43, G44, W72, T74, I76, D91, E92, L93, Y94, V95, D96, T98, Y99, I100, W139, L143, E145, F160, K185, D187, H188, Y190 и W191 SEQ ID NO: 2. В одном варианте осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, способный связывать PRLR, связывается с эпитопом, где эпитоп содержит по меньшей мере пять аминокислотных остатков. В другом варианте осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, способный связывать PRLR, связывается с эпитопом, где эпитоп содержит все из аминокислотных остатков E8, I9, F10, K11, C12, R25, E43, G44, W72, T74, I76, D91, E92, L93, Y94, V95, D96, T98, Y99, I100, W139, L143, E145, F160, K185, D187, H188, Y190 и W191 SEQ ID NO: 2. В конкретном варианте осуществления связывающий белок представляет собой антитело или его антигенсвязывающую часть, выбранные из группы, состоящей из Ab4, Ab7, chAb7, Ab35-Ab43 и Ab53-Ab55.
В другом аспекте изобретение относится к связывающему белку, например, антителу или его антигенсвязывающему фрагменту, способным связывать PRLR, который связывается с эпитопом в PRLR, содержащим 13, 14, 15, 16, 17, 18, 19, 20, 21 или все из аминокислотных остатков R25, T141, L143, E145, R147, E155, W156, E157, I158, H159, F160, A161, G162, Q163, Q164, F167, S171, R183, K185, D187, H188, W191 и W194 SEQ ID NO: 2. В одном варианте осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, способный связывать PRLR, связывается с эпитопом, где эпитоп содержит по меньшей мере 15 аминокислотных остатков. В некоторых вариантах осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, способный связывать PRLR, связывается с эпитопом, где эпитоп содержит все из аминокислотных остатков R25, T141, L143, E145, R147, E155, W156, E157, I158, H159, F160, A161, G162, Q163, Q164, F167, S171, R183, K185, D187, H188, W191 и W194 SEQ ID NO: 2. В конкретном варианте осуществления связывающий белок представляет собой антитело или его антигенсвязывающую часть, выбранные из группы, состоящей из Ab3, Ab8, chAb8 и Ab44-Ab52.
В другом аспекте изобретение относится к связывающему белку, например, антителу или его антигенсвязывающему фрагменту, способным связывать PRLR, который связывается с эпитопом в PRLR, содержащим по меньшей мере один, два, три, четыре или все из аминокислотных остатков R25, K185, D187, H188 или W191 SEQ ID NO: 2. В некоторых вариантах осуществления связывающий белок, например, антитело или его антигенсвязывающий фрагмент, способные связывать PRLR, связывается с эпитопом, где эпитоп содержит все из аминокислотных остатков R25, K185, D187, H188 или W191 SEQ ID NO: 2. В конкретном варианте осуществления связывающий белок представляет собой антитело или его антигенсвязыващую часть, выбранные из группы, состоящей из Ab1, Ab3, Ab4, Ab6-Ab8, chAb6, chAb7, chAb8, Ab14-Ab25 и Ab35-Ab55.
В другом аспекте изобретение относится к связывающему белку, например, к антителу или его антигенсвязывающему фрагменту, способному связывать PRLR, который связывается с эпитопом в PRLR, содержащим аминокислоты 91-96 SEQ ID NO: 2. В конкретном варианте осуществления связывающий белок представляет собой антитело или его антигенсвязывающую часть, выбранные из группы, состоящей из Ab1, Ab4, Ab6, Ab7, chAb6, chAb7, Ab14-Ab25, Ab35-Ab43 и Ab53-Ab55.
В другом аспекте изобретение относится к связывающему белку, например, к антителу или его антигенсвязывающему фрагменту, способному связыват