Конъюгат антитело-лекарственное средство
Иллюстрации
Показать всеИзобретение относится к области биохимии. Описана группа изобретений, включающая конъюгат антитело-лекарственное средство для лечения опухоли и/или рака, лекарственное средство, противоопухолевое лекарственное средство и/или противораковое лекарственное средство, содержащие вышеуказанный конъюгат антитело-лекарственное средство, фармацевтическую композицию, способ лечения опухоли и/или рака, промежуточное соединение лекарственное средство-линкер, линкер для получения вышеуказанного конъюгата антитело-лекарственное средство. Конъюгат антитело-лекарственное средство содержит в себе противоопухолевое соединение, конъюгированное с антителом через линкер, имеющий структуру, представленную следующей формулой: -L1-L2-LP-NH-(CH2)n1-La-Lb-Lc-, где антитело присоединено к концу L1, а противоопухолевое соединение присоединено к концу Lc с помощью атома азота аминогруппы в положение 1 в качестве положения для соединения. Предложенное изобретение расширяет арсенал средств с противоопухолевой активностью. 7 н. и 46 з.п. ф-лы, 22 ил., 75 пр.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к конъюгату антитело-лекарственное средство, содержащему противоопухолевое лекарственное средство, конъюгированное через фрагмент линкерной структуры с антителом, способным обеспечивать направленную доставку лекарственного средства к опухолевым клеткам, при этом конъюгат применяют в качестве противоопухолевого лекарственного препарата.
Уровень техники
Конъюгат антитело-лекарственное средство (ADC), содержащий цитотоксическое лекарственное средство, конъюгированное с антителом, антиген которого экспрессируется на поверхности опухолевых клеток, и которое также связано с антигеном, способным к клеточной интернализации, позволяет селективно доставлять лекарственное средство в опухолевые клетки, и, предполагается, что в результате этого происходит аккумуляция лекарственного средства в опухолевых клетках и гибель опухолевых клеток (см., непатентные публикации 1-3). В качестве примера конъюгата антитело-лекарственное средство (ADC) может быть приведен милотарг (гемтузумаб озогамицин), одобренный в качестве терапевтического средства при остром миелолейкозе, в котором калихеамицин конъюгирован с анти-CD33 антителом. Кроме того, недавно был одобрен в качестве терапевтического средства при лимфоме Ходжкина и анапластической крупноклеточной лимфоме адцетрис (брентуксимаб ведотин), в котором ауристатин E конъюгирован с анти-CD30 антителом (см., непатентную публикацию 4). Лекарственные средства, содержавшиеся в конъюгатах антитело-лекарственное средство, которые были одобрены до настоящего времени, осуществляют направленную доставку лекарственного средства в ДНК или тубулин.
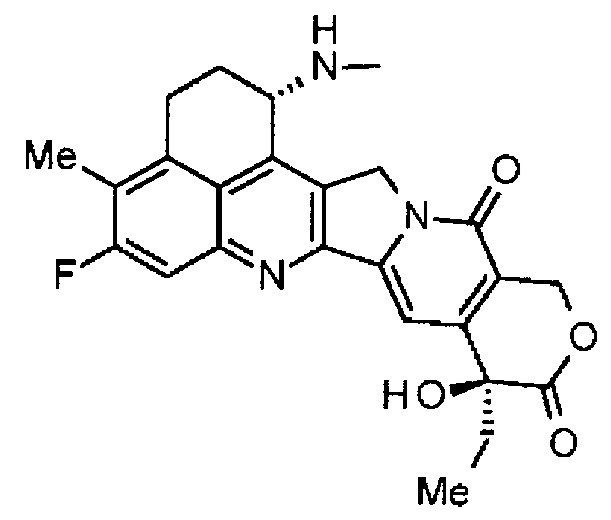
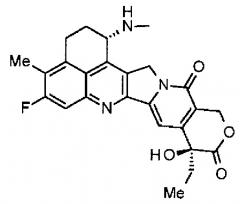
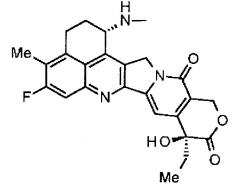
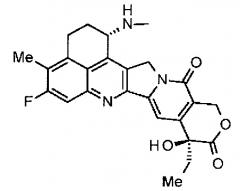
Что касается противоопухолевых средств, то известны низкомолекулярные соединения, производные камптотецина, соединения, которые ингибируют топоизомеразу I с проявлением противоопухолевого эффекта. Среди них, противоопухолевое соединение, представленное формулой ниже
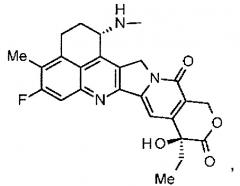
(эксатекан, химическое название: (1S,9S)-1-амино-9-этил-5-фтор-2,3-дигидро-9-гидрокси-4-метил-1H,12H-бензо[де]пирано-[3',4':6,7]индолизино[1,2-b]хинолин-10,13(9H,15H)дион) представляет собой водорастворимое производное камптотецина (патентная публикация 1 и 2). В отличие от иринотекана, применяемого в клинике в настоящее время, для эксатекана требуется активация ферментом. Кроме того, его ингибирующая активность в отношении топоизомеразы II выше, чем в случае SN-38, который является основным фармацевтически активным веществом препаратов иринотекана и топотекана, также используемых в клинике, и он проявляет более сильное разрушающее действие in vitro в отношении различных опухолевых клеток. В частности, он проявляет активность против опухолевых клеток, которые обладают резистентностью к SN-38 или другим подобным веществам вследствие экспрессии P-гликопротеина. Кроме того, в модели опухоли человека, подкожно трансплантируемой мышам, эксатекан проявляет мощный противоопухолевый эффект и уже прошел клинические испытания, но еще не доступен на рынке фармацевтических препаратов (см., непатентные публикации 5-10). Пока остается неясным, может или не может эксатекан оказывать эффективное воздействие в форме конъюгата антитело-лекарственное средство.
DE-310 представляет собой комплекс, в котором эксатекан конъюгирован с биоразлагаемым полимером карбоксиметилдекстран-полиспиртом через GGFG пептидный спейсер (патентная публикация 3). Превращая эксатекан в форму полимерного пролекарства, можно поддерживать сохранение на высоком уровне свойства крови, а также улучшать пассивную целенаправленную доставку в область опухоли вследствие повышенной проницаемости вновь образовавшихся кровеносных сосудов внутри опухоли и ретенции в тканях опухоли. В случае DE-310, в результате расщепления пептидного спейсера ферментом, эксатекан и эксатекан с глицином, соединенным с аминогруппой, непрерывно высвобождается в качестве основного активного вещества. Вследствие этого, улучшается фармакокинетика, и на основе доклинических исследований различных моделей оценки опухоли было обнаружено, что DE-310 обладает более высокой эффективностью, чем эксатекан, введенный в чистом виде, даже если доза эксатекана в форме DE-310 ниже, чем в случае введения эксатекана в чистом виде. Было проведено клиническое исследование препарата DE-310, и его эффективность была подтверждена на людях, причем в этом исследовании делалось предположение, что основное активное вещество накапливается в опухоли, а не в здоровых тканях, однако, также имеются данные, указывающие на то, что накопление DE-310 и основного активного вещества в опухоли сильно не отличается от накопления в здоровых тканях у людей, и, поэтому, пассивная целенаправленная доставка DE-310 у людей не наблюдается (см., непатентные публикации 11-14). В результате, DE-310 также не был внедрен в лечебную практику, но остается неясным вопрос о том, может или не может эксатекан эффективно выполнять функцию лекарственного средства, предназначенного для такой целенаправленной доставки.
В качестве соединения, имеющего отношение к DE-310, также известен комплекс, в котором структурный фрагмент, представленный -NH(CH2)4C(=O)-, вводят между -GGFG-спейсером и эксатеканом с образованием структуры -GGFG-NH(CH2)4C(=O)-, используемый в качестве спейсерной структуры, (патентная публикация 4). Однако противоопухолевое действие комплекса точно не известно.
Список цитируемой литературы
Патентные публикации
[Патентная публикация 1] Выложенный патент Японии № 5-59061.
[Патентная публикация 2] Выложенный патент Японии № 8-337584.
[Патентная публикация 3] Международная публикация № WO 1997/46260.
[Патентная публикация 4] Международная публикация № WO 2000/25825.
Непатентные публикации
[Непатентная публикация 1] Ducry, L., et al. Bioconjugate Chem. (2010) 21, 5-13; Antibody-Drug Conjugates: Linking cytotoxic payloads to monoclonal antibodies.
[Непатентная публикация 2] Alley, S.C., et al. Current Opinion in Chemical Biology (2010) 14, 529-537; Antibody-drug conjugates: targeted drug delivery for cancer.
[Непатентная публикация 3] Damle N.K. Expert Opin. Biol. Ther. (2004) 4, 1445-1452; Tumour-targeted chemotherapy with immunoconjugates of calicheamicin.
[Непатентная публикация 4] Senter P.D., et al. Nature Biotechnology (2012) 30, 631-637; The discovery and development of brentuximab vedotin for use in relapsed Hodgkin lymphoma and systemic anaplastic large cell lymphoma.
[Непатентная публикация 5] Kumazawa, E., Tohgo, A., Exp. Opin. Invest. Drugs (1998) 7, 625-632; Antitumour activity of DX-8 951f: a new camptothecin derivative.
[Непатентная публикация 6] Mitsui, I., Kumazawa, E., Hirota, Y., et al. Jpn J. Cancer Res. (1995) 86, 776-782; A new water-soluble camptothecin derivative, DX-8951f, exhibits potent antitumor activity against human tumors in vitro and in vivo.
[Непатентная публикация 7] Takiguchi, S., Tohgo, A., et al. Jpn J. Cancer Res. (1997) 88, 760-769; Antitumor effect of DX-8951, a novel camptothecin analog, on human pancreatic tumor cells and their CPT-11-resistant variants cultured in vitro and xenografted into nude mice.
[Непатентная публикация 8] Joto, N. et al. Int J Cancer (1997) 72, 680-686; DX-8951f, a water-soluble camptothecin analog, exhibits potent antitumor activity against a human lung cancer cell line and its SN-38-resistant variant.
[Непатентная публикация 9] Kumazawa, E. et al. Cancer Chemother. Pharmacol. (1998) 42, 210-220; Potent and broad antitumor effects of DX-8951f, a water-soluble camptothecin derivative, against various human tumors xenografted in nude mice.
[Непатентная публикация 10] De Jager, R., et al. Ann N Y Acad Sci (2000) 922, 260-273; DX-8951f: summary of phase I clinical trials.
[Непатентная публикация 11] Inoue, K. et al. Polymer Drugs in the Clinical Stage, Edited by Maeda et al. (2003), 145-153; CM-dextran-polyalcohol-camptothecin conjugate, DE-310 with a novel carrier system and its preclinical data.
[Непатентная публикация 12] Kumazawa, E. et al. Cancer Sci (2004) 95, 168-175; DE-310, a novel macromolecular carrier system for the camptothecin analog DX-8951f: Potent antitumor activities in various murine tumor models.
[Непатентная публикация 13] Soepenberg, O. et al. Clinical Cancer Research, (2005) 11, 703-711; Phase I and pharmacokinetic study of DE-310 in Patients with Advanced Solid Tumors.
[Непатентная публикация 14] Wente M. N. et al. Investigational New Drugs (2005) 23, 339-347; DE-310, a macromolecular prodrug of the topoisomerase-I-inhibitor exatecan (DX-8951), in patients with operable solid tumors.
Сущность изобретения
Техническая задача
При лечении опухоли с помощью антитела, неудовлетворительный противоопухолевый эффект может наблюдаться даже тогда, когда антитело распознает антиген и связывает опухолевые клетки, и существуют обстоятельства, при которых требуется более эффективное противоопухолевое антитело. Кроме того, многие противоопухолевые низкомолекулярные соединения имеют недостаток, связанный с их безопасностью, например, связанный с побочным эффектом и токсичностью, это свойственно даже соединениям, которые обладают отличным противоопухолевым действием, и, поэтому важной задачей остается достижение более высокого терапевтического эффекта за счет дополнительного повышения безопасности. Поэтому, задачей настоящего изобретения является создание противоопухолевого лекарственного средства, которое обладает высоким терапевтическим действием и которое характеризуется исключительными свойствами с точки зрения противоопухолевого действия и безопасности.
Способы решения задачи
Авторы изобретения считали, что если противоопухолевое соединение эксатекан превратить в конъюгат антитело-лекарственное средство путем конъюгирования при помощи фрагмента линкерной структуры с антителом, которое способно обеспечивать направленную доставку в опухолевые клетки, которое способно распознавать опухолевые клетки, способно связывать опухолевые клетки, способно к интернализации в опухолевых клетках, которое обладает активностью, приводящей к гибели опухолевых клеток, или характеризуется другими подобными свойствами, то противоопухолевое соединение может быть более надежно доставлено в опухолевые клетки с целью проявления его специфического противоопухолевого действия в опухолевых клетках, и за счет этого, несомненно, может быть достигнут противоопухолевый эффект, и можно также ожидать повышения активности антитела, приводящей к гибели опухолевых клеток, и может быть также уменьшена доза противоопухолевого соединения по сравнению с дозой при введении соединения в чистом виде, и, благодаря чему, может быть ослаблено воздействие противоопухолевого соединения на здоровые клетки, что позволяет достигать более высокой степени безопасности.
В связи с этим, авторы изобретения создали линкер со специфической структурой, смогли получить конъюгат антитело-лекарственное средство, в котором антитело и эксатекан конъюгированы друг с другом через линкер и продемонстрировали высокое противоопухолевое действие, оказываемое этим конъюгатом, в результате чего и было создано настоящее изобретение.
В частности, настоящее изобретение характеризуется приведенным ниже отличительным признаком.
[1] Конъюгат антитело-лекарственное средство, в котором противоопухолевое соединение, представленное следующей формулой:
конъюгировано с антителом через линкер, имеющий структуру, представленную следующей формулой: -L1-L2-LP-NH-(CH2)n1-La-Lb-Lc-.
В данном случае, антитело присоединено к концу L1, противоопухолевое соединение присоединено к концу Lc с помощью атома азота аминогруппы в положение 1 в качестве положения для соединения,
где
n1 представляет целое число от 0 до 6,
L1 представляет -(сукцинимид-3-ил-N)-(CH2)n2-C(=O)-, -CH2-C(=O)-NH-(CH2)n3-C(=O)-, -C(=O)-цик.Гекс(1,4)-CH2-(N-ли-3-диминицкус)- или -C(=O)-(CH2)n4-C(=O)-,
где n2 представляет целое число от 2 до 8, n3 представляет целое число от 1 до 8, n4 представляет целое число от 1 до 8,
L2 представляет -NH-(CH2-CH2-O)n5-CH2-CH2-C(=O)-, -S-(CH2)n6-C(=O)- или одинарную химическую связь,
где n5 представляет целое число от 1 до 6, n6 представляет целое число от 1 до 6,
LP представляет пептидный остаток, состоящий от 2 до 7 аминокислот,
La представляет -C(=O)-NH-, -NR1-(CH2)n7-, -O- или одинарную химическую связь,
где n7 представляет целое число от 1 до 6, R1 представляет атом водорода, алкильную группу, имеющую от 1 до 6 углеродных атомов, -(CH2)n8-COOH, или -(CH2)n9-OH, n8 представляет целое число от 1 до 4, n9 представляет целое число от 1 до 6,
Lb представляет -CR2(-R3)-, -O-, -NR4-, или одинарную химическую связь,
где R2 и R3 каждый независимо представляет атом водорода, алкильную группу, имеющую от 1 до 6 углеродных атомов, -(CH2)na-NH2, -(CH2)nb-COOH или -(CH2)nc-OH, R4 представляет атом водорода или алкильную группу, имеющую от 1 до 6 углеродных атомов, na представляет целое число от 0 до 6, nb представляет целое число от 1 до 4, nc представляет целое число от 1 до 4, при условии, что когда na равняется 0, R2 и R3 не являются одинаковыми,
Lc представляет -CH2- или -C(=O)-,
-(сукцинимид-3-ил-N)- имеет структуру, представленную следующей формулой:
,
которая присоединена к антителу в ее положении 3 и присоединена к метиленовой группе в линкерной структуре, имея эту структуру на атоме азота в положении 1,
-(N-ли-3-диминицкус)- имеет структуру, представленную следующей формулой:
,
которая присоединена к L2 в ее положении 3 и присоединена к метиленовой группе в линкерной структуре, имея эту структуру на атоме азота в положении 1,
цик.Гекс(1,4) представляет 1,4-циклогексиленовую группу, и когда L2 представляет собой -S-(CH2)n6-C(=O)-, L1 представляет собой -C(=O)- цик.Гекс(1,4)-CH2-(N-ли-3-диминицкус)-.
Настоящее изобретение дополнительно характеризуется каждым из приведенных ниже отличительных признаков.
[2] Конъюгат антитело-лекарственное средство по пункту [1], где Lc представляет собой -C(=O)-.
[3] Конъюгат антитело-лекарственное средство по пункту [1] или [2], где связь между антителом и L1 является тиоэфирной связью, которая образуется на месте дисульфидной связи, присутствующей в шарнирной части антитела, дисульфидной связью, которая образуется на месте дисульфидной связи, присутствующей в шарнирной части антитела, или амидной связью, которая образуется на аминогруппе, присутствующей в боковой цепи аминокислоты, входящей в состав антитела, или на терминальной аминогруппе.
[4] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[3], где пептидный остаток в LP представляет собой аминокислотный остаток, включающий аминокислоту, выбранную из фенилаланина, глицина, валина, лизина, цитруллина, серина, глутаминовой кислоты и аспарагиновой кислоты.
[5] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[3], где LP представляет собой пептидный остаток, состоящий из 4 аминокислот.
[6] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[3], где LP представляет собой -GGFG-.
[7] конъюгат антитело-лекарственное средство, где противоопухолевое соединение, представленное следующей формулой:
конъюгировано с антителом через линкер, имеющий структуру, представленную следующей формулой: -L1-L2-LP-NH-(CH2)n1-La-Lb-Lc-.
В данном случае, антитело присоединено к концу L1, противоопухолевое соединение присоединено к концу Lc с помощью атома азота аминогруппы в положение 1 в качестве положения для соединения,
где
n1 представляет целое число от 0 до 6,
L1 представляет -(сукцинимид-3-ил-N)-(CH2)n2-C(=O)-, -CH2-C(=O)-NH-(CH2)n3-C(=O)-, -C(=O)- цик.Гекс(1,4)-CH2-(N-ли-3-диминицкус)- или -C(=O)-(CH2)n4-C(=O)-,
где n2 представляет целое число от 2 до 8, n3 представляет целое число от 1 до 8, n4 представляет целое число от 1 до 8,
L2 представляет -NH-(CH2-CH2-O)n5-CH2-CH2-C(=O)-, -S-(CH2)n6-C(=O)- или одинарную химическую связь,
где n5 представляет целое число от 1 до 6, n6 представляет целое число от 1 до 6,
LP представляет тетрапептидный остаток GGFG,
La представляет -O- или одинарную химическую связь,
Lb представляет -CR2(-R3)- или одинарную химическую связь,
где R2 и R3 каждый представляет атом водорода,
Lc представляет -C(=O)-,
-(сукцинимид-3-ил-N)- имеет структуру, представленную следующей формулой:
,
которая присоединена к антителу в ее положении 3 и присоединена к метиленовой группе в линкерной структуре, имея эту структуру на атоме азота в положении 1,
-(N-ли-3-диминицкус)- имеет структуру, представленную следующей формулой:
,
которая присоединена к L2 в ее положении 3 и присоединена к метиленовой группе в линкерной структуре, имея эту структуру на атоме азота в положении 1,
цик.Гекс(1,4) представляет 1,4-циклогексиленовую группу, и когда L2 представляет собой -S-(CH2)n6-C(=O)-, L1 представляет собой -C(=O)- цик.Гекс(1,4)-CH2-(N-ли-3-диминицкус)-.
[8] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[7], где L1 представляет собой -(сукцинимид-3-ил-N)-(CH2)n2-C(=O)- или -CH2-C(=O)-NH-(CH2)n3-C(=O)-.
[9] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[7], где L1 представляет собой -(сукцинимид-3-ил-N)-(CH2)n2-C(=O)-.
[10] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[7], где L1 представляет собой -C(=O)- цик.Гекс(1,4)-CH2-(N-ли-3-диминицкус)- или -C(=O)-(CH2)n4-C(=O)-.
[11] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[9], где n2 представляет собой целое число от 2 до 5, и L2 представляет собой одинарную химическую связь.
[12] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[9], где n2 представляет собой целое число от 2 до 5, L2 представляет собой -NH-(CH2CH2O)n5-CH2-CH2-C(=O)-, и n5 равняется 2 или 4.
[13] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[12], где -NH-(CH2)n1-La-Lb-Lc- представляет собой подструктуру, имеющую длину цепи от 4 до 7 атомов.
[14] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[12], где -NH-(CH2)n1-La-Lb-Lc- представляет собой подструктуру, имеющую длину цепи в 5 или 6 атомов.
[15] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[14], где -NH-(CH2)n1-La-Lb-Lc- представляет собой
-NH-(CH2)3-C(=O)-,
-NH-CH2-O-CH2-C(=O)- или
-NH-(CH2)2-O-CH2-C(=O)-.
[16] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[15], где фрагмент лекарственное средство-линкерная структура представляет собой один фрагмент лекарственное средство-линкерная структура, выбранный из группы, состоящей из следующих фрагментов лекарственное средство-линкерная структура:
-(сукцинимид-3-ил-N)-CH2CH2-C(=O)-GGFG-NH-CH2CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2CH2CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2-O-CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2-O-CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2-C(=O)-(NH-DX),
-CH2-C(=O)-NH-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX),
-C(=O)-CH2CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX),
-C(=O)-цик.Гекс(1,4)-CH2-(N-ли-3-диминицкус)-S-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX),
где -(сукцинимид-3-ил-N)- имеет структуру, представленную следующей формулой:
,
которая присоединена к антителу в ее положении 3 и присоединена к метиленовой группе в линкерной структуре, имея эту структуру на атоме азота в положении 1,
-(N-ли-3-диминицкус)- имеет структуру, представленную следующей формулой:
,
которая присоединена к L2 в ее положении 3 и присоединена к метиленовой группе в линкерной структуре, имея эту структуру на атоме азота в положении 1,
цик.Гекс(1,4) представляет 1,4-циклогексиленовую группу,
-(NH-DX) представляет группу, представленную следующей формулой:
,
где атом азота аминогруппы в положении 1 является положением присоединения, и
-GGFG- представляет пептидный остаток -Gly-Gly-Phe-Gly-.
[17] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[9] и [11]-[14], где фрагмент лекарственное средство-линкерная структура, имеющий лекарственное средство, присоединенное к -L1-L2-LP-NH-(CH2)n1-La-Lb-Lc-, представляет собой один фрагмент лекарственное средство-линкерная структура, выбранный из следующей группы:
-(сукцинимид-3-ил-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2-O-CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2-O-CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX).
В приведенных выше фрагментах, -(сукцинимид-3-ил-N)- имеет структуру, представленную следующей формулой:
,
которая присоединена к антителу в ее положении 3 и присоединена к метиленовой группе в линкерной структуре, имея эту структуру на атоме азота в положении 1, и
-(NH-DX) представляет группу, представленную следующей формулой:
,
где атом азота аминогруппы в положении 1 является положением присоединения.
[18] Конъюгат антитело-лекарственное средство, где противоопухолевое соединение, представленное следующей формулой:
конъюгировано с антителом через линкер, имеющий структуру, представленную следующей формулой: -L1-L2-LP-NH-(CH2)n1-La-Lb-Lc-.
В данном случае, антитело присоединено к концу L1, противоопухолевое соединение присоединено к концу Lc,
где
n1 представляет целое число от 0 до 6,
L1 представляет -(сукцинимид-3-ил-N)-(CH2)n2-C(=O)- и присоединен к антителе через тиоэфирную связь, которая образуется на месте дисульфидной связи, присутствующей в шарнирной части антитела,
где n2 представляет целое число от 2 до 8,
L2 представляет -NH-(CH2-CH2-O)n5-CH2-CH2-C(=O)- или одинарную химическую связь,
где n5 представляет целое число от 1 до 6,
LP представляет тетрапептидный остаток GGFG,
La представляет -O- или одинарную химическую связь,
Lb представляет -CR2(-R3)- или одинарную химическую связь,
где R2 и R3 каждый представляет атом водорода,
Lc представляет -C(=O)- и
-(сукцинимид-3-ил-N)- имеет структуру, представленную следующей формулой:
,
которая присоединена к антителу в ее положении 3 и присоединена к метиленовой группе в линкерной структуре, имея эту структуру на атоме азота в положении 1.
[19] Конъюгат антитело-лекарственное средство по пункту [18], где
n2 равняется 2, L2 представляет собой -NH-(CH2-CH2-O)n5-CH2-CH2-C(=O)-, n5 равняется 2, n1 равняется 3, и оба La и Lb представляют собой одинарные химические связи,
n2 равняется 5, L2 представляет собой одинарную химическую связь, n1 равняется 1, La представляет собой -O-, и Lb представляет собой -CR2(-R3)-, или
n2 равняется 5, L2 представляет собой одинарную химическую связь, n1 равняется 2, La представляет собой -O-, и Lb представляет собой -CR2(-R3)-.
[20] Конъюгат антитело-лекарственное средство по пункту [18] или [19], где n2 представляет собой целое число от 2 до 5, и L2 представляет собой одинарную химическую связь.
[21] Конъюгат антитело-лекарственное средство по пункту [18] или [19], где n2 представляет собой целое число от 2 до 5, L2 представляет собой -NH-(CH2CH2O)n5-CH2-CH2-C(=O)-, и n5 равняется 2 или 4.
[22] Конъюгат антитело-лекарственное средство по любому из пунктов [18]-[21], где -NH-(CH2)n1-La-Lb-Lc- представляет собой
-NH-(CH2)3-C(=O)-,
-NH-CH2-O-CH2-C(=O)- или
-NH-(CH2)2-O-CH2-C(=O)-.
[23] Конъюгат антитело-лекарственное средство по любому из пунктов [18]-[22], где фрагмент лекарственное средство-линкерная структура представляет собой один фрагмент лекарственное средство-линкерная структура, выбранный из группы, состоящей из следующих фрагментов лекарственное средство-линкерная структура:
-(сукцинимид-3-ил-N)-CH2CH2-C(=O)-GGFG-NH-CH2CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2CH2CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2-O-CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2-O-CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2-C(=O)-(NH-DX).
В приведенных выше фрагментах, -(сукцинимид-3-ил-N)- имеет структуру, представленную следующей формулой:
,
которая присоединена к антителу в ее положении 3 и присоединена к метиленовой группе в линкерной структуре, имея эту структуру на атоме азота в положении 1, и
-(NH-DX) представляет группу, представленную следующей формулой:
,
где атом азота аминогруппы в положении 1 является положением присоединения.
[24] Конъюгат антитело-лекарственное средство по пункту [23], где фрагмент лекарственное средство-линкерная структура, имеющий лекарственное средство, присоединенное к -L1-L2-LP-NH-(CH2)n1-La-Lb-Lc-, представляет собой один фрагмент лекарственное средство-линкерная структура, выбранный из следующей группы:
-(сукцинимид-3-ил-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2-O-CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2-O-CH2-C(=O)-(NH-DX),
-(сукцинимид-3-ил-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX).
В приведенных выше фрагментах, -(сукцинимид-3-ил-N)- имеет структуру, представленную следующей формулой:
,
которая присоединена к антителу в ее положении 3 и присоединена к метиленовой группе в линкерной структуре, имея эту структуру на атоме азота в положении 1, и
-(NH-DX) представляет группу, представленную следующей формулой:
где атом азота аминогруппы в положении 1 является положением присоединения.
[25] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[24], где среднее число единиц выбранного одного фрагмента лекарственное средство-линкерная структура, конъюгированного с одним антителом, находится в диапазоне от 1 до 10.
[26] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[24], где среднее число единиц выбранного одного фрагмента лекарственное средство-линкерная структура, конъюгированного с одним антителом, находится в диапазоне от 2 до 8.
[27] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[24], где среднее число единиц выбранного одного фрагмента лекарственное средство-линкерная структура, конъюгированного с одним антителом, находится в диапазоне от 3 до 8.
[28] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[27], где антитело представляет собой антитело, обладающее одним или более из свойств, таких как распознавание клетки-мишени, связывание клетки-мишени, интернализация в клетке-мишени и повреждение клетки-мишени.
[29] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[27], где клетка, которая является мишенью для конъюгата антитело-лекарственное средство, представляет собой опухолевую клетку.
[30] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[27], где антитело представляет собой анти-A33 антитело, анти-B7-H3 антитело, анти-CanAg антитело, анти-CD20 антитело, анти-CD22 антитело, анти-CD30 антитело, анти-CD33 антитело, анти-CD56 антитело, анти-CD70 антитело, анти-CEA антитело, анти-Cripto антитело, анти-EphA2 антитело, анти-G250 антитело, анти-MUC1 антитело, анти-GPNMB антитело, анти-интегрин антитело, анти-PSMA антитело, анти-тенасцин-C антитело, анти-SLC44A4 антитело или анти-мезотелин антитело.
[31] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[27], где антитело представляет собой анти-B7-H3 антитело, анти-CD30 антитело, анти-CD33 антитело или анти-CD70 антитело.
[32] Конъюгат антитело-лекарственное средство по любому из пунктов [1]-[27], где антитело представляет собой анти-B7-H3 антитело.
[33] Лекарственное средство, содержащее конъюгат антитело-лекарственное средство по любому из пунктов [1]-[32], его соль или его гидрат.
[34] Противоопухолевое лекарственное средство и/или противораковое лекарственное средство, содержащее конъюгат антитело-лекарственное средство по любому из пунктов [1]-[32], его соль или его гидрат.
[35] Противоопухолевое лекарственное средство и/или противораковое лекарственное средство по пункту [34], которое применяют при лечении рака легких, рака почки, рака уротелия, колоректального рака, рака предстательной железы, мультиформной глиобластомы, рака яичников, рака поджелудочной железы, рака молочной железы, меланомы, рака печени, рака мочевого пузыря, рака желудка или рака пищевода.
[36] Фармацевтическая композиция, содержащая конъюгат антитело-лекарственное средство по любому из пунктов [1]-[32], его соль или его гидрат в качестве активного компонента, и фармацевтически приемлемый компонент, используемый в качестве вспомогательного вещества.
[37] Фармацевтическая композиция по пункту [36], которую применяют при лечении рака легких, рака почки, рака уротелия, колоректального рака, рака предстательной железы, мультиформной глиобластомы, рака яичников, рака поджелудочной железы, рака молочной железы, меланомы, рака печени, рака мочевого пузыря, рака желудка или рака пищевода.
[38] Способ лечения опухоли и/или рака, включающий введение конъюгата антитело-лекарственное средство по любому из пунктов [1]-[32], его соль или его гидрат.
[39] Промежуточное соединение лекарственное средство-линкер, представленное следующей формулой:
Q-(CH2)nQ-C(=O)-L2a-LP-NH-(CH2)n1-La-Lb-Lc-(NH-DX).
В этой формуле, Q представляет (малеимид-N-ил)-, HS-, X-CH2-C(=O)-NH- или (пирролидин-2,5-дион-N-ил)-O-C(=O)-,
X представляет атом брома или атом йода,
nQ представляет целое число от 2 до 8,
L2a представляет -NH-(CH2-CH2-O)n5-CH2-CH2-C(=O)- или одинарную химическую связь,
где n5 представляет целое число от 1 до 6,
LP представляет пептидный остаток, состоящий от 2 до 7 аминокислот, выбранных из фенилаланина, глицина, валина, лизина, цитруллина, серина, глутаминовой кислоты и аспарагиновой кислоты,
n1 представляет целое число от 0 до 6,
La представляет -C(=O)-NH-, -NR1-(CH2)n7-, -O- или одинарную химическую связь,
где n7 представляет целое число от 1 до 6, R1 представляет атом водорода, алкильную группу, имеющую от 1 до 6 углеродных атомов, -(CH2)n8-COOH или -(CH2)n9-OH, n8 представляет целое число от 1 до 4, n9 представляет целое число от 1 до 6,
Lb представляет -CR2(-R3)-, -O-, -NR4- или одинарную химическую связь,
где R2 и R3 каждый независимо представляет атом водорода, алкильную группу, имеющую от 1 до 6 углеродных атомов, -(CH2)na-NH2, -(CH2)nb-COOH или -(CH2)nc-OH, R4 представляет атом водорода или алкильную группу, имеющую от 1 до 6 углеродных атомов, na представляет целое число от 0 до 6, nb представляет целое число от 1 до 4, nc представляет целое число от 1 до 4, при условии, что когда na равняется 0, R2 и R3 не являются одинаковыми,
Lc представляет -CH2- или -C(=O)-,
(малеимид-N-ил)- представляет собой группу, представленную следующей формулой:
,
где атом азота является положением присоединения,
(пирролидин-2,5-дион-N-ил) представляет собой группу, представленную следующей формулой:
,
где атом азота является положением присоединения, и -(NH-DX) представляет собой группу, представленную следующей формулой:
,
где атом азота аминогруппы в положении 1 является положением присоединения.
[40] Промежуточное соединение лекарственное средство-линкер по пункту [39], где Lc представляет собой -C(=O)-.
[41] Промежуточное соединение лекарственное средство-линкер по пункту [39] или [40], где LP представляет собой пептидный остаток, состоящий из 4 аминокислот.
[42] Промежуточное соединение лекарственное средство-линкер по любому из пунктов [39]-[41], где LP представляет собой -GGFG-.
[43] Промежуточное соединение лекарственное средство-линкер по любому из пунктов [39]-[42], где -NH-(CH2)n1-La-Lb- представляет собой
-NH-CH2CH2-,
-NH-CH2CH2CH2-,
-NH-CH2CH2CH2CH2-,
-NH-CH2CH2CH2CH2CH2-,
-NH-CH2-O-CH2- или
-NH-CH2CH2-O-CH2-.
[44] Промежуточное соединение лекарственное средство-линкер по любому из пунктов [39]-[42], где -NH-(CH2)n1-La-Lb- представляет собой
-NH-CH2CH2CH2-,
-NH-CH2-O-CH2- или
-NH-(CH2)2-O-CH2-.
[45] Промежуточное соединение лекарственное средство-линкер по любому из пунктов [39]-[44], где nQ представляет собой целое число от 2 до 6.
[46] Промежуточное соединение лекарственное средство-линкер по пункту [43], где
Q представляет собой (малеимид-N-ил)-,
nQ представляет собой целое число от 2 до 5, и
L2a представляет собой одинарную химическую связь.
[47] Промежуточное соединение лекарственное средство-линкер по пункту [44], где
Q представляет собой (малеимид-N-ил)-,
nQ представляет собой целое число от 2 до 5, и
L2a представляет собой одинарную химическую связь.
[48] Промежуточное соединение лекарственное средство-линкер по любому из пунктов [39]-[42], где
Q представляет с