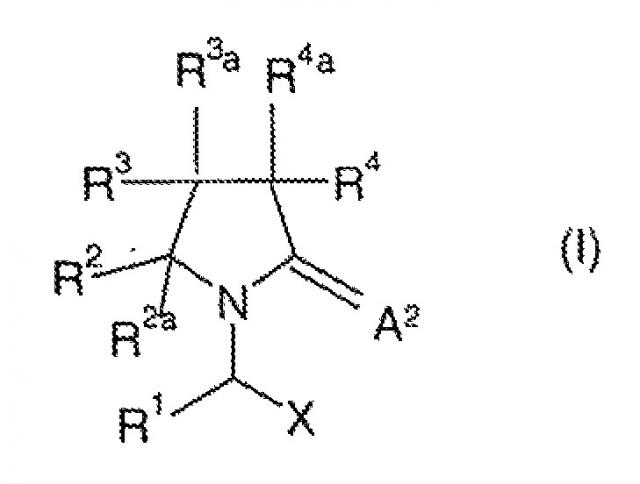
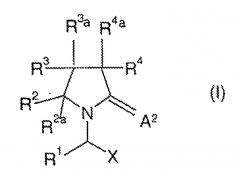
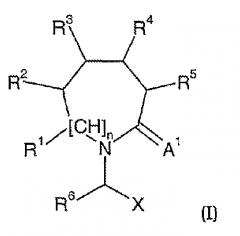
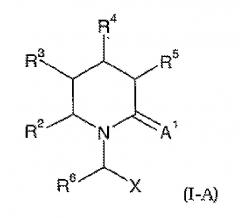
Способы и композиции для улучшения когнитивных функций
Иллюстрации
Показать всеГруппа изобретений относится к медицине, а именно к неврологии и психиатрии, и может быть использована для лечения когнитивного нарушения, связанного с расстройством центральной нервной системы (ЦНС), у субъекта, нуждающегося в этом или находящегося в группе риска его возникновения. При этом расстройством ЦНС является вызывающее потерю памяти умеренное когнитивное нарушение, деменция, болезнь Альцгеймера (AD), продромальная фаза AD, посттравматическое стрессовое расстройство (PTSD), шизофрения, боковой амиотрофический склероз (ALS) или когнитивное нарушение, связанное с противоопухолевой терапией. Предложены способы лечения, задержки или замедления прогрессирования когнитивного нарушения, связанного с расстройством центральной нервной системы (ЦНС), а также уменьшения скорости снижения когнитивных способностей при указанном состоянии, включающие стадию введения указанному субъекту леветирацетама или его фармацевтически приемлемой соли в количестве 125-250 мг в день. Предложены также фармацевтические композиции для перорального введения один раз в сутки, предназначенные для осуществления способов, содержащие 125-250 мг леветирацетама или его фармацевтически приемлемой соли, где леветирацетам или его фармацевтически приемлемая соль находится в форме, подходящей для пролонгированного высвобождения. Группа изобретений обеспечивает улучшение или нормализацию когнитивных функций у субъекта с расстройством ЦНС, а также предотвращение или замедление прогрессирования указанного расстройства ЦНС, сопровождающегося когнитивными нарушениями. 6 н. и 1 з.п. ф-лы, 28 ил., 6 табл., 3 пр.
Реферат
В настоящей заявке испрашивается приоритет и преимущество предварительной заявки на патент США № 61/441251, поданной 9 февраля 2011 г, содержание и описание которой во всей своей полноте включены в настоящее описание посредством ссылки.
Область техники, к которой относится изобретение
Настоящее изобретение относится к способам и композициям для лечения расстройств центральной нервной системы (CNS, ЦНС), сопровождающихся когнитивными нарушениями. В частности, настоящее изобретение относится к применению ингибиторов гликопротеина синаптических везикул 2А (SV2A), как отдельно, так и в комбинации с вальпроатом, при лечении расстройств центральной нервной системы (ЦНС), которые сопровождаются когнитивными нарушениями, у пациента, нуждающегося в подобном лечении или находящегося в группе риска развития подобных расстройств, в том числе, без ограничений, при лечении пациентов, имеющих или находящихся в группе риска развития возрастного когнитивного нарушения, умеренного когнитивного нарушения (MCI), вызывающего потерю памяти умеренного когнитивного нарушения (aMCI), возрастного ухудшения памяти (AAMI), возрастного снижения когнитивных способностей (ARCD), слабоумия, болезни Альцгеймера (AD), продромальной фазы болезни Альцгеймера, посттравматического стрессового расстройства (PTSD), шизофрении, бокового амиотрофического склероза и когнитивного нарушения, связанного с противоопухолевой терапией.
Уровень техники
Когнитивные способности могут снижаться как нормальное следствие старения организма или как последствие расстройства ЦНС.
Значительная часть пожилого населения испытывает снижение когнитивных способностей, которое превышает снижение когнитивных способностей, характерное для обычного старения. Подобная возрастная потеря когнитивных функций клинически характеризуется прогрессирующей потерей памяти, ухудшением мыслительного процесса, снижением уровня интеллектуальной деятельности и потерей способности связывать слова или понятия. Умеренное когнитивное нарушение (MCI), возрастное ухудшение памяти (AAMI), возрастное снижение когнитивных способностей (ARCD) или расстройства, выделяемые в сходную клиническую группу, относятся к тем расстройствам, которые связаны с подобным возрастным снижением когнитивных функций. По некоторым оценкам, только в США насчитывается более 16 миллионов людей с AAMI (Barker et al., 1995), а MCI, по оценкам, затрагивает 5,5-7 миллионов людей в США в возрасте старше 65 лет (Plassman et al., 2008).
Другие расстройства центральной нервной системы (ЦНС), такие как слабоумие, болезнь Альцгеймера (AD), продромальная фаза болезни Альцгеймера, посттравматическое стрессовое расстройство (PTSD), шизофрения, боковой амиотрофический склероз и когнитивное нарушение, связанное с противоопухолевой терапией, также сопровождаются ухудшением когнитивных способностей.
Таким образом, существует потребность в эффективном лечении расстройств центральной нервной системы (ЦНС), сопровождающихся когнитивными нарушениями, и в улучшения когнитивных функций у пациентов с диагнозом возрастного когнитивного нарушения, MCI, вызывающего потерю памяти MCI, AAMI, ARCD, слабоумия, AD, продромальной фазы болезни Альцгеймера, PTSD, шизофрении, бокового амиотрофического склероза (ALS), когнитивного нарушения, связанного с противоопухолевой терапией, и аналогичных расстройств центральной нервной системы (ЦНС), сопровождающихся ухудшением когнитивных способностей, или существует потребность в лечении пациентов, находящихся в группе риска развития подобных нарушений.
Сущность изобретения
В соответствии с первым аспектом настоящего изобретения, предлагается способ лечения или улучшения когнитивных функций, способ задержки или замедления прогрессирования когнитивных нарушений или способ уменьшения скорости снижения когнитивных способностей у субъекта, страдающего от расстройства центральной нервной системы (ЦНС), которое сопровождается когнитивными нарушениями, или находящегося в группе риска возникновения подобного расстройства, при этом способ включает стадию введения указанному субъекту терапевтически эффективного количества ингибитора SV2A или его фармацевтически приемлемой соли, гидрата, сольвата или полиморфной модификации. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы улучшают или нормализуют когнитивные функции у указанного субъекта. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы задерживают или замедляют прогрессирование когнитивных нарушений у указанного субъекта. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы уменьшают скорость снижения когнитивных функций у указанного субъекта. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы предотвращают или замедляют прогрессирование указанного расстройства ЦНС, сопровождающегося когнитивными нарушениями, у указанного субъекта. В других связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы облегчают, снижают интенсивность симптомов или замедляют прогрессирование одного или нескольких симптомов, связанных с указанным расстройством ЦНС, которое сопровождается когнитивными нарушениями, у указанного субъекта.
В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения расстройство ЦНС, сопровождающееся когнитивными нарушениями, представляет собой возрастное когнитивное нарушение, такое, как умеренное когнитивное нарушение (MCI), возрастное ухудшение памяти (AAMI), возрастное снижение когнитивных способностей (ARCD). В одном связанном с данным аспектом варианте осуществления настоящего изобретения MCI представляет собой вызывающее потерю памяти умеренное когнитивное нарушение. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения расстройство ЦНС, сопровождающееся когнитивными нарушениями, представляет собой слабоумие, болезнь Альцгеймера (AD), продромальную фазу болезни Альцгеймера, посттравматическое стрессовое расстройство (PTSD), шизофрению, боковой амиотрофический склероз (ALS) или когнитивное нарушение, связанное с противоопухолевой терапией. В одном связанном с данным аспектом варианте осуществления настоящего изобретения субъектом, страдающим от подобного расстройства ЦНС или когнитивного нарушения, является пациент-человек.
Ингибитор SV2A или его фармацевтически приемлемая соль, гидрат, сольват или полиморфная модификация, которые пригодны для использования в способах и композициях, в соответствии с данным аспектом настоящего изобретения, включают такие, которые описаны, например, в заявке на патент США 12/580464, международной заявке PCT/US2009/005647, заявке на патент США 61/105847, заявке на патент США 61/152631 и заявке на патент США 61/175536. Тем не менее, в способах и композициях, в соответствии с данным аспектом настоящего изобретения, может быть использован любой ингибитор SV2A или его фармацевтически приемлемая соль, гидрат, сольват или полиморфная модификация. В других вариантах осуществления настоящего изобретения ингибитор SV2A выбран из группы ингибиторов SV2A, указанных в международных патентных заявках WO2010/144712; WO2010/002869; WO2008/132139; WO2007/065595; WO2006/128693; WO2006/128692; WO2005/054188; WO2004/087658; WO2002/094787; WO2001/062726; патентах США №№ 7465549; 7244747; 5334720; 4696943; 4696942; заявках на патент США с номерами 20090312333; 20090018148; 20080081832; 2006258704; и патентах Великобритании №№ 1039113 и 1309692, или их фармацевтически приемлемых солей, гидратов, сольватов или полиморфных модификаций. В других вариантах осуществления настоящего изобретения ингибитор SV2A выбран из группы, которая включает леветирацетам, бриварацетам и селетрацетам или их производные, или аналоги, или их фармацевтически приемлемые соли, гидраты, сольваты или полиморфные модификации. В других вариантах осуществления настоящего изобретения ингибитором SV2A является леветирацетам или его производное, или его аналог, или его фармацевтически приемлемая соль, гидрат, сольват или полиморфная модификация. В других вариантах осуществления настоящего изобретения ингибитором SV2A является бриварацетам или его производное, или его аналог, или его фармацевтически приемлемая соль, гидрат, сольват или полиморфная модификация. В других вариантах осуществления настоящего изобретения ингибитором SV2A является селетрацетам или его производное, или его аналог, или его фармацевтически приемлемая соль, гидрат, сольват или полиморфная модификация.
В других связанных с данным аспектом вариантах осуществления настоящего изобретения указанный ингибитор SV2A или его фармацевтически приемлемую соль, гидрат, сольват или полиморфную модификацию можно вводить с дозами, как описано, например, в заявке на патент США 12/580464, международной патентной заявке PCT/US2009/005647, заявке на патент США 61/105847, заявке на патент США 61/152631, заявке на патент США 61/175536 и заявке на патент США 61/441251. В других связанных с данным аспектом вариантах осуществления настоящего изобретения указанный ингибитор SV2A или его фармацевтически приемлемую соль, гидрат, сольват или полиморфную модификацию вводят раз в 12 или 24 часа с суточной дозой приблизительно от 0,1 до 0,2 мг/кг, или приблизительно от 0,01 до 2,5 мг/кг, или приблизительно от 0,1 до 2,5 мг/кг, или приблизительно от 0,4 до 2,5 мг/кг, или приблизительно от 0,6 до 1,8 мг/кг, или приблизительно от 0,04 до 2,5 мг/кг, или приблизительно от 0,06 до 1,8 мг/кг, или приблизительно от 2,0 до 4,0 мг/кг, или приблизительно от 2,0 до 3,0 мг/кг, или приблизительно от 3,0 до 4,0 мг/кг, или приблизительно от 0,2 до 0,4 мг/кг, или приблизительно от 0,2 до 0,3 мг/кг, или приблизительно от 0,3 до 0,4 мг/кг, или приблизительно 0,001-5 мг/кг, или приблизительно 0,001-0,5 мг/кг, или приблизительно 0,01-0,5 мг/кг.
В соответствии со вторым аспектом настоящего изобретения, предлагается способ лечения или улучшения когнитивных функций, способ задержки или замедления прогрессирования когнитивного нарушения или способ уменьшения скорости снижения когнитивных способностей у субъекта, страдающего от расстройства центральной нервной системы (ЦНС), которое сопровождается когнитивными нарушениями, или находящегося в группе риска возникновения подобного расстройства, при этом способ включает стадию введения указанному субъекту терапевтически эффективного количества ингибитора SV2A или его фармацевтически приемлемой соли, гидрата, сольвата или полиморфной модификации в комбинации с вальпроатом, или его аналогом, производным или его фармацевтически приемлемой солью. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы улучшают или нормализуют когнитивные функции у указанного субъекта. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы задерживают или замедляют прогрессирование когнитивных нарушений у указанного субъекта. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы уменьшают скорость снижения когнитивных функций у указанного субъекта. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы предотвращают или замедляют прогрессирование указанного расстройства ЦНС, сопровождающегося когнитивными нарушениями, у указанного субъекта. В других связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы облегчают, снижают интенсивность симптомов или замедляют прогрессирование одного или нескольких симптомов, связанных с указанным расстройством ЦНС, которое сопровождается когнитивными нарушениями, у указанного субъекта.
В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанный ингибитор SV2A и/или вальпроат вводят в дозах, которые являются субтерапевтическими, по сравнению с дозами, при которых указанные соединения являются терапевтически эффективными при введении каждого вещества в отсутствие другого.
В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения расстройство ЦНС, сопровождающееся когнитивными нарушениями, представляет собой возрастное когнитивное нарушение, такое как умеренное когнитивное нарушение (MCI), возрастное ухудшение памяти (AAMI), возрастное снижение когнитивных способностей (ARCD). В одном связанном с данным аспектом варианте осуществления настоящего изобретения MCI представляет собой вызывающее потерю памяти умеренное когнитивное нарушение. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения расстройство ЦНС, сопровождающееся когнитивными нарушениями, представляет собой слабоумие, болезнь Альцгеймера (AD), продромальную фазу болезни Альцгеймера, посттравматическое стрессовое расстройство (PTSD), шизофрению или когнитивное нарушение, связанное с противоопухолевой терапией. В одном варианте осуществления настоящего изобретения субъектом, страдающим от подобного когнитивного нарушения, является пациент-человек.
Ингибитор SV2A или его фармацевтически приемлемая соль, гидрат, сольват или полиморфная модификация, которые пригодны для использования в способах и композициях, в соответствии с данным аспектом настоящего изобретения, включают такие, которые описаны, например, в заявке на патент США 12/580464, международной заявке PCT/US2009/005647, заявке на патент США 61/105847, заявке на патент США 61/152631, заявке на патент США 61/175536 и заявке на патент США 61/441251. Тем не менее, в способах и композициях, в соответствии с данным аспектом настоящего изобретения, может быть использован любой ингибитор SV2A или его фармацевтически приемлемая соль, гидрат, сольват или полиморфная модификация. В других вариантах осуществления настоящего изобретения ингибитор SV2A выбран из группы ингибиторов SV2A, указанных в международных патентных заявках WO2010/144712; WO2010/002869; WO2008/132139; WO2007/065595; WO2006/128693; WO2006/128692; WO2005/054188; WO2004/087658; WO2002/094787; WO2001/062726; патентах США №№ 7465549; 7244747; 5334720; 4696943; 4696942; заявках на патент США с номерами 20090312333; 20090018148; 20080081832; 2006258704; и патентах Великобритании №№ 1039113 и 1309692, или из их фармацевтически приемлемых солей, гидратов, сольватов или полиморфных модификаций. В других вариантах осуществления настоящего изобретения ингибитор SV2A выбран из группы, которая включает леветирацетам, бриварацетам и селетрацетам или их производные, или аналоги, или их фармацевтически приемлемые соли, гидраты, сольваты или полиморфные модификации. В других вариантах осуществления настоящего изобретения ингибитором SV2A является леветирацетам или его производное, или его аналог, или его фармацевтически приемлемая соль, гидрат, сольват или полиморфная модификация. В других вариантах осуществления настоящего изобретения ингибитором SV2A является бриварацетам или его производное, или его аналог, или его фармацевтически приемлемая соль, гидрат, сольват или полиморфная модификация. В других вариантах осуществления настоящего изобретения ингибитором SV2A является селетрацетам или его производное, или его аналог, или его фармацевтически приемлемая соль, гидрат, сольват или полиморфная модификация.
В других связанных с данным аспектом вариантах осуществления настоящего изобретения указанный ингибитор SV2A или его фармацевтически приемлемую соль, гидрат, сольват или полиморфную модификацию, который вводят в комбинации с вальпроатом или его аналогом, производным или его фармацевтически приемлемой солью, можно вводить с дозами, которые раскрываются, например, в заявке на патент США 12/580464, международной патентной заявке PCT/US2009/005647, заявке на патент США 61/105847, заявке на патент США 61/152631, заявке на патент США 61/175536 и заявке на патент США 61/441251. В других связанных с данным аспектом вариантах осуществления настоящего изобретения указанный ингибитор SV2A или его фармацевтически приемлемую соль, гидрат, сольват или полиморфную модификацию, который вводят в комбинации с вальпроатом или его аналогом, производным или его фармацевтически приемлемой солью, вводят раз в 12 или 24 часа с суточной дозой приблизительно от 0,01 до 1 мг/кг, или приблизительно от 0,001 до 1 мг/кг, или приблизительно от 0,1 мг/кг до 5 мг/кг, или приблизительно от 0,05 мг/кг до 0,5 мг/кг.
В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения вальпроат или его аналог, производное или его фармацевтически приемлемая соль, который вводят в комбинации с ингибитором SV2A или его фармацевтически приемлемой солью, гидратом, сольватом или полиморфной модификацией, вводят с суточной дозой таким образом, чтобы общее содержание вальпроата в плазме крови субъекта поддерживалось на уровне от 0,5 до 5 мкг/мл.
В других связанных с данным аспектом вариантах осуществления настоящего изобретения указанный ингибитор SV2A или его фармацевтически приемлемую соль, гидрат, сольват или полиморфную модификацию и вальпроат или его аналог, производное или его фармацевтически приемлемую соль вводят одновременно или последовательно, или в виде одной композиции, или в виде отдельных композиций, находящихся в одной упаковке. В других связанных с данным аспектом вариантах осуществления настоящего изобретения указанный ингибитор SV2A или его фармацевтически приемлемую соль, гидрат, сольват или полиморфную модификацию и вальпроат или его аналог, производное или его фармацевтически приемлемую соль вводят по различным маршрутам. Используемый здесь термин "комбинация" включает введение любого из указанных препаратов или использование любых путей введения.
В соответствии с третьим аспектом настоящего изобретения, предлагается фармацевтическая композиция, содержащая ингибитор SV2A или его фармацевтически приемлемую соль. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанный ингибитор SV2A присутствует в количестве 0,07-60 мг, 0,07-350 мг, 25-60 мг, 25-125 мг, 50-250 мг, 5-140 мг, 0,7-180 мг, 125-240 мг, 3-50 мг или 3-60 мг. В других связанных с данным аспектом вариантах осуществления настоящего изобретения указанный ингибитор SV2A присутствует в количестве 0,05-35 мг.
В соответствии с четвертым аспектом настоящего изобретения, предлагается фармацевтическая композиция, содержащая ингибитор SV2A или его фармацевтически приемлемую соль в комбинации с вальпроатом или его аналогом, производным или его фармацевтически приемлемой солью. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанный ингибитор SV2A или его фармацевтически приемлемая соль присутствует в количестве 0,05-35 мг, 0,07-60 мг, 0,07-350 мг, 25-60 мг, 25-125 мг, 50-250 мг, 5-15 мг, 5-30 мг, 5-140 мг, 0,7-180 мг, 125-240 мг, 3-50 мг или 0,07-50 мг, или 3-60 мг. В других связанных с данным аспектом вариантах осуществления настоящего изобретения количество ингибитора SV2A или его фармацевтически приемлемой соли, гидрата, сольвата или полиморфной модификации составляет меньше чем 350 мг, меньше чем 250 мг, меньше чем 200 мг, меньше чем 150 мг, меньше чем 100 мг, меньше чем 50 мг, меньше чем 35 мг, меньше чем 10 мг, меньше чем 5 мг, меньше чем 1 мг, меньше чем 0,5 мг, меньше чем 0,1 мг, меньше чем 0,07 мг или меньше чем 0,05 мг.
В соответствии с пятым аспектом настоящего изобретения, предлагается способ лечения или улучшения когнитивных функций, способ задержки или замедления прогрессирования когнитивных нарушений или способ уменьшения скорости снижения когнитивных способностей у субъекта, страдающего от расстройства центральной нервной системы (ЦНС), которое сопровождается когнитивными нарушениями, или находящегося в группе риска возникновения подобного расстройства, при этом способ включает стадию введения указанному субъекту терапевтически эффективного количества леветирацетама или его фармацевтически приемлемой соли. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы улучшают или нормализуют когнитивные функции у указанного субъекта. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы задерживают или замедляют прогрессирование когнитивных нарушений у указанного субъекта. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы уменьшают скорость снижения когнитивных функций у указанного субъекта. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы предотвращают или замедляют прогрессирование указанного расстройства ЦНС, сопровождающегося когнитивными нарушениями, у указанного субъекта. В других связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы облегчают, снижают интенсивность симптомов или замедляют прогрессирование одного или нескольких симптомов, связанных с указанным расстройством ЦНС, которое сопровождается когнитивными нарушениями, у указанного субъекта.
В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения расстройство ЦНС, сопровождающееся когнитивными нарушениями, представляет собой возрастное когнитивное нарушение, такое, как умеренное когнитивное нарушение (MCI), возрастное ухудшение памяти (AAMI), возрастное снижение когнитивных способностей (ARCD). В одном связанном с данным аспектом варианте осуществления настоящего изобретения MCI представляет собой вызывающее потерю памяти умеренное когнитивное нарушение. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения расстройство ЦНС, сопровождающееся когнитивными нарушениями, представляет собой слабоумие, болезнь Альцгеймера (AD), продромальную фазу болезни Альцгеймера, посттравматическое стрессовое расстройство (PTSD), шизофрению или когнитивное нарушение, связанное с противоопухолевой терапией. В одном варианте осуществления настоящего изобретения субъектом, страдающим от подобного когнитивного нарушения, является пациент-человек.
В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения леветирацетам или его фармацевтически приемлемую соль, гидрат, сольват или полиморфную модификацию вводят раз в 12 или 24 часа с суточной дозой приблизительно от 1 до 2 мг/кг, или приблизительно от 0,1 до 2,5 мг/кг, или приблизительно от 0,4 до 2,5 мг/кг, или приблизительно от 0,6 до 1,8 мг/кг, или приблизительно от 2,0 до 3,0 мг/кг, или приблизительно от 3,0 до 4,0 мг/кг, или приблизительно от 2,0 до 4,0 мг/кг, или приблизительно 0,1-5 мг/кг, или приблизительно от 70 до 140 мг, или приблизительно от 7 до 180 мг, или приблизительно 25-180 мг, или приблизительно от 40 до 130 мг, или приблизительно от 140 до 300 мг, или приблизительно от 200 до 300 мг, или приблизительно от 140 до 200 мг, или приблизительно 7-350 мг.
В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения леветирацетам или его фармацевтически приемлемую соль, гидрат, сольват или полиморфную модификацию вводят раз в 12 или 24 часа с суточной дозой в соответствии с одним из ежедневных интервалов дозировок, обозначенных как "+", которые приведены в таблице 1 или таблице 2.
В соответствии с шестым аспектом настоящего изобретения, предлагается способ лечения или улучшения когнитивных функций, способ задержки или замедления прогрессирования когнитивных нарушений или способ уменьшения скорости снижения когнитивных способностей у субъекта, страдающего от расстройства центральной нервной системы (ЦНС), которое сопровождается когнитивными нарушениями, или находящегося в группе риска возникновения подобного расстройства, при этом способ включает стадию введения указанному субъекту терапевтически эффективного количества бриварацетама или его фармацевтически приемлемой соли. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы улучшают или нормализуют когнитивные функции у указанного субъекта. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы задерживают или замедляют прогрессирование когнитивных нарушений у указанного субъекта. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы уменьшают скорость снижения когнитивных функций у указанного субъекта. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы предотвращают или замедляют прогрессирование указанного расстройства ЦНС, сопровождающегося когнитивными нарушениями, у указанного субъекта. В других связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы облегчают, снижают интенсивность симптомов или замедляют прогрессирование одного или нескольких симптомов, связанных с указанным расстройством ЦНС, которое сопровождается когнитивными нарушениями, у указанного субъекта.
В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения расстройство ЦНС, сопровождающееся когнитивными нарушениями, представляет собой возрастное когнитивное нарушение, такое, как умеренное когнитивное нарушение (MCI), возрастное ухудшение памяти (AAMI), возрастное снижение когнитивных способностей (ARCD). В одном связанном с данным аспектом варианте осуществления настоящего изобретения MCI представляет собой вызывающее потерю памяти умеренное когнитивное нарушение. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения расстройство ЦНС, сопровождающееся когнитивными нарушениями, представляет собой слабоумие, болезнь Альцгеймера (AD), продромальную фазу болезни Альцгеймера, посттравматическое стрессовое расстройство (PTSD), шизофрению или когнитивное нарушение, связанное с противоопухолевой терапией. В одном варианте осуществления настоящего изобретения субъектом, страдающим от подобного когнитивного нарушения, является пациент-человек.
В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения бриварацетам или его фармацевтически приемлемую соль, гидрат, сольват или полиморфную модификацию вводят раз в 12 или 24 часа с суточной дозой приблизительно от 0,1 до 0,2 мг/кг, или приблизительно от 0,01 до 2,5 мг/кг, или приблизительно от 0,04 до 2,5 мг/кг, или приблизительно от 0,06 до 1,8 мг/кг, или приблизительно от 0,2 до 0,4 мг/кг, или приблизительно от 7 до 15 мг, или приблизительно от 0,7 до 180 мг, или приблизительно от 2,5 до 180 мг, или приблизительно от 4,0 до 130 мг, или приблизительно от 14 до 30 мг.
В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения бриварацетам или его фармацевтически приемлемую соль, гидрат, сольват или полиморфную модификацию вводят раз в 12 или 24 часа с суточной дозой, по меньшей мере, 0,1 мг; 0,5 мг; 0,75 мг; 1,0 мг; 1,5 мг или 2,0 мг, но не более чем с суточной дозой 2,5 мг, 5 мг, 10 мг, 15 мг, 20 мг, 25 мг, 30 мг или 35 мг. В других вариантах осуществления настоящего изобретения бриварацетам или его фармацевтически приемлемую соль, гидрат, сольват или полиморфную модификацию вводят раз в 12 или 24 часа с суточной дозой, по меньшей мере, 0,0015 мг/кг, 0,0075 мг/кг, 0,01 мг/кг, 0,015 мг/кг, 0,02 мг/кг или 0,03 мг/кг, но не больше, чем с суточной дозой 0,5 мг/кг, 0,4 мг/кг, 0,3 мг/кг, 0,2 мг/кг, 0,15 мг/кг, 0,1 мг/кг, 0,05 мг/кг или 0,04 мг/кг.
В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения бриварацетам или его фармацевтически приемлемую соль, гидрат, сольват или полиморфную модификацию вводят раз в 12 или 24 часа с суточной дозой в соответствии с одним из интервалов ежедневных дозировок, обозначенных как "+", которые перечислены в таблице 3 или таблице 4. Например, бриварацетам или его фармацевтически приемлемую соль, гидрат, сольват или полиморфную модификацию можно вводить раз в 12 или 24 часа с суточной дозой 0,1-35 мг, 0,5-35 мг, 0,75-35 мг, 1,0-35 мг, 1,5-35 мг, 2,0-35 мг, 0,1-30 мг, 0,1-25 мг, 0,1-20 мг, 0,1-15 мг, 0,1-10 мг, 0,1-5 мг, 0,1-2,5 мг, 0,0015-0,5 мг/кг, 0,0075-0,5 мг/кг, 0,01-0,5 мг/кг, 0,015-0,5 мг/кг, 0,02-0,5 мг/кг, 0,03-0,5 мг/кг, 0,0015-0,4 мг/кг, 0,0015-0,3 мг/кг, 0,0015-0,2 мг/кг, 0,0015-0,15 мг/кг, 0,0015-0,1 мг/кг, 0,0015-0,05 мг/кг или 0,0015-0,04 мг/кг.
В соответствии с седьмым аспектом настоящего изобретения, предлагается способ лечения или улучшения когнитивных функций, способ задержки или замедления прогрессирования когнитивных нарушений или способ уменьшения скорости снижения когнитивных способностей у субъекта, страдающего от расстройства центральной нервной системы (ЦНС), которое сопровождается когнитивными нарушениями, или находящегося в группе риска возникновения подобного расстройства, при этом способ включает стадию введения указанному субъекту терапевтически эффективного количества селетрацетама или его фармацевтически приемлемой соли. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы улучшают или нормализуют когнитивные функции у указанного субъекта. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы задерживают или замедляют прогрессирование когнитивных нарушений у указанного субъекта. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы уменьшают скорость снижения когнитивных функций у указанного субъекта. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы предотвращают или замедляют прогрессирование указанного расстройства ЦНС, сопровождающегося когнитивными нарушениями, у указанного субъекта. В других связанных с данным аспектом вариантах осуществления настоящего изобретения указанные способы облегчают, снижают интенсивность симптомов или замедляют прогрессирование одного или нескольких симптомов, связанных с указанным расстройством ЦНС, которое сопровождается когнитивными нарушениями, у указанного субъекта.
В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения расстройство ЦНС, сопровождающееся когнитивными нарушениями, представляет собой возрастное когнитивное нарушение, такое, как умеренное когнитивное нарушение (MCI), возрастное ухудшение памяти (AAMI), возрастное снижение когнитивных способностей (ARCD). В одном связанном с данным аспектом варианте осуществления настоящего изобретения MCI представляет собой вызывающее потерю памяти умеренное когнитивное нарушение. В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения расстройство ЦНС, сопровождающееся когнитивными нарушениями, представляет собой слабоумие, болезнь Альцгеймера (AD), продромальную фазу болезни Альцгеймера, посттравматическое стрессовое расстройство (PTSD), шизофрению или когнитивное нарушение, связанное с противоопухолевой терапией. В одном варианте осуществления настоящего изобретения субъектом, страдающим от подобного когнитивного нарушения, является пациент-человек.
В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения селетрацетам или его фармацевтически приемлемую соль, гидрат, сольват или полиморфную модификацию вводят раз в 12 или 24 часа с суточной дозой, по меньшей мере, 0,1 мг, 0,5 мг, 0,75 мг, 1,0 мг, 1,5 мг или 2,0 мг, но не более чем с суточной дозой 2,5 мг, 5 мг, 10 мг, 15 мг, 20 мг, 25 мг, 30 мг или 35 мг. В других вариантах осуществления настоящего изобретения селетрацетам или его фармацевтически приемлемую соль, гидрат, сольват или полиморфную модификацию вводят раз в 12 или 24 часа с суточной дозой, по меньшей мере, 0,0015 мг/кг; 0,0075 мг/кг; 0,01 мг/кг; 0,015 мг/кг; 0,02 мг/кг или 0,03 мг/кг, но не больше, чем с суточной дозой 0,5 мг/кг, 0,4 мг/кг, 0,3 мг/кг, 0,2 мг/кг, 0,15 мг/кг, 0,1 мг/кг, 0,05 мг/кг или 0,04 мг/кг.
В некоторых связанных с данным аспектом вариантах осуществления настоящего изобретения селетрацетам или его фармацевтически приемлемую соль, гидрат, сольват или полиморфную модификацию вводят раз в 12 или 24 часа с суточной дозой в соответствии с одним из интервалов ежедневных дозировок, обозначенных как "+", которые перечислены в таблице 5 или таблице 6. Например, селетрацетам или его фармацевтически приемлемую соль, гидрат, сольват или полиморфную модификацию можно вводить раз в 12 или 24 часа с суточной дозой 0,1-35 мг, 0,5-35 мг, 0,75-35 мг, 1,0-35 мг, 1,5-35 мг, 2,0-35 мг, 0,1-30 мг, 0,1-25 мг, 0,1-20 мг, 0,1-15 мг, 0,1-10 мг, 0,1-5 мг, 0,1-2,5 мг, 0,0015-0,5 мг/кг, 0,0075-0,5 мг/кг, 0,01-0,5 мг/кг, 0,015-0,5 мг/кг, 0,02-0,5 мг/кг, 0,03-0,5 мг/кг, 0,0015-0,4 мг/кг, 0,0015-0,3 мг/кг, 0,0015-0,2 мг/кг, 0,0015-0,15 мг/кг, 0,0015-0,1 мг/кг, 0,0015-0,05 мг/кг или 0,0015-0,04 мг/кг.
Краткое описание чертежей
Фиг. 1 показывает повышенную экспрессию мРНК гена, кодирующего SV2A в зубчатой извилине гиппокампа у крыс с возрастными нарушениями (AI), по сравнению с молодыми крысами (Y) и взрослыми крысами без нарушений (AU). Нормированные сигнальные значения набора зондов фирмы Affymetrix GeneChip (ось Y), как мера экспрессии мРНК, представлены для различных крыс в зависимости от показателей обучения, как меры когнитивных нарушений.
На фигуре 2 показано влияние введения леветирацетама на сохранение пространственной памяти у шести крыс с возрастными нарушениями (AI) при проведении теста в водном лабиринте Морриса (MWM). Использовали три условия обработки: введение носителя в качестве контроля, ведение леветирацетама (5 мг/кг/день) и ведение леветирацетама (10 мг/кг/день). AI крыс обучали в течение двух дней подряд и раз в день перед проведением испытаний подвергали однократной обработке. По прошествии 24 часов провели тестирование крыс AI. Время, которое AI крысы, по прошествии 24 часов после обработки в различных условиях и двух дней обучения, проводили, плавая в заданном секторе или в заданной кольцевой зоне при проведении испытаний на сохранение в памяти, использовали в качестве меры сохранения пространственной памяти. Заданный сектор является сектором лабиринта (который представлял собой круглый бассейн), где в процессе подготовки испытаний располагалась площадка для спасения. Заданная кольцевая зона относится к точному расположению площадки для спасения во время подготовки к проведению испытаний.
На фиг. 3 показано влияние введения леветирацетама на сохранение пространственной памяти у десяти крыс с возрастными нарушениями (AI) в тесте с использованием радиального восьмирукавного лабиринта (RAM). Использовали шесть условий обработки: введение носителя в качестве контроля, введение леветирацетама (1,25 мг/кг), леветирацетама (2,5 мг/кг), леветирацетама (5 мг/кг), леветирацетама (10 мг/кг) и леветирацетама (20 мг/кг). В задании с использованием RAM применяли одночасовую задержку между презентацией подмножества рукавов (5 рукавов доступны и 3 рукава заблокированы) и завершением задания на извлечение и перемещение в восьми рукавах (доступно восемь рукавов). За 30-40 мин до проведения испытаний крыс предварительно подвергали однократной обработке с помощью лекарства или контроля. Количество ошибок, сделанных крыс после задержки, использовали в качестве меры сохранения пространственной памяти. Ошибки определялись как случаи, когда крысы заходили в рукав, из которого пища уже была удалена в компоненте испытаний перед задержкой, или когда в сессии после задержки крысы повторно посещали рукав, который они уже посетили. Парные t-тесты используют для сравнения количества ошибок между различными дозами леветирацетама и носителя в виде контроля.
На фиг. 4 показано влияние раздельного введения леветирацетама или вальпроата на сохранение пространственной памяти у десяти крыс с возрастными нарушениями (AI) в тесте с использованием радиального восьмирукавного лабиринта (RAM).
На фиг. 5 показано влияние введения леветирацетама или в комбинации с вальпроатом на сохранение пространственной памяти у десяти крыс с возрастными нарушениями (AI) в тесте с использованием радиального восьмирукавного лабиринта (RAM).
На фиг. 6 представлена изоболограмма дозы леветирацетама против дозы вальпроата. Диагональная прямая линия является линией аддитивности с зафиксированной на каждой оси минимальной эффективной дозой вальпроата и леветирацетама, когда они оценивались по отдельности.
На фиг. 7 приведен план экспериментов по исследованию леветирацетама на людях.
На фиг. 8A показана средняя активность левой CA3 aMCI пациентов, получавших плацебо, и субъектов в подобранной по возрасту контрольной группе, получавших плацебо, во время презентации приманок в качестве раз