Способ лечения рака толстой кишки человека sw620 в эксперименте
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к противоопухолевой терапии, и может быть использовано для лечения рака толстой кишки человека SW620 в эксперименте на иммунодефицитных мышах. Для этого применяют производное индолокарбазола 6-амино-12-(α-L-арабинопиранозил)индало[2,3-а]пиролло[3,4-с]карбазол-5,7-диона, которое вводят в суммарных дозах 12,5-150 мг/кг. Изобретение обеспечивает лечение рака у иммунодефицитных мышей в эксперименте. 3 табл., 3 ил., 3 пр.
Реферат
Изобретение относится к медицине, а именно к противоопухолевой терапии, и касается способа лечения рака толстой кишки человека в эксперименте.
Известен способ лечения рака толстой кишки иринотеканом [Pitot Н.С., Wender D.B., M.J., Schroeder G., Goldberg R.M., Rubin J., MaiUiard J.A., Knost J.A., Ghosh C., Kirschling R.J., Levin R., Windschitl H.E. Phase II trial of irinotecan in patients with metastatic colorectal carcinoma // J din Oncol. 1997; 15(8): 2910-9]. При лечении диссеминированного рака толстой кишки иринотекан вызывает до 25% объективных эффектов, но его применение сопровождается дозолимитирующей гастроинтестинальной токсичностью [Противоопухолевая химиотерапия / Под ред. Роланда Т. Скила, пер. с англ. М., Гэотар-Медиа, 2011. - 1022 с.].
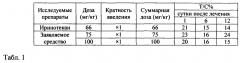
Сущность способа состоит в том, что иринотекан вводили внутривенно в однократной дозе 66 мг/кг иммунодефицитным мышам Balb/c nude с подкожными (п/к) ксенографтами рака толстой кишки человека SW620. [Sabatino М.А., Colombo Т., Geroni С., Marchini S., Broggini M. Enhancement of in vivo antitumor activity of classical anticancer agents by combination with the new, glutathione-interacting DNA minor groove-binder, brostallicin // Clin Cancer Res. 2003 Nov 1; 9(14): 5402-8]. Оценку эффективности иринотекана сравнивали с контрольной группой мышей без лечения, которым не вводили противоопухолевое средство, в динамике по стандартному показателю Т/С (treatment/control) - отношение размера опухоли у животных опытной группы к контрольной. Критерием эффективности являлось значение Т/С≤42%. Установлено, что после окончания терапии иринотеканом в дозе 66 мг/кг значение показателя Т/С=21-15-30% на 1, 6 и 12 сутки соответственно.
Недостатком прототипа является гастроинтестинальная токсичность, кратковременный максимальный противоопухолевый достоверный эффект только на 6-е сутки после окончания лечения на уровне Т/С=15% (р=0,0005).
Задачей изобретения является создание более эффективного и менее токсичного способа лечения рака толстой кишки человека в эксперименте.
Поставленная задача решается тем, что для лечения рака толстой кишки человека SW620 в эксперименте применяется производное индолокарбазола - ингибитора топоизомераз, тормозящего репликацию ДНК - 6-амино-12-(α-L-арабинопиранозил)индоло[2,3-а]пиролло[3,4-с]карбазол-5,7-дион.
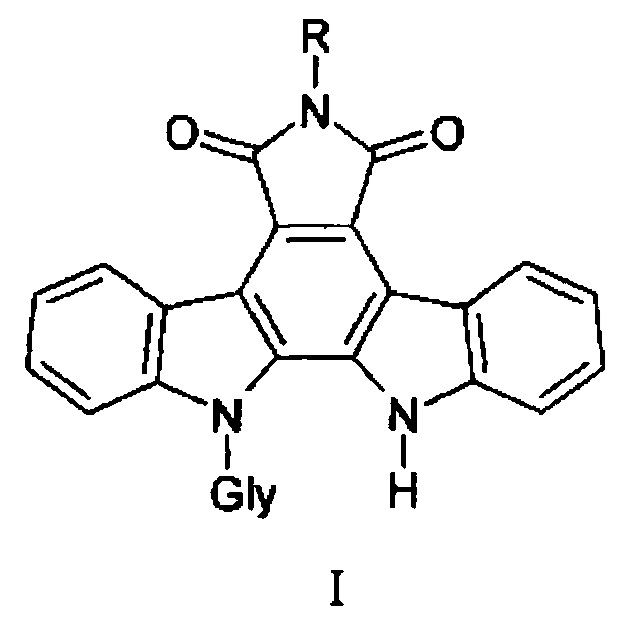
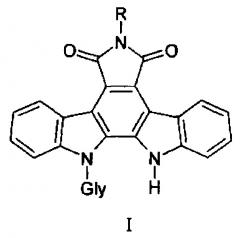
Данное соединение относится к производным индолокарбазола общей формулы 1.
где Gly - остатки пентоз (L-арабинозы, D-рибозы, D-ксилозы) и гексозы (D-галактозы). R - аминогруппа, бензамидогруппа, (пиридин-2-ил) аминогруппа, ацетамидогруппа или карбамидогруппа.
Известно, что данное соединение обладает выраженной цитотоксической активностью на культуре клеток рака толстой кишки человека НСТ-116, LS174T, рака яичников SKOV3 и пролонгированной противоопухолевой активностью при меланоме В-16, эпидермоидной карциноме легкого Льюиса и аденокарциноме толстой кишки АКАТОЛ [Патент РФ №2548045].
В заявляемом способе соединение применяется на ксенографтах перевиваемого рака толстой кишки человека SW620 in vivo.
Техническим результатом заявляемого способа является повышение эффективности и снижение токсичности.
Заявляемый способ лечения осуществляется следующим образом.
Животным с подкожными (и/к) ксенографтами перевиваемой опухоли толстой кишки человека SW620 (n=10) внутривенно (в/в) вводили исследуемое соединение однократно или многократно в диапазоне доз 12,5-150 мг/кг. Лечение начинали через 48 часов после подкожной трансплантации взвеси опухолевой ткани. Мышам контрольных групп вводили 0,9% раствор натрия хлорида в том же режиме.
Оценку проводили по стандартному показателю - торможению роста опухоли, рассчитанному по соотношению средних объемов опухолей у мышей, которые получали исследуемое соединение, и в контрольной группе, Т/С% (treatment/control) в сравнении с контрольной группой без лечения (КРО), принимая в группе КРО Т/С=100% и используя Т/С≤42% в качестве критерия для экспериментов с опухолями человека [Трещалина Е.М., Жукова О.С., Герасимова Г.К. и др. Методические указания по изучению противоопухолевой активности фармакологических веществ // Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / Под общей ред. Р.У. Хабриева. М.: Медицина, 2005. С. 637-651].
Для расчета показателей Т/С в течение 12-ти дней после введения троекратно на 1, 6 и 12 сутки измеряли объемы опухолей с помощью системы, состоящей из электронного цифрового штангенциркуля 500-716-11, 0-150 мм IP67 («Mitutoyo», Япония), соединенного SPC 0,5 CZA625 с персональным компьютером. Полученная величина (размер опухоли) использована для расчета Ttest с обработкой индивидуальных и средних объемов (средняя арифметическая) и величин стандартного отклонения (m).
О переносимости лечения исследуемым соединением судили по поведению и состоянию мышей во время проведения опыта, а также по результатам аутопсии, выявляли симптомы гастроинтестинальной токсичности (кровенаполнение и/или нарушение моторики кишечника).
Исследование проводили на 8 недельных половозрелых иммунодефицитных мышах-самцах Balb/c nude массой тела 20-22 г из разведения ФГБУ «РОНЦ им. Н.Н. Блохина» Минздрава России. Для перевивки использовали 20% опухолевую взвесь рака толстой кишки человека SW620 в питательной среде 199. Каждой мыши подкожно в область правой подмышечной впадины трансплантировали по 0,2 мл взвеси, т.е. по 40 мг опухолевой ткани на мышь [Трещалина Е.М., Жукова О.С., Герасимова Г.К. и др. Методические указания по изучению противоопухолевой активности фармакологических веществ // Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / Под общей ред. Р.У. Хабриева. М.: Медицина, 2005. С. 637-651].
Изобретение иллюстрируется примерами 1-2, табл. 1-3, фиг. 1-3.
Пример 1. В опыте использованы мыши-самки Balb/c nude с п/к ксенографтами рака толстой кишки человека SW620 (n=10).
В таблице 1 представлены уровни торможения роста опухоли SW620 по стандартному показателю Т/С после окончания лечения на 1, 6 и 12 сутки. Исследуемое соединение вводили однократно внутривенно в дозах 75, 100 и 150 мг/кг.
В результате после окончания лечения в двух однократных дозах 75 и 100 мг/кг наблюдали возрастающий во времени по уровню и степени достоверности дозозависимый противоопухолевый эффект: при дозе 75 мг/кг Т/С=23% (р=0,0005), 16% (р=0,00003) и 24% (р=0,00010), при дозе 100 мг/кг Т/С=16% (р=0,0004), 15% (р=0,0005) и 24% (р=0,0005), соответственно срокам после лечения. Гибели от токсичности и видимых патологических изменений внутренних органов, в том числе со стороны желудочно-кишечного тракта, не наблюдали.
На фиг. 1 представлена динамика роста подкожных ксенографтов рака толстой кишки человека SW620 под действием исследуемого соединения в диапазоне доз.
Увеличение дозы до 150 мг/кг сопровождалось гибелью мышей от токсичности.
Пример 2. В опыте использованы мыши-самки Balb/c nude с п/к ксенографтами рака толстой кишки человека SW620 (n=10). Исследуемое соединение изучено в режиме двукратного внутривенного введения с интервалом 96 часов в диапазоне разовых доз 25, 50 и 75 мг/кг (суммарно 50, 100 и 150 мг/кг).
В таблице 2 представлены уровни торможения роста опухоли по стандартному показателю Т/С на 1, 6 и 12 сутки после окончания лечения в режиме двукратного внутривенного введения с интервалом 96 часов в диапазоне разовых доз 25, 50 и 75 мг/кг (суммарно 50, 100 и 150 мг/кг).
Показано, что исследуемое соединение при двукратном применении оказывало значимый достоверный противоопухолевый эффект, возрастающий во времени по уровню и степени достоверности. На 1, 6 и 12 сутки после лечения при разовой дозе 25 мг/кг (суммарно 50 мг/кг) Т/С=35% (р=0,00000002), 13% (р=0,000002) и 19% (р=0,00004); при разовой дозе 50 мг/кг (суммарно 100 мг/кг) Т/С=28% (р=0,0002), 6% (р=0,000001) и 6% (р=0,0004); при разовой дозе 75 мг/кг (суммарно 150 мг/кг) Т/С=23% (р=0,0006), 2% (р=0,00004) и 2% (р=0,00005) соответственно. Максимально эффективные результаты получены при двукратном применении с использованием суммарной дозы 150 мг/кг, которые представлены на фиг. 2. Гибели от токсичности и видимых патологических изменений внутренних органов, в том числе со стороны желудочно-кишечного тракта, не наблюдали.
Пример 3. В опыте использованы мыши-самки Balb/c nude с п/к ксенографтами рака толстой кишки человека SW620 (n=10). Для завершения характеристики терапевтического диапазона проведено изучение эффективности малых терапевтических доз исследуемого агента.
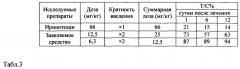
В таблице 3 представлены уровни торможения роста опухоли по стандартному показателю Т/С на 1, 6 и 12 сутки после окончания лечения. Исследуемое соединение вводили двукратно внутривенно с интервалом 96 часов в диапазоне разовых доз 6,3 и 12,5 мг/кг (суммарно 12,5 и 25 мг/кг).
Показано, что в группах мышей, получавших исследуемое соединение двукратно в разовой дозе 6,3 мг/кг (суммарно 12,5 мг/кг) значимый и достоверный противоопухолевый эффект отсутствовал в течение 12 суток после окончания лечения, T/Cmin=87% (критерий Т/С≤42%). При разовой дозе 12,5 мг/кг (суммарно 25 мг/кг) торможение роста опухоли было выше критерия эффективности, но на достоверном уровне, T/Cmin=57% (р<0,05).
На фиг. 3 представлена динамика роста подкожных ксенографтов SW620 под действием исследуемого соединения при этой схеме введения. Гибели от токсичности и видимых патологических изменений внутренних органов, в том числе со стороны желудочно-кишечного тракта, не наблюдали.
Таким образом, применение производного индолокарбазола 6-амино-12-(α-L-арабинопиранозил)индало[2,3-а]пиролло[3,4-с]карбазол-5,7-дион для лечения рака толстой кишки человека SW620 в эксперименте, способствует повышению эффективности способа в сравнении с прототипом, в том числе при малых терапевтических дозах, и понижению его токсичности.
Применение производного индолокарбазола 6-амино-12-(α-L-арабинопиранозил)индало[2,3-а]пиролло[3,4-с]карбазол-5,7-дион для лечения рака толстой кишки человека SW620 в эксперименте на иммунодефицитных мышах в суммарных дозах 12,5-150 мг/кг.