Способы лечения гепатита с
Иллюстрации
Показать всеГруппа изобретений относится к медицине и предназначена для лечения вируса гепатита С. Используют пан-генотипические ингибиторы ВГС, в частности метил {(2S,3R)-1-[(2S)-2-{5-[(2R,5R)-1-{3,5-дифтор-4-[4-(4-фторфенил)пиперидин-1-ил]фенил}-5-(6-фтор-2-{(2S)-1-N-(метоксикарбонил)-O-метил-L-треонил]пирролидин-2-ил}-1H-бензимидазол-5-ил)пирролидин-2-ил)-6-фтор-1H-бензимидазол-2-ил}пирролидин-1-ил]-3-метокси-1-оксобутан-2-ил}карбамат совместно с ингибитором протеазы HCV или полимеразы HCV. При этом пациента не генотипируют для указанного лечения, лечение длится не менее 24 недель и не включает введения интерферона. Группа изобретений позволяет повысить эффективность лечения. 2 н. и 11 з.п. ф-лы, 3 табл., 2 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0001] Настоящее изобретение относится к ингибиторам пан-генотипического ВГС и к способам их использования для лечения ВГС инфекции.
ИЗВЕСТНЫЙ УРОВЕНЬ ТЕХНИКИ
[0002] Вирус гепатита С (ВГС) представляет собой РНК вирус, принадлежащий к роду Hepacivirus семейства Flaviviridae. Вирион оболочкового ВГС содержит геном РНК с позитивными цепями, кодирующий все известные вирус-специфические белки в единой, непрерывной, открытой считывающей рамке. Такая открытая считывающая рамка включает приблизительно 9500 нуклеотидов и кодирует один крупный полипротеин, содержащий около 3000 аминокислот. Указанный полипротеин состоит из капсидного белка, оболочковых белков E1 и E2, связанных с мембранными белками p7, и не-структурных белков NS2, NS3, NS4A, NS4B, NS5A и NS5B.
[0003] ВГС инфекция связана с прогрессирующим патологиями печени, включая цирроз и гепатоклеточную карциному. Хронический гепатит C можно лечить пэгинтерфероном-альфа в комбинации с рибавирином. При этом остаются существенные ограничения по эффективности и толерантности, так как многие пациенты страдают от побочных эффектов, и удаление вируса из организма часто оказывается несоответствующим требованиям. Поэтому существует необходимость в создании новых лекарственных средств для лечения инфекции ВГС.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
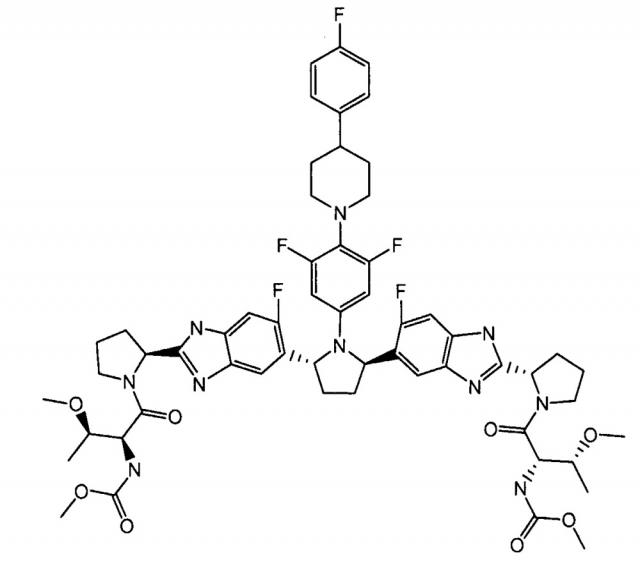
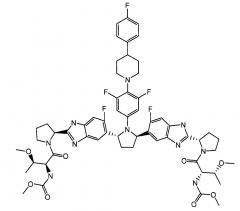
[0004] Неожиданно было обнаружено, что метил {(2S,3R)-1-[(2S)-2-{5-[(2R,5R)-1-{3,5-дифтор-4-[4-(4-фторфенил)пиперидин-1-ил]фенил}-5-(6-фтор-2-{(2S)-1-N-(метоксикарбонил)-O-метил-L-треонил]пирролидин-2-ил}-1H-бензимидазол-5-ил)пирролидин-2-ил)-6-фтор-1H-бензимидазол-2-ил}пирролидин-1-ил]-3-метокси-1-оксобутан-2-ил}карбамат (здесь и далее "соединение 1") и его фармацевтически приемлемые соли являются ингибиторами пан-генотипического ВГС. Указанные соединения являются эффективными в отношении ингибирования широкого круга ВГС генотипов и вариантов, таких как ВГС генотипы 1, 2, 3, 4, 5 и 6.
[0005] Соответственно, первый аспект настоящего изобретения отличается тем, что предложены способы лечения ВГС. Такие способы включают введение пациенту эффективного количества соединения 1 или его фармацевтически приемлемой соли пациенту с ВГС, независимо от специфического генотипа (генотипов) ВГС, который присутствует у этого пациента. Поэтому, такого пациента предпочтительно не генотипируют до лечения, и лечение можно начинать без предварительного скринирования пациента на специфические генотипы ВГС.
[0006] В одном варианте указанного аспекта настоящего изобретения, указанный пациент инфицирован генотипом 2, таким как генотип 2a или 2b. В другом варианте указанного аспекта настоящего изобретения, указанный пациент инфицирован генотипом 3, таким как генотип 3a. В другом варианте указанного аспекта настоящего изобретения, указанный пациент инфицирован генотипом 4, таким как генотип 4a. В еще одном варианте указанного аспекта настоящего изобретения, указанный пациент инфицирован генотипом 5, таким как генотип 5a. И в еще одном варианте указанного аспекта настоящего изобретения, указанный пациент инфицирован генотипом 6, таким как генотип 6a.
[0007] В другом варианте указанного аспекта настоящего изобретения, соединение 1 или его соль комбинируют или совместно вводят с другим анти-ВГС агентом. Нелимитирующие примеры указанных других анти-ВГС агентов включают ингибиторы ВГС полимеразы, ингибиторы ВГС протеазы, другие ингибиторы ВГС NS5A, CD81 ингибиторы, ингибиторы циклофилина или ингибиторы участка внутренней посадки рибосомы (IRES). В одном из примеров указанный пациент инфицирован генотипом 2, таким как генотип 2a или 2b. В другом примере указанный пациент инфицирован генотипом 3, таким как генотип 3a. В другом примере указанный пациент инфицирован генотипом 4, таким как генотип 4a. В еще одном примере указанный пациент инфицирован генотипом 5, таким как генотип 5a. И в еще одном примере указанный пациент инфицирован генотипом 6, таким как генотип 6a.
[0008] В еще одном варианте указанного аспекта настоящего изобретения, соединение 1 или его соль комбинируют или совместно вводят с ингибитором протеазы ВГС или с ингибитором полимеразы ВГС. В одном из примеров, указанный пациент инфицирован генотипом 2, таким как генотип 2a или 2b. В другом примере указанный пациент инфицирован генотипом 3, таким как генотип 3a. В другом примере указанный пациент инфицирован генотипом 4, таким как генотип 4a. В еще одном примере указанный пациент инфицирован генотипом 5, таким как генотип 5a. И в еще одном примере указанный пациент инфицирован генотипом 6, таким как генотип 6a.
[0009] В другом варианте указанного аспекта настоящего изобретения, соединение 1 или его соль комбинируют или совместно вводят с ингибитором протеазы ВГС. В одном из примеров, указанный пациент инфицирован генотипом 2, таким как генотип 2a или 2b. В другом примере указанный пациент инфицирован генотипом 3, таким как генотип 3a. В другом примере указанный пациент инфицирован генотипом 4, таким как генотип 4a. В еще одном примере указанный пациент инфицирован генотипом 5, таким как генотип 5a. И в еще одном примере указанный пациент инфицирован генотипом 6, таким как генотип 6a.
[0010] В другом варианте указанного аспекта настоящего изобретения, соединение 1 или его соль комбинируют или совместно вводят с ингибитором полимеразы ВГС. В одном из примеров, указанный пациент инфицирован генотипом 2, таким как генотип 2a или 2b. В другом примере указанный пациент инфицирован генотипом 3, таким как генотип 3a. В другом примере указанный пациент инфицирован генотипом 4, таким как генотип 4a. В еще одном примере указанный пациент инфицирован генотипом 5, таким как генотип 5a. И в еще одном примере указанный пациент инфицирован генотипом 6, таким как генотип 6a.
[0011] В другом варианте указанного аспекта настоящего изобретения, соединение 1 или его соль комбинируют или совместно вводят с ингибитором протеазы ВГС и ингибитором полимеразы ВГС. В одном из примеров, указанный пациент инфицирован генотипом 2, инфицирован генотипом 3, таким как генотип 3a. В другом примере указанный пациент инфицирован генотипом 4, таким как генотип 4a. В еще одном примере указанный пациент инфицирован генотипом 5, таким как генотип 5a. И в еще одном примере указанный пациент инфицирован генотипом 6, таким как генотип 6a.
[0012] В рассматриваемом аспекте настоящего изобретения, также как в каждом и любом варианте и примере, раскрытом здесь и далее, лечение предпочтительно длится меньше чем 24 недели и не включает введения интерферона указанному пациенту. Такое лечение может, например, включать введение указанному пациенту соединения 1 или его фармацевтически приемлемой соли вместе с ингибитором протеазы ВГС или ингибитором полимеразы ВГС или с комбинацией ингибитора протеазы ВГС и ингибитора полимеразы ВГС. Например, лечение может включать введение указанному пациенту соединения 1 или его фармацевтически приемлемой соли вместе с ингибитором протеазы ВГС. В другом примере лечение может включать введение указанному пациенту соединения 1 или его фармацевтически приемлемой соли вместе с ингибитором полимеразы ВГС. В еще другом примере лечение может включать введение указанному пациенту соединения 1 или его фармацевтически приемлемой соли вместе с комбинацией ингибитора протеазы ВГС и ингибитора полимеразы ВГС.
[0013] В рассматриваемом аспекте настоящего изобретения, также как в каждом и в любом варианте и примере, раскрытом здесь и далее, лечение предпочтительно длится не больше, чем 12 недель (например, лечение длится 8, 9, 10, 11 или 12 недель; предпочтительно, лечение длится 12 недель), и не включает введения интерферона указанному пациенту. Такое лечение может, например, включать введение указанному пациенту соединения 1 или его фармацевтически приемлемой соли, вместе с ингибитором протеазы ВГС, или ингибитором полимеразы ВГС, или с комбинацией ингибитора протеазы ВГС и ингибитора полимеразы ВГС. Например, лечение может включать введение указанному пациенту соединения 1 или его фармацевтически приемлемой соли вместе с ингибитором протеазы ВГС. В другом примере лечение может включать введение указанному пациенту соединения 1 или его фармацевтически приемлемой соли вместе с ингибитором полимеразы ВГС. В еще другом примере лечение может включать введение указанному пациенту соединения 1 или его фармацевтически приемлемой соли вместе с комбинацией ингибитора протеазы ВГС и ингибитора полимеразы ВГС.
[0014] В рассматриваемом аспекте настоящего изобретения, также как в каждом и в любом варианте и примере, раскрытом здесь и далее, лечение может включать или может не включать введение указанному пациенту рибавирина; например, лечение может включать введение указанному пациенту рибавирина.
[0015] Во втором аспекте настоящее изобретение отличается способами лечения ВГС. Такие способы включают введение пациенту с ВГС эффективного количества соединения 1 или его фармацевтически приемлемой соли, где указанный пациент инфицирован генотипом 2, 3, 4, 5 или 6 ВГС.
[0016] В одном варианте указанного аспекта настоящего изобретения, указанный пациент инфицирован генотипом 2, таким как генотип 2a или 2b. В другом варианте указанного аспекта настоящего изобретения, указанный пациент инфицирован генотипом 3, таким как генотип 3a. В другом варианте указанного аспекта настоящего изобретения, указанный пациент инфицирован генотипом 4, таким как генотип 4a. В еще одном варианте указанного аспекта настоящего изобретения, указанный пациент инфицирован генотипом 5, таким как генотип 5a. И в еще одном варианте указанного аспекта настоящего изобретения, указанный пациент инфицирован генотипом 6, таким как генотип 6a.
[0017] В другом варианте указанного аспекта настоящего изобретения, соединение 1 или его соль комбинируют или совместно вводят с другим анти-ВГС агентом. Нелимитирующие примеры указанных других анти-ВГС агентов включают ингибиторы полимеразы ВГС, ингибиторы протеазы ВГС, другие ингибиторы NS5A ВГС, ингибиторы CD81, ингибиторы циклофилина, или ингибиторы участка внутренней посадки рибосомы (IRES). В одном из примеров, указанный пациент инфицирован генотипом 2, таким как генотип 2a или 2b. В другом примере указанный пациент инфицирован генотипом 3, таким как генотип 3a. В другом примере указанный пациент инфицирован генотипом 4, таким как генотип 4a. В еще одном примере указанный пациент инфицирован генотипом 5, таким как генотип 5a. И в еще одном примере указанный пациент инфицирован генотипом 6, таким как генотип 6a.
[0018] В еще одном варианте указанного аспекта настоящего изобретения, соединение 1 или его соль комбинируют или совместно вводят с ингибитором протеазы ВГС или с ингибитором полимеразы ВГС. В одном из примеров, указанный пациент инфицирован генотипом 2, таким как генотип 2a или 2b. В другом примере указанный пациент инфицирован генотипом 3, таким как генотип 3a. В другом примере указанный пациент инфицирован генотипом 4, таким как генотип 4a. В еще одном примере указанный пациент инфицирован генотипом 5, таким как генотип 5a. И в еще одном примере указанный пациент инфицирован генотипом 6, таким как генотип 6a.
[0019] В другом варианте указанного аспекта настоящего изобретения, соединение 1 или его соль комбинируют или совместно вводят с ингибитором протеазы ВГС. В одном из примеров, указанный пациент инфицирован генотипом 2, таким как генотип 2a или 2b. В другом примере указанный пациент инфицирован генотипом 3, таким как генотип 3a. В другом примере указанный пациент инфицирован генотипом 4, таким как генотип 4a. В еще одном примере указанный пациент инфицирован генотипом 5, таким как генотип 5a. И в еще одном примере указанный пациент инфицирован генотипом 6, таким как генотип 6a.
[0020] В другом варианте указанного аспекта настоящего изобретения, соединение 1 или его соль комбинируют или совместно вводят с ингибитором полимеразы ВГС. В одном из примеров, указанный пациент инфицирован генотипом 2, таким как генотип 2a или 2b. В другом примере указанный пациент инфицирован генотипом 3, таким как генотип 3a. В другом примере указанный пациент инфицирован генотипом 4, таким как генотип 4a. В еще одном примере указанный пациент инфицирован генотипом 5, таким как генотип 5a. И в еще одном примере указанный пациент инфицирован генотипом 6, таким как генотип 6a.
[0021] В другом варианте указанного аспекта настоящего изобретения, соединение 1 или его соль комбинируют или совместно вводят с ингибитором протеазы ВГС и ингибитором полимеразы ВГС. В одном из примеров, указанный пациент инфицирован генотипом 2, таким как генотип 2a или 2b. В другом примере указанный пациент инфицирован генотипом 3, таким как генотип 3a. В другом примере указанный пациент инфицирован генотипом 4, таким как генотип 4a. В еще одном примере указанный пациент инфицирован генотипом 5, таким как генотип 5a. И в еще одном примере указанный пациент инфицирован генотипом 6, таким как генотип 6a.
[0022] В рассматриваемом аспекте настоящего изобретения, также как в каждом и любом варианте и примере, раскрытом здесь и далее, лечение предпочтительно длится меньше чем 24 недели и не включает введения интерферона указанному пациенту. Такое лечение может, например, включать введение указанному пациенту соединения 1 или его фармацевтически приемлемой соли вместе с ингибитором протеазы ВГС или ингибитором полимеразы ВГС или с комбинацией ингибитора протеазы ВГС и ингибитора полимеразы ВГС. Например, лечение может включать введение указанному пациенту соединения 1 или его фармацевтически приемлемой соли вместе с ингибитором протеазы ВГС. В другом примере лечение может включать введение указанному пациенту соединения 1 или его фармацевтически приемлемой соли вместе с ингибитором полимеразы ВГС. В еще другом примере лечение может включать введение указанному пациенту соединения 1 или его фармацевтически приемлемой соли вместе с комбинацией ингибитора протеазы ВГС и ингибитора полимеразы ВГС.
[0023] В рассматриваемом аспекте настоящего изобретения, также как в каждом и любом варианте и примере, раскрытом здесь и далее, лечение предпочтительно длится не больше, чем 12 недель (например, лечение длится 8, 9, 10, 11 или 12 недель; предпочтительно, лечение длится 12 недель), и не включает введения интерферона указанному пациенту. Такое лечение может, например, включать введение указанному пациенту соединения 1 или его фармацевтически приемлемой соли вместе с ингибитором протеазы ВГС или ингибитором полимеразы ВГС или с комбинацией ингибитора протеазы ингибитора полимеразы ВГС. Например, лечение может включать введение указанному пациенту соединения 1 или его фармацевтически приемлемой соли вместе с ингибитором протеазы ВГС. В другом примере лечение может включать введение указанному пациенту соединения 1 или его фармацевтически приемлемой соли вместе с ингибитором полимеразы ВГС. В еще другом примере лечение может включать введение указанному пациенту соединения 1 или его фармацевтически приемлемой соли вместе с комбинацией ингибитора протеазы ВГС и ингибитора полимеразы ВГС.
[0024] В рассматриваемом аспекте настоящего изобретения, также как в каждом и в любом варианте и примере, раскрытом здесь и далее, лечение может включать или может не включать введение указанному пациенту рибавирина; например, лечение включает введение указанному пациенту рибавирина.
[0025] Настоящее изобретение также отличается тем, что Соединение 1 или его фармацевтически приемлемая соль предназначены для использования для лечения пациента с ВГС независимо от специфического генотипа (генотипов) ВГС, который имеется у пациента. Такие способы использования проиллюстрированы в раскрытом выше первом аспекте настоящего изобретения, включая каждый и любой вариант и пример, раскрытые здесь и далее.
[0026] Настоящее изобретение далее отличается тем, что Соединение 1 или его фармацевтически приемлемую соль для использования для лечения пациента, инфицированного ВГС генотипа 2, 3, 4, 5, или 6. Такие применения проиллюстрированы в раскрытом выше втором аспекте настоящего изобретения, включая каждый и любой вариант и пример, раскрытые здесь и далее.
[0027] Другие особенности, цели и преимущества настоящего изобретения очевидны с учетом приводимого далее описания. Однако, следует понимать, что подробное описание, хотя и относится к предпочтительным вариантам настоящего изобретения, представлено только с целью иллюстрации, но не ограничения. Различные изменения и модификации в объеме настоящего изобретения станут очевидны специалистам в данной области из подробного описания.
ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНОГО ВАРИАНТА ОСУЩЕСТВЛЕНИЯ
НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
[0028] Соединение 1, также известное как метил {(2S,3R)-1-[(2S)-2-{5-[(2R,5R)-1-{3,5-дифтор-4-[4-(4-фторфенил)пиперидин-1 -ил]фенил}-5-(6-фтор-2-{(2S)-1-N-(метоксикарбонил)-O-метил-L-треонил]пирролидин-2-ил}-1H-бензимидазол-5-ил)пирролидин-2-ил]-6-фтор-1H-бензимидазол-2-ил}пирролидин-1-ил]-3-метокси-1-оксобутан-2-ил}карбамат, раскрыто в опубликованной патентной заявке США No. 2012/0004196, полное содержание которой включено в описание по ссылке.
Соединение 1
[0029] Было обнаружено, что соединение 1 имеет значения EC50 меньше, чем 10 пМ против стабильных субгеномных репликонов с NS5A, полученных из широкого круга клинически релевантных генотипов ВГС, таких как генотипы ВГС 1a, 1b, 2a, 2b, 3a, 4a, 5a и 6a. В анализах временной экспрессии субгеномного репликона было обнаружено, что соединение 1 имеет значение EC50 меньше, чем 5 пМ, против многих вариантов ВГС, которые устойчивы к другим ингибиторам NS5A, таким как вариант T24A генотипа 2a, варианты L28F и L31V генотипа 2b, варианты M28T и Y93H генотипа 3a, варианты L28V и L30H генотипа 4a, варианты L28I, L31F и L31V генотипа 5a, и варианты L31V, T58N и T58A генотипа 6a. Значения EC50 определяют в присутствии 5% фетальной телячьей сыворотки, но в отсутствии человеческой плазмы в соответствии с раскрытыми далее процедурами.
[0030] Настоящее изобретение отличается использованием соединения 1 или его фармацевтически приемлемой соли для лечения ВГС, как раскрыто в описании выше. В любом раскрытом здесь способе использования, соединение 1 или его фармацевтически приемлемую соль можно приготовить в подходящей жидкой или твердой лекарственной форме. Предпочтительно, соединение 1 или его соль приготавливают в виде твердой композиции, включающей соединение 1 (или его фармацевтически приемлемую соль) в аморфной форме, фармацевтически приемлемый гидрофильный полимер и необязательно фармацевтически приемлемое поверхностно-активное вещество.
[0031] Нелимитирующий способ получения аморфной формы соединения 1 (или его фармацевтически приемлемой соли) происходит путем создания твердых дисперсий с полимерным носителем. В том смысле, как здесь использован, термин "твердая дисперсия" определяет систему в твердом состоянии (в противоположность жидкому или газообразному состоянию), включающую по меньшей мере два компонента, в которой один компонент диспергирован в другом компоненте или компонентах. Например, активный ингредиент или комбинацию активных ингредиентов можно диспергировать в матрице, состоящей из фармацевтически приемлемого гидрофильного полимера (полимеров) и фармацевтически приемлемого поверхностно-активного вещества (веществ). Термин "твердая дисперсия" охватывает системы, содержащие маленькие частицы одной фазы, диспергированные в другой фазе. Размеры таких частиц часто бывают меньше, чем 400 мкм, например, меньше чем 100, 10 или 1 мкм. Если твердая дисперсия, состоящая из компонент, такова, что указанная система химически и физически однородна, или гомогенна по всему объему, или состоит из одной фазы (как определено термодинамически), такую твердую дисперсию называют "твердым раствором". Стекловидный раствор представляет собой твердый раствор, в котором растворенное вещество растворено в стекловидном растворителе.
[0032] В любом из раскрытых в описании способов можно использовать твердую композицию, которая включает (1) соединение 1 (или его фармацевтически приемлемую соль) в аморфной форме, (2) фармацевтически приемлемый гидрофильный полимер и (3) фармацевтически приемлемое поверхностно-активное вещество. Соединение 1 (или его соль) и полимер предпочтительно приготавливают в виде твердой дисперсии. Поверхностно-активное вещество может быть также включено в ту же самую твердую дисперсию; или указанное поверхностно-активное вещество можно отдельно скомбинировать или смешать с твердой дисперсией.
[0033] Гидрофильный полимер может, например, и без ограничений, иметь Tg по меньшей мере 50°C, более предпочтительно по меньшей мере 60°C, и наиболее предпочтительно по меньшей мере 80°C, включая, но ими не ограничиваясь, от 80°C до 180°C, или от 100°C до 150°C. Предпочтительно, если гидрофильный полимер является водорастворимым полимером. Нелимитирующие примеры подходящих гидрофильных полимеров включают, но ими не ограничиваются, гомополимеры или сополимеры N-виниллактамов, такие как гомополимеры или сополимеры N-винилпирролидона (например, поливинилпирролидон (ПВП), или сополимеры N-винилпирролидона и винилацетата или винилпропионата); сложные эфиры целлюлозы или простые эфиры целлюлозы, такие как алкилцеллюлозы (например, метилцеллюлоза или этилцеллюлоза), гидроксиалкилцеллюлозы (например, гидроксипропилцеллюлоза), гидроксиалкилалкилцеллюлозы (например, гидроксипропилметилцеллюлоза), и фталаты целлюлозы или сукцинаты (например, ацетат-фталат целлюлозы и фталат гидроксипропилметилцеллюлозы, сукцинат гидроксипропилметилцеллюлозы, или ацетат-сукцинат гидроксипропилметилцеллюлозы); высокомолекулярные оксиды полиалкилена, такие как полиэтиленоксид, полипропиленоксид, и сополимеры этиленоксида и пропиленоксида; полиакрилаты или полиметакрилаты, такие как сополимеры метакриловая кислота/этилакрилат, сополимеры метакриловая кислота/метилметакрилат, сополимеры бутилметакрилат/2-диметиламиноэтилметакрилат, поли(гидроксиалкилакрилаты), и поли(гидроксиалкилметакрилаты); полиакриламиды; полимеры винилацетата, такие как сополимеры винилацетата и кротоновой кислоты, и частично гидролизованный поливинилацетат (также именуемый как частично омыленный "поливиниловый спирт"); поливиниловый спирт; олиго- или полисахариды, такие как каррагенаны, галактоманнаны и ксантановая камедь; полигидроксиалкилакрилаты; полигидроксиалкилметакрилаты; сополимеры метилметакрилата и акриловой кислоты; полиэтиленгликоли (ПЭГи); или любые их смеси.
[0034] Нелимитирующие примеры предпочтительных гидрофильных полимеров включают поливинилпирролидон (ПВП) K17, ПВП K25, ПВП K30, ПВП K90, гидроксипропилметилцеллюлозу (ГПМЦ) E3, ГПМЦ E5, ГПМЦ E6, ГПМЦ E15, ГПМЦ K3, ГПМЦ A4, ГПМЦ A15, ГПМЦ ацетат-сукцинат (AS) LF, ГПМЦ AS MF, ГПМЦ AS HF, ГПМЦ AS LG, ГПМЦ AS МГ, ГПМЦ AS HG, ГПМЦ фталат (P) 50, ГПМЦ P 55, Ethocel 4, Ethocel 7, Ethocel 10, Ethocel 14, Ethocel 20, коповидон (сополимер винилпирролидон-винилацетат 60/40), поливинилацетат, сополимер метакрилат/метакриловая кислота (Eudragit) L100-55, Eudragit L100, Eudragit S100, полиэтиленгликоль (ПЭГ) 400, ПЭГ 600, ПЭГ 1450, ПЭГ 3350, ПЭГ 4000, ПЭГ 6000, ПЭГ 8000, полоксамер 124, полоксамер 188, полоксамер 237, полоксамер 338, и полоксамер 407.
[0035] Из них предпочтительны гомополимеры или сополимеры N-винилпирролидона, такие как сополимеры N-винилпирролидона и винилацетата. Нелимитирующий пример предпочтительного полимера представляет собой сополимер 60 масс. % N-винилпирролидона и 40 масс. % винилацетата. Другие предпочтительные полимеры включают, без ограничений, гидроксипропилметилцеллюлозу (ГПМЦ, также известную как гипромеллоза в USP), такие как гидроксипропилметилцеллюлоза степени чистоты E5 (ГПМЦ-E5); и ацетат-сукцинат гидроксипропилметилцеллюлозы (ГПМЦ-AS).
[0036] Используемое фармацевтически приемлемое поверхностно-активное вещество может быть неионным поверхностно-активным веществом.
Предпочтительно, поверхностно-активное вещество имеет значение HLB (показатель гидрофильно-липофильного баланса) порядка 2-20. Твердые композиции, используемые в настоящем изобретении, могут также включать смесь фармацевтически приемлемых поверхностно-активных веществ, с по меньшей мере одним поверхностно-активным веществом со значением HLB по меньшей мере 10, и по меньшей мере другим поверхностно-активным веществом, со значением HLB ниже 10.
[0037] Нелимитирующие примеры подходящих фармацевтически приемлемых поверхностно-активных веществ включают производные полиоксиэтиленированного касторового масла, например, полиоксиэтиленглицерин тририцинолеат или полиоксил 35 касторовое масло (кремофор® EL; BASF Corp.), или полиоксиэтиленглицерин оксистеарат, такой как полиэтиленгликоль 40 гидрированное касторовое масло (кремофор® RH 40, также известное как полиоксил 40 гидрированное касторовое масло, или макроголглицерин гидроксистеарат), или полиэтиленгликоль 60 гидрированное касторовое масло (кремофор® RH 60 или моноэфир жирной кислоты полиоксиэтиленсорбитана), такие как моноэфир жирной кислоты полиоксиэтилен (20) сорбитана, например, полиоксиэтилен (20) сорбитан моноолеат (Tween® 80), полиоксиэтилен (20) сорбитан моностеарат (Tween® 60), полиоксиэтилен (20) сорбитан монопальмитат (Tween® 40), или полиоксиэтилен (20) сорбитан монолаурат (Tween® 20). Другие нелимитирующие примеры подходящих поверхностно-активных веществ включают полиоксиэтиленалкиловые простые эфиры, например, полиоксиэтилен (3) лауриловый простой эфир, полиоксиэтилен (5) цетиловый простой эфир, полиоксиэтилен (2) стеариловый простой эфир, полиоксиэтилен (5) стеариловый простой эфир; полиоксиэтиленалкилариловые простые эфиры, например, полиоксиэтилен (2) нонилфениловый простой эфир, полиоксиэтилен (3) нонилфениловый простой эфир, полиоксиэтилен (4) нонилфениловый простой эфир, полиоксиэтилен (3) октилфениловый простой эфир; сложные эфиры жирных кислот полиэтиленгликоля, например, ПЭГ-200 монолаурат, ПЭГ-200 дилаурат, ПЭГ-300 дилаурат, ПЭГ-400 дилаурат, ПЭГ-300 дистеарат, ПЭГ-300 диолеат; моноэфиры жирной кислоты алкиленгликоля, например, пропиленгликоль монолаурат (лаурогликоль®); сложные эфиры жирных кислот сахарозы, например, моностеарат сахарозы, дистеарат сахарозы, монолаурат сахарозы, дилаурат сахарозы; сложные моноэфиры жирных кислот сорбитана, такие как (Span® 20), сорбитан моноолеат, сорбитан монопальмитат (Span® 40), или сорбитан стеарат. Другие подходящие поверхностно-активные вещества включают, но ими не ограничиваются, блоксополимеры этиленоксида и пропиленоксида, также известные как блоксополимеры полиоксиэтилен-полиоксипропилена или полиоксиэтилен-полипропиленгликоля, такие как Полоксамер® 124, Полоксамер® 188, Полоксамер® 237, Полоксамер® 388 или Полоксамер® 407 (BASF Wyandotte Corp.). Как раскрыто выше, смесь поверхностно-активных веществ можно использовать в твердой композиции, используемой в настоящем изобретении.
[0038] Нелимитирующие примеры предпочтительных поверхностно-активных веществ включают полисорбат 20, полисорбат 40, полисорбат 60, полисорбат 80, кремофор RH 40, кремофор EL, Gelucire 44/14, Gelucire 50/13, D-альфа-токоферил полиэтиленгликоль 1000 сукцинат (витамин E TPGS), пропиленгликоль лаурат, натрийлаурилсульфвт и сорбитан монолаурат.
[0039] Твердая дисперсия, которую используют в настоящем изобретении, предпочтительно, представляет собой твердый раствор, и более предпочтительно стекловидный раствор.
[0040] В одном варианте твердые композиции, используемые в настоящем изобретении, включают аморфную твердую дисперсию или твердый раствор, который включает соединение 1 (или его фармацевтически приемлемую соль) и фармацевтически приемлемый гидрофильный полимер. Твердая композиция также включает фармацевтически приемлемое поверхностно-активное вещество, которое, предпочтительно, приготавливают в форме аморфной твердой дисперсии или в виде твердого раствора. Гидрофильный полимер можно выбрать, например, из группы, состоящей из гомополимера N-виниллактама, сополимера N-виниллактама, сложного эфира целлюлозы, простого эфира целлюлозы, полиалкиленоксида, полиакрилата, полиметакрилата, полиакриламида, поливинилового спирта, полимера винилацетата, олигосахарида и полисахарида. В качестве нелимитирующего примера, гидрофильный полимер выбирают из группы, состоящей из гомополимера N-винилпирролидона, сополимера N-винилпирролидона, сополимера N-винилпирролидона и винилацетата, сополимера N-винилпирролидона и винилпропионата, поливинилпирролидона, метилцеллюлозы, этилцеллюлозы, гидроксиалкилцеллюлозы, гидроксипропилцеллюлозы, гидроксиалкилалкилцеллюлозы, гидроксипропилметилцеллюлозы, фталата целлюлозы, сукцината целлюлозы, ацетата-фталата целлюлозы, фталата гидроксипропилметилцеллюлозы, сукцината гидроксипропилметилцеллюлозы, ацетат-сукцината гидроксипропилметилцеллюлозы, полиэтиленоксида, полипропиленоксида, сополимера этиленоксида и пропиленоксида, сополимера метакриловая кислота/этилакрилат, сополимера метакриловая кислота/метилметакрилат, сополимера бутилметакрилат/2-диметиламиноэтилметакрилат, поли(гидроксиалкилакрилата), поли(гидроксиалкилметакрилата), сополимера винилацетата и кротоновой кислоты, частично гидролизованного поливинилацетата, каррагенана, галактоманнана и ксантановой камеди. Предпочтительно, гидрофильный полимер выбирают из поливинилпирролидона (ПВП) K17, ПВП K25, ПВП K30, ПВП K90, гидроксипропилметилцеллюлозы (ГПМЦ) E3, ГПМЦ E5, ГПМЦ E6, ГПМЦ E15, ГПМЦ K3, ГПМЦ A4, ГПМЦ A15, ГПМЦ ацетат сукцината (AS) LF, ГПМЦ AS MF, ГПМЦ AS HF, ГПМЦ AS LG, ГПМЦ AS МГ, ГПМЦ AS HG, ГПМЦ фталата (P) 50, ГПМЦ P 55, Ethocel 4, Ethocel 7, Ethocel 10, Ethocel 14, Ethocel 20, коповидона (сополимера винилпирролидон-винилацетата 60/40), поливинилацетата, сополимера метакрилат/метакриловая кислота (Eudragit) L100-55, Eudragit L100, Eudragit S100, полиэтиленгликолей (ПЭГ) 400, ПЭГ 600, ПЭГ 1450, ПЭГ 3350, ПЭГ 4000, ПЭГ 6000, ПЭГ 8000, полоксамера 124, полоксамера 188, полоксамера 237, полоксамера 338 или полоксамера 407. Более предпочтительно, гидрофильный полимер выбирают из гомополимеров винилпирролидона (например, ПВП со значениями К по Фикентшеру от 12 до 100, или ПВП со значениями К по Фикентшеру от 17 до 30), или сополимеров 30-70 масс .% N-винилпирролидона (ВП) и 70-30 масс. % винилацетата (ВА) (например, сополимер 60 масс. % ВП и 40 масс. % ВА). Поверхностно-активное вещество можно выбрать, например, из группы, состоящей из полиоксиэтиленглицерин тририцинолеата или полиоксила 35 касторового масла (кремофор® EL; BASF Corp.) или полиоксиэтиленглицерин оксистеарата, моноэфира жирной кислоты полиоксиэтилен сорбитана, алкилового простого эфира полиоксиэтилена, алкиларилового простого эфира полиоксиэтилена, сложного эфира жирной кислоты полиэтиленгликоля, сложного моноэфира жирной кислоты алкиленгликоля, сложного эфира жирной кислоты сахарозы, и сложного моноэфира жирной кислоты сорбитана. В качестве нелимитирующих примеров, поверхностно-активное вещество выбирают из группы, состоящей из полиэтиленгликоль 40 гидрированного касторового масла (кремофор® RH 40, также известное как полиоксил 40 гидрированное касторовое масло или макрогол глицерин гидроксистеарат), полиэтиленгликоль 60 гидрированного касторового масла (кремофор® RH 60), сложного моноэфира жирной кислоты полиоксиэтилен (20) сорбитана (например, полиоксиэтилен (20) сорбитан моноолеата (Tween® 80), полиоксиэтилен (20) сорбитан моностеарата (Tween® 60), полиоксиэтилен (20) сорбитан монопальмитата (Tween® 40) или полиоксиэтилен (20) сорбитан монолаурата (Tween® 20)), полиоксиэтилен (3) лаурилового простого эфира, полиоксиэтилен (5) цетилового простого эфира, полиоксиэтилен (2) стеарилового простого эфира, полиоксиэтилен (5) стеарилового простого эфира, полиоксиэтилен (2) нонилфенилового простого эфира, полиоксиэтилен (3) нонилфенилового простого эфира, полиоксиэтилен (4) нонилфенилового простого эфира, полиоксиэтилен (3) октилфенилового простого эфира, ПЭГ-200 монолаурата, ПЭГ-200 дилаурата, ПЭГ-300 дилаурата, ПЭГ-400 дилаурата, ПЭГ-300 дистеарата, ПЭГ-300 диолеата, пропиленгликоль монолаурата, моностеарата сахарозы, дистеарата сахарозы, монолаурата сахарозы, дилаурата сахарозы, сорбитан монолаурата, сорбитан моноолеата, сорбитан монопальмитата и сорбитан стеарата. Предпочтительно, поверхностно-активное вещество выбирают из полисорбата 20, полисорбата 40, полисорбата 60, полисорбата 80, кремофора RH 40, кремофора EL, Gelucire 44/14, Gelucire 50/13, D-альфа-токоферил полиэтиленгликоль 1000 сукцината (витамина E TPGS), пропиленгликоль лаурата, лаурилсульфата натрия, или сорбитан монолаурата. Более предпочтительно, поверхностно-активное вещество выбирают из сорбитан монолаурата или D-альфа-токоферил полиэтиленгликоль 1000 сукцината.
[0041] Используемая в настоящем изобретении твердая дисперсия, предпочтительно, включает или состоит из одной фазы (определяется термодинамически), в которой соединение 1, или комбинацию соединения 1 и другого анти-ВГС агента, молекулярно диспергируют в матрице, содержащей фармацевтически приемлемый гидрофильный полимер (полимеры). В таких случаях, термический анализ твердой дисперсии с помощью дифференциальной сканирующей калориметрии (DSC) обычно демонстрирует только один пик Tg, и такая твердая дисперсия не содержит детектируемого кристаллического соединения 1 по данным рентгеновской порошковой дифракционной спектроскопии.
[0042] Твердую композицию, используемую в настоящем изобретении, можно получить различными способами, такими как, без ограничений, экструзия расплава, сушка распылением, совместное осаждение, сушка вымораживанием, или другими способами удаления растворителя, причем предпочтительны экструзия расплава и сушка распылением. Процесс экструзии расплава обычно включает стадии приготовления расплава, который включает активный ингредиент (ингредиенты), гидрофильный полимер (полимеры) и предпочтительно поверхностно-активное вещество (вещества), и затем охлаждение расплава до его отверждения. "Плавление" означает переход в жидкое или резиноподобное состояние, в котором можно один компонент внедрить, предпочтительно внедрить гомогенно, в другой компонент или компоненты. Во многих случаях, полимерный компонент (компоненты) расплавится и другие компоненты, включая активный ингредиент (ингредиенты) и поверхностно-активное вещество (вещества), растворяться в расплаве, образуя при этом раствор. Плавление обычно включает нагревание выше точки размягчения полимера (полимеров). Получение расплава можно осуществить различными способами. Смешивание компонентов можно осуществить до, во время или после образования расплава. Например, компоненты можно смешать вначале, и затем расплавить, или одновременно смешать и расплавить. Расплав также можно гомогенизировать для более эффективного диспергирования активного ингредиента (ингредиентов). Кроме того, может оказаться удобным вначале расплавить полимер (полимеры) и затем добавить его и гомогенизировать активный ингредиент (ингредиенты). В одном из примеров все материалы, за исключением поверхностно-активного вещества (веществ), смешивают и подают в экструдер, тогда как поверхностно-активное вещество (вещества) расплавляют отдельно и подают под давлением во время экструзии.
[0043] Чтобы начать процесс экструзии расплава, активный ингредиент (ингредиенты) (например, соединение 1, или комбинацию соединения 1 и по меньшей мере другого анти-ВГС агента) можно использовать в их твердых формах, таких как соответствующие им кристаллические формы. Активный ингредиент (ингредиенты) можно также использовать в виде раствора или дисперсии в подходящем жидком растворителе, таком как спирты, алифатические углеводороды, сложные эфиры и, в некоторых случаях, жидкий диоксид углерода. Растворитель можно удалить, например, испаряя его после получения расплава.
[0044] Различные добавки также можно включить в расплав, например, регуляторы текучести (например, коллоидная двуокись кремния), связующие, смазывающие вещества, наполнители, разрыхлители, пластификаторы, красители или стабилизаторы (например, антиокислители, светостабилизаторы, акцепторы радикалов и стабилизаторы против активности микроорганизмов).
[0045] Плавление и/или смешивание можно осуществлять в аппаратах, которые обычно используют для такой цели. Особенно подходящие представляют собой экструдеры или месильные машины. Подходящие экструдеры включают одношнековые экструдеры, или экструдеры со шнеками, находящимися в зацеплении, или многошнековые экструдеры, предпочтительно, двухшнековые экструдеры, которые могут быть с одинаковым направлением вращения или с вращением в противоположном н