Фосфониевые соли на основе бетулиновой кислоты, обладающие цитотоксической активностью в отношении аденокарциномы предстательной железы
Иллюстрации
Показать всеИзобретение относится к солям формул 1-5, которые могут быть применены в медицине.
Предложены новые соли на основе бетулиновой кислоты, обладающие цитотоксичностью с улучшенной селективностью в отношении клеток аденокарциомы предстательной железы. 1 з.п. ф-лы, 1 табл., 6 пр.
Реферат
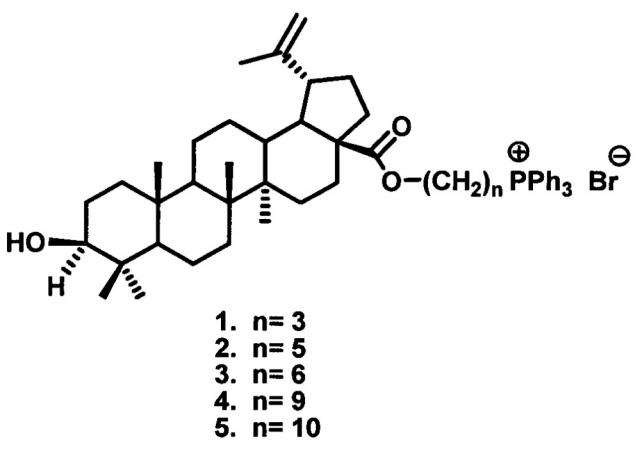
Изобретение относится к области органической химии, в частности, к новым фосфониевым солям на основе лупанового тритерпеноида - бетулиновой кислоты формулы 1-5:
которые могут найти применение в фармакологии и медицине.
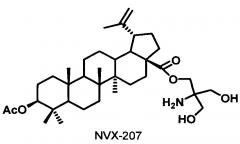
Природные пентациклические тритерпеноиды лупанового ряда характеризуются широким спектром биологической активности, в частности, противоопухолевой (Planta Med. 2009, 75, 1549-1560), относительной легкостью получения из растительного сырья и огромной сырьевой базой. Некоторые из них, например, соединение NVX-207 проходит клинические испытания в качестве противоопухолевого препарата (Eur. J. Clin. Invest. 2009, 39, 5, 384-394).
К настоящему времени "классическая" химиотерапия, мишенью для которой является жизненно важные белки и нуклеиновые кислоты клетки, достигла своей эффективности. Опухолевые клетки быстро приобретают резистентность к известным противоопухолевым препаратам, а применение новых цитостатиков со сходным механизмом действия редко приводит к значительным успехам. Изменение структуры цитостатиков, увеличение доз, использование ингибиторов лекарственной резистентности не позволяют добиться увеличения терапевтического индекса, т.е. летального повреждения опухолевых клеток без развития острой токсичности для организма в целом. В настоящее время все большую популярность получает новое направление противоопухолевой терапии - таргетная терапия. Среди большого числа таргетных соединений, которые действуют на определенные мишени опухолевой клетки, выделяют митохондриально-направленные противоопухолевые соединения.
В ряде исследований показано, что тритерпеноиды лупанового ряда вызывают гибель опухолевых клеток посредством активации апоптоза по митохондриальному пути (Cancer Res. 1997, 57, 4956-4964; BioMed Res. Int. 2015, 2015, 584189). Изучение механизма гибели показало, что под действием тритерпеноидов наблюдается выход проапоптотических белков из межмембранного митохондриального пространства в цитоплазму. Бетулиновая кислота стимулирует открытие митохондриальных транзитных пор (МТП). Открытие МТП приводит к утечке протонов, нарушению функционирования дыхания и как следствие - выходу в цитоплазму митохондриальных апоптотических белков (Apoptosis 2009, 14, 191-202)
Известно, что катион трифенилфосфония (ТРР) селективно накапливается в раковых клетках (Biomed. Pharmacother. 1985, 39, 220-226).
Соединения, содержащие трифенилфосфониевую группу (ТРР), предложены в качестве митохондриальных агентов, влияющих на ингибирование пролиферации опухолевых клеток (Anti-Cancer Drug Des. 1989, 4, 265-280.) Серия митохондриально-направленных соединений на основе бетулина и бетулиновой кислоты, содержащих ТРР группу, была синтезирована и определена их цитотоксичность на опухолевых линиях различного генеза.
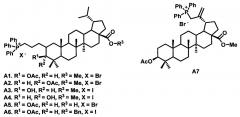
Так, цитотоксическая активность трифенилфосфониевых солей бетулиновой кислоты Al (IC50=1.20 μM), А2 (IC50=1.15 μМ) и А5 (IC50 1.10 μМ) в отношении клеток мастоцитомы Р-815 превысила активность бетулиновой кислоты (IC50 41.00 μM) в ~35-40 раз. В отношении клеток опухоли Эрлиха соединения Al, А2 и А5 проявили цитотоксичность в интервале IC50 2.30÷1.37 μМ, в то время как бетулиновая кислота была малоактивна (IC50 54.00 μМ) (патент РФ №2551647, опубл. 12.11.2012).
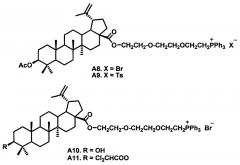
Цитотоксичная активность солей А8 (IC50 0.98 μМ), А10 (IC50 0.74 μМ) и A11 (IC50 0.95 μМ) в отношении опухолевых клеток нейробластомы (TET21N), АН (IC50 0.70 μМ) в отношении опухолевых клеток карциномы молочной железы (MCF-7) превысила активность бетулиновой кислоты для MCF-7 и эфира бетулиновой кислоты с дихлоруксусной кислотой в отношении к TET21N (Med. Chem. Commun., 2017, 8, 1934-1945).
Высокая цитотоксичность была установлена для соединения А12 в отношении опухолевых клеток миелоидной лейкемии K562 (IC50 0.57 μМ), промиелоцитарного лейкоза HL-60 (IC50 0.6 μМ), плоскоклеточного рака пищевода ЕСА-109 (IC50 0.78 μМ), карциномы легкого А 549 (IC50 0.61 μМ) (J. Med. Chem. 2017, 60, 6353-6363). Для соединения А13 установлена высокая цитотоксичность в отношении опухолевых клеток промиелоцитарного лейкоза HL-60 (IC50 0.32 μМ) (J. Med. Chem. 2017, 60, 6353-6363).
Найдено, что соединение А14 обладает высокой активностью в отношении винбластин резистентных клеток MCF-7/Vinb (IC50 составляет 0.045 μМ) (J. Nat. Prod., 2017, 80, 8, 2232-2239).
Наиболее структурно близким аналогом заявляемым соединениям является производное бетулиновой кислоты А15 (Med. Chem. Commun., 2017, 8, 1934-1945), где ТРР группа присоединена ковалентно к С-28 углеродному атому лупанового остова через алкильный спейсер С4. Цитотоксичность соединения А15 определена в отношении опухолевых клеток нейробластомы (TET21N) и опухолевых клеток карциномы молочной железы (MCF-7).
Авторами в уровне техники не выявлены фосфониевые соли на основе бетулиновой кислоты, проявляющие цитотоксическую активность в отношении опухолевой клеточной линии РС-3 (аденокарцинома предстательной железы человека).
По данным ВОЗ, смертность от злокачественных новообразований в развитых странах занимает третье место в структуре общей смертности, уступая лишь ишемической болезни сердца и цереброваскулярным нарушениям. Среди онкологических заболеваний существенную часть представляют гормон зависимые опухоли репродуктивной системы.
Рак предстательной железы (РПЖ) считается сегодня одной из самых серьезных медицинских проблем среди мужского населения. В Европе РПЖ является наиболее распространенной солидной неоплазмой (опухолью), заболеваемость которой составляет 214 случаев на 1000 мужчин, опережая рак легких и колоректальный рак. К тому же в настоящее время РПЖ занимает 2-е место среди основных причин смерти от рака у мужчин. Широкое распространение и применение в клинической онкологии получили антрациклиновые антибиотики, в частности, доксорубицин. Однако применение доксорубицина, как и других химиотерапевтических средств, сопряжено с развитием побочных эффектов, в некоторых случаях требующих снижения дозы или полной отмены препарата. Кроме того, со временем развивается резистентность опухолевых клеток к цитостатическому действию доксорубицина.
Задачей изобретения является разработка новых соединений на основе природного лупанового тритерпеноида - бетулиновой кислоты, обладающие высокой противоопухолевой активностью в отношении аденокарциомы простаты и расширяющие арсенал известных лекарственных средств указанного назначения.
Технический результат - новые фосфониевые соли на основе бетулиновой кислоты, обладающие цитотоксической активностью в отношении аденокарциномы предстательной железы на уровне доксорубицина.
Технический результат достигается заявляемыми фосфониевыми солями на основе бетулиновой кислоты формулы (1-5), получаемыми нагреваниием С-28 галогеналкильных эфиров бетулиновой кислоты (6-10) с трифенилфосфином в ацетонитриле в атмосфере аргона по схеме 1
Исходные С-28 галогеналкильные эфиры бетулиновой кислоты (6-10) синтезированы по известной методике: (J. Asian Nat. Prod. Res. 2014, V. 16, 34-42).
Изобретение иллюстрируется примерами получения заявляемых соединений (1-5) и исследования их противоопухолевой активности.
Пример 1. О-(3-Трифенилфосфониопропил)-3β-гидроксилуп-20(29)-ен-28-оат бромид (1) Смесь 1.5 г (2.5 ммоль) соединения 6, 15 мл ацетонитрила и 1.4 г (5.2 ммоль) трифенилфосфина нагревают при кипении в атмосфере аргона 4-5 ч (контроль методом ТСХ). Затем растворитель удаляют отгонкой в вакууме (12 Торр), осадок растворяют в 3 мл CHCl3, осаждают петролейным эфиром и отфильтровывают. Выход 1.8 г (90%). Белый порошок, Т пл.=155°С, [α]D20=-1.0 (С 1.0 CHCl3). ИКС, ν, см-1: 3378 (С3-ОН), 3060, 2943, 2869, 1722 (С=O), 1641 (С=С), 1588, 1439, 1377, 1295, 1154, 1040, 997. 1H ЯМР (CDCl3, 400 МГц)δ, м.д.: 0.73, 0.76, 0.79, 0.93, 0.97 (15Н, с, Н-(23-27)), 1.66 (3Н, с, Н-30), 2.9 (1Н, м, Н-19), 3.16 (1Н, д.д, J=11.1, 4.7 Гц, Н-3), 3.7 (2Н, м, CH2P), 4.46 (2Н, м, С(O)O-CH2), 4.6 (1Н, с, HA-29), 4.7 (1Н, с, HB-29), 7.6-7.8 (15Н, м, Н-Сар); 13С ЯМР (CDCl3, 400 МГц) δС, м.д.: 14.7, 15.4, 16.0, 16.1, 18.2, 19.2, 19.3, 20.8, 22.5, 22.6, 25.4, 27.3, 28.0, 29.0, 29.6, 30.5, 32.0, 36.9, 37.1, 38.1, 38.8, 40.6, 42.3, 46.8, 49.3, 50.4, 55.2, 56.5, 62.8, 63.4, 72.2., 78.7, 109.7, 117.5 (СН, д, J=88.8 Гц, Сипсо), 130.28 (СН, д, J=13.2 Гц, Смета), 133.98 (СН, д, J=11.0 Гц, Сорто), 135.15 (СН, д, J=2.9 Гц, Спара), 150.2, 175.6; 31Р ЯМР (CDCl3, 400 МГц) δР, м.д.: 25.4; Масс спектр (MALDI-TOF), m/z: 681.6 [М-Br]+(вычислено 761.6: [М]+)
Пример 2. О-(5-Трифенилфосфониопентил)-3β-гидроксилуп-20(29)-ен-28-оат бромид (2) получают аналогично примеру 1 из 1.1 г (1.8 ммоль) соединения 7, 15 мл ацетонитрила и 0.95 г (3.6 ммоль) трифенилфосфина. Выход 1.8 г (95%). Белый порошок, Т пл.=150°С, [α]D20=+0.5 (С 1.0 СНС13). ИКС, ν, см-1: 3393 (С3-ОН), 2941, 2868, 1718 (С=O), 1641 (С=С), 1588, 1439, 1376, 1242, 1176, 1046, 983. 1Н ЯМР (CDCl3, 400 МГц)δ, м.д.: 0.74, 0.77, 0.83, 0.93, 0.95 (15Н, с, Н-(23-27)), 1.65 (3Н, с, Н-30), 2.9 (1H, м, Н-19), 3.16 (1Н, д.д, J - 11.1, 4.7 Гц, Н-3), 3.9 (2Н, м, CH2P), 4.0 (2Н, м, С(O)O-CH2), 4.57 (1Н, с, HA-29), 4.7 (1Н, с, HB-29), 7.7-7.9 (15Н, м, Н-Сар); 13С ЯМР (CDCl3, 400 МГц) δС, м.д.: 14.6, 15.3, 16.0, 16.1, 18.2, 19.3, 20.9, 22.2, 22.5, 22.8, 25.5, 26.6, 26.7, 27.4, 28.0, 28.2, 29.6, 29.5, 29.6, 30.6, 32.0, 34.3, 37.0, 37.1, 38.2, 38.7, 39.3, 40.7, 42.3, 47.0, 49.3, 50.5, 55.3, 56.4, 63.2, 78.8, 109.5, 118.4 (СН, д, J=88.8 Гц, Сипсо), 130.28 (СН, д, J=13.2 Гц, Смета), 133.98 (СН, д, J=11.0 Гц, Сорто), 135.15 (СН, д, J=2.9 Гц, Спара), 150.5, 176.0;31Р ЯМР(CDCl3, 400 МГц) δР, м.д.: 24.3 Масс спектр (MALDI-TOF), m/z: 710.6 [М-Br]+(вычислено 790.6:[М]+)
Пример 3. О-(6-Трифенилфосфониогексил)-3β-гидроксилуп-20(29)-ен-28-оат бромид (3) получают аналогично примеру 1 из 0.57 г (0.9 ммоль) соединения 8, 15 мл ацетонитрила и 0.49 г (1.8 ммоль) трифенилфосфина. Выход 0.7 г (85%). Белый порошок, Т пл.=158-162°С, [α]D20=+2.3 (С 0.87 СНС13). ИКС, ν, см-1: 3369 (С3-ОН), 2941, 2866, 1718 (С=O), 1640 (С=С), 1588, 1438, 1376, 1318, 1176, 1047, 983. 1Н ЯМР (CDCl3, 400 МГц)δ, м.д.: 0.74, 0.77, 0.85, 0.93, 0.95 (15Н, с, Н-(23-27)), 1.66 (3H, с, Н-30), 2.95 (1H, м, Н-19), 3.17 (1Н, д.д, J=11.1, 4.7 Гц, Н-3), 3.9 (2Н, м, CH2P), 4.0 (2Н, м, С(O)O-CH2), 4.57 (1H, с, НА-29), 4.68 (1Н, с, HB-29), 7.7-7.9 (15Н, м, Н-Сар); 13С ЯМР (CDCl3, 400 МГц) δС, м.д.: 14.6, 15.3, 16.0, 16.1, 18.2, 19.3, 20.9, 22.5, 22.6, 22.6, 23.0, 25.2, 25.5, 25.7, 25.7, 27.4, 28.0, 28.3, 29.6, 29.9, 30.0, 30.6, 32.1, 34.3, 37.0, 37.1, 38.2, 38.7, 38.8, 40.7, 42.3, 47.0, 49.3, 50.3, 55.3, 56.5, 63.7, 78.9, 109.5, 118.4 (СН, д, J=88.8 Гц, Сипсо), 130.4 (СН, д, J=13.2 Гц, Смета), 133.7 (СН, д, J=11.0 Гц, Сорто), 135.0 (СН, д, J=2.9 Гц, Спара), 150.6, 176.1; 31Р ЯМР (CDC13, 400 МГц) δР, м.д.: 24.9 Масс спектр (MALDI-TOF), m/z: 801.59 [М-Br]+ (вычислено 881.6: [М]+)
Пример 4. О-(9-Трифенилфосфониононил)-3β-гидроксилуп-20(29)-ен-28-оат бромид (4) получают аналогично примеру 1 из 0.5 г (0.75 ммоль) соединения 9, 15 мл ацетонитрила и 0.4 г (1.5 ммоль) трифенилфосфина. Выход 0.6 г (95%). Т пл.=105°С, [α]D20=+1.3 (С 1.0 СНС13). ИКС, ν, см-1: 3371 (С3-ОН), 2936, 2864, 1719 (С=O), 1641 (С=С), 1588, 1484, 1376, 1271, 1176, 1046, 983. 1Н ЯМР (CDCl3, 400 МГц)δ, м.д.: 0.74, 0.80, 0.89, 0.95 (15Н, с, Н-(23-27)), 1.67 (3H, с, Н-30), 2.9 (1Н, м, Н-19), 3.16 (1H, д.д, J=11.1, 4.7 Гц, Н-3), 3.7 (2Н, м, CH2P), 4.0 (2Н, т, J=6.4 Гц С(O)O-CH2), 4.57 (1H, с, HA-29), 4.7 (1Н, с, HB-29), 7.7-7.9 (15Н, м, Н-Сар); 13С ЯМР(СОС13, 400 МГц) δС, м.д.: 14.7, 15.3, 16.0, 16.1, 18.2, 19.3, 20.9, 22.6, 22.7, 22.75, 25.5, 26.0, 27.3, 28.0, 28.6, 29.0, 29.1, 29.6, 30.3, 30.4, 30.6, 30.8, 32.2, 34.3, 37.0, 37.2, 38.3, 38.7, 40.7, 42.4, 47.0, 49.4, 50.5, 55.3, 56.5, 63.9, 78.9, 109.5, 118.4 (СН, д, J=88.8 Гц, Сипсо), 130.28 (СН, д, J=13.2 Гц, Смета), 133.98 (СН, д, J=11.0 Гц, Сорто), 135.15 (СН, д, J=2.9 Гц, Спара), 150.6, 176.2; 31Р ЯМР(CDC13, 400 МГц) δР, м.д.: 24.3 Масс спектр (MALDI-TOF), m/z: 843.9 [M-Br]+ (вычислено 923.9:[М]+)
Пример 5. О-(10-Трифенилфосфониодецил)-3β-гидроксилуп-20(29)-ен-28-оат бромид (5) получают аналогично примеру 1 из 1.35 г (1.9 ммоль) соединения 10, 15 мл ацетонитрила и 1 г (3.9 ммоль). Выход 1.5 г (89%). Белый порошок, Т пл.=110°С, [α]D20=+2.7 (С 1.0 CHCl3). ИКС, ν, см-1: 3393 (С3-ОН), 2933, 2863, 1720 (С=O), 1641 (С=С), 1588, 1484, 1376, 1269, 1176, 1047, 984. 1Н ЯМР (CDCl3, 400 МГц)δ, м.д.: 0.69, 0.75, 0.85, 0.91 (15Н, с, Н-(23-27)), 1.63 (3H, с, Н-30), 2.9 (1Н, м, Н-19), 3.12 (1Н, д.д, J=11.1, 4.7 Гц, Н-3), 3.6 (2Н, м, CH2P), 4.0 (2Н, т, J=6.4 Гц С(O)O-CH2), 4.53 (1H, с, HA-29), 4.66 (1Н, с, HB-29), 7.7-7.9 (15Н, м, Н-Сар); 13С ЯМР(CDCl3, 400 МГц) δС, м.д.: 14.6, 15.4, 15.9, 16.0, 18.2, 19.3, 20.8, 22.6, 22.65, 22.75, 25.5, 26.0, 27.3, 28.0, 28.6, 29.1, 29.3, 29.6, 30.3, 30.5, 30.6, 32.1, 34.3, 37.0, 37.1, 38.2, 38.7, 38.8, 40.7, 42.3, 47.0, 49.3, 50.5, 55.3, 56.5, 63.8, 78.8, 109.5, 118.3 (СН, д, J=88.8 Гц, Сипсо), 130.28 (СН, д, J=13.2 Гц, Смета), 133.98 (СН, д, J=11.0 Гц, Сорто), 135.15 (СН, д, J=2.9 Гц, Спара), 150.6, 176.2; 31Р ЯМР (CDCl3, 400 МГц) δР, м.д.: 24.8; Масс спектр (MALDI-TOF), w/z: 777.6 [M-Br]+ (вычислено 857.6: [М]+)
Пример 6. Биологическая активность
Использовались линия опухолевых клеток РС-3 (аденокарцинома предстательной железы человека), нормальные первичные фибробласты кожи человека (HSF). Клетки культивировали асептически на поверхности культуральных фласков в стандартных условиях: в базовой питательной среде DMEM, содержащей 10% фетальной бычьей сыворотки, 2 mM L-глутамина, 100 U/мл пенициллина и 100 мкг/мл стрептомицина при 37°С в увлажненной воздушной атмосфере с 5% CO2.
Для исследования цитотоксичности клетки высаживали на поверхности 96-луночного планшета в питательной среде. Добавляли к клеткам растворы соединений до конечной концентрации от 2 нМ до 12,5 мкМ и культивировали 3 суток в стандартных условиях. Цитотоксичность соединений оценивали с помощью МТТ-теста согласно стандартному протоколу (The molecular probes handbook. A guide to fluorescent probes and labeling technologies. Editors I. Johnson, M. T. Z. Spence, 11th Edition, 2010, Life technologies, 1060 p)
Жизнеспособность клеток оценивалась как процент от контрольных клеток, выращенных без соединений (жизнеспособность контрольных клеток 100%). Полумаксимальные ингибирующие концентрации (IC50) рассчитывались по кривым жизнеспособности клеток с использованием программного обеспечения OriginPro 8.0.
На основании полученных результатов по цитотоксичности фосфониевых солей бетулиновой кислоты 1-5 можно сделать следующие выводы:
Заявляемые соединения обладают более высокой цитотоксичностью по сравнению с доксорубицином при длине линкера n=3, 5 (соединения 1, 2). Индекс селективности (IS), т.е. отношение значений IC50 для клеток HSF и клеток РС-3, наилучший у соединений 1 и 2, и составляет 17.1 и 11.8 соответственно. Для доксорубицина индекс селективности составляет 8.5.
Таким образом, соединения 1, 2 - фосфониевые соли бетулиновой кислоты обладают высокой цитотоксичностью в отношении опухолевых клеток РС-3 с высокой селективностью в сравнении с нормальными клетками, что свидетельствует о возможности их использования в качестве противоопухолевых препаратов.
Заявлены новые фосфониевые соли на основе бетулиновой кислоты, обладающие высокой цитотоксичностью в отношении аденокарциомы предстательной железы и расширяющие арсенал известных лекарственных средств указанного назначения. Выявлены соединения, превышающие уровень активности доксорубицина и в сравнении с этим препаратом с более высоким индексом селективности по отношению к нормальным клеткам.
1. Фосфониевые соли на основе бетулиновой кислоты формулы 1-5
2. Фосфониевые соли на основе бетулиновой кислоты по п. 1, обладающие цитотоксичностью в отношении аденокарциомы простаты.