Стабилизирующая композиция для биологических материалов
Иллюстрации
Показать всеГруппа изобретений касается стабилизации биологически активного материала. Предложены: сухая композиция в аморфном стеклообразном состоянии для стабилизации биологически активного материала, содержащая указанный биологически активный материал, от 10% до 50% по меньшей мере одного дисахарида, от более чем 10% до 80% по меньшей мере одного олигосахарида, от 0,1% до 10% по меньшей мере одного полисахарида, от 0,5% до 40% по меньшей мере одного гидролизованного белка и по меньшей мере одну соль карбоновой кислоты в количестве 0,5-20%, при этом проценты указаны относительно общей массы композиции, при этом указанный биологически активный материал представляет собой: живую бактерию, гриб, фаг, фермент, белок или пестицид (варианты). Также предложены способ ее получения и продукты ее содержащие (варианты), обеспечивающие повышенную стабильность биологически активного материала. 6 н. и 19 з.п. ф-лы, 20 ил., 1 табл.
Реферат
ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА РОДСТВЕННЫЕ ЗАЯВКИ
[1] Настоящая заявка частично является продолжением заявки на патент США №13/378106, поданной 29 марта 2012 г, которая соответствует национальной фазе международной заявки PCT/US 11/22821, поданной 28 января 2011 г, испрашивающей приоритет согласно предварительной заявке на патент США №61/299 315, поданной 28 января 2010 г. Настоящая заявка также частично является продолжением заявки на патент США №13/208459, поданной 12 августа 2011 г, испрашивающей приоритет согласно предварительной заявке на патент США №61/373711, поданной 13 августа 2010 г. Настоящая заявка также испрашивает приоритет согласно предварительной заявке на патент США №61/614994, поданной 23 марта 2012 г, предварительной заявке на патент США №61/642094, поданной 3 мая 2012 г, и предварительной заявке на патент США №61/646337, поданной 13 мая 2012 г. Содержание всех перечисленных выше заявок, таким образом, включено в настоящий документ посредством ссылок для всех целей.
ОБЛАСТЬ ТЕХНИКИ
[2] Сохранение структуры и функций биологических материалов во время длительного хранения при высоких температурах и влажности имеет фундаментальное значение для пищевой, нутрицевтической и фармацевтической промышленности. Сохранение свойств чувствительных биологических материалов, таких как белки, ферменты, клетки, бактерии и вирусы, часто необходимо при длительном хранении для последующего использования. Несмотря на то, что было опробовано множество способов стабилизации биологических материалов при хранении, многие из них не подходят для чувствительных биологически активных материалов, таких как живые или аттенуированные бактерии и вирусы. Например, традиционная сублимационная сушка сочетает нагрузки, связанные как с замораживанием, так и с высушиванием. Этап замораживания указанного процесса может оказывать нежелательные эффекты, такие как денатурация белков и ферментов и разрыв клеток.
[3] Существует потребность в стабилизирующей композиции, подходящей для широкого диапазона биологических материалов и обеспечивающей высокий уровень стабилизации и предохранения биологических материалов на протяжении длительных периодов времени при повышенных температурах и варьирующей влажности, которые могут возникать, например, при транспортировке и хранении материалов, с сохранением при этом значительного уровня активности при регидрировании. Также существует потребность в стабилизирующих композициях, которые могут применяться при таблетировании с целью избежать чрезмерной потери активности биологических материалов, многие из которых чувствительны к высокому давлению и температуре, возникающим во время таблетирования.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[4] Согласно одному аспекту в настоящем изобретении предложена сухая стабилизирующая композиция для биологически активного материала, содержащая углеводный компонент, содержащий приблизительно от 10% до 80% олигосахарида, приблизительно от 5% до 30% дисахарида и приблизительно от 1% до 10% полисахарида; и белковый компонент, содержащий приблизительно от 0,5% до 40% гидролизованных животных или растительных белков от общей массы указанной композиции. Указанная композиция может быть скомбинирована с биологически активным материалом.
[5] Согласно другому аспекту в настоящем изобретении предложен способ получения описанной выше композиции, скомбинированной с биологически активным материалом, включающий: (a) комбинирование биологически активного материала по меньшей мере с углеводным компонентом и белковым компонентом в водном растворителе с образованием вязкой суспензии; (b) быстрое замораживание указанной суспензии в жидком азоте с образованием твердых замороженных частиц, гранул, капель или нитей; (c) первичное высушивание путем удаления воды в вакууме из продукта этапа (b) при поддержании его при температуре выше температуры замораживания; и (d) вторичное высушивание продукта этапа (c) при максимальном вакууме и температуре 20°C или выше на протяжении времени, достаточного для снижения водной активности до уровня менее 0,3 Aw.
[6] Согласно другому аспекту в настоящем изобретении предложена таблетка, пилюля или пеллета, полученная путем компактирования чувствительного биологически активного материала, внедренного в сухую стеклообразную и аморфную композицию, содержащую один или большее число сахаров и один или большее число гидролизованных белков, причем указанные сахара включают приблизительно от 10% до 60%, а указанные гидролизованные белки включают приблизительно от 1% до 40% от общей сухой массы указанной композиции.
[7] Согласно еще одному аспекту в настоящем изобретении предложен способ получения вышеупомянутой таблетки, пилюли или пеллеты, включающий компактирование чувствительного биологически активного материала, внедренного в сухую стеклообразную и аморфную композицию, отличающийся тем, что указанная сухая стеклообразная и аморфная композиция получена при помощи способа, включающего: (а) комбинирование биологически активного материала по меньшей мере с одним или с большим числом сахаров, и с одним или с большим числом гидролизованных белков в водном растворителе с образованием вязкой суспензии; (b) быстрое замораживание указанной суспензии в жидком азоте с образованием твердых замороженных частиц, гранул, капель или нитей; (с) первичное высушивание путем удаления воды в вакууме из продукта этапа (b) при поддержании его при температуре выше температуры замораживания; и (d) вторичное высушивание продукта этапа (с) при максимальном вакууме и температуре 20°С или выше на протяжении времени, достаточного для снижения водной активности до уровня менее 0,3 Aw.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[8] На фиг. 1 показано повышение стабильности коммерчески доступных пробиотических бактерий и пробиотических бактерий в сухой композиции согласно настоящему изобретению.
[9] На фиг. 2 показано влияние разных молярных отношений усилителей стеклообразования и смеси углеводов в указанной композиции на стабильность пробиотика (L. paracasei) в условиях ускоренного хранения (37°C и 33% отн. вл.).
[10] На фиг. 3 показано влияние композиции согласно настоящему изобретению на стабильность при хранении пробиотической бактерии L. acidophilus. Стабильность сухой пробиотической бактерии тестировали в условиях ускоренного хранения при 24°C и 33% отн. вл. на протяжении 537 дней.
[11] На фиг. 4 показано влияние различных усиливающих стеклообразование соединений на стабильность при хранении пробиотической бактерии L. acidophilus. Стабильность сухой пробиотической бактерии тестировали в условиях ускоренного хранения при 24°C и 43% отн. вл. на протяжении 180 дней.
[12] На фиг. 5 показано влияние различных пропорций белковых гидролизатов/сахаров на стабильность при хранении (35°C и 43% отн. вл.) пробиотической бактерии Bifidobacterium lactis.
[13] На фиг. 6 представлена оптимизация рН для максимальной стабильности пробиотика L. rhamnosus (в условиях ускоренного хранения при 40°C и 33% отн. вл. на протяжении 8 недель).
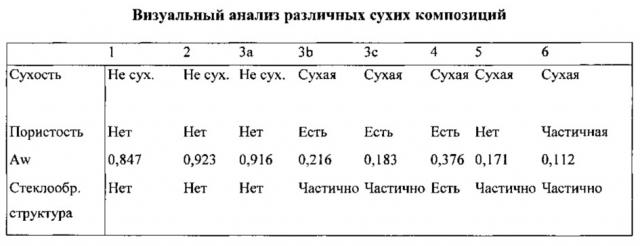
[14] На Фиг. 7 и 8 показан визуальный и микроскопический анализ различных высушенных композиций, содержащих разные матрицы и стеклообразующие агенты, в виде замороженных твердых гранул в соответствии со способом согласно настоящему изобретению.
[15] На Фиг. 9 показано влияние формы культуры L. rhamnosus: свежей, в виде замороженных гранул или сухого порошка, на исходные значения КОЕ в сухой композиции.
[16] На Фиг. 10 показано влияние температуры замораживания композиции, содержащей L. rhamnosus, в виде твердых гранул, замороженных в жидком азоте или в аппарате для глубокого замораживания при температуре -80°C, и в виде незамороженной вязкой суспензии при +4°C, на исходные значения КОЕ бактерий в сухой композиции. Результаты показывают исключительно эффект температуры замораживания суспензии без дополнительного этапа продувки перед высушиванием.
[17] На Фиг. 11 показано влияние температуры замораживания композиции, содержащей Bifidobacterium animalis в виде замороженных твердых гранул в жидком азоте, и в виде незамороженной вязкой суспензии при +4°C, на исходное значение КОЕ бактерии в сухой композиции. Результаты показывают исключительно эффект температуры замораживания суспензии без дополнительного этапа продувки перед высушиванием.
[18] На Фиг. 12 показано влияние продолжительности продувки замороженных твердых гранул в вакууме на исходное число КОЕ L. rhamnosus в сухой композиции.
[19] На Фиг. 13 показаны параметры высушивания композиции в сублимационной сушилке в соответствии со способом согласно настоящему изобретению.
[20] На Фиг. 14 показаны технологические потери и потери при высушивании L. rhamnosus в композициях и способах высушивания согласно настоящему изобретению.
[21] На Фиг. 15 показаны тренды стабильности для композиции с сухой пробиотической бактерией L. rhamnosus при хранении при 40°C и 33% относительной влажности.
[22] На Фиг. 16 показана стабильность при хранении при 40°C и 43% отн. вл. L. acidophilus sp, лиофилизированной обычным способом или включенной в состав предложенной композиции с помощью способов согласно настоящему изобретению.
[23] На Фиг. 17 показана стабильность при хранении при 40°C и 43% отн. вл, а также при 30°C и 60% отн. вл. L. rhamnosus sp, лиофилизированной обычным способом или включенной в состав предложенной композиции с помощью способов согласно настоящему изобретению.
[24] Фиг. 18 демонстрирует влияние прессования в таблеточном прессе на жизнеспособность и стабильность при хранении при 40°C и 43% отн. вл. пробиотика L. rhamnosus, стабилизированного и защищенного в композиции согласно настоящему изобретению.
[25] Фиг. 19 иллюстрирует влияние таблетирования со смесью мультивитаминов и минеральных веществ и хранения при воздействии температуры 40°C и 43% отн. вл. на жизнеспособность пробиотика L. rhamnosus, стабилизированного и защищенного в композиции согласно настоящему изобретению.
[26] Фиг. 20 иллюстрирует влияние прессования в таблеточном прессе на активность ферментов протеазы и липазы в свободной форме или защищенных в композиции согласно настоящему изобретению. Указанные ферменты либо индивидуально таблетировали, либо смешивали в равных пропорциях и затем таблетировали.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ОПРЕДЕЛЕНИЯ
[27] Следует понимать, что терминология, используемая в настоящем документе, предназначена исключительно для описания конкретных вариантов реализации, а не для ограничения. В настоящем описании и прилагаемой формуле изобретения формы единственного числа, в том числе сопровождаемые определением «указанный(ая)», включают соответствующие формы множественного числа, если содержание явно не подразумевает иное. Соответственно, например, упоминание «белка» включает единственный белок или комбинацию двух или более белков; упоминание «фермента», «бактерии» и т.д. включает единственный тип или смеси нескольких типов, и т.д.
[28] В описании и в формуле настоящего изобретения используется, в соответствии с приведенными ниже определениями, следующая терминология.
[29] Термины «биологически активный ингредиент», «биологически активный материал» и «биологический материал» относятся к микроорганизмам или ингредиентам, обеспечивающим биологическую активность. Биологически активные материалы, подходящие для применения согласно настоящему изобретению, включают, не ограничиваясь перечисленными, пептиды, белки, ферменты, гормоны, нуклеиновые кислоты, антитела, лекарственные средства, вакцины, дрожжи, грибы, бактерии (пробиотические или другие), почвенные микробы, вирусы и/или суспензии клеток.
[30] Термин «биологическая композиция» относится к составам, находящимся в форме, однозначно эффективно обеспечивающей биологическую активность биологически активных ингредиентов или агентов.
[31] Термины «усилитель стеклообразования», «соединение, стимулирующее стеклообразование» и «стеклообразующий агент» используются в настоящем документе взаимозаменяемо, обозначая химическое соединение, обладающее способностью к формированию аморфной или стеклообразной структуры ниже критической температуры, температуры перехода в стеклообразное состояние (Tg). При образовании стеклообразной структуры биологические вещества могут быть внедрены в указанную стеклообразную структуру. Усилители стеклообразования, подходящие для применения согласно настоящему изобретению, включают, не ограничиваясь перечисленными, соли органических кислот, таких как молочная кислота, аскорбиновая кислота, малеиновая кислота, щавелевая кислота, малоновая кислота, яблочная кислота, янтарная кислота, лимонная кислота, глюконовая кислота, глутаминовая кислота и т.п. Соли могут включать катионы, такие как натрий, калий, кальций, магний, фосфат и т.п.Другие подходящие усилители стеклообразования включают белки, белковые гидролизаты, полипептиды и аминокислоты. Также включена комбинация стеклообразующих агентов в составе одной композиции. Способ, используемый для получения стеклообразной структуры для целей настоящего изобретения, обычно представлен техникой сублимации и/или испарения растворителя. В идеальном варианте соединения, являющиеся GRAS-соединениями, предпочтительнее соединений, не являющихся GRAS-соединениями.
[32] Термин «сахара» относится к сахаридам, состоящим в основном из атомов углерода, водорода и кислорода. Подходящие сахариды включают редуцирующие и нередуцирующие сахара, а также сахарные спирты и дисахариды. Два моносахарида, соединенные вместе, образуют дисахарид. Два моносахарида, используемые для получения дисахарида, могут быть одинаковыми или разными. Примеры дисахаридов, подходящих для применения в композиции согласно настоящему изобретению, включают сахарозу, трегалозу, лактозу, мальтозу, изомальтозу. Могут также применяться сульфатированные дисахариды.
[33] Термин «углеводы» или «полигидроксисоединения» относится к сахаридам, в основном состоящим из углерода, водорода и кислорода. Сахарид, как правило, состоит из сахарного остова из повторяющихся структурных единиц, связанных линейным или нелинейным образом, часть которых содержит положительно или отрицательно заряженные химические группы. Число повторяющихся единиц может варьировать от двух до нескольких миллионов. Подходящие сахариды включают редуцирующие и нередуцирующие сахара и сахарные спирты, дисахариды, олигосахариды, водорастворимые полисахариды и их производные. Два моносахарида, связанные друг с другом, образуют дисахарид. Два моносахарида, используемые для получения дисахарида, могут быть одинаковыми или разными. Примеры дисахаридов, подходящих для применения в смеси углеводов согласно настоящему изобретению, включают сахарозу, трегалозу, лактозу, мальтозу, изомальтозу. Могут также применяться сульфатированные дисахариды. Небольшое число связанных друг с другом моносахаридов (как правило, от трех до двадцати) образует олигосахарид. Моносахариды, используемые для получения олигосахарида, могут быть одинаковыми или разными сахарными компонентами. Примеры олигосахаридов, подходящих для применения, включают инулин, мальтодекстрины, декстраны, фруктоолигосахариды (ФОС), галактоолигосахариды (ГОС), маннан-олигосахариды (МОС) и их комбинации. Значительное число связанных друг с другом моносахаридов (как правило, более двадцати) образует полисахарид. Моносахариды, используемые для получения полисахарида, могут быть одинаковыми или разными сахарными компонентами. Примеры подходящих для применения полисахаридов включают, не ограничиваясь перечисленными, метилцеллюлозу, гидроксипропилцеллюлозу, гидроксиэтилцеллюлозу и гипромеллозу; растворимые крахмалы или фракции крахмалов, ксантановую камедь, гуаровую камедь, пектины, карраген, галактоманнан, геллановую камедь, включая любые их производные, ацетатфталат целлюлозы (АФЦ), карбоксиметилцеллюлозу, альгинат натрия, соли альгиновой кислоты, гидроксипропилметилцеллюлозу (ГПМЦ), аравийскую камедь, камедь бобов рожкового дерева, хитозан и производные хитозана, коллаген, полигликолевую кислоту, крахмалы, модифицированные крахмалы и цикл о декстрины.
[34] Термин «гидролизованный белок» относится к белку, подвергнутому частичному или полному кислотному или ферментативному гидролизу для получения гидролизованного белка с молекулярной массой от приблизительно 1 кДа до приблизительно 50 кДа. В некоторых вариантах реализации, включающих «глубоко гидролизованный белок» согласно настоящему описанию, по меньшей мере 20% указанного белкового субстрата преобразовано в пептиды с молекулярной массой от 200 до 2000 дальтон. Гидролизованный белок имеет приблизительно такой же аминокислотный состав, что и полноразмерный белок, и может быть получен из любого числа коммерческих источников. Так как гидролизованный белок является гипоаллергенным, может быть целесообразным его применение в определенных пищевых продуктах для гиперчувствительных потребителей, таких как дети младшего возраста и пожилые люди.
[35] «Стабильный» состав или композиция представляет собой такой(ую) состав или композицию, в котором(ой) биологически активный материал по существу сохраняет физическую стабильность, химическую стабильность и/или биологическую активность при хранении. Стабильность может быть измерена при заданных условиях температуры и влажности на протяжении выбранного периода времени. Для оценки ожидаемого срока годности при хранении до фактического истечения данного срока хранения материала может применяться анализ трендов. Для живых бактерий, например, стабильность определяют как период времени, в течение которого происходит снижение значения КОЕ/г сухого состава на 1 логарифмическую единицу в заранее определенных условиях температуры и влажности, и периода времени.
[36] Термин «жизнеспособность» в отношении бактерии относится к способности образовывать колонию (число КОЕ, или колониеобразующих единиц) на питательной среде, подходящей для роста указанной бактерии. Жизнеспособность в отношении вирусов относится к способности инфицировать подходящую клетку-хозяина и воспроизводиться в ней, что приводит к образованию пятна на газоне клеток-хозяев.
[37] «Обычная» комнатная температура или «обычные» условия представляют собой температуру или условия в любой момент времени в определенной среде. Как правило, обычная комнатная температура составляет 22-25°C, обычное атмосферное давление и обычная влажность легко могут быть измерены и варьируют в зависимости от времени года, погоды и климатических условий, высоты и т.д.
[38] Термин «водная активность» или «Aw» в контексте содержащих высушенные композиции составов относится к доступности воды и отражает энергетический статус воды в системе. «Aw» определяют как отношение давления пара воды над образцом к давлению пара чистой воды при той же температуре. Водная активность чистой дистиллированной воды равна единице, т.е. Aw = 1,0.
[39] Термин «относительная влажность» или «отн. вл.» в контексте стабильности при хранении относится к количеству водного пара в воздухе при определенной температуре. Относительная влажность обычно меньше необходимой для насыщения воздуха и выражается в процентах от влажности насыщения.
[40] Термин «сухой» и вариации указанного термина относятся к физическому обезвоженному или безводному состоянию, т.е. по существу отсутствию жидкости. Высушивание включает, например, высушивание распылением, сушку в псевдоожиженном слое, лиофилизацию и вакуумную сушку.
[41] Термин «лиофилизация» или сублимационная сушка относится к получению сухой формы композиции быстрым замораживанием и дегидрированием в замороженном состоянии (иногда называемом сублимацией). Лиофилизацию проводят при температуре, обеспечивающей кристаллизацию сахаров. Указанный процесс может проводиться в вакууме, достаточном для поддержания продукта в замороженном виде, согласно некоторым вариантам реализации - ниже приблизительно 2000 миллиторр.
[42] Этап «первичного удаления воды», «первичное высушивание» или «высушивание жидкости» в отношении процессов, описанных в настоящем документе, относится к дегидрированию, которое начинают после размораживания замороженных частиц и продолжают до момента начала вторичного высушивания. Как правило, основная часть первичного высушивания происходит за счет интенсивного испарения при поддержании температуры продукта на уровне значительно ниже температур источника нагрева. Этот процесс может проводиться в вакууме, достаточном для поддержания продукта в размороженном виде, согласно некоторым вариантам реализации более чем приблизительно >2000 миллиторр.
[43] Термин «вторичное высушивание» в отношении процессов, описанных в настоящем документе, относится к этапу высушивания, который проводят при температурах состава, близких к температуре источника нагрева. Указанный процесс может проводиться в вакууме, достаточном для снижения водной активности состава, согласно некоторым вариантам реализации менее чем приблизительно 1000 миллиторр. В ходе стандартного процесса высушивания на этапе вторичного высушивания водная активность состава снижается до Aw, равного 0,3 или менее.
[44] Настоящее изобретение включает композиции и способы высушивания для предохранения чувствительных биологически активных материалов, таких как пептиды, белки, гормоны, нуклеиновые кислоты, антитела, лекарственные средства вакцины, дрожжи, бактерии (пробиотические или другие), вирусы и/или суспензии клеток, при хранении.
[45] Композиции и способы высушивания согласно настоящему изобретению решают проблему получения малозатратных и подходящих для промышленных масштабов производства сухих составов, содержащих чувствительные биологически активные материалы, такие как пептиды, белки, гормоны, нуклеиновые кислоты, антитела, лекарственные средства, вакцины, дрожжи, бактерии, вирусы и/или суспензии клеток, с существенно увеличенным сроком годности в сухом состоянии. В настоящем изобретении предложена защитная композиция и способ высушивания, включающая(ий) биологический материал, окруженный аморфной стеклообразной структурой из высокорастворимых соединений. Процесс высушивания включает: смешивание биологического материала и композиции с получением жидкой суспензии, быстрое замораживание указанной содержащей композицию суспензии в жидком азоте с образованием капель, нитей или гранул с последующим высушиванием биологически активного материала в стеклообразной сахарной структуре путем испарения жидкости в режиме пониженного давления при нагревании композиции.
[46] Настоящее изобретение основано на примечательном открытии, заключающемся в том, что биологические материалы могут быть защищены стеклообразной структурой с сохранением активности по существу. При комбинировании биологического материала с содержащей композицию смесью и высушивании в соответствии с настоящим изобретением превосходная стабильность достигалась при длительном воздействии жестких условий температуры и влажности. Настоящее изобретение включает композиции, содержащие биологический материал, смесь растворимых углеводов и стимулирующие стеклообразование соли карбоновой кислоты. Композиции согласно настоящему изобретению заведомо отличаются по физической структуре и функции от невязких или концентрированных композиций с сахарами, высушиваемых просто с помощью стандартного способа сублимационной сушки. Например, в патенте США №6919172 описана аэрозольная порошковая композиция для легочного введения, содержащая смесь различных углеводов и цитрата натрия. Однако в описанной в указанном патенте композиции отсутствует дополнительное белковое соединение, критически важное для повышения стабильности и получения требуемой физической структуры при высушивании растворов, содержащих высокие концентрации Сахаров. Также описанная в указанном патенте композиция не обладает вязкой или гидрогелевой структурой, позволяющей осуществлять эффективное высушивание размороженного или незамороженного раствора для стимуляции стеклообразования. Напротив, композиция и процесс высушивания согласно настоящему изобретению позволяют решить все указанные проблемы при обеспечении наилучшей стабильности биологического материала. На существующем уровне техники также неизвестен дополнительный карбоксильный компонент, действующий синергически с гидролизованными белками, защищая и стабилизируя биологический материал.
[47] На существующем уровне техники стимуляция стеклообразной структуры обычно достигается при вспенивании или кипении раствора в вакууме, что способствует эффективному высушиванию. Этап вспенивания, как правило, приводит к интенсивному кипению и разбрызгиванию раствора, что является неизбежным последствием высушивания незамороженного раствора; в результате возможна только очень незначительная загрузка раствора во флакон или сосуд (см, например, патент США №6534087, где толщина готового вспененного продукта составляет менее чем 2 мм). Композиции и способы высушивания согласно настоящему изобретению позволяют избежать кипения и вспенивания указанного состава, позволяя, таким образом, загружать значительное больше материала в зону высушивания, в результате чего масштаб производства может быть легко увеличен для получения значительных количеств материала без применения специально разработанных сосудов, лотков или оборудования.
[48] В сочетании с предложенной с настоящем изобретении композицией для получения водной защитной среды в соответствии с настоящим изобретением может использоваться широкий спектр биологических материалов. Указанная защитная среда может затем подвергаться высушиванию с применением способов согласно настоящему изобретению для получения стабильного сухого порошка с указанным биологическим материалом. Указанные биологические материалы включают без ограничения: ферменты, такие как ферменты поджелудочной железы, липаза, амилаза, протеаза, фитаза, лактатдегидрогеназа; белки, такие как инсулин; вакцины; вирусы, такие как аденовирус; клетки, включая прокариотические клетки (включая бактерии и грибы) и эукариотические клетки, другие биологические материалы, включая лекарственные средства, нуклеиновые кислоты, пептиды, гормоны, витамины, каротеноиды, минеральные вещества, антибиотики, микробиоциды, фунгициды, гербициды, инсектициды, спермициды, антитела и липидные пузырьки.
[49] Как было показано, целесообразно использование композиций и способов высушивания согласно настоящему изобретению, в частности, для пробиотических бактерий. Стабильный сухой пробиотический порошок получают в соответствии с композициями и способами согласно настоящему изобретению, включая смешивание свежих, замороженных или сухих культур пробиотических бактерий со смесью углеводов и стимулирующих стеклообразование соединений, быстрое замораживание вязкого состава в жидком азоте для получения замороженных твердых капель, нитей или гранул, и высушивание с помощью предварительного применения вакуума, достаточного для увеличения температуры состава до значений, превышающих температуру замерзания, и использования источника нагревания с температурой 20°C и выше для облегчения первичного удаления воды. Поддержание температуры указанного состава выше точки замерзания может осуществляться путем регулировки вакуума и передачи тепла составу. Для завершения процесса высушивания и дополнительного уменьшения водной активности указанного состава до уровня менее Aw 0,3 или ниже проводят этап вторичного высушивания при максимальном вакууме и повышении температуры до 70°C включительно. Такая композиция способна сохранять стабильность в условиях хранения с температурой 40°C и 33% отн. вл. на протяжении 30 дней или более, как видно из фиг. 15.
[50] В частности, как было показано, целесообразно использование композиций и способов высушивания согласно настоящему изобретению для живых микроорганизмов, таких как пробиотическая бактерия, в прессованных таблетках. Стабильный сухой биологический порошок получают в соответствии с композициями и способами согласно настоящему изобретению, включая смешивание свежих, замороженных или сухих культур одноклеточных организмов со смесью Сахаров, гидролизованных белков и антиоксиданта, и, потенциально, включением дополнительных количеств полисахаридов и олигосахаридов и стимулирующих стеклообразование соединений, быстрое замораживание вязкого состава в жидком азоте для получения замороженных твердых капель, нитей или гранул, испарение воды путем предварительного применения вакуума, достаточного для увеличения температуры состава выше его температуры замораживания, и использования источника нагревания с температурой 20°C и выше, что облегчает первичное удаление воды. Поддержание температуры указанного состава на уровне выше точки замерзания может быть осуществлено путем доведения вакуума и передачи тепла или теплового облучения состава. Для завершения процесса высушивания и дополнительного уменьшения водной активности указанного состава до уровня менее Aw 0,3 или ниже, проводят этап вторичного высушивания при максимальном вакууме и повышении температуры до 70°C включительно.
КОМПОЗИЦИИ СОГЛАСНО НАСТОЯЩЕМУ ИЗОБРЕТЕНИЮ
[51] Согласно некоторым вариантам реализации состав содержит смесь углеводов дисахаридов, олигосахаридов и полисахаридов, куда внедрен биологически активный материал. Примеры подходящих полисахаридов включают, не ограничиваясь перечисленными, ацетатфталат целлюлозы (АФЦ), карбоксиметилцеллюлозу, пектин, альгинат натрия, соли альгиновой кислоты, гидроксипропилметилцеллюлозу (ГПМЦ), метилцеллюлозу, каррагинан, геллановую камедь, гуаровую камедь, аравийскую камедь, ксантановую камедь, камедь бобов рожкового дерева, хитозан и производные хитозана, коллаген, полигликолевую кислоту, крахмалы и модифицированные крахмалы. Примеры подходящих олигосахаридов включают, не ограничиваясь перечисленными, циклодекстрины, фруктаны, инулин, ФОС, мальтодекстрины, декстраны и т.д.; и их комбинации. Примеры подходящего дисахарида включают, не ограничиваясь перечисленными, лактозу, трегалозу, сахарозу и т.д. Согласно конкретному варианту реализации подходящий типовой полисахарид представляет собой альгинат натрия или геллановую камедь. Согласно другим вариантам реализации указанный состав содержит, в процентах по массе от общего содержания сухого вещества, 0,1-20% альгината натрия.
[52] Согласно некоторым вариантам реализации смесь углеводов содержит, в процентах по массе от общего содержания сухого вещества, 0, 1-10% полисахаридов, 1-10% олигосахаридов и 10-90% дисахаридов. Согласно дополнительному варианту реализации смесь углеводов содержит дисахариды, олигосахариды и полисахариды в массовых долях 10:0,1-4:0,1-2, или отличается тем, что массовые доли дисахаридов/олигосахаридов/полисахаридов составляют от приблизительно 10:0,2:0,1 до приблизительно 10:2:1.
[53] Согласно некоторым вариантам реализации фракция дисахаридов в смеси углеводов включает различные сахара и сахарные спирты. Подходящие дисахариды представляют собой дисахариды, не кристаллизующиеся и/или не повреждающие и не дестабилизирующие биологически активный материал в составе при температурах замораживания (например, ниже чем -20°C) и во время удаления воды. Например, биологически активный материал может быть высушен в присутствии стеклообразующих Сахаров, таких как сахароза, лактоза или трегалоза, что способствует сохранению молекулярной структуры на протяжении процесса высушивания и придает структурную жесткость аморфной матрице в сухом состоянии. Подходящий дисахарид будет эффективно замещать воду при снижении влагосодержания при высушивании, предотвращать повреждение клеточных мембран и денатурацию ферментов (см. обзор Crowe et al, 1998). Другие функции дисахарида в указанной композиции могут включать защиту биологически активного материала от повреждающего воздействия света, кислорода, окислительных агентов и влажности. Подходящий дисахарид должен легко растворяться в растворе. В частности, трегалоза представляет собой представляющее интерес защитное средство, поскольку является нередуцирующим дисахаридом, обнаруживаемым в растениях и живых организмах (например, бактериях, грибах и беспозвоночных, таких как насекомые и нематоды), остающихся в состоянии покоя (спячки) на протяжении периодов засухи. В некоторых случаях может быть целесообразным включение двух или большего числа разных дисахаридов, например, смеси трегалозы и сахарозы, для подавления образования кристаллов, увеличения стабильности высушенного состава с биологически активным материалов при хранении на протяжении длительных периодов времени и снижения расходов.
[54] Согласно некоторым вариантам реализации фракция олигосахаридов в смеси углеводов включает инулин, мальтодекстрины, декстраны, фруктоолигосахариды (ФОС), галактоолигосахариды (ГОС), маннан-олигосахариды (МОС) и их комбинации. Указанные олигосахариды разрешают несколько проблем, связанных с применением монокомпонентной трегалозы в качестве защитного средства для ряда биологических материалов, которые необходимо предохранить. При высокой эффективности в отношении защиты биологического материала при дегидрировании и регидрировании монокомпонентная трегалоза в качестве стабилизатора не обеспечивает требуемой стабильности при хранении на протяжении длительных периоды времени, в частности, при высоких температурах и/или во влажной среде. Указанная проблема в настоящем изобретении решена добавлением олигосахаридов, например, инулина, в смесь углеводов.
[55] Подходящие типовые массовые доли сахаридов в смеси углеводов: 10:0,1-10:0,1-2 дисахаридов/олигосахаридов/полисахаридов; согласно некоторым вариантам реализации массовые доли дисахаридов/олигосахаридов/полисахаридов составляют от приблизительно 10:0,2:0,1 до приблизительно 5:10:1. Согласно некоторым вариантам реализации смесь углеводов содержит, в процентах по массе от общего содержания сухого вещества, 10-90% дисахаридов, 1-10% олигосахаридов и 0,1-10% полисахаридов. Согласно другим вариантам реализации смесь углеводов содержит в процентах по массе от общего содержания сухого вещества 10-50% дисахаридов, 10-80% олигосахаридов и 0,1-10% полисахаридов.
[56] Согласно конкретному варианту реализации состав содержит смесь олигосахаридов. Указанная смесь олигосахаридов сокращает ряд проблем, связанных с применением единственного олигосахарида как монокомпонента в качестве стимулирующего стеклообразование материала в композиции. Высокоэффективно повышая температуру перехода в стеклообразное состояние, олигосахариды, однако, проявляют тенденцию к быстрой кристаллизации и осаждению, и, соответственно, фрагментации стеклообразной аморфной структуры, в частности, при высоких температурах и/или во влажной среде. Указанная проблема была решена в настоящем изобретении путем добавления смеси олигосахаридов вместо олигосахарида одного типа, согласно некоторым вариантам реализации - смеси фруктанов и декстринов с низким ДЭ. Согласно некоторым вариантам реализации смесь углеводов содержит, в процентах по массе от общего содержания сухого вещества, 5-40% фруктанов и 5-40% декстринов с низким ДЭ.
[57] Одна из подходящих композиций содержит от приблизительно 0,5% до приблизительно 90% углеводного компонента, включая по меньшей мере дисахарид, олигосахарид и полисахарид, и белковый компонент, содержащий от приблизительно 0,5% до приблизительно 40% гидролизованного белка. Согласно некоторым вариантам реализации композиция содержит от приблизительно 30% до приблизительно 70% углеводного компонента и приблизительно 1% до приблизительно 40% усиливающего стеклообразование компонента, такого как белок гидролизованный белок и карбоновая кислота, при этом указанный углеводный компонент содержит от приблизительно 10% до 90%, или от приблизительно 40% до 80% дисахарида; от приблизительно 1% до приблизительно 10%, или от приблизительно 5% до 10% олигосахарида; и от приблизительно 0,1 до приблизительно 10%, или от приблизительно 5% до приблизительно 10% полисахарида. Указанная композиция также содержит соль органической кислоты, которая считается еще одним усиливающим стеклообразование компонентом и