Способ диагностики рака легкого по анализу выдыхаемого пациентом воздуха на основе анализа биоэлектрических потенциалов обонятельного анализатора крысы
Иллюстрации
Показать всеИзобретение относится к медицине, в частности к исследованию и анализу газообразных биологических материалов, и может быть использовано для диагностики рака легкого у человека. Способ основан на анализе выдыхаемого пациентом воздуха путем анализа биоэлектрических потенциалов обонятельного анализатора крысы. Для этого имплантируют в верхнюю поверхность обонятельной луковицы крысы микроэлектродную матрицу с рабочими электродами и, по меньшей мере, одним референтным электродом, имплантированным в кость. Регистрируют биоэлектрические сигналы обонятельной луковицы в заданном диапазоне частот 1-250 Гц в момент вдоха. Извлекают при анализе цифровых рядов шесть групп первичных признаков: коэффициенты кросс-корреляции амплитуд биоэлектрического сигнала между отведениями, коэффициенты кросс-корреляции амплитуд частот между отведениями, бинарные векторы амплитуд сигнала, числовые характеристики распределения амплитуд сигнала, числовые характеристики распределения коэффициентов Фурье и числовые характеристики распределения коэффициентов вейвлета Добеши-4 для каждого отведения. Проводят обработку каждой группы признаков отдельной многослойной нейронной сетью (МНС). Формируют вторичные признаки, выраженные в виде вероятностных оценок классов проб воздуха от МНС после обработки первичных признаков. Проводят обучение каждой МНС для вычисления весовых коэффициентов классификации по алгоритму обратного распространения ошибки на дополнительно сформированном массиве указателей класса проб воздуха, предъявляемых крысе заданное количество раз от заданного количества источников. Идентифицируют класс пробы воздуха путем расчета шести групп первичных признаков биоэлектрического сигнала. Вычисляют шестью МНС предварительные вероятностные оценки принадлежности предъявляемой крысе пробы воздуха к отрицательному классу, связанному с отсутствием биомаркера рака легкого. Вычисляют предварительные оценки принадлежности к положительному классу, связанному с наличием биомаркера рака легкого. И вычисляют седьмую МНС итоговой вероятности класса пробы воздуха и выбора класса с максимальной вероятностью при усреднении по всем вдохам крысы пробы воздуха в качестве результата распознавания. Способ обеспечивает повышение точности распознавания выдыхаемого пациентом воздуха и упрощение исследования за счет исключения обучения крысы распознавать вещества в выдыхаемом воздухе. 4 з.п. ф-лы, 18 ил., 2 табл.
Реферат
Область техники
Изобретение относится к медицине, а именно к исследованию и анализу газообразных биологических материалов, в частности продуктов дыхания и может быть использовано для диагностики рака легкого у человека с использованием регистрации биоэлектрической активности от обонятельной луковицы крысы.
Уровень техники
Известно использование в качестве биомаркеров в выдыхаемом пациентом воздухе низкомолекулярных белков, характерных для ранней стадии рака легкого. Анализ конденсата выдыхаемого воздуха (КВВ) является перспективным неинвазивным методом оценки состояния дыхательной системы. Многие исследователи указывают на важность анализа протеома КВВ для раннего выявления заболеваний респираторного тракта, в т.ч. диагностики рака легкого (РЛ) (Рябоконь A.M., Анаев Э.Х., Кононихин А.С., Стародубцева Н.Л., Киреева Г.Х., Попов И.А., Кукаев Е.Н., Бармин В.В., Багров В.А., Пикин О.В., Николаев Е.Н., Варфоломеев С.Д. Сравнительный протеомный анализ конденсата выдыхаемого воздуха у пациентов с раком легкого методом масс-спектрометрии высокого разрешения // Пульмонология. 2014. Т. 1 С. 1-10) [1]. Методом жидкостной хроматографии и тандемной масс спектрометрии была проведена идентификация потенциальных белков - онкомаркеров в КВВ. Образцы КВВ были собраны с помощью одноразового портативного конденсора R-Tube. Было показано, что группа кератинов более выражена у онкологических больных по сравнению с практически здоровыми лицами. В КВВ доноров основной группы были определены, в частности, 6 белков, в т.ч. b- и a-субъединицы гемоглобина, ядерный убиквитиновый казеин (NUCKS), белки группы высокой мобильности (HMG-I/HMQ-Y), лактоферрин. Большинство выявленных белков было предложено в качестве панели для диагностики РЛ. Однако необходимы дальнейшие исследования для определения диагностической значимости предложенных биомаркеров и их роли в патогенезе РЛ.
В статье (Фёдоров В.И., Карапузиков А.А., Старикова М.К. Белки, пептиды и аминокислоты выдыхаемого воздуха как маркеры бронхо-легочных заболеваний // Бюллетень сибирской медицины. 2013. N12 (6). Р. 167-174. DOI:10.20538/1682-0363-2013-6-167-174) [2] показано присутствие в конденсате выдыхаемого воздуха больных немелкоклеточным раком легких интерлейкинов (ИЛ) и фактора некроза опухоли а. Показано, что содержание этих веществ отчетливо коррелирует с тяжестью заболевания. При воспалительных заболеваниях в КВВ детектируются различные интерлейкины: ИЛ-1β, ИЛ-6, ИЛ-8, ИЛ-10, ИЛ-12р70 и фактор некроза опухоли α, являющиеся четкими индикаторами воспалительных реакций. Показано, что у больных с воспалением легких концентрация всех исследованных интерлейкинов выше, чем у здоровых лиц. Наряду с цитокинами и хемокинами, в выдыхаемом воздухе содержатся различные белки, в частности C-реактивный белок, являющийся маркером воспаления, муцин и альбумин. У больных немелкоклеточным раком легких в КВВ повышено содержание лептина и эндотелина-1 по сравнению со здоровыми субъектами, причем их концентрация наиболее высоко в IV стадии заболевания.
Появились работы, в которых с помощью масс-спектрометрии установлено, что в выдыхаемом воздухе пациентов с РЛ присутствует устойчивый набор летучих органических соединений, в основном производных алканов. С использованием этих маркеров был разработан тест на наличие заболевания, который продемонстрировал специфичность на уровне 80%. Результат анализа не зависел от стадии рака (Вакс В.Л., Домрачева Е.Г., Собакинская Е.А., Черняева М.Б. Анализ выдыхаемого воздуха: физические методы, приборы и медицинская диагностика // Успехи физиологических наук. 2014. 184. С. 739-758) [3].
В работе D. Poli с соавторами создана предварительная модель для выявления заболевания РЛ на основе регистрации в выдыхаемом воздухе органических соединений (13 алифатических и ароматических углеводородов, 9 альдегидов) и перекиси в конденсате. Специфичность анализа составила - 71%. (Poli D. in Breath Analysis Summit. Intern. Conf. on Breath Research, 11-14 September 2011. Parma. Italy. Abstract Book (Piacenza: Nuova Editrice Berti. 2011) P. 194) [4].
Из многочисленных патентных источников выявлены устройства и способы диагностики РЛ по выдыхаемому воздуху.
Известен способ анализа образцов выдыхаемого воздуха на биомаркеры различных заболеваний, в том числе и рака легкого, основанный на использовании сенсоров на основе нанотрубок (заявка US 8366630 В2, МПК G01N 27/22, G01N 33/0034, G01N 27/414, B82Y 15/00, G01N 33/497, G01N 27/02, G01N 27/04, G01N 33/0047, G01N 2033/4975, дата публикации 05-02-2013. Carbon nanotube structures in sensor apparatuses for analyzing biomarkers in breath samples) [5]. Онкологическое заболевание определяют по обнаружению органических соединений, содержащих функциональные группы, принадлежащие к различным классам: алканов, циклоалканов, аренов, аминов, эфиров и др. Заболевание диагностируется в случае обнаружения соединения с определенными функциональными группами на основе статистического анализа, включающего (как минимум) один из таких статистических методов, как метод главных компонент (principal component analysis, РСА), вычисление радиально-базисных функций (radial bias function, REF), линейный дискриминантный анализ (linear discriminant analysis, LDA), искусственные нейронные сети и др. Указанный способ включает в себя диагностику различных заболеваний (артрит, атеросклероз, сахарный диабет второго типа и др.), в т.ч., различных видов рака (предстательной железы, почек, легкого). Однако, как любая универсальная система, для диагностики какого-то определенного вида заболеваний, например, рака легкого, требует сложной настройки для использования именно тех компонентов системы, которые подходят в данном случае, что усложняет всю процедуру, включая пробоподготовку, и увеличивает ее стоимость.
Известна система анализа дыхания и способ диагностики астмы, туберкулеза и рака легких (заявка US 2010/0137733 А1, МПК А61В 5/08, дата публикации 03-06-2010, Breath analysis systems and methods for asthma, tuberculosis and lung cancer diagnostics and disease management) [6]. Данная система используется для диагностики и последующего мониторинга состояния пациента с обнаруженным заболеванием. Для диагностики рака система включает маску для забора воздуха, которая соединена с системой анализа и распознавания. Диагностирование заболевания происходит на основании определения в пробе определенных летучих органических соединений (ЛОС) методом газовой хроматографии. ЛОС представляют собой группу химических соединений, включающую 4-метилоктан, 2,4-диметилгептан, изопропиловый спирт, толуол, изопрен, алкан, уксусную кислоту, ацетон, 2,6,11-триметил додекан, 3,7-диметил-ундекан, 2,3-диметил гептан и их комбинации. Прибор подвижно соединен с детекторной матрицей, анализирующей полученной пробы.
Известен способ диагностики рака легкого, основанный на обнаружении методом масс-спектрометрии с предварительным газохроматографическим разделением веществ в выдыхаемом пациентом воздухе циклогексил изотиоцианата (RU 2538625, МПК А61В 5/08, G01N 33/497, дата публикации 10-01-2015) [7]. Указанное вещество может служить маркером рака вне зависимости от его локализации, степени и формы для экспресс-диагностики онкологических заболеваний организма при скрининговом обследовании населения. При обследовании лиц без признаков онкозаболевания данное соединение не обнаруживалось. Согласно указанному способу, выдыхаемый выдыхаемый воздух отбирается в емкости, изготовленные из инертного материала. После отбора фиксированное количество газообразного образца при помощи аспиратора в заданных постоянных условиях прокачивается через трубку, заполненную сорбентом. Таким образом полученные и концентрированные на сорбенте образцы подвергаются дальнейшему анализу на хромато-масс-спектрометре, снабженном термодесорбером.
Европейской группой по изучению опухолевых маркеров (EGTM) рекомендовано определение следующих опухолевых маркеров: при мелкоклеточном раке легкого - нейрон-специфической энолазы (НСЕ), маркера, ассоциированного с опухолями нейроэндокринной дифференцировки; при немелкоклеточном - CYFRA 21.1 (наиболее информативного при плоскоклеточном раке) и РЭА (при аденокарциноме и крупноклеточной карциноме). (Кадагидзе З.Г., Шелепова В.М. Опухолевые маркеры в современной клинической практике // Вестник Московского Онкологического Общества. 2007. №1. С. 56-59) [8].
Известен многоканальный «электронный нос» на пьезосенсорах (RU 2327984 С1, МПК G01N 33/00, дата публикации 27-06-2008) [9], с использованием которого по специальной программе проводят обработку полученных откликов, их преобразование в диаграммы или рисунки, сопоставление с банком данных и принятие решения по результатам анализа. Микропроцессоры фиксируют сигналы одновременно всех пьезосенсоров во всех ячейках (с 1-го по i-тый сенсор для каждой ячейки) в парах анализируемой пробы или без нагрузки. Сигналы преобразуются и передаются в компьютер или другое устройство по кабелю, анализируются по определенному алгоритму и формируются в кинетический «визуальный отпечаток» запаха, который представляет собой суммарный отклик матрицы пьезосенсоров и несет аналитическую информацию. Изобретение позволяет анализировать газообразные пробы различного состава, в том числе мало отличающиеся друг от друга, содержащие определяемые компоненты на уровне микроконцентраций и повысить селективность определения легколетучих соединений в газовых смесях за счет двух-n-кратного увеличения количества сенсоров при сохранении объема корпуса ячейки детектирования.
Известно аппарат для скрининга (ЕР 1234540 А1, МПК А61В 5/0484, А61В 5/0478, A61N 1/05, A01K 67/00, G01N 33/50, G01N 33/15, дата публикации 2002-08-28) [10], которое содержит средство для введения к обонятельной выстилке слизистой носа, тестируемого животного стимулирующее соединение, микроэлектродную матрицу, часть которой имплантирована в обонятельную луковицу испытуемого животного для измерения электрического сигнала, генерируемого в обонятельной луковице в ответ на стимулирующее соединение, средство обработки для анализа корреляции между электрическим сигналом и физиологическим ответом, индуцированным у подопытного животного. Аппарат для скрининга измеряет паттерн стимуляции обонятельной луковицы, который формируется, когда обонятельная выстилка стимулируется веществом, которое представляет собой компонент наркотика и вводится к обонятельной выстилке организма. Устройство скрининга затем анализирует паттерн стимуляции таким образом, чтобы проверить корреляцию между паттерном стимуляции и физиологической реакцией, вызванной в организме веществом, которое активирует или подавляет мозг через стимуляцию обонятельной выстилки. Электродная матрица крепится на обонятельной луковице экспериментального животного. Измерительный электрод содержит субстрат, сформированный из изолирующей пленки и шестнадцати микроэлектродов, которые расположены на поверхности субстрата в форме 4×4 матрицы. Субстрат имеет толщину от 1 мкм до 100 мкм и формируется в виде квадрата, каждая сторона которого составляет около 2 мм. Шаг между парой соседних микроэлектродов составляет около 500 мкм. Изобретение применяется для лечения сниженной обонятельной чувствительности и включает шаги: введение компонента вещества возбуждающего обонятельную луковицу; измерение электрического сигнала, генерируемого в обонятельной луковице экспериментального животного, когда компонент вещества, воздействующий на обонятельную слизистую, управляет обонятельной выстилкой экспериментального животного для получения паттерна электрического сигнала: определение корреляции между электрическим паттерном сигнала, а также тип и уровень физиологического ответа, индуцированного у подопытного животного паттерном электрического сигнала; и подача паттерна электрического сигнала, который является достаточным для генерирования, предполагаемой физиологической реакции, к обонятельной луковице тестируемого животного в виде паттерна стимуляции. Устройство используется для тестирования фармацевтических препаратов.
Известно электроэнцефалографическое устройство для маленьких животных и измерительная система, используемая для него, (WO 2011132756 (А1), МПК А61В 5/0408, А61В 5/0478, A01K 67/00, А61В 5/0492, А61В 5/0476, А61В 5/055, дата публикации 2011-10-27) [11]. Задачей изобретения является регистрация ЭЭГ головного мозга маленького животного для фармакологического скрининга в сочетании с фМРТ. Предложена структура электродов, содержащая основание, которое покрывает кожу головы или головного мозга небольшого животного и имеет множество сквозных отверстий для электродов. Каждый из множества электродов содержит внутреннюю и внешнюю трубку, пространство между которыми заполнено энцефалографической пастой и физраствором. Система используется для не инвазивной регистрации ЭЭГ одновременно с функциональной магниторезонансной томографией (фМРТ), а также электрокардиограммой (ЭКГ) и инфракрасной спектроскопией.
Известна система и способ для обнаружения активности мозга в ответ на химический раздражитель включает имплантацию электродов в мозг субъекта и измерение амплитуды соответствующих мозговых волн до и после введения химического раздражителя (WO 2005037100 А1, МПК А61В 5/0484, А61В 5/04847, А61В 5/4011, дата публикации 2005-04-28) [12]. Химический стимул представляет собой соединение или смесь соединений микробного, бактериального или фитохимического происхождения. Химический стимул, который вызывает желаемое изменение, может быть использован в фармацевтической, пищевой, косметической или другой промышленной продукции, потребляемой человеком или животным, или использоваться в целях повышения уровня чувствительности при вкусовых и запаховых дисфункциях. Система использует два измерительных электрода: один в структурах лимбической системы (гиппокампе или миндалине), а другой в орбитофронтальной коре или области вентральной покрышки, референтный электрод, имплантирован в пириформную кору или обонятельную луковицу головного мозга крысы, мыши. Измеряют амплитуду альфа, бета, гамма, дельта, или тета волн мозга. Исследуемые вещества вводят перорально или назально с помощью специального модуля. Система содержит средство для обработки и анализа корреляции между измеренным электрическим сигналом и мозговой активностью. Предъявляемыми химическими стимулами являются запах или вкус. Система используется в терапевтических целях.
Известен способ и устройство для управления перемещением животного посредством стимуляции мозга (US 2013098310 А1, МПК A01K 15/02, B62D 63/02, A01K 1/03, A61N 1/36, A61N 1/372, G06N 3/06, Н02Н 1/00, A61N 1/08, дата публикации 2013-04-25) [13]. Микроэлектродная матрица имплантирована в различные зоны головного мозга крысы для дистанционного управления животным для поиска и спасения людей. Изобретение может быть использовано для целей правоохранительных органов, военных и других целей. В зависимости от выбора зоны стимуляции головного мозга, подкрепленных стимуляцией центра удовольствия, крыса перемещается по команде пользователя в заданных направлениях, в которых обучается искать целевые запахи и может автономно нести электронные датчики в недоступные или опасные места для проведения различных миссий, в том числе для поиска людей, похороненных в куче щебня, правоохранительных операций и обнаружения взрывчатых веществ, химикатов и других опасных материалов. Это изобретение направлено на решение вышеуказанных и других проблем путем создания способа и устройства для телеуправления, наведения и тренировки обнаружению запаха, свободно перемещающегося животного через стимуляцию его мозга. В одной из возможных конструкций, используются шестнадцать электродов, имплантированных в мозг животного. Электроды имплантируют в вентральную область покрышки или другие области латерального гипоталамуса для стимуляции центра удовольствия при обучении распознавания запахов. Однако, известный способ связан с выработкой условных рефлексов животного на получение награды.
Известно изобретение, связанное с оценкой запаха (WO 9844843 (А1), МПК А61В 5/0484, дата публикации 1998-10-15) [14]. В описанной системе регистрируют электроэнцефалограмму (ЭЭГ) в 16 областях (четырех центральных Fz, Cz, Pz, Oz и 12 боковых Fp1, Fp2, F3, F4, С3, C4, Р3, P4, Т3, T4, Т5, Т6). Электроокулограмму (ЭОГ) регистрировали для выделения артефактов соответствующих глазным движениям. Связанные с событием потенциалы (ССП) регистрировали в ответ на зрительный стимул, который мог быть ассоциирован с запахом. Примерами, использовавшихся зрительных стимулов, являются фрукты, цветы, овощи, здания, люди, продукты питания, на открытом воздухе и т.д. В целом было 150 фотографий в каждом классе, и они были представлены на экране VDU перед субъектом в случайном порядке.
Описываемая система оценки запахов используется для улучшения восприятия выпускаемой продукции на основе регистрации ЭЭГ и ССП человека, тогда как разрабатываемое изобретение для диагностики заболеваний.
Известен метод анализа мозговой активности субъекта (WO 2016059055 (А1), МПК А61В 5/00; А61В 5/055; G06T 7/00, дата публикации 2016-04-21) [15]. Система может быть использована для диагностики различных состояний мозга здорового человека (сон/бодрствование), а также состояний мозга, связанных с психическими расстройствами (такими как депрессия, шизофрения, аутизм). Данная система используется для диагностики мозговых дисфункций человека по регистрируемой активности мозга.
Из анализа предшествующего уровня техники следует, что задача диагностики РЛ по выдыхаемому воздуху решалась многочисленными коллективами исследователей аппаратными методами с использованием сложного аналитического оборудования и широкого спектра биомаркеров.
Наиболее близким аналогом по выполнению - использование электрической активности мозга крысы для обнаружения малых количеств вещества, к настоящему изобретению является детектор наркотиков на основе обоняния животного (CN 1865996, МПК А61В 5/00, G01N 33/00, дата публикации 2006-11-22, Drug detector based on animal olfactory sensation) [16], принимаемый за прототип, который включает: видеокамеру, микроэлектродную матрицу, референтный электрод, закрепленный винтами на черепе животного, предусилитель, фильтр, четырехрукавный лабиринт для подачи запахов крысе и компьютерную систему управления и анализа. На этапе обучения животное помещают в центральную область лабиринта, исследуемое вещество - в камеру на конце одного из рукавов. При правильном выборе камеры крыса получает стимуляцию центра удовольствия с одновременной подачей пищи. Наблюдение за поведением животного ведется с помощью видеокамеры, подключенной к персональному компьютеру. Электрическую активность мозга крысы при правильном выборе места нахождения летучего вещества записывают на карту сбора данных. В реальных условиях биоэлектрическая активность мозга крысы сравнивается с активностью, содержащейся в базе данных, и на основе анализа совпадений делают вывод о наличии наркотика в проверяемом объекте.
Недостатками известного способа являются трудоемкость и сложность его реализации, обусловленная необходимостью предварительного обучения животного с пищевым подкреплением, визуальным наблюдением, дополнительной стимуляцией центра удовольствия, и отсутствие данных о чувствительности способа выявления заданного вещества, которая зависит от концентрации паров вещества и расстояния до обонятельного анализатора крысы. Сведения о возможности диагностики РЛ по выдыхаемому воздуху отсутствуют.
Раскрытие изобретения.
Технический результат заключается в расширении арсенала технических средств, а именно использование абонятельного анализатора крысы для выявления маркеров рака легких в выдыхаемом воздухе. Это очевидно проще, нежели использование сложной и дорогой аппаратуры типа масспектрометров или нанотрубок.
В сравнении с известными способами анализа анализатора крысы, техническим результатом является повышение точности распознавания выдыхаемого пациентом воздуха на положительную, связанную с наличием биомаркера РЛ, и отрицательную, связанную с отсутствием биомаркера РЛ, реакцию и упрощение способа за счет исключения обучения крысы распознавать вещества в выдыхаемом воздухе.
Технический результат достигается тем, что способ диагностики рака легкого по выдыхаемому воздуху на основе анализа биоэлектрических потенциалов обонятельного анализатора крысы заключается в имплантации в верхнюю поверхность обонятельной луковицы крысы микроэлектродной матрицы с восемью электродами, имплантации в носовую кость референтного электрода, регистрации биоэлектрической активности обонятельной луковицы в диапазоне частот 1-250 Гц на фазе вдоха, извлечении шести групп первичных признаков, представляющих собой 1) коэффициенты кросс-корреляции амплитуд сигнала между отведениями, 2) коэффициенты кросс-корреляции амплитуд частот между отведениями, 3) бинарные вектора амплитуд сигнала, 4) числовые характеристики распределения амплитуд сигнала, 5) числовые характеристики распределения коэффициентов Фурье и 6) числовые характеристики распределения коэффициентов вейвлета Добеши-4 каждого отведения, обработки каждой группы признаков отдельной многослойной нейронной сетью (МНС), формировании вторичных признаков, выраженных в виде вероятностных оценок классов проб воздуха от МНС обработки первичных признаков, обучении каждой МНС для вычисления весовых коэффициентов классификации по алгоритму обратного распространения ошибки на дополнительно сформированном массиве указателей класса пробы воздуха, предъявляемых крысе заданное количество раз от заданного количества источников, идентификации класса пробы воздуха путем расчета шести групп первичных признаков сигнала, вычислении шестью МНС предварительных вероятностных оценок принадлежности предъявляемой крысе пробы воздуха к отрицательному, связанному с отсутствием биомаркера РЛ или положительному классу, связанному с наличием биомаркера рака, вычислении седьмой МНС итоговой вероятности класса пробы воздуха и выбора класса с максимальной вероятностью при усреднении по всем вдохам крысы пробы воздуха в качестве результата распознавания.
В предпочтительном выполнении способа:
- крысу размещают в посадочном месте контейнера;
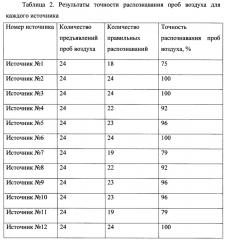
- количество проб воздуха от каждого источника для формирования обучающей выборки составляет 10, при количестве источников проб воздуха для каждого класса – 10;
- биоэлектрические сигналы от обонятельной луковицы крысы передают по радиоканалу.
Повышение точности распознавания проб воздуха на положительную, связанную с наличием биомаркера РЛ и отрицательную, связанную с отсутствием биомаркера РЛ достигается за счет двухуровневой структуры обработки биоэлектрического сигнала.
Первый уровень обработки содержит шесть МНС обработки первичных признаков: 1) коэффициентов кросс-корреляции амплитуд сигнала между отведениями, 2) коэффициентов кросс-корреляции амплитуд частот между отведениями, 3) бинарных векторов амплитуд сигнала, 4) числовых характеристик распределения амплитуд сигнала, 5) числовых характеристик распределения коэффициентов Фурье и 6) числовых характеристик распределения коэффициентов вейвлета Добеши-4 каждого отведения.
Второй уровень содержит одну МНС обработки вторичных признаков - вероятностных оценок классов проб воздуха от МНС первого уровня.
Регистрация биоэлектрического сигнала обонятельной луковицы крысы в диапазоне частот 1-250 Гц соответствует наличию отклика обонятельной системы на изменение состава воздуха.
Количество проб воздуха каждого класса 100, обусловлено минимальным числом примеров для обучения классификатора.
Заявляемое изобретение поясняется фигурами чертежей.
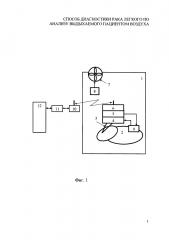
Фиг. 1 - Блок-схема устройства для осуществления заявляемого способа.
Фиг. 2 - Блок-схема процессора для обработки биоэлектрических сигналов крысы.
Фиг. 3 - Блок-схема структуры комитета многослойных нейронных сетей.
Фиг. 4 - Блок-схема обучения комитета многослойных нейронных сетей.
Фиг. 5 - Блок-схема запоминания временных отрезков биоэлектрических сигналов для каждого класса.
Фиг. 6 - Иллюстрация выделения по сигналу дыхания временного отрезка биоэлектрических сигналов длительностью τ с задержкой Δt после начала вдоха t0.
Фиг. 7 - Блок-схема формирования массивов входных векторов aj для каждой j-ой МНС первого уровня комитета.
Фиг. 8 - Блок-схема предобработки массива входных векторов αj для каждой j-ой МНС первого уровня комитета.
Фиг. 9 - Блок-схема формирования общего для всех МНС обучающего массива выходных бинарных переменных β из текстовых названий классов b.
Фиг. 10 - Блок-схема выполнения алгоритма обратного распространения ошибки для каждой j-ой МНС.
Фиг. 11 - Структурная схема многослойной нейронной сети.
Фиг. 12 - Функциональная схема узлового элемента скрытого слоя и выходного слоя многослойной нейронной сети.
Фиг. 13 - Блок-схема выполнения прямопоточных вычислений выходных векторов θ.
Фиг. 14 - Блок-схема выполнения обратнопоточных вычислений ошибок Δw весовых коэффицентов w и их модификации w=w+Δw.
Фиг. 15 - Иллюстрация результата работы линейного и нелинейного классификатора, где: а - нелинейное расположение примеров двух классов проб воздуха, изображенных точками светлого и темного цвета, b - применение линейного классификатора, не способного разделить области принадлежности примеров разных классов, с - применение нелинейного классификатора, позволяющего разделить области принадлежности примеров разных классов.
Фиг. 16 - Блок-схема нейросетевой классификации.
Фиг. 17 - Блок-схема запоминания временного отрезка биоэлектрического сигнала для распознавания.
Фиг. 18 - Блок-схема определения класса предъявляемой крысе пробы воздуха.
Блок-схема устройства для осуществления способа (фиг. 1) содержит портативный контейнер 1, в котором выполнено посадочное место для размещения крысы 2 (на чертеже не показано). В обонятельную луковицу крысы имплантирована микроэлектродная матрица 3, содержащая 8 электродов, которые подключены к входу усилителя биоэлектрических сигналов 4, который подключен к источнику питания 5. Выход усилителя биоэлектрических сигналов 4 соединен с приемо-передающим радио-модулем 6. В контейнере 1 установлен вытяжной вентилятор 7, подключенный к источнику питания 8. На брюшине крысы 1 в специальной жилетке на площадке установлен датчик дыхания 9. Выход приемо-передающего радио-модуля 6 через радио-модуль приема сигнала 10 и модуль согласования шины USB подключен ко входу персонального компьютера 12.
Сигналы с электродов, отводящих электрическую активность с обонятельной луковицы крысы, поступают на входы усилителя биоэлектрических сигналов 4, который выполнен на основе многофункциональной микросхемы ADS1299, управляемой микроконтроллером STM32F102 для обеспечения необходимого усиления входного сигнала и преобразования его в цифровую форму. Полученные цифровые данные принимаются микроконтроллером ADS1299 и передаются в приемо-передающий радио-модуль 6.
Для передачи и приема данных через радиоканал используются сигналы SCK, MISO и MOSI шины SPI. Переключение радио-модуля 6 на микросхеме NRF24L01 из пассивного состояния в активное осуществляется сигналами СЕ и CS, поступающими из микроконтроллера, установленного в усилителе биоэлектрических сигналов 4.
Питание усилителя биоэлектрических сигналов 4 и приемо-передающего радио-модуля 6 осуществляется от литий-полимерной аккумуляторной батареи напряжением 3,7 В и емкостью 200 mA типа 042030. Управление зарядом и разрядом аккумуляторной батареи осуществляется микросхемой МАХ1551. В качестве датчика дыхания использован акселерометр ADXL302.
При выдыхании воздуха пациентом в трубку, заканчивающуюся воронкой (на чертеже не показано), установленной перед носом крысы, потенциальные биомаркеры РЛ попадают на обонятельную слизистую крысы, где происходит их взаимодействие с белками-рецепторами и возбуждение рецепторов, которое вызывает отклик в гломерулах обонятельной луковицы крысы. Электрическая активность, отводимая с поверхности обонятельной луковицы с помощью микроэлектродной матрицы 3, регистрируется усилителем биоэлектрических сигналов 4 и через приемо-передающий радио-модуль 6 поступает на USB вход персонального компьютера 12 для анализа и обработки.
Система анализа и обработки биоэлектрической активности обонятельной луковицы крысы (фиг. 2) содержит блок обучения комитета многослойной нейронной сети (МНС) 13 и блок нейросетевой классификации 14.
Блок-схема 15 (фиг. 3) содержит блок МНС обработки амплитуд сигнала 16, блок МНС обработки коэффициентов кросс-корреляции амплитуд сигнала 17, блок МНС обработки бинарных векторов амплитуд сигнала 18, блок МНС обработки коэффициентов Фурье 19, блок МНС обработки коэффициентов кросс-корреляции амплитуд частот 20, блок МНС обработки коэффициентов вейвлета Добеши-4 21 и блок МНС обработки оценок классификации проб воздуха 22.
Блок-схема 13 (фиг. 4) содержит блоки запоминания временных отрезков Fi биоэлектрического сигнала для каждого i-го класса и названия класса bi 23, формирования обучающих массивов входных векторов aj каждой j-ой МНС первого уровня 24, формирования обучающих массивов входных векторов а7 МНС второго уровня 25, предобработки массивов входных векторов aj каждой j-ой МНС 26, формирования общего для всех МНС обучающего массива выходных бинарных переменных β из текстовых названий запахов b 27 и выполнения алгоритма обратного распространения ошибки для каждой j-ой МНС 28.
Блок-схема 23 (фиг. 5) содержит блоки подачи крысе пробы воздуха i-го класса 29, запоминания временного отрезка Fi биоэлектрического сигнала длительностью τ с задержкой Δt после начала вдоха t0 пробы воздуха i-го класса 30, запоминания текстового названия класса пробы воздуха bi 31 и смены источника проб воздуха i-го класса 32.
Блок-схема 24 (фиг. 7) содержит блоки фильтрации временных отрезков Fi биоэлектрического сигнала полосовым фильтром в диапазоне частот f1-f2 33, формирования массива матриц xij из значений амплитуд сигнала всех отведений 34, формирования массива матриц xij из значений коэффициентов кросс-корреляции значений амплитуд сигнала между отведениями 35, формирования массива бинарных векторов xij, соответствующих максимумам амплитуд сигнала по одному из отведений 36, расчета частотно-амплитудного спектра временных отрезков Fi биоэлектрического сигнала в диапазоне частот f1-f2 37, формирования массива матриц xij из значений коэффициентов Фурье всех отведений 38, формирования массива векторов xij из коэффициентов кросс-корреляции значений амплитуд частот между отведениями 39, формирования массива матриц xij из значений коэффициентов разложения вейвлета Добеши-4 для каждого отведения 40, объединения массивов матриц xij каждого i-го класса пробы воздуха в обучающие массивы входных векторов xij для каждой j-ой МНС первого уровня 41, объединения массивов векторов xij каждого i-го класса пробы воздуха в обучающие массивы входных векторов xj для каждой j-ой МНС первого уровня 42, расчета значений максимума, среднего, дисперсии, коэффициентов асимметрии и эксцесса для каждого отведения из матрицы xj и объединение их в вектор aj 43, формирования вектора aj из компонентов вектора xj 44. Блок-схема 26 (фиг. 8) осуществляет преобразование для каждой j-ой МНС массива входных векторов aj=(aj1,aj2,…,ajnj) в массив векторов αj=(αj1,aj2,…,αjnj) путем стандартизации значений массива {aj} для каждой компоненты вектора aj.
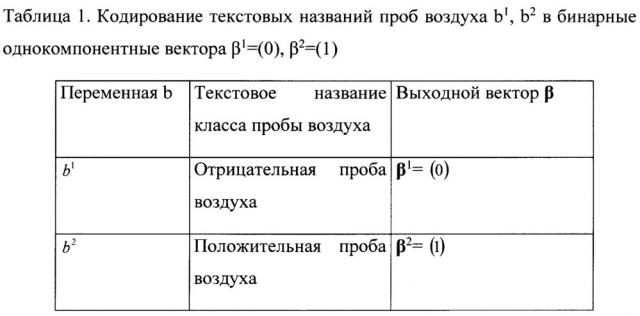
Блок-схема 27 (фиг. 9) осуществляет формирование общего для всех МНС обучающего массива выходных бинарных переменных β из текстовых названий классов b. Кодирование осуществляется в соответствии с таблицей 1.
Блок-схема 28 (фиг. 10) содержит блоки выполнения прямопоточных вычислений выходных векторов θ 45 и выполнения обратнопоточных вычислений ошибок Δw весовых коэффициентов w и их модификации w=w+Δw 46.
Структурная схема многослойной нейронной сети (фиг. 11) содержит входной, скрытый и выходной слой.
Функциональная схема узлового элемента скрытого слоя и выходного слоя многослойной нейронной сети (фиг. 12) содержит сумматор 47, вычисляющий скалярное произведение входного сигнала на вектор весовых коэффициентов w, и нелинейный преобразователь 48.
Блок-схема 45 (фиг. 13) производит в МНС прямопоточные послойные преобразования над входными векторами α для получения выходного вектора θ.
Блок-схема 46 (фиг. 14) производит обратнопоточные послойные вычисления в МНС весовых коэффициентов w.
Блок-схема 14 (фиг. 16) содержит блоки запоминания отрезка биоэлектрического сигнала Fi для распознавания 49, формирования массивов входных векторов aj для каждой j-ой МНС первого уровня 24, предобработки массивов входных векторов aj для каждой j-ой МНС первого уровня 26, выполнения прямопоточных вычислений выходных векторов θj для каждой j-й МНС первого уровня 45, формирования массива входных векторов а7 для МНС второго уровня 25, предобработки массива входных векторов а7 для МНС второго уровня 26, выполнения прямопоточных вычислений выходных векторов θ7 для МНС второго уровня 45 и определения класса предъявляемой пробы воздуха 50.
Блок-схема 49 (фиг. 17) содержит блоки подачи крысе пробы воздуха i-го класса 29 и запоминания временного отрезка Fi биоэлектрического сигнала длительностью τ с интервалом задержки Δt после начала вдоха t0 пробы воздуха i-го класса 30.
Блок-схема 50 (фиг. 18) осуществляет определение класса предъявляемой пробы воздуха путем усреднения компонент выходных векторов θ7 по всем вдохам крысы предъявляемой пробы воздуха и порогового преобразования вектора θ в бинарный код β текстового названия класса пробы воздуха b.
Сигнал передается в процессор 12 на обучение комитету МНС 13, если МНС не обучены, или на классификацию 14, если МНС обучены (фиг. 2). Комитет МНС 15 имеет двухуровневую структуру (фиг. 3). Первый уровень состоит из шести МНС обработки первичных признаков: МНС обработки амплитуд сигнала 16, МНС обработки коэффициентов кросс-корреляции амплитуд сигнала 17, МНС обработки бинарных векторов амплитуд сигнала 18, МНС обработки коэффициентов Фурье 19, МНС обработки коэффициентов кросс-корреляции амплитуд частот 20, МНС обработки коэффициентов вейвлета Добеши-4 21. Первый уровень выполняет оценки принадлежности анализируемого сигнала к определенному классу на основе специализированных признаков для каждой из шести МНС. Обучение МНС этого уровня приводит к автоматической настройке классификатора запахов на значимые признаки биоэлектрического сигнала обонятельной луковицы. Второй уровень состоит из одной МНС обработки оценок классификации проб воздуха 22. Второй уровень служит для расчета итоговой оценки принадлежности пробы воздуха к одному из классов на основе оценок специализированных МНС первого уровня. Настройка МНС второго уровня приводит к автоматическому подавлению «шумовых» оценок МНС первого уровня, увеличивая итоговую точность классификации.
Обучение МНС начинают с запоминания обучающих временных отрезков Fi восьмиканального биоэлектрического сигнала и названий классов проб воздуха bi для каждого i-го класса (блок 23) (фиг. 4).
Для подачи пробы воздуха крысе в окружающее пространство в области носа крысы источником воздуха производится выдох i-го из двух классов проб воздуха: проба воздуха от здорового источника (отрицательная проба воздуха) и проба воздуха от больного источника (положительная проба воздуха) (блок 29) (фиг. 5). Во время подачи пробы происходит запоминание временного отрезка Fi восьмиканального биоэлектрического сигнала длительностью τ=500 мс с задержкой Δt=50 мс от момента начала вдоха t0 (блок 30) и запоминание текстового названия класса пробы bi (блок 31). Начало вдоха соответствует локальному максимуму на графике сигнала дыхания (фиг. 6), который регистрировался датчиком дыхания, размещенного над брюшиной крысы и фиксирующего дыхание по движению брюшины. Подаются 10 проб воздуха i-го класса от каждого источника при 10 источниках для каждого из двух классов проб воздуха.
Из временных отрезков Fi восьмиканального биоэлектрического сигнала формируются массивы входных векторов aj для каждой j-ой из шести МНС первого уровня (блок 24) (фиг. 7). Для первых трех