Способ калибровки и измерения сигнала и устройство для обнаружения и/или идентификации целевых бактерий (варианты)
Иллюстрации
Показать всеГруппа изобретений относится к области биохимии. Предложен способ калибровки и измерения сигнала, а также устройство для обнаружения и/или идентификации целевых бактерий. Устройство содержит узел детектора с корпусом, детектором и заслонкой. Корпус задает канал для приема контейнера для образца и задает объем обнаружения для помещения канала во взаимодействие с детектором. Заслонка выполнена с возможностью перемещения между первым и вторым положением для изолирования объема обнаружения от канала корпуса. При этом заслонка задает калибровочный разъем, где калибровочный разъем помещает калибровочный источник света во взаимодействие с детектором при первом положении заслонки, а во втором положении заслонки калибровочный разъем изолирован от объема обнаружения. Способ включает передачу первого сигнала от калибровочного источника света в изолированный от канала объем обнаружения, обнаружение первого светового сигнала посредством детектора, перемещение заслонки и помещение канала в оптическую связь с объемом обнаружения для обнаружения испущенного из контейнера второго светового сигнала. Изобретения обеспечивают быстрое обнаружение и идентификацию бактериальных видов в клинических образцах. 3 н. и 12 з.п. ф-лы, 97 ил.
Реферат
Перекрестная ссылка на родственные заявки
По настоящей заявке испрашивается приоритет заявки на патент США № 13/802461, озаглавленной «Systems and Methods for Detection of Cells using Engineered Transduction Particles», поданной 13 марта 2013, по которой испрашивается приоритет предварительной заявки на патент США № 61/779177, озаглавленной «Non-Replicative Transduction Particles and Transduction Particle-Based Reporter Systems», поданной 13 марта 2013, каждая из которых включена в настоящее описание посредством ссылки во всей ее полноте.
УРОВЕНЬ ТЕХНИКИ
Варианты осуществления, описанные в настоящем описании, относятся к системам и способам для обнаружения клеток с применением сконструированных трансдукционных частиц. Более конкретно, варианты осуществления, описанные в настоящем описании, относятся к способам для обнаружения бактерий с применением дефектных по репликации трансдукционных частиц в качестве репортерной системы. Варианты осуществления, описанные в настоящем описании, также относятся к контейнеру и устройству, в пределах которого обнаружение бактерий может быть выполнено в интегрированной замкнутой системе с функциональностью ухода.
Обнаружение бактерий, особенно, устойчивых к лекарственным препаратам, является критическим шагом в диагностировании и ограничении распространения бактериальных инфекций. Например, MRSA является устойчивой к лекарственным препаратам версией обычных бактерий Staphylococcus aureus, носителями которых является значительная часть населения в США. Большинство инфекций MRSA возникает в больницах, и может давать высокую смертность (инфекции MRSA убивают приблизительно 19000 человек в США каждый год). Соответственно, существует потребность в эффективной, точной и быстрой идентификации бактериальных штаммов (включая их фенотип и/или генотип и другие молекулярные мишени), которые вызывают инфекцию, таких как MRSA. Особенно важной является возможность идентификации бактериального фенотипа и/или генотипа и других молекулярных мишеней для множества различных образцов (например, человеческие образцы, экологические образцы, растительные образцы, ветеринарные образцы, пищевые образцы и т.п.), с тем чтобы соответствующий курс лечения и контроля мог быть начат своевременно.
Один известный способ для идентификации бактерий включает культивирование бактерий. Культивирование имеет высокую чувствительность, но часто занимает от двух до трех дней (или даже дольше) до получения результата, и поэтому является неподходящим для целей быстрой диагностики или эффективного скрининга. Известные способы культивирования часто выполняются с применением систем, требующих для выполнения анализов хорошо обученного персонала, и поэтому являются неподходящими для применения в множестве различных ситуаций. Известные способы культивирования также являются подверженными загрязнению, которое может привести к ложным положительным результатам и/или ошибочной идентификации бактерий. Кроме того, известные способы культивирования используют специально настроенные протоколы культивирования для идентификации различных видов бактерий, таким образом, проверка широкой бактериальной панели может быстро повысить стоимость.
Прямой бактериальный иммунологический анализ, то есть обнаружение с применением реакции антитела-антигена, представляет собой еще один способ для обнаружения бактерий. Известные способы иммунологического анализа могут выдавать результаты быстрее и с более низкой стоимостью, чем культивирование, но они часто ограничены доступностью селективных антител для представляющего интерес бактериального штамма, и доступные антитела являются подверженными перекрестной реактивности. Такие известные способы также являются менее чувствительными, чем культивирование, в результате чего часто, при этом, имеется требование бактериальной амплификации, которое может увеличить время анализа.
Другие известные способы для обнаружения бактериальных клеток включают выделение и анализ нуклеиновой кислоты, такой как ДНК или РНК. Известные способы для выделения нуклеиновых кислот из образца часто включают несколько обязательных этапов приготовления образцов, для которых требуется дорогое и специализированное оборудование. В частности, такие этапы включают 1) удаление белков из образца, содержащего бактерии или клетки, посредством добавления протеазы; 2) разрушение оставшегося объемного образца с целью высвобождения нуклеиновых кислот, содержавшихся в нем (также называемое лизисом клетки); 3) осаждение нуклеиновой кислоты из образца; 4) промывание и/или другая подготовка нуклеиновой кислоты к дальнейшему анализу; 5) анализ нуклеиновой кислоты с целью идентификации вида. После подготовки образца известные способы анализа могут включать полимеразную цепную реакцию (PCR), генное секвенирование, генный "фингерпринтинг", флуоресценцию, иммунологическое обследование, электрохимическое иммунологическое исследование, микрочипы, любой другой соответствующий способ или комбинацию указанного. PCR имеет широкое коммерческое применение, но часто требует множество этапов, включающих использование дорогих реагентов и аппаратуры. Множество известных способов, включающих PCR, не являются подходящими для «настольного» тестирования (например, они требуют относительно квалифицированного персонала). Кроме того, известные способы PCR используют термоциклирование и/или повышенные температуры, которые могут повысить стоимость, время и/или сложность анализа. Наконец, поскольку в способах PCR для обнаружения последовательностей ДНК лизируются клетки образца, такие способы не могут различить живые и мертвые клетки.
Некоторые известные системы и способы для идентификации клеток включают использование бактериофагов для идентификации и/или обнаружения определенных бактерий. В некоторых известных способах фаги, которые помечены репортерными молекулами, могут применяться для нацеливания и инфицирования конкретного бактериального штамма. После инфицирования фаги могут проходить литический цикл (то есть повреждать клеточную стенку, уничтожая целевые бактерии) и/или лизогенный цикл (то есть репликацию фага вместе с бактериями без уничтожения бактерий), после которого производится обнаружение амплифицированного потомства фага. Такие известные способы, полагающиеся на обнаружение фага, часто включают ограничивающие или сложные этапы шаги. Например, некоторые известные основанные на обнаружении фагов способы для идентификации полагаются на репликацию фага (во время которой бактерии могут подвергаться лизированию), и обычно требуют культивирования клеток для способствования данному процессу. Некоторые известные основанные на обнаружении фагов способы требуют удаления или "развязывания" специфично связанных фагов из образцов с использованием тщательно измеренных и/или контролируемых по pH реагентов. Кроме того, некоторые известные основанные на обнаружении фагов способы полагаются на тщательное измерение количества добавленного фага и/или включают открытие или закрытие реакционной камеры для добавления/удаления реагентов, что может привести к загрязнению и/или преждевременному смешиванию реагентов, что приведет к ошибочным результатам и сделает анализ сложным по своей природе.
Другие основанные на фагах способы используют бактериофагов, которые сконструированы для доставки в целевые бактерии нуклеотида, который может содержать репортерный ген, который вызывает в целевой бактерии экспрессию репортерной молекулы. Некоторые известные способы включают фаги, которые реплицируются во время анализа, однако, это может привести к нежелательному лизированию клеток, внутри которых должны продуцироваться репортерные молекулы. Другие известные основанные на фагах способы используют бактериофаги, в которых функции репликации подавляются в условиях анализа. Такие известные способы, однако, являются трудными для реализации вследствие жесткого диапазона условий (например, температурных условий), при которых функции репликации останутся подавленными. Такие способы не являются легко управляемыми, и, таким образом, могут привести к литической активности. Другие способы предлагают использовать умеренных фагов, которые проходят лизогенный цикл вместо литического цикла. Такие известные способы, однако, также являются подверженными спорадической литической активности. Внедрение нативных жизненных циклов фагов также может привести к ограничению спектра хозяев репортерного фага вследствие иммунитета к вторичной инфекции целевыми клетками, которые могут быть лизогенизированы с профагом. Таким образом, хотя известные способы данного типа были выполнены в академических условиях, они неприменимы в клинических условиях.
В дополнение к вышеописанным недостаткам относительно использования основанных на фагах способов методов способы не используют автоматизацию или аппаратуру для того, чтобы предоставить "блужданию" систему идентификации бактериофага. Например, множество известных систем не обеспечивают эксплуатацию закрытой системы и/или измерение сигнала, который продуцируется определенными репортерными молекулами, например, в качестве примера, реакции флэш-люминесценции. Таким образом, известные системы и способы требуют квалифицированного персонала и тщательного обращения с образцами, что может повысить вероятность ложных положительных или отрицательных результатов.
Таким образом, существует потребность в улучшенном устройстве и способах для быстрого, экономически выгодного и гибкого обнаружения и идентификации бактериальных видов в клинических образцах.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Системы и способы для обнаружения и/или идентификации целевых клеток (например, бактерий) с применением сконструированных вирусных векторов и/или трансдукционных частиц описаны в настоящем описании. В некоторых вариантах осуществления способ включает смешивание некоторого количества трансдукционных частиц в пределах образца. Трансдукционные частицы ассоциированы с целевой клеткой. Трансдукционные частицы являются нереплицируемыми, и сконструированы как содержащие молекулу нуклеиновой кислоты, разработанную с тем, чтобы вызывать продуцирование группы репортерных молекул в целевой клетке. В образце и трансдукционных частицах поддерживается экспрессия группы репортерных молекул, когда целевая клетка присутствует в образце. Принимают сигнал, ассоциированный с количеством репортерных молекул. В некоторых вариантах осуществления величина сигнала не зависит от количества трансдукционных частиц, превышающего предварительно заданное количество.
В некоторых вариантах осуществления контейнер содержит корпус, элемент доставки и привод. Корпус, который может быть съемно соединен с реакционной камерой, задает объем реагента. Элемент доставки соединен с корпусом и задает канал между объемом реагента и реакционной камерой, когда корпус соединен с реакционной камерой. Первая концевая часть элемента доставки расположена в пределах объема реагента, и вторая концевая часть элемента доставки расположена за пределами объема реагента. Привод имеет блок плунжера, расположенный в пределах объема реагента, который может перемещаться в пределах объема реагента вдоль продольной оси корпуса с целью формирования потока или реагент из объема реагента через канал. Элемент доставки сконфигурирован для направления потока реагента, выходящего из второй концевой части элемента доставки в выходном направлении, не параллельном продольной оси корпуса.
В некоторых вариантах осуществления устройство содержит узел удержания, узел активации и привод. Узел удержания включает первое захватное устройство, второе захватное устройство и смещающий элемент. Первое захватное устройство и второе захватное устройство сконфигурированы для контактирования с первой частью контейнера для образцов с целью ограничения перемещения контейнера для образцов. Контейнер для образцов задает реакционный объем и объем реагента. Элемент активации подвижно соединен с узлом удержания и сконфигурирован для зацепления второй части контейнера для образцов с целью передачи реагента из объема реагента в реакционный объем. Привод сконфигурирован для перемещения элемента активации относительно узла удержания между первым положением и вторым положением. В первом положении поверхность элемента активации контактирует с поверхностью узла удержания с целью поддержания первого захватного устройства и второго захватного устройства в открытой конфигурации. Во втором положении поверхность элемента активации находится на расстоянии от поверхности узла удержания с тем, чтобы смещающий элемент приводил первое захватное устройство и второе захватное устройство в закрытую конфигурацию. Блок плунжера элемента активации сконфигурирован для перемещения в пределах объема реагента, когда элемент активации перемещается в направлении второго положения.
Краткое описание чертежей
Фиг. 1 представляет собой блочную диаграмму системы для идентификации бактерий согласно варианту осуществления
Фиг. 2 и 3 представляют собой схематические иллюстрации картриджа согласно варианту осуществления, в первой конфигурации и второй конфигурации.
Фиг. 4 иллюстрирует блок-схему способа для обнаружения целевой клетки в образце, согласно варианту осуществления.
Фиг. 5 представляет собой схематическую иллюстрацию трансдукционной частицы и сконструированной молекулы нуклеиновой кислоты, содержащейся в ней, согласно варианту осуществления.
На фиг. 6 показана схематическая иллюстрация способа для идентификации целевой клетки, согласно варианту осуществления.
На фиг. 7A и 7B показана схематическая иллюстрация трансдукционных частиц, взаимодействующих с целевыми клетками в первый раз (фиг. 7A) и во второй раз (фиг. 7B), согласно варианту осуществления.
Фиг. 8 иллюстрирует блок-схему способа для идентификации жизнеспособной целевой клетки, согласно варианту осуществления.
Фиг. 9 представляет собой схематическую иллюстрацию состава сконструированной нуклеиновой кислоты, согласно варианту осуществления.
Фиг. 10 иллюстрирует блок-схему способа для генотипной идентификации целевой клетки, согласно варианту осуществления.
На фиг. 11 показана схематическая иллюстрация генотипного способа для идентификации целевой клетки, согласно варианту осуществления.
Фиг. 12-14 представляют собой схематические поперечные разрезы контейнера для образцов согласно варианту осуществления, в первой конфигурации, второй конфигурации и третьей конфигурации, соответственно.
Фиг. 15-17 представляют собой виды сбоку контейнера в сборе согласно варианту осуществления, в первой конфигурации, второй конфигурации и третьей конфигурации, соответственно.
Фиг. 18 представляет собой вид в перспективе контейнера в сборе согласно варианту осуществления.
На фиг. 19 показано покомпонентное изображение контейнера в сборе с фиг. 18.
На фиг. 20 показан вид сверху корпуса, входящего в состав контейнера в сборе с фиг. 19.
На фиг. 21 вид снизу в перспективе корпуса, входящего в состав контейнера в сборе с фиг. 19.
На фиг. 22 показан вид в перспективе контейнера для реагентов, входящего в состав контейнера в сборе с фиг. 19, согласно варианту осуществления.
Фиг. 23-25 представляют собой боковые виды в разрезе части контейнера с фиг. 19 в первой конфигурации, второй конфигурации и третьей конфигурации, соответственно.
На фиг. 26 показан вид в перспективе контейнера в сборе, согласно варианту осуществления.
На фиг. 27 показан вид снизу в перспективе корпуса, входящего в состав контейнера в сборе с фиг. 26.
На фиг. 28 показан боковой вид в разрезе контейнера в сборе с фиг. 26.
Фиг. 29 представляет собой боковой вид в разрезе контейнера в сборе, согласно варианту осуществления.
Фиг. 30-32 представляют собой боковые виды в разрезе контейнера в сборе согласно варианту осуществления, в первой конфигурации, второй конфигурации и третьей конфигурации, соответственно.
На фиг. 33 показано покомпонентный боковой вид в разрезе контейнера в сборе, согласно варианту осуществления.
Фиг. 34-36 представляют собой боковые виды в разрезе контейнера в сборе с фиг. 33 в первой конфигурации, второй конфигурации и третьей конфигурации, соответственно.
Фиг. 37 и 38 представляют собой боковые поперечные схематические иллюстрации контейнера в сборе согласно варианту осуществления в первой конфигурации и второй конфигурации, соответственно.
Фиг. 39 и 40 представляют собой боковые поперечные схематические иллюстрации контейнера в сборе согласно варианту осуществления в первой конфигурации и второй конфигурации, соответственно.
Фиг. 41 представляет собой боковую поперечную схематическую иллюстрацию контейнера в сборе, согласно варианту осуществления.
Фиг. 42 иллюстрирует блок-схему способа обнаружения сигнала, согласно варианту осуществления.
Фиг. 43-45 представляют собой схематические виды сбоку части устройства согласно варианту осуществления, в первой конфигурации, второй конфигурации и третьей конфигурации, соответственно.
Фиг. 46-48 представляют собой схематические виды сбоку части устройства согласно варианту осуществления, в первой конфигурации, второй конфигурации и третьей конфигурации, соответственно.
Фиг. 49 и 50 представляют собой схематические виды сбоку блока обнаружения устройства согласно варианту осуществления, в первой конфигурации и второй конфигурации, соответственно.
На фиг. 51 показан вид в перспективе устройства, согласно варианту осуществления.
На фиг. 52 показан наклонный вид спереди устройства с фиг. 51 с открытой крышкой.
На фиг. 53 показан наклонный вид спереди корпуса, входящего в состав устройства с фиг. 51.
На фиг. 54 показан вид сзади корпуса, показанного на фиг. 53.
На фиг. 55-57 показаны виды в перспективе части внутренних компонентов и подсистем устройства с фиг. 51 с корпусом, удаленным для ясности.
На фиг. 58 показан вид в перспективе источника питания, входящего в состав устройства с фиг. 51.
На фиг. 59 показан вид в перспективе процессора, входящего в состав устройства с фиг. 51.
На фиг. 60 показан вид в перспективе коммуникационного модуля, входящего в состав устройства с фиг. 51.
На фиг. 61 показан вид в перспективе устройства с фиг. 51 в первой конфигурации.
На фиг. 62 показан вид в перспективе картриджа, входящего в состав устройства с фиг. 51.
На фиг. 63 показан вид в перспективе приемника картриджа, входящего в состав устройства с фиг. 51.
Фиг. 64 представляет собой вид сбоку картриджа с фиг. 62 и приемника картриджа с фиг. 63 в соединенной конфигурации.
На фиг. 65 показан вид в перспективе узла нагревателя, входящего в состав устройства с фиг. 51.
Фиг. 66 представляет собой частичное изображение в разобранном виде узла нагревателя с фиг. 65.
На фиг. 67 показан вид сзади блока нагревателя с фиг. 65.
Фиг. 68 представляет собой вид в перспективе узла привода, входящего в состав устройства с фиг. 51, согласно варианту осуществления.
На фиг. 69 показан вид спереди узла привода с фиг. 68.
На фиг. 70 и 71 показан узел привода с фиг. 68 в первой конфигурации и второй конфигурации, соответственно.
На фиг. 72 показан вид в перспективе системы электронной схемы для управления узлом привода, входящим в состав устройства с фиг. 51.
На фиг. 73 показан вид в перспективе узла манипулятора согласно варианту осуществления, входящему в состав устройства с фиг. 51.
На фиг. 74 показано покомпонентное изображение узла манипулятора Фиг. 73.
На фиг. 75 показан вид сбоку узла манипулятора с фиг. 73 в первой (или «открытое захватное устройство») конфигурации.
На фиг. 76 показан вид сбоку узла манипулятора с фиг. 73 во второй (или «закрытое захватное устройство») конфигурации.
На фиг. 77 показан вид в перспективе узла манипулятора с фиг. 73 во второй («закрытое захватное устройство») конфигурации и транспортировка контейнера.
На фиг. 78 и 79 показан вид сбоку узла манипулятора с фиг. 73 в первой («открытое захватное устройство») конфигурации и зацепление контейнера.
На фиг. 80 показано боковое поперечное сечение узла манипулятора с фиг. 78 в открытой конфигурации и зацепление контейнера в операции «первого погружения».
На фиг. 81 показано боковое поперечное сечение узла манипулятора с фиг. 73 во второй («закрытое захватное устройство») конфигурации.
Фиг. 82 и 83 представляют собой виды сбоку и в перспективе, соответственно, узла манипулятора с фиг. 73 в третьей конфигурации («закрытое захватное устройство») конфигурации, зацепляющей контейнер в операции «второго погружения».
На фиг. 84 показано боковое сечение узла манипулятора с фиг. 82.
На фиг. 85 показан вид в перспективе узла детектора, согласно варианту осуществления, входящему в состав устройства с фиг. 51.
На фиг. 86 показан вид сверху части узла детектора с фиг. 85.
На фиг. 87 показан вид в перспективе узла детектора с фиг. 85 с удаленным корпусом.
На фиг. 88 показано покомпонентное изображение узла детектора с фиг. 85 с удаленным корпусом.
На фиг. 89 показан вид в перспективе заслонки, включенной в состав узла детектора с фиг. 85, согласно варианту осуществления.
На фиг. 90 показано боковое поперечное сечение заслонки с фиг. 89.
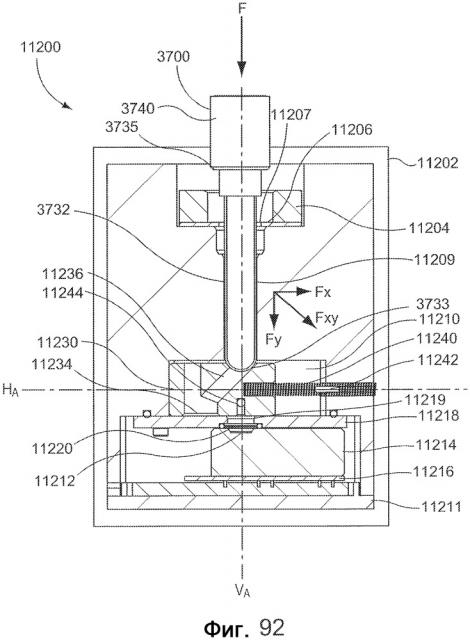
Фиг. 91-94 представляют собой боковые виды в разрезе узла детектора с фиг. 85 в первой конфигурации, второй конфигурации, третьей конфигурации и четвертой конфигурации, соответственно.
На фиг. 95 показан вид в перспективе электрической схемы, включенной в состав устройства с фиг. 51 для управления узлом детектора с фиг. 85, согласно варианту осуществления.
Фиг. 96 иллюстрирует блок-схему способа для приема сигнала, согласно варианту осуществления.
Фиг. 97 иллюстрирует блок-схему способа для манипулирования контейнером, согласно варианту осуществления.
ПОДРОБНОЕ ОПИСАНИЕ
Системы и способы для обнаружения и/или идентификации целевых клеток (например, бактерий) с применением сконструированных вирусных векторов и/или трансдукционных частиц описаны в настоящем описании. В некоторых вариантах осуществления способ включает смешивание некоторого количества трансдукционных частиц в пределах образца. Трансдукционные частицы ассоциированы с целевой клеткой. Другими словами, трансдукционные частицы разработаны для связывания и доставки молекулы нуклеиновой кислоты в целевую клетку. Трансдукционные частицы являются нереплицируемыми, и сконструированы как содержащие молекулу нуклеиновой кислоты, разработанную для вызывания продуцирования группы репортерных молекул в целевой клетке. В образце и трансдукционных частицах поддерживается экспрессия группы репортерных молекул, когда целевая клетка присутствует в образце. Принимают сигнал, ассоциированный с количеством репортерных молекул. В некоторых вариантах осуществления величина сигнала не зависит от количества трансдукционных частиц, когда оно превышает предварительно заданное количество.
В некоторых вариантах осуществления способ для обнаружения целевой клетки включает смешивание с образцом группы трансдукционных частиц, ассоциированных с целевой клеткой. Трансдукционные частицы сконструированы как содержащие молекулу нуклеиновой кислоты, разработанную для вызывания продуцирования группы репортерных молекул в целевой клетке. Трансдукционные частицы свободны от ДНК дикого типа, которая способна демонстрировать вирусные функции дикого типа, ассоциированные с вирусом, из которого получена группа трансдукционных частиц. Образец и группа трансдукционных частиц поддерживаются таким образом, что группа репортерных молекул экспрессируется только тогда, когда целевая клетка присутствует в образце. Затем принимают сигнал, ассоциированный с некоторым количеством репортерных молекул. В некоторых вариантах осуществления величина сигнала не зависит от количества трансдукционных частиц, когда оно превышает предварительно заданное количество. Другими словами, в некоторых вариантах осуществления, мощность сигнала по существу независима от количества группы трансдукционных частиц.
В некоторых вариантах осуществления способ для обнаружения целевой клетки включает смешивание в пределах образца группы трансдукционных частиц, ассоциированных с целевой клеткой. Группа трансдукционных частиц разработана как неспособная к лизогенной репликации, и как содержащая молекулу нуклеиновой кислоты, разработанную для вызывания. Образец и группа трансдукционных частиц поддерживаются таким образом, что группа репортерных молекул экспрессируется только тогда, когда целевая клетка присутствует в образце. Способ также включает прием сигнала, ассоциированного с количеством репортерных молекул в группе.
В некоторых вариантах осуществления контейнер содержит корпус, первый привод и второй привод. Корпус сконфигурирован для съемного соединения с реакционной камерой (которая, например, может содержать образец, включающий целевую клетку). Корпус задает первый объем реагента и второй объем реагента, и содержит элемент доставки, который задает первый канал между первым объемом реагента и реакционной камерой и второй канал между вторым объемом реагента и реакционной камерой. Первый привода имеет блок плунжера, расположенный в пределах первого объема реагента, и блок зацепления, сконфигурированный с возможностью манипулирования им с целью перемещения блока плунжера в пределах первого объема реагента. Второй привод имеет блок плунжера, расположенный в пределах второго объема реагента, и блок зацепления второго привода, сконфигурированный с возможностью манипулирования им с целью перемещения блока плунжера в пределах второго объема реагента. Блок зацепления второго привода, по меньшей мере, частично окружает блок зацепления первого привода.
В некоторых вариантах осуществления контейнер содержит корпус, элемент доставки и привод. Корпус, который может быть съемно соединен с реакционной камерой (которая, например, содержит целевую клетку), задает объем реагента. Элемент доставки соединен с корпусом и задает канал между объемом реагента и реакционной камерой, когда корпус соединен с реакционной камерой. Первая концевая часть элемента доставки расположена в пределах объема реагента, и вторая концевая часть элемента доставки расположена за пределами объема реагента. Привод имеет блок плунжера, расположенный в пределах объема реагента, который может быть перемещен в пределах объема реагента вдоль продольной оси корпуса с целью создания потока или реагент из объема реагента через канал. Элемент доставки сконфигурирован для направления потока реагента, выходящего из второй концевой части элемента доставки в выходном направлении, не параллельном продольной оси корпуса.
В некоторых вариантах осуществления контейнер содержит корпус, элемент доставки, и привод. Корпус задает объем реагента и съемно соединен с реакционной камерой. Элемент доставки соединен с корпусом и задает канал между объемом реагента и реакционной камерой, когда корпус соединен с реакционной камерой. Первая концевая часть элемента доставки расположена в пределах объема реагента и задает первую часть канала. Вторая концевая часть элемента доставки расположена вне корпуса и задает вторую часть канала. Центральная линия второй части канала имеет угловое смещение относительно центральной линии первой части канала. Привод имеет блок плунжера, расположенный в пределах объема реагента, и сконфигурирован с возможностью перемещения в пределах камеры реагента вдоль продольной оси корпуса с целью создания потока реагента от объема реагента через канал.
В некоторых вариантах осуществления способ для обнаружения целевой клетки включает размещение реакционной камеры, содержащей образец и группу репортерных молекул, в функциональном соединении с детектором. Реагент передают в реакционную камеру через элемент доставки таким образом, что реагент протекает вдоль поверхности реакционной камеры и в образец. Таким образом минимизируется аэрация образца и реагента и/или образование пузырьков в пределах образца. Реагент разработан для реагирования с группой репортерных молекул с целью обеспечения возможности и/или улучшения выдачи сигнала, ассоциированного с количеством групп репортерных молекул. Сигнал принимается детектором.
В некоторых вариантах осуществления устройство содержит элемент удержания, элемент активации и привод. Элемент удержания сконфигурирован для контактирования с первой частью контейнера для образцов, который задает реакционный объем и объем реагента, с целью ограничения перемещения контейнера для образцов. Элемент активации соединен с элементом удержания и сконфигурирован для зацепления второй части контейнера для образцов с целью передачи реагента из объема реагента в реакционный объем. Привод сконфигурирован для перемещения элемента активации относительно элемента удержания между первым положением, вторым положением и третьим положением. В первом положении элемент удержания сконфигурирован с расположением на расстоянии от первой части контейнера для образцов. Во втором положении элемент активации сконфигурирован с расположением на расстоянии от второй части контейнера для образцов, и элемент удержания сконфигурирован для контактирования с первой частью контейнера для образцов. В третьем положении элемент активации сконфигурирован для зацепления со второй частью контейнера для образцов с целью передачи реагента таким образом, чтобы элемент удержания находился в контакте с первой частью контейнера для образцов.
В некоторых вариантах осуществления устройство содержит узел удержания, узел активации и привод. Узел удержания включает первое захватное устройство, второе захватное устройство и смещающий элемент. Первое захватное устройство и второе захватное устройство сконфигурированы для контактирования с первой частью контейнера для образцов с целью ограничения перемещения контейнера для образцов. Контейнер для образцов задает реакционный объем и объем реагента. Элемент активации подвижно соединен с узлом задержания и сконфигурирован для зацепления второй части контейнера для образцов с целью передачи реагента от объема реагента в реакционный объем. Привод сконфигурирован для перемещения элемента активации относительно узла удержания между первым положением и вторым положением. В первом положении поверхность элемента активации контактирует с поверхностью узла удержания с целью поддержания обслужить первого захватного устройства и второго захватного устройства в открытой конфигурации. Во втором положении поверхность элемента активации размещена на расстоянии от поверхности узла удержания таким образом, чтобы смещающий элемент приводил первое захватное устройство и второе захватное устройство в закрытую конфигурацию. Блок плунжера элемента активации сконфигурирован для перемещения в пределах объема реагента, когда элемент активации перемещается в направлении второго положения.
В некоторых вариантах осуществления устройство содержит корпус и заслонку, имеющую часть, подвижно размещаемую в пределах корпуса между первым положением заслонки и вторым положением заслонки. Корпус задает канал, сконфигурированный для приема контейнера для образцов, и дополнительно задает объем обнаружения, сконфигурированный для приведения канала во взаимодействие с детектором. Корпус содержит первую уплотняющую поверхность и вторую уплотняющую поверхность. Первая часть контейнера для образцов и первая уплотняющая поверхность сконфигурированы для изолирования объема обнаружения от объема за пределами корпуса, когда вторая часть (например, дальняя концевая часть) контейнера для образцов расположена в пределах объема обнаружения. Уплотняющая поверхность заслонки и вторая уплотняющая поверхность корпуса сконфигурированы для изолирования объема обнаружения от канала корпуса, когда заслонка находится в первом положении заслонки. Канал корпуса находится во взаимодействии с объемом обнаружения, когда заслонка находится во втором положении заслонки.
В некоторых вариантах осуществления устройство содержит корпус и заслонку, имеющую часть, размещен с возможностью перемещения в пределах корпуса между первым положением заслонки и вторым положением заслонки. Корпус задает канал, сконфигурированный для приема контейнера для образцов, и также задает объем обнаружения, сконфигурированный для помещения канала во взаимодействие с детектором. Блок активизации заслонки сконфигурирован для зацепления дальней концевой части контейнера для образцов с целью перемещения заслонки из первого положения заслонки во второе положение заслонки, когда дальняя концевая часть контейнера перемещается в направлении объема обнаружения. Уплотняющая поверхность заслонки и уплотняющая поверхность корпуса сконфигурированы для изолирования объема обнаружения от канала корпуса, когда заслонка находится в первом положении заслонки. Канал корпуса находится во взаимодействии с объемом обнаружения, когда заслонка находится во втором положении заслонки.
В некоторых вариантах осуществления устройство содержит корпус и заслонку, расположенную в пределах корпуса между первым положением заслонки и вторым положением заслонки. Корпус задает канал, сконфигурированный для приема контейнера для образцов, и также задает объем обнаружения, сконфигурированный для помещения канала во взаимодействие с детектором. Заслонка задает калибровочный разъем, сконфигурированный для приема калибровочного источника света, такого как, например, LED. Уплотняющая поверхность заслонки и соответствующая уплотняющая поверхность корпуса сконфигурированы для изолирования объема обнаружения от канала корпуса, когда заслонка находится в первом положении заслонки. Калибровочный разъем находится во взаимодействии с объемом обнаружения, когда заслонка находится в первом положении заслонки. Канал корпуса находится во взаимодействии с объемом обнаружения, и калибровочный разъем изолирован от объема обнаружения, когда заслонка находится во втором положении заслонки.
В некоторых вариантах осуществления способ для приема сигнала включает прием первого сигнала, ассоциированного с величиной светового излучения в объеме обнаружения в первый раз. Объем обнаружения оптически изолирован от канала подвижной заслонкой, которая находится в первом положении. Способ также включает приложение силы к контейнеру для образцов, по меньшей мере, частично расположенному в пределах канала, таким образов, что дальняя концевая часть контейнера для образцов перемещает заслонку из первого положения во второе положение, и таким образом, что дальняя концевая часть контейнера для образцов располагается в пределах объема обнаружения. В этой конфигурации канал находится в оптической связи с объемом обнаружения. Способ также включает прием второго сигнала, ассоциированного с величиной светового излучения в объеме обнаружения во второй раз, когда дальняя концевая часть контейнера для образцов находится в объеме обнаружения.
Как описано в настоящем описании, термины "ген", "ДНК" и "нуклеотид" означают целую генетическую последовательность или часть генетической последовательности целевых бактерий или вектора.
Как описано в настоящем описании, термин "плазмида" означает сконструированный ген, последовательность и/или молекулу, содержащуюся в пределах вектора, который содержит регуляторные элементы, последовательности нуклеиновых кислот, гомологичные целевым генам, и различные репортерные конструкции для вызывания экспрессии репортерных молекул в пределах жизнеспособной клетки и/или когда внутриклеточная молекула присутствует в пределах целевой клетки.
Системы, устройства и способы для обнаружения и идентификации целевых клеток (например, бактерий) могут включать трансдукционную частицу, которая может идентифицировать и связываться с целевой клеткой и доставлять в целевую клетку сконструированный нуклеотид. Как показано на блочной диаграмме с фиг. 1, в некоторых вариантах осуществления система 100 содержит генетически сконструированную трансдукционн