Производное циклического амина и его фармацевтическое применение
Иллюстрации
Показать всеИзобретение относится к области органической химии, а именно к производному циклического амина или к его фармакологически приемлемой соли общей формулы (I), где атом углерода, отмеченный значком *, является асимметрическим атомом углерода, и А обозначает группу, представленную общей формулой (IIa), (IIb) или (IIc), где R1 представляет собой метильную группу или этильную группу, необязательно замещенную атомом галогена, R2 представляет собой атом водорода или алкилкарбонильную группу, содержащую от 2 до 5 атомов углерода, каждый R3 независимо представляет собой метильную группу или этильную группу, и n представляет собой 1 или 2. Также изобретение относится к лекарственному средству, анальгетику и терапевтическому агенту на основе соединения формулы (I). Технический результат: получено производное циклического амина, обладающее анальгетическим действием, в частности, в отношении невропатической боли и/или синдрома фибромиалгии. 5 н. и 5 з.п. ф-лы, 18 ил., 8 табл., 19 пр.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0001]
Настоящее изобретение относится к производному циклического амина и к его фармацевтическому применению.
УРОВЕНЬ ТЕХНИКИ
[0002]
Боль представляет собой неприятный сенсорный и эмоциональный опыт, связанный с фактическим или возможным повреждением тканей. По причине возникновения боль классифицируется на ноцицептивную боль, невропатическую боль и психогенную боль. В качестве боли, вызванной неизвестной причиной, известен синдром фибромиалгии.
[0003]
Невропатическая боль представляет собой патологическую боль, вызванную дисфункцией периферической или центральной нервной системы, в частности, боль, вызванную, например, прямым повреждением и угнетением нервной ткани, несмотря на отсутствие ноцицептивного стимула к ноцицептору. В качестве терапевтического средства при невропатической боли используют противосудорожный препарат, антидепрессант, анксиолитическое лекарственное средство или противоэпилептическое лекарственное средство (габапентин, прегабалин или тому подобное).
[0004]
Синдром фибромиалгии представляет собой расстройство, при котором системная боль является ведущим симптомом, а нейропсихиатрические и нейровегетативные симптомы являются вторичными симптомами. В качестве терапевтических средств при синдроме фибромиалгии в основном используют прегабалин, который был одобрен в Соединенных Штатах и Японии, дулоксетин и милнаципран, которые были одобрены в Соединенных Штатах. Также используются лекарственные средства, которые не были одобрены в качестве терапевтического средства при синдроме фибромиалгии, то есть нестероидное противовоспалительное средство, опиоидное соединение, антидепрессант, противосудорожный лекарственный препарат и противоэпилептический препарат. Однако нестероидные противовоспалительные средства и опиоидные соединения, как правило, имеют слабый терапевтический эффект (непатентная литература 1).
[0005]
Кроме этого, в патентном документе 1 описано, что замещенные пиперидины обладают кардиотонической активностью. В патентном документе 2 раскрыто, что производные имидазола обладают ингибирующим эффектом в отношении FXa. В патентном документе 3 было высказано предположение, что замещенные пиперидины возможно обладают эффективностью в качестве лекарственного средства против избыточного веса или ожирения. В патентном документе 4 описано, что производное имидазола обладает анальгетическим действием.
Перечень цитируемой литературы
Патентная литература
[0006]
Патентный документ 1: патент Франции 2567885
Патентный документ 2: патентная публикация Японии (Kokai) № 2006-008664
Патентный документ 3: международная публикация WO2003/031432
Патентный документ 4: международная публикация WO2013/147160
Непатентная литература
[0007]
Непатентный документ 1: Pain and Therapy, vol. 2, p.87-104, 2013
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Техническая задача
[0008]
Терапия традиционным терапевтическим средством при невропатической боли, однако, часто связана с неблагоприятным воздействием на центральную нервную систему (например, головокружение, тошнота или рвота). Для обеспечения продолжительного введения при лечении невропатической боли было необходимым разработать новое терапевтическое средство.
[0009]
Даже прегабалин, дулоксетин и милнаципран, которые были одобрены в качестве терапевтических средств при синдроме фибромиалгии, не обеспечивают клинически удовлетворительного терапевтического эффекта против синдрома фибромиалгии, а их лекарственная эффективность значительно меняется среди пациентов. В этом контексте было крайне желательным разработка нового терапевтическое средства для лечения синдрома фибромиалгии, обладающего сильной фармакологической активностью и оказывающего терапевтический эффект у самых разных пациентов.
[0010]
Следует отметить, что в патентном документе 1 предполагалось, что описанные в нем замещенные пиперидины обладают эффективностью при лечении мигрени, а в патентном документе 4 раскрыто, что описанное в нем производное имидазола обладает анальгетическим действием. Однако не предоставлено ни какого-либо описания самого соединения, обладающего обезболивающим эффектом и раскрытого в настоящем изобретении, ни предположения о связи анальгетического действия с химической структурой. В патентном документе 2, в котором описаны производные имидазола, и в патентном документе 3, в котором описаны замещенные пиперидины, не раскрыта и не указана возможность обезболивающего действия, которым эти соединения обладают.
[0011]
В данных обстоятельствах целью настоящего изобретения является соединение, обладающее анальгетическим действием, в частности, в отношении невропатической боли и/или синдрома фибромиалгии.
Решение задачи
[0012]
Авторы настоящего изобретения провели интенсивные исследования с целью решения вышеупомянутых задач. В результате было обнаружено производное циклического амина, обладающее сильным анальгетическим действием, в частности, в отношении невропатической боли и/или синдрома фибромиалгии.
[0013]
Более конкретно, настоящее изобретение относится к производному циклического амина, представленному следующей общей формулой (I) или к его фармакологически приемлемой соли.
[Формула 1]
,
где атом углерода, отмеченный значком *, является асимметрическим атомом углерода, и А обозначает группу, представленную общей формулой (IIa), (IIb) или (IIc),
[Формула 2]
,
где R1 представляет собой метильную группу или этильную группу, необязательно замещенную атомом галогена, R2 представляет собой атом водорода или алкилкарбонильную группу, содержащую от 2 до 5 атомов углерода, каждый R3 независимо представляет собой метильную группу или этильную группу, и n представляет собой 1 или 2.
[0014]
В вышеуказанном производном циклического амина предпочтительным является, когда А обозначает группу, представленную общей формулой (IIa), где R1, более предпочтительно, представляет собой метильную группу или этильную группу, необязательно замещенную атомом фтора; и, еще более предпочтительно, метильную группу, этильную группу, дифторметильную группу или 2,2,2-трифторэтильную группу. Описание анальгетического действия может быть дополнено определением, указанным выше.
[0015]
В вышеуказанном производном циклического амина предпочтительным является, когда А обозначает группу, представленную общей формулой (IIb) или (IIc), где R1, более предпочтительно, представляет собой метильную группу или этильную группу, необязательно замещенную атомом фтора, и, еще более предпочтительно, метильную группу, этильную группу, дифторметильную группу или 2,2,2-трифторэтильную группу. Описание анальгетического действия может быть дополнено определением, указанным выше.
[0016]
В вышеуказанном производном циклического амина предпочтительным является, когда А обозначает группу, представленную общей формулой (IIа), и асимметрический атом углерода, отмеченный значком *, имеет S стереохимическую конфигурацию, где R1, более предпочтительно, представляет собой метильную группу или этильную группу, необязательно замещенную атомом фтора, и, еще более предпочтительно, метильную группу, этильную группу, дифторметильную группу или 2,2,2-трифторэтильную группу. Описание анальгетического действия может быть дополнено определением, указанным выше.
[0017]
Настоящее изобретение относится также к лекарственному средству, содержащему производное циклического амина, представленное вышеуказанной общей формулой (I), или его фармакологически приемлемую соль в качестве активного ингредиента.
[0018]
Лекарственное средство, предпочтительно, представляет собой обезболивающее средство и, особенно предпочтительно, терапевтическое средство для лечения невропатической боли или терапевтическое средство для лечения синдрома фибромиалгии.
[0019]
Настоящее изобретение относится также к фармацевтической композиции, содержащей производное циклического амина, представленное вышеуказанной общей формулой (I), или его фармакологически приемлемую соль и, например, фармакологически приемлемое вспомогательное средство.
[0020]
Настоящее изобретение относится также к производному циклического амина, представленному вышеуказанной общей формулой (I), или к его фармакологически приемлемой соли для применения в медицине.
[0021]
Настоящее изобретение относится также к производному циклического амина, представленному вышеуказанной общей формулой (I), или к его фармакологически приемлемой соли для применения при лечении боли. Болью, предпочтительно, является невропатическая боль или синдром фибромиалгии.
[0022]
Настоящее изобретение относится также к применению производного циклического амина, представленного вышеуказанной общей формулой (I), или его фармакологически приемлемой соли при лечении боли. Болью, предпочтительно, является невропатическая боль или синдром фибромиалгии.
[0023]
Настоящее изобретение относится также к применению производного циклического амина, представленного вышеуказанной общей формулой (I), или его фармакологически приемлемой соли при получении лекарственного средства для лечения боли. Болью, предпочтительно, является невропатическая боль или синдром фибромиалгии.
[0024]
Настоящее изобретение относится также к способу лечения боли, включающему введение терапевтически эффективного количества производного циклического амина, представленного вышеуказанной общей формулой (I), или его фармакологически приемлемой соли нуждающемуся в этом пациенту. Болью, предпочтительно, является невропатическая боль или синдром фибромиалгии.
Положительные эффекты изобретения
[0025]
Производное циклического амина по настоящему изобретению или его фармакологически приемлемая соль обладают сильным анальгетическим действием, в частности, в отношении к невропатической боли и/или синдрому фибромиалгии.
Краткое описание рисунков
[0026]
[Фигура 1]. На фигуре 1 представлен график, показывающий действие соединения по примеру 1 на модели с частичной лигатурой седалищного нерва (пероральное введение).
[Фигура 2]. На фигуре 2 представлен график, показывающий действие соединения по примеру 2 на модели с частичной лигатурой седалищного нерва (пероральное введение).
[Фигура 3]. На фигуре 3 представлен график, показывающий действие соединения по примеру 3 на модели с частичной лигатурой седалищного нерва (пероральное введение).
[Фигура 4]. На фигуре 4 представлен график, показывающий действие соединения по примеру 4 на модели с частичной лигатурой седалищного нерва (пероральное введение).
[Фигура 5]. На фигуре 5 представлен график, показывающий действие соединения по примеру 5 на модели с частичной лигатурой седалищного нерва (пероральное введение).
[Фигура 6]. На фигуре 6 представлен график, показывающий действие соединения по примеру 7 на модели с частичной лигатурой седалищного нерва (пероральное введение).
[Фигура 7]. На фигуре 7 представлен график, показывающий действие соединения по примеру 8 на модели с частичной лигатурой седалищного нерва (пероральное введение).
[Фигура 8]. На фигуре 8 представлен график, показывающий действие соединения по примеру 9 на модели с частичной лигатурой седалищного нерва (пероральное введение).
[Фигура 9]. На фигуре 9 представлен график, показывающий действие соединения по примеру 10 на модели с частичной лигатурой седалищного нерва (пероральное введение).
[Фигура 10]. На фигуре 10 представлен график, показывающий действие соединения по примеру 11 на модели с частичной лигатурой седалищного нерва (пероральное введение).
[Фигура 11]. На фигуре 11 представлен график, показывающий действие соединения по примеру 12 на модели с частичной лигатурой седалищного нерва (пероральное введение).
[Фигура 12]. На фигуре 12 представлен график, показывающий действие соединения по примеру 13 на модели с частичной лигатурой седалищного нерва (пероральное введение).
[Фигура 13]. На фигуре 13 представлен график, показывающий действие соединения по примеру 11 на модели фибромиалгии у крысы (пероральное введение).
[Фигура 14]. На фигуре 14 представлен график, показывающий действие соединения по сравнительному примеру 1 на модели с частичной лигатурой седалищного нерва в сравнении с действием соединения по примеру 11, показанного на фигуре 10 (пероральное введение).
[Фигура 15]. На фигуре 15 представлен график, показывающий действие соединений по сравнительным примерам 3-6 на модели с частичной лигатурой седалищного нерва в сравнении с действием соединения по примеру 11, показанного на фигуре 10 (пероральное введение).
[Фигура 16]. На фигуре 16 представлен график, показывающий действие соединения по сравнительному примеру 1 на моделях фибромиалгии у крысы в сравнении с действием соединения по примеру 11, показанного на фигуре 13 (пероральное введение).
[Фигура 17]. На фигуре 17 представлен график, показывающий кривые «концентрация в плазме-время» для соединения по примеру 11 у обезьян яванских макак (внутривенное введение и пероральное введение).
[Фигура 18]. На фигуре 18 представлен график, показывающий кривые «концентрация в плазме-время» для соединения по сравнительному примеру 2 у обезьян яванских макак (внутривенное введение и пероральное введение).
Описание вариантов осуществления изобретения
[0027]
Термины, используемые далее в описании, если не указано иное, имеют следующие значения.
[0028]
Отличительным признаком является тот факт, что производное циклического амина по настоящему изобретению представлено следующей общей формулой (I).
[Формула 3]
где атом углерода, отмеченный значком *, представляет собой асимметрический атом углерода, и А обозначает группу, представленную общей формулой (IIa), (IIb) или (IIc).
[Формула 4]
где R1 представляет собой метильную группу или этильную группу, необязательно замещенную атомом галогена, R2 представляет собой атом водорода или алкилкарбонильную группу, содержащую от 2 до 5 атомов углерода, каждый R3 независимо представляет собой метильную группу или этильную группу, и n представляет собой 1 или 2.
[0029]
В вышеуказанном производном циклического амина предпочтительным является, когда А обозначает группу, представленную общей формулой (IIa), и R1, предпочтительно, представляет собой метильную группу или этильную группу, необязательно замещенную атомом фтора, и, более предпочтительно, метильную группу, этильную группу, дифторметильную группу или 2,2,2-трифторэтильную группу.
[0030]
В вышеуказанном производном циклического амина предпочтительным является, когда А обозначает группу, представленную общей формулой (IIb) или (IIc), в которой R1, предпочтительно, представляет собой метильную группу или этильную группу, необязательно замещенную атомом фтора; и, более предпочтительно, метильную группу, этильную группу, дифторметильную группу или 2,2,2-трифторэтильную группу.
[0031]
В вышеуказанном производном циклического амина предпочтительным является, когда А обозначает группу, представленную общей формулой (IIа), и асимметрический атом углерода, обозначенный значком *, имеет S стереохимическую конфигурацию, где R1, предпочтительно, представляет собой метильную группу или этильную группу, необязательно замещенную атомом фтора; и, более предпочтительно, метильную группу, этильную группу, дифторметильную группу или 2,2,2-трифторэтильную группу.
[0032]
В варианте осуществления вышеуказанного производного циклического амина по настоящему изобретению А обозначает группу, представленную общей формулой (IIa), R1 представляет собой метильную группу или этильную группу, необязательно замещенную атомом фтора, R2 представляет собой атом водорода или алкилкарбонильную группу, содержащую от 2 до 5 атомов углерода, и каждый R3 независимо представляет собой метильную группу или этильную группу. В этом варианте осуществления предпочтительной является стереохимическая конфигурация асимметрического атома углерода, отмеченного значком *, в виде S.
[0033]
В варианте осуществления вышеуказанного производного циклического амина по настоящему изобретению А обозначает группу, представленную общей формулой (IIa), R1 представляет собой метильную группу, этильную группу, дифторметильную группу или 2,2,2-трифторэтильную группу, R2 представляет собой атом водорода или алкилкарбонильную группу, содержащую от 2 до 5 атомов углерода, и каждый R3 независимо представляет собой метильную группу или этильную группу. В этом варианте осуществления предпочтительной является стереохимическая конфигурация асимметрического атома углерода, отмеченного значком *, в виде S.
[0034]
В варианте осуществления вышеуказанного производного циклического амина по настоящему изобретению А обозначает группу, представленную общей формулой (IIa), R1 представляет собой метильную группу или 2,2,2-трифторэтильную группу, R2 представляет собой атом водорода или алкилкарбонильную группу, имеющую 2 атома углерода, и R3 представляет собой метильную группу. В этом варианте осуществления предпочтительной является стереохимическая конфигурация асимметрического атома углерода, отмеченного значком *, в виде S.
[0035]
В варианте осуществления вышеуказанного производного циклического амина по настоящему изобретению A представляет собой группу, представленную общей формулой (IIb), где R1 представляет собой метильную группу или этильную группу, необязательно замещенную атомом фтора, R2 представляет собой атом водорода или алкилкарбонильную группу, содержащую от 2 до 5 атомов углерода, каждый R3 независимо представляет собой метильную группу или этильную группу, и n представляет собой 1 или 2. В этом варианте осуществления предпочтительной является стереохимическая конфигурация асимметрического атома углерода, отмеченного значком *, в виде S.
[0036]
В варианте осуществления вышеуказанного производного циклического амина по настоящему изобретению А обозначает группу, представленную общей формулой (IIb), R1 представляет собой метильную группу, этильную группу, дифторметильную группу или 2,2,2-трифторэтильную группу, R2 представляет собой атом водорода или алкилкарбонильную группу, содержащую от 2 до 5 атомов углерода, каждый R3 независимо представляет собой метильную группу или этильную группу, и n представляет собой 1 или 2. В этом варианте осуществления предпочтительной является стереохимическая конфигурация асимметрического атома углерода, отмеченного значком *, в виде S.
[0037]
В варианте осуществления вышеуказанного производного циклического амина по настоящему изобретению A представляет собой группу, представленную общей формулой (IIb), R1 представляет собой метильную группу или 2,2,2-трифторэтильную группу, R2 представляет собой атом водорода или алкилкарбонильную группу, имеющую 2 атома углерода, R3 представляет собой метильную группу, и n представляет собой 1 или 2. В этом варианте осуществления предпочтительной является стереохимическая конфигурация асимметрического атома углерода, отмеченного значком *, в виде S.
[0038]
В варианте осуществления вышеуказанного производного циклического амина по настоящему изобретению A представляет собой группу, представленную общей формулой (IIc), где R1 представляет собой метильную группу или этильную группу, необязательно замещенную атомом фтора, где R1 представляет собой атом водорода или алкилкарбонильную группу, содержащую от 2 до 5 атомов углерода, и R3 представляет собой метильную группу или этильную группу. В этом варианте осуществления предпочтительной является стереохимическая конфигурация асимметрического атома углерода, отмеченного значком *, в виде S.
[0039]
В варианте осуществления вышеуказанного производного циклического амина по настоящему изобретению A представляет собой группу, представленную общей формулой (IIc), R1, предпочтительно, представляет собой метильную группу, этильную группу, дифторметильную группу или 2,2,2-трифторэтильную группу, R2 представляет собой атом водорода или алкилкарбонильную группу, содержащую от 2 до 5 атомов углерода, и R3 представляет собой метильную группу или этильную группу. В этом варианте осуществления предпочтительной является стереохимическая конфигурация асимметрического атома углерода, отмеченного значком *, в виде S.
[0040]
В варианте осуществления вышеуказанного производного циклического амина по настоящему изобретению А обозначает группу, представленную общей формулой (IIс), R1 представляет собой метильную группу или 2,2,2-трифторэтильную группу, R2 представляет собой атом водорода или алкилкарбонильную группу, имеющую 2 атома углерода, и R3 представляет собой метильную группу. В этом варианте осуществления предпочтительной является стереохимическая конфигурация асимметрического атома углерода, отмеченного значком *, в виде S.
[0041]
«Атом галогена» относится к атому фтора, атому хлора, атому брома или атому йода.
[0042]
«Метильная группа или этильная группа, необязательно замещенная атомом галогена» относится к метильной группе или этильной группе, в которой атомы водорода независимо и необязательно заменены на атом галогена, как указано выше. Например, можно указать метильную группу или этильную группу, или дифторметильную группу, 2-фторэтильную группу, 2-хлорэтильную группу, 2,2-дифторэтильную группу или 2,2,2-трифторэтильную группу.
[0043]
«Алкилкарбонильная группа, содержащая от 2 до 5 атомов углерода» относится к группе, полученной путем связывания линейной, разветвленной или циклической насыщенной углеводородной группы, имеющей от 1 до 4 атомов углерода, с карбонильной группой. Например, можно указать ацетильную группу, н-пропионильную группу, н-бутирильную группу, изобутирильную группу или валерильную группу.
[0044]
Конкретные примеры предпочтительного соединения в качестве производного циклического амина, представленного вышеуказанной общей формулой (I) (в данном документе называемого производным циклического амина (I)), показаны в таблице 1-1 и таблице 1-2; однако настоящее изобретение ими не ограничивается.
[0045]
[Таблица 1-1]
| Структурная формула | Структурная формула | Структурная формула |
[0046]
[Таблица 1-2]
| Структурная формула | Структурная формула | Структурная формула |
[0047]
Следует отметить, что, когда производное циклического амина (I) имеет изомеры, такие как энантиомеры и стереоизомеры, любой из изомеров и их смеси включены в производное циклического амина (I). Кроме того, когда образуются конформационные изомеры, такие изомеры и их смеси включены в производное циклического амина (I). Желаемый изомер может быть получен известным способом или аналогичным способом. Например, когда присутствует энантиомер производного циклического амина (I), энантиомер, отделенный от производного циклического амина (I), включен в производное циклического амина (I).
[0048]
Желаемый энантиомер может быть получен известным способом (например, используется оптически активное синтетическое промежуточное соединение, или рацемическая смесь конечного продукта подвергается известному способу обработки или аналогичному способу (например, оптическому разделению)).
[0049]
Пролекарство или фармакологически приемлемая соль производного циклического амина (I) также включены в объем настоящего изобретения. Пролекарство производного циклического амина (I) относится к соединению, которое ферментативно или химически превращается в производное циклического амина (I) in vivo. Активная форма пролекарства производного циклического амина (I) представляет собой производное циклического амина (I); однако и пролекарство самого производного циклического амина (I) может обладать активностью.
[0050]
В качестве пролекарства производного циклического амина (I), например, можно указать соединение, полученное алкилированием, фосфорилированием или борированием гидроксильной группы производного циклического амина (I). Каждое из этих соединений может быть синтезировано из производного циклического амина (I) в соответствии с известным способом.
[0051]
Пролекарство производного циклического амина (I) может быть превращено в производное циклического амина (I) в физиологических условиях, как описано в литературе («Development of pharmaceutical products», Hirokawa-Shoten Ltd., vol. 7, p. 163-198, 1990, и Progress in Medicine, vol. 5, p. 2157-2161, 1985).
[0052]
Производное циклического амина (I) может быть мечено изотопом. Примеры используемых при мечении радиоизотопов включают 2H, 3H, 13C, 14C, 15N, 15O, 18O и/или 125I.
[0053]
В качестве фармакологически приемлемой соли производного циклического амина (I) можно указать, например, неорганическую соль, такую как гидрохлорид, сульфат, фосфат или гидробромид; или органическую соль, такую как оксалат, малонат, цитрат, фумарат, лактат, малат, сукцинат, тартрат, ацетат, трифторацетат, малеат, глюконат, бензоат, салицилат, ксинафоат, памоат, аскорбат, адипат, метансульфонат, п-толуолсульфонат или циннамат. Эти соли могут присутствовать в форме гидрата, сольвата или кристаллического полиморфа.
[0054]
Производное циклического амина (I) может быть синтезировано способами получения, которые описаны ниже. Следует отметить, что каждое производное циклического амина (I), полученное следующими далее способами получения, может быть выделено/очищено известными способами (например, экстракцией растворителями, перекристаллизацией и/или хроматографией) и превращено в желаемые соли известными способами или аналогичным способом. Когда производное циклического амина (I) получают в форме соли, его можно превратить в производное циклического амина (I) или другую желаемую соль известным способом или аналогичным способом.
[0055]
В отдельных реакциях способов получения, которые описаны ниже, если исходное соединение имеет гидроксильную группу, аминогруппу или карбоксильную группу, в эти группы может быть введена защитная группа. Желаемое соединение может быть получено удалением защитной группы, если необходимо, после реакции.
[0056]
В качестве защитной группы для гидроксильной группы, можно указать, например, тритильную группу, аралкильную группу, содержащую от 7 до 10 атомов углерода (например, бензильную группу), или замещенную силильную группу (например, триметилсилильную группу, триэтилсилильную группу или трет-бутилдиметилсилильную группу).
[0057]
В качестве защитной группы для аминогруппы можно указать, например, алкилкарбонильную группу, содержащую от 2 до 6 атомов углерода (например, ацетильную группу), бензоильную группу, алкилоксикарбонильную группу, содержащую от 2 до 8 атомов углерода (например, трет-бутоксикарбонильную группу или бензилоксикарбонильную группу), аралкильную группу, содержащую от 7 до 10 атомов углерода (например, бензильную группу) или фталоильную группу.
[0058]
В качестве защитной группы для карбоксильной группы можно указать, например, алкильную группу, содержащую от 1 до 6 атомов углерода (например, метильную группу, этильную группу или трет-бутильную группу), или аралкильную группу, содержащую от 7 до 10 атомов углерода (например, бензильную группу).
[0059]
Удаление защитной группы, которое зависит от вида защитной группы, может осуществляться в соответствии с известным способом (например, Greene, T. W., «Greene,s Protective Groups in Organic Synthesis», Wiley-Interscience) или аналогичным способом.
[0060]
1. Получение соединения (Ia):
1-1. Способ получения соединения (Ia-a):
[Формула 5]
где отдельные условные символы имеют значения, определенные выше.
[0061]
(Стадия 1)
Соединение (Ia-a), которое представляет собой производное циклического амина (I), где A обозначает группу, представленную общей формулой (IIa), может быть получено, например, реакцией альдольной конденсации соединения (IIIА) и соединения (IV) в присутствии основания.
[0062]
В качестве соединения (IIIA) и соединения (IV), используемых в реакции альдольной конденсации, можно непосредственно использовать коммерчески доступные соединения; однако они могут быть синтезированы, например, в соответствии со способами получения, которые описаны ниже.
[0063]
В качестве основания, которое используется в реакции альдольной конденсации, можно указать диизопропиламид лития, трет-бутоксид калия, гидрид натрия, фениллитий или трет-бутиллитий.
[0064]
Количество основания, используемого в реакции альдольной конденсации, составляет, предпочтительно, от 0,5 до 10 молей на 1 моль соединения (IIIA) и, более предпочтительно, от 0,8 до 5 молей.
[0065]
Количество соединения (IV), используемого в реакции альдольной конденсации, составляет, предпочтительно, от 0,5 до 3 молей на 1 моль соединения (IIIA) и, более предпочтительно, от 0,8 до 1,5 молей.
[0066]
Реакцию альдольной конденсации обычно проводят в растворителе. Растворитель, который не ингибирует реакцию, выбирают соответствующим образом. В качестве растворителя можно указать, например, галогенированный углеводород, такой как дихлорметан, хлороформ или 1,2-дихлорэтан; или простой эфир, такой как тетрагидрофуран или 1,4-диоксан. Может использоваться смесь этих растворителей.
[0067]
В реакции альдольной конденсации температура реакции, предпочтительно, составляет от -78°C до 100°C и, более предпочтительно, от -78°C до 50°C.
[0068]
В реакции альдольной конденсации время реакции, которое изменяется в зависимости от условий реакции, составляет, предпочтительно, от 5 минут до 48 часов и, более предпочтительно, от 30 минут до 24 часов.
[0069]
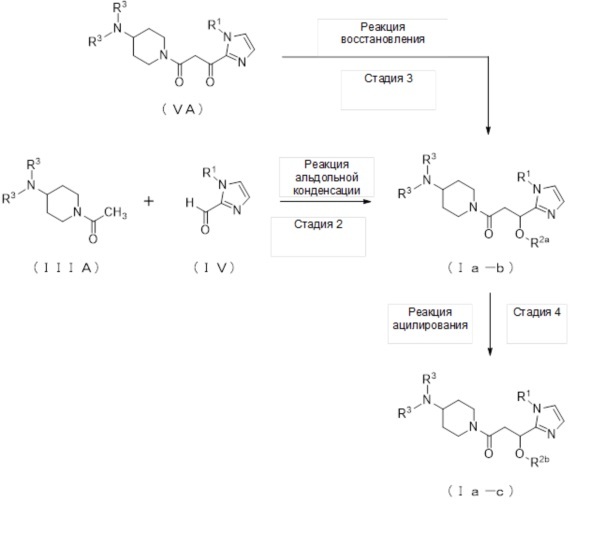
1-2. Способ получения соединений (Ia-b) и (Ia-c):
[Формула 6]
где R2а представляет собой атом водорода, R2b представляет собой алкилкарбонильную группу, содержащую от 2 до 5 атомов углерода, и значение других условных символов такое, как определено выше.
[0070]
(Стадия 2)
Соединение (Ia-b), которое представляет собой производное циклического амина (I), где A обозначает группу, представленную общей формулой (IIa) и R2 представляет собой атом водорода, может быть получено, например, реакцией альдольной конденсации соединения (IIIА) и соединения (IV) в присутствии основания.
[0071]
В качестве соединения (IIIA) и соединения (IV), используемых в реакции альдольной конденсации, можно непосредственно испо