Композиция для приготовления противоопухолевого средства и способ приготовления противоопухолевого средства на ее основе
Иллюстрации
Показать всеИзобретение относится к фармакологии и касается композиции для приготовления противоопухолевого средства в виде раствора для инъекций. Композиция содержит аллоферон в концентрации от 0,05 до 0,1 мас.%, цис-дихлордиамминплатину в концентрации от 0,01 до 0,05 мас.% и воду. Композиция по изобретению характеризуется противоопухолевой активностью и пониженной токсичностью. 1 ил., 3 табл., 5 пр.
Реферат
Изобретение относится к фармакологии и касается композиции для приготовления противоопухолевого средства, которое представляет собой комплекс солей двухвалентной платины и пептида аллоферон и к фармацевтическим композициям, содержащим указанные комплексы. Может найти применение для изготовления препаратов, использующихся в онкологии.
Поиск новых препаратов противоопухолевого действия занимает одно из центральных мест современной биофизики, молекулярной биологии, химии и медицины. Среди известных препаратов противоопухолевого действия особое место занимают препараты на основе металлических комплексов, наиболее известными из которых являются комплексы на основе платины.
Использование комплексов платины в противораковой химиотерапии хорошо известно специалистам. При этом в данном качестве используются, прежде всего, препараты двухвалентной платины - платины (II). Для лечения рака обычно применяются такие платиносодержащие препараты, как цисплатин (cisplatin), карбоплатин (carboplatin), оксаплатин (oxaliplatin) и другие. Однако эти соединения оказываются полезными для лечения не всех типов опухолей, к тому же, некоторые типы раковых клеток могут проявлять резистентность к этим лекарствам. Одним из самых больших недостатков упомянутых платиносодержащих препаратов является то, что они отличаются высокой нейротоксичностью, ототоксичностью, нефротоксичностью, миелосупрессией и вызывают большое количество нежелательных побочных эффектов.
Платиновые препараты обладают широким спектром противоопухолевого действия. Наиболее изученный препарат этого класса противоопухолевых средств - цис-дихлордиаминоплатинид (ДДП) активен против опухолей различного генезиса: спонтанных, перевивных, индуцированных вирусами и химическими канцерогенами. Основной недостаток ДДП - его высокая токсичность, в результате которой нарушается работа почек, костного мозга и желудочно-кишечного тракта (Биологические аспекты координационной химии, ред. К.Б. Яцимирского. Киев. ''Наукова думка''. 1979 г. стр. 149-180).
Противоопухолевая активность комплексных соединений платины (II) связана с образованием прочных связей с азотистыми основаниями ДНК (в основном с гуанином), что приводит к апоптозу опухолевых клеток. Известно, что в клетки попадает далеко не весь введенный препарат. его часть выводится из кровяного русла почками, главным образом в неизменном виде или в виде тетрамминных комплексов. Именно поэтому главным ''пострадавшим'' от побочных эффектов платиновых лекарств оказывается система выделения.
Препарат ДДП (торговое название «Цисплатин») применяется в достаточно высоких дозах, что повышает вероятность возникновения осложнений, связанных с токсичностью препаратов платины.
Исследования различных комплексов платины на животных и клинические испытания ДДП и некоторых его аналогов обнаружили разнообразие в биологических свойствах комплексов платины: противоопухолевой активности и побочного действия. Было показано, что незначительные изменения в молекулярной структуре комплекса могут вызывать радикальные их изменения в биологической активности. Существование связи между структурой комплексного соединения и его противоопухолевой активностью стимулирует поиск новых содержащих платину препаратов - высокоактивных и вместе с тем низкотоксичных.
Сразу после обнаружения противоопухолевого эффекта (ДДП), многие лаборатории по всему миру предприняли исследования его структурных аналогов. Несмотря на то, что молекулярные механизмы их воздействия на клеточные структуры остаются далекими от понимания, достигнуты определенные успехи - увеличена растворимость, снижена токсичность, увеличена клеточная проницаемости и др. К сожалению, очень немногие из найденных лекарств по терапевтическому индексу (отношение активность/токсичность) превзошли ДДП.
При создании новых противоопухолевых препаратов на основе ДДП используют в основном два метода: 1. химическую модификацию молекулы путем введения в нее различных заместителей (как правило, заместители вводятся на место одного или двух атомов хлора), 2. образование комплекса ДДП с другим соединением, в том числе обладающим собственной биологической активностью.
Первый путь привел к созданию таких, вошедших в клиническую практику, противоопухолевых препаратов как: карбоплатин (циклобутан-1,1-дикарбоксилато)диаминплатина), оксалиплатин ([(1R,2R)-1,2-циклогександиамин-N,N'][оксалато(2)-O,O'] платина).
Введением пиридинового кольца в молекулу ДДП был создан препарат пириплатин. Введением в ДДП больших по размеру колец Стивен Дж. Липпард (Stephen J Lippard) с коллегами получили препарат фенантриплатин, показавший в исследованиях на ряде клеток эффективность более высокую, чем цисплатин.
Конденсацией цисплатина с желчными кислотами Энцо Бартоли, Бениамино Палмиери, Алессандро Медичи (патент WO/2003/095470 «Platinum complexes having antitumor activity») создали препарат, имеющий пониженную токсичность и эффективный при опухолях семенников и яичников.
Группой авторов разработан препарат S-малатоаммин (цикло-пентиламин)платина (П) (патент RU 2128042 «Противопухолевое средство», Чельцов-Бебутов П.А. и другие), показавший эффективность по отношению к ряду опухолей резистентных к цисплатину. Платина известна склонностью к образованию координационных комплексных соединений. Поэтому еще одним способом создания платиносодержащих противоопухолевых препаратов является связывание платины в них в комплексы с различными лигандами. Лиганды могут быть различной природы: как низко - так и высокомолекулярными соединениями, как инертными, так и биологически активными.
Описаны комплексы платины с гуминовыми кислотами - патенты РФ 2182482 «Способ получения антиракового средства» и РФ 2178702 «Антираковое средство» авторов Трофимов В.А.; Шипов В.П.; Пигарев Е.С., Попов А.И.; Иванов В.Н. и патент РФ №2368379 «Противоопухолевое средство» Шипов В.П., Пигарев Е.С., Федорос Е..И., Трофимова Н.П.
Авторы патентов в качестве соединения платины используют как цисплатин, так тетрахлороплатинат калия и другие соединения платины, а в качестве гуминовых веществ аммониевые соли лигногуминовых кислот. Изобретение обеспечивает уменьшение токсичности препарата при одновременном повышении эффективности лечения раковых заболеваний.
При этом необходимо отметить, что используемые в качестве лиганда гуминовые кислоты обладают собственной биологической активностью - антиоксидантной, противовоспалительной, противовирусной и иммуномодулирующей.
Известен патент SU 1813089 A3 Волченковой И.И., Майданевич Н.Н., Бударина Л.И., Шалимова С.А., Трохименко Е.П., Кейсевич Л.В. «Способ получения комплексного соединения платины (II) с ДНК, обладающего противоопухолевой активностью», в котором водный, содержащий ДНК и хлорид натрия, раствор смешивают с водным раствором ДДП.
Способ позволяет получить средство, сочетающее высокую противоопухолевую активность с выраженным иммуномодулирующим действием. Развитием этой работы является патент WO 2010074662 A1 O.S. Sokyrko с соавторами «Противоопухолевое средство, способ его получения и способ его стабилизации»
В работе Екимова А.А., Алексеевой Г.М., Караваевой А.В.. «Комплексные соединения платины с дипептидами: биологическая активность», Фармация, 2014, №6, с. 52-54 получены и описаны биядерные комплексы цис-дихлородиамминплатины с дипептидами - D,L-аланил- D,L-аланином (Ala-Ala). D.L-аланил-глицином (Ala-Gly) D,L-аланил-L-лейцином (Ala-Leu), D,L-аланил-L-норлейцином (Ala-nLeu). Введение в координационную сферу платины дипептидов способствует изменению спектра противоопухолевого действия из-за целенаправленной доставки соединения к опухолевой клетке, а также снижению влияния токсичности на организм.
Наряду с цитостатиками, к которым относятся вышеописанные препараты платины, в лечении рака нашли применение рекомбинантные белки из группы интерферонов в качестве активаторов противоопухолевого иммунитета и ингибиторов пролиферации опухолевых клеток. Интерфероны применяются для лечения множественной миеломы (Zee et al., J. Clin. Oncol., 1998, 16,8, p. 2834-2839), болезни Ходжкина (Aviles et al. Leuk. Lymphoma, 1998, 30, 5-6, p. 651-656), миелоидной лейкемии (Gilbert, Cancer, 1998, 83, 6, p. 1205-13). С этой же целью в лечении онкологических заболеваний используют вещества - индукторы интерферонов, такие как: неовир, циклоферон и другие.
К категории индукторов интерферонов относится и олигопептид аллоферон, обладающий высокой противовирусной активностью.
На основе аллоферона создан противовирусный лекарственный препарат «Аллокин-альфа, лиофилизат для приготовления раствора для подкожного введения, 1 мг» (Р N002829/01). Аллокин-альфа эффективен при терапии пациентов страдающих хронической папилломавирусной инфекцией, вызванной онкогенными вирусами папилломы человека; в комплексной терапии хронического рецидивирующего герпеса 1 и 2 типов; в составе комплексной терапии среднетяжелой (желтушной) формы острого гепатита В. Как известно, папиломовирусы и вирусы герпеса являются онкогенными. Имеются сведения о противоопухолевых свойствах аллоферонов, основанных на активации механизмов противоопухолевого иммунитета - интерферонов и естественных киллеров (Chernysh et al., Proceedings of National Academy of Science, 2002, 99, p. 12628-12632). Отличительным свойством пептидов семейства аллоферонов является их высокая комплексообразующая активность. Изучены комплексы аллоферона-1 и его аналогов с большим количеством переходных металлов, в том числе с медью (M. Kuczer and other. J. Inorganic Biochemistry, 111, 2012, 40-49), никелем и другими. Известно также (M. Kuczer and other, Inorganic Chemistry, 2013, 52, 5951-5961), что такие комплексы могут обладать биологической активностью. В патенте RU 2470031, Киселев О.И., Ершов Ф.И. «Биологически активные пептидные комплексы» показано, что уровень индукции интерферона-альфа вызываемый цинковым комплексом аллоферона существенно выше, чем это установлено для аллоферона и циклоферона.
Наиболее близким решением является АЛЛОФЕРОНЫ-ИММУНОМОДУЛИРУЮЩИЕ ПЕПТИДЫ (патент RU 2172322, опубликовано: 20.08.2001), в котором описываются новые соединения общей формулы I: X1-His-Gly-X2-His-Gly-Val-Х3 или их фармацевтически приемлемые соли, или эфиры, или амиды, где X1 отсутствует либо содержит не менее 1 аминокислоты, Х2 содержит не менее 1 аминокислоты либо представляет собой пептидную связь; Х3 отсутствует либо содержит не менее 1 аминокислоты, причем указанные аминокислоты выбраны из групп: алифатической, ароматической или гетероциклической. Соединения стимулируют антивирусную, антимикробную и противоопухолевую активность иммунной системы человека.
Задачей настоящего изобретения является создание композиции для приготовления противоопухолевого препарата, который бы объединял противоопухолевую эффективность соединений платины и веществ, обладающих интерфероногенной активностью. Объединение может позволить снизить концентрацию платины и, тем самым, обеспечить уменьшение токсичности препарата.
Техническим результатом изобретения является возможность на основе композиции изготавливать различные виды препаратов для инъекций или лиофилизата, которые имеют одновременно противоопухолевую эффективность и пониженную токсичность.
Указанный технический результат достигается тем, что заявлена композиция для приготовления противоопухолевого средства в виде раствора для инъекций или лиофилизата, содержащая аллоферон, отличающаяся тем, что в качестве активного компонента используется комплексное соединение двухвалентной платины с олигопептидом аллоферон. Предпочтительно, в качестве соли платины используют цис-дихлордиамминплатину.
Способ приготовления противоопухолевого средства на основе вышеописанной композиции характеризующийся тем, что аллоферон постепенно вводят в раствор цисплатина с концентрацией 0,05%, полученный раствор перемешивают в течение 15 мин, после чего стерилизуют фильтрацией через фильтр с размером пор 0,2 мкм, затем разливают в ампулы.
Предпочтительно, формируют раствор, который имеет концентрацию ДДП от 0,01 до 0,05% и аллоферона от 0,05 до 0,1%.
Осуществление изобретения
Известно семейство цитокиноподобных пептидов - аллофероны, обладающих высокой противовирусной активностью (RU 2172322 Черныш С.И., Ким Су Ин, Беккер Г.П., Махалдиани Н.Б., Хоффманн Ж., Бюле Ф. «Аллофероны - иммуномодулирующие пептиды»). Механизм действия аллоферонов состоит в индукции синтеза эндогенных интерферонов и активации системы естественных киллеров.
Как известно из курса общей химии, платина обладает большой склонностью к образованию комплексных соединений.
Поставленная задача решается созданием противоопухолевого лекарственного средства, активным началом которого является комплексное соединение двухвалентной платины с пептидом аллоферон. Оно обладает пониженной токсичностью и большей эффективностью, связанной с сочетанием противоопухолевых свойств как солей платины (II), так и аллоферонов.
Предлагаемый препарат может являться как раствором для инъекций, так и лиофилизатом.
Возможность достижения цели изобретения подтверждается следующими примерами приготовления различных препаратов на основе заявленной композиции.
Пример 1.
Мольное соотношение АЛФ : ДДП равно 1:1.
В химический стакан, содержащий 10 мл 0,9% раствора натрия хлорида, вводят 5 мг сухой цис-дихлордиамминплатины. Раствор перемешивают до полного растворения соли. Затем в раствор добавляют 10 мг аллоферона. Раствор перемешивают в течение 15 мин, после чего стерилизуют фильтрацией через фильтр с размером пор 0,2 мкм, разливают по 2 мл в ампулы, которые запаивают. Полученный раствор имеет концентрацию ДДП 0,5 мг/мл (0,05%) и аллоферона 1,0 мг/мл (0,10%).
Пример 2.
Мольное соотношение АЛФ : ДДП равно 1:2.
В химический стакан, содержащий 10 мл 0,9% раствора натрия хлорида, вводят 5 мг сухой цис-дихлордиамминплатины. Раствор перемешивают до полного растворения соли. Затем в раствор добавляют 5 мг аллоферона. Раствор перемешивают в течение 15 мин, после чего стерилизуют фильтрацией через фильтр с размером пор 0,2 мкм, разливают по 2 мл в ампулы, которые запаивают. Полученный раствор имеет концентрацию ДДП 0,5 мг/мл (0,05%) и аллоферона 0,5 мг/мл (0,05%).
Пример 3.
Мольное соотношение АЛФ : ДДП равно 1:1.
В химический стакан, содержащий 10 мл 0,9% раствора натрия хлорида, вводят 5 мг сухой цис-дихлордиамминплатины. Раствор перемешивают до полного растворения соли. Затем в раствор последовательно добавляют 40 мг маннитола и 10 мг аллоферона. Раствор перемешивают в течение 15 мин, после чего стерилизуют фильтрацией через фильтр с размером пор 0,2 мкм, разливают по 2 мл во флаконы типа ФИ-5 или 4D. Флаконы помещают в камеру сублимационной сушилки и высушивают в стандартном режиме. После окончания процесса флаконы закрывают пробками и укупоривают колпачками алюминиевыми.
Полученный раствор имеет концентрацию ДДП 0,5 мг/мл (0,05%) и аллоферона 1,0 мг/мл (0,10%).
Пример 4.
Мольное соотношение АЛФ : ДДП равно 1:2.
В химический стакан, содержащий 10 мл 0,9% раствора натрия хлорида, вводят 5 мг сухой цис-дихлордиамминплатины. Раствор перемешивают до полного растворения соли. Затем в раствор последовательно добавляют 40 мг маннитола и 5 мг аллоферона. Далее соответственно примеру 3. Полученный раствор имеет концентрацию ДДП 0,5 мг/мл (0,05%) и аллоферона 0,5 мг/мл (0,05%).
Пример 5. Определение противоопухолевой активности
Эффективность предложенного изобретения продемонстрирована на примере препарата, полученного на основе товарного лекарственного средства Цисплатин-Тева содержащий 0,5 мг/мл платины.
Сравнительному исследованию подвергнуто три материала:
- Плацебо (раствор натрия хлорида 0,9%)
- Препарат сравнения Цисплатин-Тева (препарат 1)
- Препарат, описанный в примере 1 (препарат 2).
Испытание противоопухолевой активности проводилось на модели перевивной солидной опухоли Эрлиха. Штамм перевиваемого солидного рака Эрлиха мышей был получен из банка опухолевых штаммов ФГУ НИИ онкологии им. Петрова.
В работе использовались беспородные мыши обоего пола массой 18-20 г. Животных содержали в естественном режиме освещения со свободным доступом к стандартному корму и воде. Опухоль перевивали подкожно в количестве 107 клеток в объеме 0,2 мл. Животные были распределены по группам случайным образом. Для проведения эксперимента было сформировано три группы:
Группа 1 (n = 10). Животные получали физиологический раствор (плацебо),
- Группа 2 (n = 9). Животные получали препарат №1.
- Группа 3 (n = 9). Животные получали препарат №2.
На 13, 16, 22 и 25 дни эксперимента измеряли длину и ширину опухолевых узлов. Объем опухоли рассчитывали по формуле:
где а - больший, b - меньший линейный размер узла. Препараты и плацебо вводили подкожно в районе инъекции клеток опухоли на 3, 6, 9,13, 16 и 20 сутки после перевивки в объеме 0,2 мл каждой мыши.
Оценку противоопухолевой активности исследуемых агентов проводили сравнивая динамику роста опухолей в соответствии с принятыми в экспериментальной онкологии методами (Методические рекомендации по доклиническому изучению средств, обладающих способностью ингибировать процесс метастазирования и повышать эффективность цитостатической терапии злокачественных опухолей /Под ред. Е.Д. Гольдберга, А.Б. Сыркина. М., 1992).
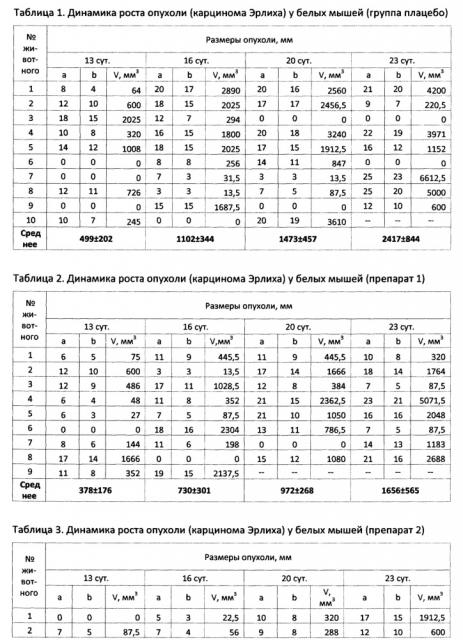
Полученные данные изучения размеров опухоли у белых мышей показаны ниже в в таблицах 1, 2 и 3, а также на Фиг.
На Фиг. показана динамика роста перевивной карциномы Эрлиха у белых мышей в условиях применения химиопрепаратов. При этом Препараты №1 (Цис-платин) и №2 проявляют противоопухолевые свойства. Препарат на основе композиции №2, где в качестве активного компонента используется комплексное соединение двухвалентной платины с олигопептидом аллоферон, оказался значительно (втрое) эффективнее по сравнению с Цис-платином.
Композиция для приготовления противоопухолевого средства в виде раствора для инъекций, характеризующаяся тем, что она содержит аллоферон в концентрации от 0,05 до 0,1 мас. %, цис-дихлордиамминплатину в концентрации от 0,01 до 0,05 мас. % и воду.