Трициклические соединения в качестве ингибиторов иммуносупрессии, опосредуемой метаболизированием триптофана
Иллюстрации
Показать всеИзобретение относится к соединению формулы (I), в которой n принимает значение 0; связь α представляет собой одинарную связь; кольцо A представляет собой ароматическое кольцо, где i) V и X представляют собой N, W и Z представляют собой CH и Y представляет собой C; или ii) V, Y и Z представляют собой N, W представляет собой CH и X представляет собой C; или iii) V, W и Y представляют собой N, X представляет собой C и Z представляет собой CH; R2 представляет собой -CН2-RA, RA представляет собой -C(O)R3 или -C(ORB)(R3)(RC), RB представляет собой атом водорода; каждый R3 представляет собой C3-8-циклоалкил или 6-членный гетероциклил, содержащий один атом азота в качестве гетероатома, C3-8-циклоалкил необязательно замещен двумя группами R31; 6-членный гетероциклил необязательно замещен одной группой R31; каждый R31 независимо представляет собой атом галогена или -C(O)N(R)2, и RC представляет собой атом водорода; и каждый R независимо представляет собой атом водорода или R10, R10 представляет собой фенил, необязательно замещенный C1-6-алкильной группой. Изобретение также относится к индивидуальным соединениям и к фармацевтической композиции. Технический результат: получены новые соединения формулы (I), обладающие IDO/TDO-ингибирующей активностью. 3 н. и 15 з.п. ф-лы, 4 ил., 19 пр.
Реферат
УРОВЕНЬ ТЕХНИКИ
Область техники, к которой относится изобретение
[0001]
Данное изобретение относится к соединениям и способам ингибирования индоламин-2,3-диоксигеназы (ИДО (IDO)) и триптофан-2,3-диоксигеназы (ТДО (TDO)); кроме того, изобретение относится к способу лечения заболеваний и нарушений, опосредуемых дефицитом триптофана.
Описание предшествующего уровня техники
[0002]
Триптофан (Trp) является незаменимой аминокислотой, необходимой для биосинтеза белков, никотиновой кислоты и нейротрансмиттера 5-гидрокситриптамина (серотонина). Ферменты индоламин-2,3-диоксигеназа 1 (также известная как INDO1 или IDO1 (ИДО1)), индоламин-2,3-диоксигеназа 2 (также известная как INDOL1 или IDO2 (ИДО2)) и триптофан-2,3-диоксигеназа (TDO (ТДО)) катализируют первую и лимитирующую скорость стадию при расщеплении L-триптофана до N-формилкинуренина. Хотя эти ферменты катализируют одну и ту же реакцию, компартментализация ИДО и ТДО, как полагают, опосредует их разные биологические роли. ИДО1 обычно экспрессирует в клетках желудочно-кишечного и легочного эпителия, придатках яичника, плаценте, пДК (pDC) в дренирующих лимфоузлах и клетках опухолей. ИДО2 экспрессирует преимущественно в головном мозге и плаценте, но некоторые сплайс-варианты также обнаруживают в печени, тонкой кишке, селезенке, плаценте, вилочковой железе, легком, головном мозге, почках и толстой кишке. ТДО экспрессирует преимущественно в печени и контролирует истечение пищевого Trp к путям метаболизма серотонина и кинуренина.
[0003]
Выравнивание аминокислотных последовательностей ИДО1 и ИДО2 обнаруживает высоко консервативные признаки, которые опосредуют связывание гема и субстрата. Даже в том случае, когда идентичность аминокислотной последовательности между ИДО1 и ИДО2 или ИДО1 и ТДО не является особенно высокой, существенные остатки, определенные как являющиеся важными для каталитической активности путем мутагенеза ИДО и ТДО и с помощью кристаллографического анализа, являются высоко консервативными между ИДО1, ИДО2 и ТДО, подтверждая структурную и функциональную аналогию в механизме диоксигенирования триптофана. Несмотря на структурное сходство на активном сайте, ИДО1 и ТДО имеют разную субстратную специфичность, причем ТДО является почти единственно специфичным для L-Trp и производных L-Trp, замещенных в 5- и 6-ом положениях индольной группы, при том, что ИДО1 может воспринимать и оксигенировать более широкий ряд субстратов, таких как D-Trp, триптамин, серотонин и 1-метил-L-Trp.
[0004]
В человеческих клетках стимуляция IFN-γ индуцирует активацию ИДО1, которая приводит к истощению Trp, прекращая за счет этого рост Trp-зависимых внутриклеточных патогенов, таких как Toxoplasma gondii и Chlamydia trachomatis. Активность ИДО1 также оказывает антипролиферативное действие на многих опухолевых клетках, и индукцию ИДО1 наблюдали in vivo во время отторжения аллогенных опухолей, что указывает на возможную роль этого фермента в процессе отторжения опухоли.
[0005]
Обнаружено, что клетки HeLa, культивированные вместе с лимфоцитами периферической крови (ЛПК (PBL)), приобретают иммуноингибиторный фенотип через повышающую регуляцию метаболического пути ИДО. Снижение пролиферации ЛПК при лечении интерлейкином-2 (IL-2), как полагают, является результатом ИДО, высвобожденной опухолевыми клетками в ответ на секрецию IFN-γ ЛПК. Этот эффект инвертируют за счет обработки 1-метил-триптофаном (1МТ), специфическим ингибитором ИДО. Предполагают, что активность ИДО в опухолевых клетках может способствовать ослаблению противоопухолевых реакций (Logan, et al., 2002, Immunology, 105: 478-87).
[0006]
Некоторый набор данных подтверждает, что ИДО вовлечены в возникновение иммунной толерантности. Изучение беременности млекопитающих, опухолевой резистентности, хронических инфекций и аутоиммунных заболеваний показало, что клетки, экспрессирующие ИДО, могут подавлять реакции Т-клеток и стимулировать толерантность. Ускоренный катаболизм Trp наблюдали при заболеваниях и нарушениях, ассоциирующихся с клеточной иммунной активацией, таких как инфекция, злокачественное новообразование, аутоиммунные заболевания и СПИД, а также во время беременности. Полагают, что ИДО хронически индуцируется ВИЧ-инфекцией, и, кроме того, растет за счет оппортунистических инфекций, и что хроническая потеря Trp инициирует механизмы, ответственные за кахексию, слабоумие и диарею и, вероятно, за иммуносупрессию больных СПИДом (Brown, et al., 1991, Adv. Exp. Med. Biol., 294: 425-35). В связи с этим недавно было показано, что ингибирование ИДО может повысить уровни вирус-специфических Т-клеток, и одновременно понизить число зараженных вирусом макрофагов в мышиных моделях ВИЧ (Portula et al., 2005, Blood, 106:2382-90).
[0007]
ИДО, как полагают, играет роль в иммуносупрессивных процессах, которые предупреждают отторжение плода в утробе. Более 40 лет назад установили, что во время беременности генетически несовместимое оплодотворенное яйцо млекопитающего приживается, вопреки тому, что можно было прогнозировать с помощью трансплантационной иммунологии ткани (Medawar, 1953, Symp. Soc. Exp. Biol. 7: 320-38). Анатомическое разделение матери и зародыша и антигенная недоразвитость зародыша не могут полностью объяснить выживание фетального аллотрансплантата. Последнее внимание сфокусировано на иммунологической толерантности матери. Так как ИДО экспрессируют клетки синцитиотрофобласта человека и концентрация системного трипофана падает во время нормальной беременности, была выдвинута гипотеза, что экспрессия ИДО при трансплацентраном барьере необходима для предупреждения иммунологического отторжения фетального аллотрансплантата. Для проверки этой гипотезы беременных мышей (несущих сингенные или аллогенные зародыши) подвергали воздействию 1МТ и наблюдали быстрое индуцированное Т-клетками отторжение всех аллогенных оплодотворенных яиц. Таким образом, за счет катаболизирования триптофана оплодотворенное яйцо млекопитающего, как оказывается, подавляет активность Т-клеток и защищает себя от отторжения, и блокирование катаболизма триптофана во время мышиной беременности дает возможность материнским Т-клеткам провоцировать отторжение фетального аллотрансплантата (Munn, et al., 1998, Science 281: 1191-3).
[0008]
Другое доказательство механизма иммунорезистентности опухоли на основе расщепления триптофана с помощью ИДО вытекает из наблюдения, что большинство опухолей человека конститутивно экспрессирует ИДО и что экспрессия ИДО иммуногенными мышиными опухолевыми клетками предупреждает их отторжение преиммунизированными мышами. Этот эффект сопровождается потерей специфических Т-клеток на участке опухоли и может быть частично инвертирован путем системного лечения мышей с помощью ингибитора ИДО при отсутствии заметной токсичности. Следовательно, это подтверждает тот факт, что эффективность терапевтической вакцинации раковых больных может быть улучшена за счет одновременного введения ингибитора ИДО (Uyttenhove et al., 2003, Nature Med., 9: 1269-74). Также показано, что ингибитор ИДО, 1-МТ, можно усилить с помощью химиотерапевтических средств, чтобы уменьшить рост опухоли у мышей, подтверждая, что ингибирование ИДО также может усилить противоопухолевую активность обычных цитотоксических схем лечения (Muller et al., 2005, Nature Med., 11:312-9).
[0009]
Аналогичную ситуацию наблюдают с ТДО. Показано, что значительная часть первичных опухолей человека экспрессирует повышенный уровень ТДО или ТДО плюс ИДО (Pilotte et al. 2012, P.N.A.S). Более того, фармакологическое ингибирование активности ТДО с помощью ингибиторов ТДО приводит к иммуноопосредуемому отторжению опухолей, сверхэкспрессирующих ТДО, что означает, что ТДО, точно так, как и ИДО1, может опосредовать стимулирующие развитие опухолей иммуносупрессорные эффекты.
[0010]
Одним из механизмов, вносящим вклад в иммунологическую невосприимчивость в отношении опухолей, может быть презентирование опухолевых антигенов с помощью толерогенного носителя АПК (АРС). Также описана субпопуляция человеческих ИДО-экспрессирующих антигенпрезентирующих клеток, которая со-экспрессирует CD123 (IL3RA) и CCR6 и ингибирует пролиферацию Т-клеток. Как зрелые, так и незрелые CD123-позитивные дендритные клетки подавляют активность Т-клеток, и эту ИДО-супрессивную активность блокируют с помощью 1МТ (Munn, et al., 2002, Science 297: 1867-70). Также показано, что дренирующие опухоль лимфоузлы (TDLN) мышей содержат субпопуляцию плазмацитоидных дендритных клеток (пДК (pDС)), которые конститутивно экспрессируют иммуносупрессивные уровни ИДО. Несмотря на содержание только 0,5% клеток лимфоузлов in vitro, эти пДК потенциально подавляют реакции Т-клеток на антигены, предоставленные самими пДК, а также доминантным образом подавляют реакции Т-клеток на третьи антигены, предоставленные несупрессивными АПК. В пределах популяции пДК большую часть функциональной ИДО-опосредуемой супрессивной активности выделили с новой субпопуляцией пДК, со-экспрессирующих маркер В-линии дифференцировки CD19. Таким образом, выдвинута гипотеза, что ИДО-опосредуемая супрессия пДК в TDLN создает локальную микросреду, которая потенциально подавляет реакции носителя противоопухолевых Т-клеток (Munn, et al., 2004, J. Clin. Invest., 114(2): 280-90).
[0011]
ИДО расщепляет индольный фрагмент триптофана, серотонина и мелатонина и инициирует продуцирование нейроактивных и иммунорегуляторных метаболитов, обобщенно известных как кинуренины. За счет локального истощения триптофана и роста проапоптозных кинуренинов ИДО, экспрессированная дендритными клетками (ДК (DC)), может сильно воздействовать на пролиферацию и выживание Т-клеток. Индукция ИДО в ДК могла бы быть общим механизмом деленационной толерантности, обусловленной регуляторными Т-клетками. Так как такие толерогенные реакции, как можно ожидать, функционируют при ряде физиологических условий, метаболизм триптофана и продуцирование кинуренина могли бы показать критическое взаимодействие между иммунной и нервной системами (Grohmann, et al., 2003, Trends Immunol., 24: 242-8).
[0012]
Разрабатываются маломолекулярные ингибиторы ИДО для лечения или предупреждения связанных с ИДО заболеваний, таких как заболевания, описанные выше. Например, в публикации PCT WO 99/29310 сообщается о способах изменения опосредуемого Т-клетками иммунитета, включающих изменение локальных внеклеточных концентраций триптофана и метаболитов триптофана с использованием ингибитора ИДО, такого как 1-метил-DL-триптофан, п-(3-бензофуранил)-DL-аланин, п-[3-бензо(b)тиенил]-DL-аланин и 6-нитро-L-триптофан (Munn, 1999). В публикации WO 03/087347, также опубликованной как европейский патент 1501918, представлены способы получения антигенпрезентирующих клеток для усиления или снижения толерантности Т-клеток (Munn, 2003). Соединения, проявляющие ингибирующую индоламин-2,3-диоксигеназу (ИДО) активность, также представлены в публикациях WO 2004/094409, WO 2009/073620, WO 2009/132238, WO 2011/056652 и WO 2012/142237. В частности, соединения публикации WO 2012/142237 охватывают ряд трициклических имидазоизоиндолов с потенциальной ИДО-ингибирующей активностью.
Сущность изобретения
[0013]
В свете экспериментальных данных, указывающих на роль ИДО и/или ТДО при иммуносупрессии, резистентности и/или отторжении опухоли, хронических инфекциях, ВИЧ-инфекции, СПИДе (включая такие его проявления, как кахексия, слабоумие и диарея), при аутоиммунных заболеваниях или нарушениях (таких как ревматоидный артрит) и при иммунологической толерантности и предупреждении отторжения плода в утробе, желательны терапевтические средства, направленные на подавление расщепления триптофана путем ингибирования активности ИДО1, ИДО2 и/или ТДО. Специфические или двойные ингибиторы ИДО1, ИДО2 и/или ТДО могут быть использованы для активации Т-клеток и, следовательно, для усиления активации Т-клеток, когда Т-клетки подавлены из-за беременности, злокачественного новообразования или вируса, такого как ВИЧ. Ингибирование ИДО также может быть важной терапевтической стратегией для больных с неврологическими или психоневрологическими заболеваниями или нарушениями, такими как депрессия. Соединения, композиции или способы данного изобретения помогают удовлетворить современную потребность в модуляторах ИДО1, ИДО2 и ТДО.
[0014]
В настоящем изобретении описаны новые структуры, относящиеся к имидазоизоиндолам с различными электронными и гем-связывающими свойствами, которые могут специфично ингибировать ИДО1, ИДО2 или ТДО или которые могут проявлять комбинированное ингибирование расщепления триптофана, опосредуемого любым из этих ферментов.
[0015]
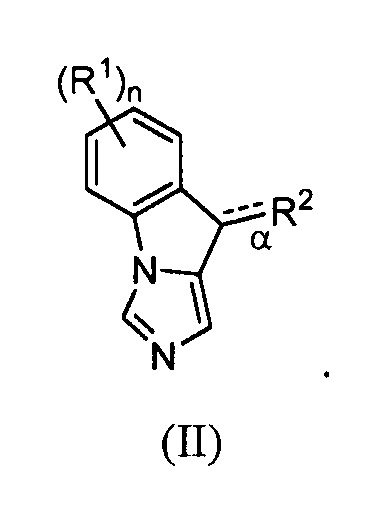
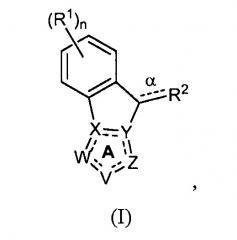
В одном аспекте изобретение включает соединения в соответствии с формулой (I) и ее таутомеры:
в которой
R1, R2 и n каждый определены в изобретении;
связь α представляет собой одинарную или двойную связь;
кольцо A представляет собой ароматическое кольцо, где
i) V и X представляют собой N, W и Z представляют собой CH и Y представляет собой C; или
ii) V, Y и Z представляют собой N, W представляет собой CH и X представляет собой C; или
iii) V, W и Y представляют собой N, X представляет собой C и Z представляет собой CH; или
iv) V и W представляют собой N или NH, X и Y представляют собой C и Z представляет собой CH.
[0016]
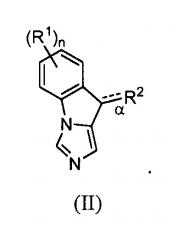
В наиболее предпочтительном варианте осуществления изобретение включает соединения формулы (I), в котором V и X представляют собой атом азота (N), W и Z представляют собой CH и Y представляет собой атом углерода (C) с образованием соединений формулы (II):
[0017]
В другом предпочтительном варианте осуществления изобретение включает соединения формулы (I), в котором V, Y и Z представляют собой атом азота (N), W представляет собой CH и X представляет собой атом углерода (C) с образованием соединений формулы (III):
[0018]
В другом варианте осуществления изобретение включает соединения формулы (I), в котором V, W и Y представляют собой атом азота (N), X представляет собой атом углерода (C) и Z представляет собой CH с образованием соединений формулы (IV):
[0019]
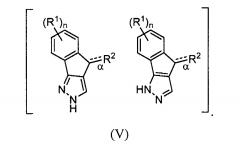
В другом варианте осуществления изобретение включает соединения формулы (I), в котором V и W представляют собой атом азота (N) или NH, соответственно или аналогично, X и Y представляют собой атом углерода (C) и Z представляет собой CH с образованием таутомерных соединений формулы (V):
[0020]
В другом предпочтительном варианте осуществления изобретение включает соединения формул II, III, IV и V, где связь альфа (α) представляет собой одинарную связь.
[0021]
В другом предпочтительном варианте осуществления изобретение включает соединения формул II, III, IV и V, где связь альфа (α) представляет собой двойную связь.
[0022]
В другом аспекте предложены фармацевтические композиции, содержащие фармацевтически приемлемый эксципиент, разбавитель или носитель и соединение в соответствии с формулами (I), (II), (III), (IV) или (V).
[0023]
В другом аспекте предложены способы (а) модуляции активности ИДО1, ИДО2 или ТДО, включающие введение ИДО1, ИДО2 или ТДО в контакт с эффективным для модуляции количеством соединения в соответствии с формулой (I) или с фармацевтической композицией, содержащей соединение в соответствии с формулой (I); (b) лечения опосредуемой ИДО1, ИДО2 или ТДО иммуносупрессии у субъекта, нуждающегося в лечении, включающие введение эффективного ингибирующего количества соединения в соответствии с формулой (I) или фармацевтической композиции, содержащей соединение в соответствии с формулой (I); (с) лечения медицинского состояния, которое имеет положительный результат от ингибирования расщепления триптофана, опосредуемого ИДО1, ИДО2, или ТДО, включающие введение эффективного количества соединения в соответствии с формулой (I) или фармацевтической композиции, содержащей соединение в соответствии с формулой (I); (d) повышения эффективности противораковой терапии, включающие введение противоракового средства и соединения в соответствии с формулой (I) или фармацевтической композиции, содержащей соединение в соответствии с формулой (I); (е) лечения опухолеспецифической иммуносупрессии, связанной с раком, включающие введение эффективного количества соединения в соответствии с формулой (I) или фармацевтической композиции, содержащей соединение в соответствии с формулой (I); и (f) лечения иммуносупрессии, связанной с инфекционным заболеванием, например, с инфекцией ВИЧ-1, включающие введение эффективного количества соединения в соответствии с формулой (I) или фармацевтической композиции, содержащей соединение в соответствии с формулой (I).
Краткое описание чертежей
[0024]
Фигура 1 описывает общую схему синтеза соединений формулы I, когда V и X представляют собой N, W и Z представляют собой CH, Y представляет собой C и связь α представляет собой одинарную связь.
[0025]
Фигура 2 описывает общую схему синтеза соединений формулы I, когда V, Y и Z представляют собой N, X представляет собой C, W представляет собой CH и связь α представляет собой одинарную связь.
[0026]
Фигура 3 описывает общую схему синтеза соединений формулы I, когда V, W и Y представляют собой атом азота (N), X представляет собой атом углерода (C), Z представляет собой CH и связь α представляет собой одинарную связь.
[0027]
Фигура 4 описывает общую схему синтеза соединений формулы I, когда V и W представляют собой N или NH, X и Y представляют собой C, Z представляет собой CH и связь α представляет собой одинарную связь.
Подробное описание изобретения
[0028]
В одном аспекте изобретение предлагает соединения формулы (I):
ее таутомеры или фармацевтически приемлемые соли соединений, в которых
n принимает значения 0, 1, 2, 3 или 4;
связь α представляет собой одинарную или двойную связь;
кольцо A представляет собой ароматическое кольцо, где
i) V и X представляют собой N, W и Z представляют собой CH и Y представляет собой C; или
ii) V, Y и Z представляют собой N, W представляет собой CH и X представляет собой C; или
iii) V, W и Y представляют собой N, X представляет собой C и Z представляет собой CH; или
iv) V и W представляют собой N или NH, X и Y представляет собой C и Z представляет собой CH;
каждый R1 независимо представляет собой атом галогена, циано-, нитро-группу, C1-4-алкил, C1-4-галогеналкил, -OR, -N(R)2, -SR, ‾C(O)OR, -C(O)N(R)2, -C(O)R, -S(O)R, -S(O)OR, -S(O)N(R)2, -S(O)2R, -S(O)2OR, ‾S(O)2N(R)2, -OC(O)R, -OC(O)OR, -OC(O)N(R)2, -N(R)C(O)R, -N(R)C(O)OR или ‾N(R)C(O)N(R)2;
R2 представляет собой -C1-4-алкил-RA или -C2-4-алкенил-R3, когда связь α представляет собой одинарную связь; и
R2 представляет собой =C(H)RA, когда связь α представляет собой двойную связь;
где
RA представляет собой -CN, -C(O)R3, -C(O)OR3, -C(O)N(R3)(RC), -C(ORB)(R3)(RC), ‾C(NHRB)(R3)(RC) или -C(=N-ORC)R3,
где
RB представляет собой атом водорода, C1-6-алкил, C1-6-галоген-алкил, -C1-6-алкил-RB1, -C(O)R3 или -S(O)2R3, -C(O)(CH2)1-4-COOR, -C(O)CH(NH2)(RD), -S(O)2OR3, -S(O)2N(R3)2, -CH2-OP(O)2(OR)2 или -P(O)(OR3)2,
где
RB1 представляет собой циано-, нитро-группу, C1-6-алкил, C1-6-галогеналкил, -OR, -N(R)2, -SR, ‾C(O)OR, -C(O)N(R)2, -C(O)R, -S(O)R, -S(O)OR, -S(O)N(R)2, ‾S(O)2R, -S(O)2OR, -S(O)2N(R)2, -OC(O)R, -OC(O)OR, ‾OC(O)N(R)2, -N(R)C(O)R, -N(R)C(O)OR или -N(R)C(O)N(R)2;
RD представляет собой атом водорода, метил, -CH(CH3)2, -CH2CH(CH3)2, ‾CH(CH3)(CH2CH3), бензил, 4-гидроксибензил, -CH2(3-индолил), ‾CH2SH, -CH2CH2SCH3, -CH2OH, -CH(CH3)OH, -(CH2)4-NH2, ‾(CH2)3-N(H)C(=NH)NH2, -CH2(4-имидазолил), -CH2COOH, ‾CH2CH2COOH, -CH2CONH2, -CH2CH2CONH2;
каждый R3 независимо представляет собой атом водорода, C1-6-алкил, C1-6-галогеналкил, арил, гетероарил, C3-8-циклоалкил, C3-8-циклоалкенил, 3-10-членный гетероциклил, арил-C1-6-алкил-, гетероарил-C1-6-алкил-, C3-8-циклоалкил-C1-6-алкил-, C3-8-цикло-алкенил-C1-6-алкил- или (3-10-членный гетероциклил)-C1-6-алкил-,
где
алкил, C3-8-циклоалкил, C3-8-циклоалкенил, 3-10-членный гетероциклил, C3-8-циклоалкил-C1-6-алкил-, C3-8-циклоалкенил-C1-6-алкил- и (3-10-членный гетероциклил)-C1-6-алкил- каждый необязательно и независимо замещен одной группой =R32 и каждый необязательно и независимо замещен одной, двумя, тремя или четырьмя группами R31;
арильная, гетероарильная, арил-C1-6-алкильная и гетероарил-C1-6-алкильная группы каждая необязательно замещена одной, двумя, тремя или четырьмя группами R31;
где
каждый R31 независимо представляет собой атом галогена, циано-, нитро-группу, C1-6-алкил, -C1-6-алкил-R33, C1-6-галоген-алкил, -OR, -N(R)2, -SR, -C(O)OR, -C(O)N(R)2, ‾C(O)R, -S(O)R, -S(O)OR, -S(O)N(R)2, -S(O)2R, -S(O)2OR, ‾S(O)2N(R)2, -OC(O)R, -OC(O)OR, -OC(O)N(R)2, -N(R)C(O)R, ‾N(R)C(O)OR, -N(R)C(O)N(R)2,
где
R33 представляет собой циано-группу, -OR, -N(R)2, -SR, -C(O)OR, -C(O)N(R)2, -C(O)R, ‾S(O)R, -S(O)OR, -S(O)N(R)2, -S(O)2R, -S(O)2OR, ‾S(O)2N(R)2, -OC(O)R, -OC(O)OR, -OC(O)N(R)2, ‾N(R)C(O)R, -N(R)C(O)OR или -N(R)C(O)N(R)2;
R32 представляет собой =O, =S, =N(R), =N(OR), =C(R34)2, =(спиро-C3-8-циклоалкил) или =(спиро-(3-10-членный гетероциклил)),
где
каждый R34 независимо представляет собой атом водорода, атом галогена, C1-6-алкил, C1-6-галогеналкил, C3-8-циклоалкил или 3-10-членный гетероциклил;
или оба R34 вместе с атомом, к которому они оба прикреплены, образуют моноциклический C3-8-циклоалкил или моноциклический 3-8-членный гетероциклил;
RC представляет собой атом водорода или C1-6-алкил;
и
каждый R независимо представляет собой атом водорода или R10,
где
R10 представляет собой C1-6-алкил, C1-6-галогеналкил, арил, гетероарил, C3-8-циклоалкил, C3-8-циклоалкенил, 3-10-членный гетероциклил, арил-C1-6-алкил, гетероарил-C1-6-алкил-, C3-8-цикло-алкил-C1-6-алкил-, C3-8-циклоалкенил-C1-6-алкил- или (3-10-членный гетероциклил)-C1-6-алкил-, каждый R10 необязательно замещен одной, двумя, тремя или четырьмя группами, каждая из которых независимо представляет собой атом галогена, циано-, нитро-группу, C1-6-алкил, C1-6-галогеналкил, -OR11, -N(R11)2, -SR11, -C(O)OR11, ‾C(O)N(R11)2, -C(O)R11, -S(O)R11, -S(O)OR11, -S(O)N(R11)2, -S(O)2R11, -S(O)2OR11, -S(O)2N(R11)2, -OC(O)R11, -OC(O)OR11, -OC(O)N(R11)2, -N(R11)C(O)R11, ‾N(R11)C(O)OR11, -N(R11)C(O)N(R11)2, где каждый R11 независимо представляет собой атом водорода или C1-6-алкил.
[0029]
Изобретение также включает разновидности формулы (I), в которых заместители выбраны из любых возможных комбинаций одной или нескольких структурных формул (I), n, R1, R2, R3, RA, RB и RC, которые определены в изобретении, включая, но без ограничения, следующие соединения:
[0030]
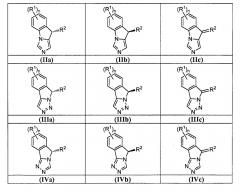
Структурные формула (I) представляет собой одну из формул (IIa)-(Vc):
[0031]
n и R1 выбирают из одной из приведенных ниже групп (1а)-(1u):
(1а) n принимает значения 1, 2, 3 или 4 и каждый R1 имеет значения, определенные для формулы (I).
(1b) n принимает значения 1, 2 или 3 и каждый R1 имеет значения, определенные для формулы (I).
(1с) n принимает значения 0, 1 или 2 каждый R1 имеет значения, определенные для формулы (I).
(1d) n принимает значения 0, 1 или 2 и каждый R1 независимо представляет собой атом галогена, -OR, -N(R)2 или -SR.
(1е) n принимает значения 0, 1 или 2 и R1 каждый независимо представляет собой атом галогена, -OR0, -N(R0)2 или -SR0, где каждый R0 независимо представляет собой атом водорода или C1-6-алкил.
(1f) n принимает значения 0, 1 или 2 и каждый R1 независимо представляет собой атом фтора, атом хлора, гидрокси- или метокси-группу.
(1g) n принимает значения 0, 1 или 2 и каждый R1 независимо представляет собой атом галогена.
(1h) n принимает значения 0, 1 или 2 и каждый R1 независимо представляет собой атом фтора или атом хлора.
(1i) n принимает значения 0 или 1 и каждый R1 имеет значения, определенные для формулы (I).
(1j) n принимает значения 0 или 1 и R1 представляет собой атом галогена, -OR, -N(R)2 или -SR.
(1k) n принимает значения 0 или 1 и R1 представляет собой атом галогена, -OR0, -N(R0)2 или -SR0; где каждый R0 независимо представляет собой атом водорода или C1-6-алкил.
(1l) n принимает значения 0 или 1 и R1 представляет собой атом фтора, атом хлора, гидрокси- или метокси-группу.
(1m) n принимает значения 0 или 1 и R1 представляет собой атом галогена.
(1n) n принимает значение 0 или 1 и R1 представляет собой атом фтора или атом хлора.
(1o) n равно 1 и R1 имеет значения, определенные для формулы (I).
(1p) n равно 1 и R1 представляет собой атом галогена, -OR, -N(R)2 или -SR.
(1q) n равно 1 и R1 представляет собой атом галогена, -OR0, -N(R0)2 или -SR0; где каждый R0 независимо представляет собой атом водорода или C1-6-алкил.
(1r) n равно 1, и R1 представляет собой атом фтора, атом хлора, гидрокси- или метокси-группу.
(1s) n равно 1 и R1 представляет собой атом галогена.
(1t) n равно 1 и R1 представляет собой атом фтора или хлора.
(1u) n равно 0.
[0032]
R2 выбирают из одной из приведенных ниже групп (2а)-(2l):
(2a) R2 представляет собой -C1-4-алкил-RA.
(2b) R2 представляет собой -C1-2-алкил-RA.
(2с) R2 представляет собой -C(H)=C(H)R3.
(2d) R2 представляет собой -C(H)=C(H)R30, где R30 представляет собой фенил, необязательно замещенный одной, двумя, тремя или четырьмя группами R31.
(2e) R2 представляет собой -C(H)=C(H)R30, где R30 представляет собой фенил, необязательно замещенный одной или двумя группами R31.
(2f) R2 представляет собой -CH2-RA, -CH2CH2-RA, -C(H)(CH3)CH2-RA или -C(H)=C(H)R3.
(2g) R2 представляет собой -CH2-RA, -CH2CH2-RA или -C(H)(CH3)CH2-RA.
(2h) R2 представляет собой -CH2-RA, -CH2CH2-RA или -C(H)=C(H)R3
(2i) R2 представляет собой -CH2-RA.
(2j) R2 представляет собой -CH2CH2-RA.
(2k) R2 представляет собой -C(H)(CH3)CH2-RA.
(2l) R2 представляет собой -CH2-RA, -CH2CH2-RA или -C(H)=C(H)R3.
(2m) R2 представляет собой =CH-RA, =CHCH2-RA или =C(H)C(H)R3.
[0033]
RА выбирают из одной из приведенных ниже групп (3а)-(3n):
(3a) RA представляет собой -CN, -C(O)OR3 или -C(O)N(R3)(RC).
(3b) RA представляет собой -C(O)R3 или -C(ORB)(R3)(RC).
(3c) RA представляет собой -C(NHRB)(R3)(RC) или -C(=N-ORC)R3.
(3d) RA представляет собой -C(NHRB)(R3)(RC), где RB представляет собой атом водорода, C1-6-алкил или -C(O)C1-6-алкил.
(3e) RA представляет собой -C(NH2)(R3)(RC).
(3f) RA представляет собой -C(O)OR3.
(3g) RA представляет собой -C(O)N(R3)(RC).
(3h) RA представляет собой -C(O)R3.
(3i) RA представляет собой -C(ORB)(R3)(RC).
(3j) RA представляет собой -C(OH)(R3)(RC).
(3k) RA представляет собой -CH(OH)(R3).
(3l) RA представляет собой -CN, -C(O)R3, -C(O)OR3, -C(O)N(R3)(RC), -C(ORB)(R3)(RC), ‾C(NHRB)(R3)(RC) или -C(=N-ORC)R3.
(3m) RA представляет собой -C(O)R3 или -C(ORB)(R3)(RC), где RB представляет собой атом водорода и RC представляет собой атом водорода или C1-6-алкил.
(3n) RA представляет собой -C(ORB)(R3)(RC), где RB представляет собой атом водорода и RC представляет собой атом водорода или C1-6-алкил.
[0034]
RВ выбирают из одной из приведенных ниже групп (4а)-(4k):
(4а) RB представляет собой атом водорода, C1-4-алкил, C1-4-галогеналкил, -C1-4-алкил-RB1, -C(O)(CH2)1-4COORB2, ‾C(O)C(NH2)RD, -P(O3)(RB2)2, -CH2-OP(O)2(OR)2, где RD представляет собой боковую цепочку природных альфа-аминокислот, -C(O)R3 или -S(O)2R3, где RB1 представляет собой циано-, нитро-группу, C1-6-алкил, C1-6-галоген-алкил, -ORB2, -N(RB2)2, -SRB2, -C(O)ORB2, -C(O)N(RB2)2, ‾C(O)RB2, ‾S(O)RB2, -S(O)ORB2, -S(O)N(RB2)2, -S(O)2RB2, -S(O)2ORB2, ‾S(O)2N(RB2)2, ‾OC(O)RB2, -OC(O)ORB2, -OC(O)N(RB2)2, -N(RB2)C(O)RB2, ‾N(RB2)C(O)ORB2 или ‾N(RB2)C(O)N(RB2)2, где каждый RB2 независимо представляет собой атом водорода или C1-4-алкил.
(4b) RB представляет собой атом водорода, C1-4-алкил, C1-4-галогеналкил, -C1-4алкил-RB1, -C(O)RB2 или -S(O)2RB2, где RB1 представляет собой -C(O)ORB3, -C(O)N(RB3)2, -S(O)2ORB3 или -S(O)2N(R 3)2, RB2 представляет собой C1-6-алкил; и RB3 представляет собой атом водорода или C1-6-алкил.
(4c) RB представляет собой атом водорода, C1-4-алкил или C1-4-галогеналкил.
(4d) RB представляет собой атом водорода или C1-4-алкил.
(4e) RB представляет собой атом водорода.
(4f) RB представляет собой C1-4-алкил.
(4g) RB представляет собой атом водорода, -C(O)RB2, -C(O)(CH2)1-4COORB2, -C(O)C(NH2)RD, -P(O)(ORB2)2, ‾CH2-OP(O)2(OR)2, -S(O)2RB2, -C(O)N(RB2)2, -S(O)2ORB2, -S(O)2N(R 3)2, где RB2 представляет собой атом водорода или C1-4-алкил.
[0035]
RС выбирают из одной из приведенных ниже групп (5а)-(5g):
(5a) RC представляет собой атом водорода или C1-4-алкил.
(5b) RC представляет собой атом водорода или C1-2-алкил.
(5c) RC представляет собой атом водорода или метил.
(5d) RC представляет собой атом водорода.
(5e) RC представляет собой C1-6-алкил.
(5f) RC представляет собой C1-4-алкил.
(5g) RC представляет собой метил.
[0036]
R3 выбирают из одной из приведенных ниже групп (6а)-(6z):
(6a) R3 представляет собой атом водорода, C1-6-алкил, арил, гетероарил, C3-8-циклоалкил, C3-8-циклоалкенил, 3-10-членный гетероциклил или C3-8-циклоалкил-C1-6-алкил-, где C1-6-алкил, C3-8-циклоалкил, C3-8-циклоалкенил, 3-10-членный гетероциклил и C3-8-циклоалкил-C1-6-алкил-, каждый необязательно замещен одной группой =R32 и одной или двумя группами R31; и арильная и гетероарильная группы каждая необязательно замещена одной или двумя группами R31.
(6b) R3 представляет собой арил, гетероарил, C3-8-циклоалкил, C3-8-циклоалкенил, 3-10-членный гетероциклил или C3-8-циклоалкил-C1-6-алкил-, где C3-8-циклоалкил, C3-8-циклоалкенил, 3-10-членный гетероциклил и C3-8-циклоалкил-C1-6-алкил- каждый необязательно и независимо замещен одной группой =R32 и каждый необязательно и независимо замещен одной или двумя группами R31; и арильная и гетероарильная группы каждая необязательно замещена одной или двумя группами R31.
(6c) R3 представляет собой фенил, пяти- или шестичленный гетероарил, моноциклический C5-8-циклоалкил, моноциклический C5-8-циклоалкенил, пяти- или шестичленный моноциклический гетероциклил или (моноциклический C5-8-циклоалкил)-C1-6-алкил-, где C5-8-циклоалкил, C5-8-циклоалкенил, 5-6-членный гетероциклил и C5-8-циклоалкил-C1-6-алкил- каждый необязательно и независимо замещен одной группой =R32 и каждый необязательно и независимо замещен одной или двумя группами R31; и фенильная и гетероарильная группа каждая необязательно замещена одной или двумя группами R31.
(6d) R3 представляет собой фенил или пяти- или шестичленный гетероарил, каждый необязательно замещенный одной или двумя группами R31.
(6е) R3 представляет собой моноциклический C5-8-циклоалкил, моноциклический C5-8-циклоалкенил, пяти- или шестичленный моноциклический гетероциклил или (моноциклический C5-8-циклоалкил)-C1-6-алкил-, каждый необязательно замещенный одной группой =R32 и одной или двумя группами R31.
(6f) R3 представляет собой где связь а представляет собой одинарную связь или двойную связь; m принимает значения 0, 1 или 2; p принимает значения 0 или 1; и где
когда связь а представляет собой одинарную связь, то Z представляет собой -C(R36)2-, -C(=R32)-, -N(R35)- или -O-, где каждый R36 независимо представляет собой атом водорода или R31; и
R35 представляет собой атом водорода, C1-6-алкил, -C(O)R, -S(O)2R, -C(O)OR, -C(O)N(R)2, -S(O)2OR или -S(O)2N(R)2;
и
когда связь а представляет собой двойную связь, то Z представляет собой -C(R36)= или -N=.
(6g) R3 представляет собой где связь а представляет собой одинарную или двойную связь; m принимает значения 0, 1 или 2; p принимает значения 0 или 1; и где
когда связь а представляет собой одинарную связь, то Z представляет собой -C(R36)2-, -C(=R32)-, -N(R35)- или -O-, где каждый R36 независимо представляет собой атом водорода или R31; и
R35 представляет собой атом водорода, C1-6-алкил, -C(O)R, -S(O)2R, -C(O)OR, -C(O)N(R)2, -S(O)2OR или -S(O)2N(R)2;
и
когда связь а представляет собой двойную связь, то Z представляет собой -C(R36)= или -N=.
(6h) Как группа (6g), где когда связь а представляет собой одинарную связь, то Z представляет собой -C(R36)2- или ‾C(=R32)‾; и когда связь а представляет собой двойную связь, то Z представляет собой -C(R36)= или -N=.
(6i) Как группа (6g), где m равно 0; когда связь а представляет собой одинарную связь, то Z представляет собой -C(R36)2- или ‾C(=R32)-; и когда связь а представляет собой двойную связь, то Z представляет собой -C(R36)= или -N=.
(6j) Как группа (6g), где связь а представляет собой одинарную связь; и Z представляет собой -C(R36)2- или -C(=R32)-.
(6k) Как группа (6g), где связь а представляет собой одинарную связь; и Z представляет собой -C(R36)2-.
(6l) Как группа (6g), где связь а представляет собой одинарную связь; и Z представляет собой -C(=R32)-.
(6m) Как группа (6g), где m равно 0; связь а представляет собой одинарную связь; и Z представляет собой -C(R36)2- или -C(=R32)-.
(6n) Как группа (6g), где m равно 0; связь а представляет собой одинарную связь; и Z представляет собой -C(R36)2-.
(6o) Как группа (6g), где m равно 0; связь а представляет собой одинарную связь; и Z представляет собой -C(=R32)-.
(6p) Как группа (6g), где связь а представляет собой одинарную связь; и Z представляет собой -C(R36)2- или -C(=R32)-, где каждый R36 независимо представляет собой атом водорода, атом галогена, C1-6-алкил, -C1-6-алкил-OH, C1-6-галогеналкил или -OH,
где
R32 представляет собой =O, =C(R34)2, =(спиро-C3-8-циклоалкил) или =(спиро-(3-8-членный гетероциклил)), где каждый R34 независимо представляет собой атом водорода, атом галогена, C1-6-алкил, C1-6-галогеналкил, C3-8-циклоалкил или 3-8-членный гетероциклил.
(6q) Как группа (6g), где m равно 0; связь а представляет собой одинарную связь; и Z представляет собой -C(R36)2- или ‾C(=R32)-, где каждый R36 независимо представляет собой атом водорода, атом галогена, C1-6-алкил, ‾C1-6-алкил-OH, C1-6-галоген-алкил или -OH,
где
R32 =O, =C(R34)2, =(спиро-C3-8-циклоалкил) или =(спиро-(3-8-членный гетероциклил)), каждый где R34 независимо пр