Способ, пробирка и устройство для приготовления композиции для заживления ран
Иллюстрации
Показать всеГруппа изобреетний относится к химико-фармацевтической промышленности и представляет собой способ приготовления композиции, содержащей обогащенную тромбоцитами плазму и гиалуроновую кислоту, причем способ включает стадии: забора цельной крови в устройство, содержащее гиалуроновую кислоту и антикоагулянт; центрифугирования указанного устройства и сбора супернатанта, содержащего указанную гиалуроновую кислоту и обогащенную тромбоцитами плазму. Данное устройство для забора крови имеет входное отверстие для ввода цельной крови; содержит вакуум, предназначенный для аспирации образца цельной крови; имеет предназначенный для использования вакуум, составляющий от 8 до 10 мл; и является стерильным. Данное устройство включено в изделие и набор для заживления ран и тканей. Изобретения включают способы заживления ран и тканей посредством композиций, полученных способом, описанным ранее. Группа изобретений обеспечивает немедленное использование полученных аутологичных клеток крови с одновременным сохранением их целостности для заживления ран и тканей. К тому же клеточные препараты в соответствии с данными изобретениями обладают лучшей жизнеспособностью и стабильностью. 8 н. и 13 з.п. ф-лы, 16 ил., 14 пр.
Реферат
Область техники
Настоящее изобретение относится к области регенерации биологических тканей. Оно касается, в частности, новых способов, пробирок и устройств для получения тромбина, тромбоцитарного концентрата и средств для заживления ран, а также композиций и их применения.
Уровень техники
Важность биологических аутологичных материалов в процессе заживления ран хорошо изучена и описана. В частности, известно, что два биологических аутологичных материала напрямую вовлечены в процесс образования структуры кровяных сгустков, создающих гемостатический барьер, роль которого заключается в обеспечении гемостаза и запечатывании раны: (1) фибрин, получаемый в процессе разделения фибриногена на две цепочки под действием тромбина, и (2) активированные мембраны тромбоцитов. Процесс заживления раны в целом представляет собой продолжение фазы коагуляции, воспалительный процесс и процесс регенерации. Фаза коагуляции (свертывание крови или образование сгустка) является сложным процессом, в рамках которого фибриновый сгусток закрывает поврежденную стенку кровеносного сосуда для остановки кровотечения, а восстановление поврежденного сосуда инициируется с помощью высвобождения цитокинов и факторов роста из альфа-гранул тромбоцитов в больших количествах. Образование кровяных сгустков (формируемых в физиологических условиях фибрином, тромбоцитами и красными кровяными клетками среди прочих компонентов крови) является естественным симптомом, возникающим в результате травмы ткани, и его роль в процессе заживления раны, а также сращивании переломов костей, хорошо известна.
Коагуляция крови является результатом комплексного взаимодействия нескольких белковых факторов свертывания в рамках коагуляционного каскада. В целом, повреждение сосудистого эндотелия обнажает эндотелиальные структуры, которые привлекают тромбоциты и индуцируют их для обратной агрегации. Белок тромбин, формируемый в течение активации пути коагуляции, вырабатывает связанные между собой нерастворимые фибриллы белка фибрина и вызывает обратную агрегацию тромбоцитов. Образующийся в результате этого тромбоцитарно-фибриновый сгусток является эффективным барьером, предотвращающим потерю крови из сосудистой системы, а также служит каркасом для последующего восстановления выстилания кровеносного сосуда.
Воспалительный процесс, который следует за образованием кровяного сгустка, стимулируется многочисленными вазоактивными медиаторами и хемотаксическими факторами (специфическими сигналами в форме белков), вырабатываемыми белыми кровяными клетками и тромбоцитами. Данные сигналы привлекают макрофаги, которые «очищают» место повреждения от бактерий и инородных частиц, а также красных кровяных клеток до миграции новых клеток. Фаза регенерации ткани затрагивает хемоаттракцию и митоз недифференцированных клеток в каркасе (или матриксе роста), формируемом кровяным сгустком. Новые клетки, которые размножаются под воздействием стимуляции тромбоцитарных факторов роста, должны заместить поврежденные или уничтоженные клетки, задержанные макрофагами. Факторы роста и многочисленные белки плазмы, также называемые сигнальными молекулами, которые способствуют миграции клеток и их делению в кровяных сгустках, играют важнейшую роль в процессе заживления ран.
Биоадгезивные запечатывающие материалы и фибриновые клеи представляют собой относительно новое техническое достижение, которое воспроизводит биологический процесс заключительной стадии коагуляции крови. Клинические отчеты описывают использование фибринового клея в таких областях хирургии, как сердечно-сосудистая, торакальная, трансплантационная, хирургия головы и горла, оральная, желудочно-кишечная, ортопедическая, неврологическая и пластическая хирургия. Во время проведения хирургии два основных компонента, включающих фибриновый клей, фибриноген и тромбин, смешиваются для образования сгустка. Сгусток прикрепляется к необходимым тканям, кости или нерву в течение нескольких секунд, но затем медленно реабсорбируется организмом в течение приблизительно 10 дней в рамках фибринолиза. Важными свойствами фибринового клея является его способность: (1) достигать гемостаза при срастаниях сосудов, в частности, в труднодоступных для наложения швов зонах, или в тех зонах, в которых расположение швов представляет чрезмерный риск; (2) контролировать кровотечения из шприцевых проколов или кровотечения в результате разрыва артерий, которые невозможно остановить исключительно с помощью наложения швов; и (3) достигать гемостаза у пациентов, проходящих курс лечения гепарином, или страдающих коагулопатией. См. Borst, Н.G., et al., J. Thorac. Cardiovasc. Surg., 84:548-553 (1982); Walterbusch, G. J, et al., Thorac Cardiovasc. Surg., 30:234-235 (1982) и Wolner, F. J, et al., Thorac. Cardiovasc. Surg., 30:236-237(1982).
Теоретически возможно усилить эффекты данных первоначальных фаз в каскадном процессе заживления с помощью отделения красных кровяных клеток и увеличения концентрации факторов роста.
Усиление свертывания крови может быть определено как образование «обогащенного сгустка (ЕС)». ЕС получают путем использования тромбоцитарных концентратов; ЕС описаны в Platelets and Megacaryocytes 2004, ч. 1 и 2 как "Структуры и сигналы", Ed. Gibbins and Mahaut-Smith, Humana Press, New Jersey. Обогащенная тромбоцитами плазма (PRP) может быть определена как аутологичный концентрат тромбоцитов в малом объеме плазмы; она была создана как аутологичный биоматериал и доказала свою применимость при заживлении ран и регенерации тканей (Marx et al., 2004, J. Oral Maxillofac. Surg., 62, 489-496). PRP состоит не только из тромбоцитарного концентрата, но также содержит факторы роста (такие как фактор роста, полученный из тромбоцитов): PDGF, сосудистый эндотелиальный фактор роста: VEGF, трансформирующий фактор роста: TGF и эпидермальный фактор роста: EGF и другие), которые активно вырабатываются тромбоцитами и известны своей фундаментальной ролью в инициации процесса заживления ран.
Например, известно, что PDGF инициирует соединительное заживление тканей, включая регенерацию и восстановление костей. PDGF также увеличивает митогенез (заживляющие клетки), ангиогенез (митоз эндотелия с образованием функционирующих капилляров) и активацию макрофагов. Известно, что VEGF, высвобождаемый лейкоцитами, обладает заметными ангиогенными, митогенными и улучающими проницаемость кровеносных сосудов свойствами по отношению к эндотелиальным клеткам. TGF-[beta] способствует клеточному митозу и дифференциации для сращивания тканей и костей, воздействует на мезенхимные стволовые клетки, остеобластные клетки-предшественники и фибробласты, а также ингибирует образование остеокластов. Известно, что EGF индуцирует эпителиальное развитие и способствует ангиогенезу. Тромбоцитарные концентраты в основном используют в дентальной импланталогии и костной хирургии, в частности в США. Были разработаны разнообразные техники получения PRP с помощью процесса центрифугирования. Тем не менее в связи с чувствительностью тромбоцитарных клеток и вариабельностью эффективности методов отделения тромбоцитов от красных кровяных клеток, существуют заметные различия среди способов приготовления тромбоцитарных концентратов. Автоматизированные установки Biomet PCCS & GPS (Marx et al., 2004, выше) обладают недостатком, заключающимся в сложности способа и чрезмерной стоимости обработки значительного по объему образца крови. В данных системах также присутствует значительная потеря ценной биологической ткани, получаемой от пациентов; таким образом, существует потребность в разработке надежного метода сбора клеток плазмы с высоким уровнем выхода, простотой использования и экономической эффективностью.
Кроме того, получение тромбоцитарных концентратов все еще требует использования относительно сложных наборов и дорогостоящего специализированного оборудования и столь же дорогостоящих трудозатрат специализированного персонала. Данный недостаток делает известные в настоящее время способы приготовления PRP неподходящими для использования на месте оказания помощи.
Далее, получение клеток в аспекте клеточной и тканевой регенерации для использования в целях трансплантации, послеоперационного восстановления или для эстетических целей сталкивается с проблемой долгосрочной консервации клеток и тканей. Криоконсервация тканей или клеток, как правило, используется для долгосрочного поддержания жизнеспособности тканей или клеток, особенно тромбоцитов, однако данная методика связана с серьезными недостатками и проблемами, такими как образование кристаллов, осмотические затруднения, агрегация, способность ингибирования синтеза белков, нагрузка на белковые экспрессии в ответ на температурный стресс. Таким образом, известно, что криоконсервация тканей или клеток оказывает влияние на жизнеспособность и стабильность клеток (Agence de sanitaire, 2003; Arnaud et al., 1999, Cryobiology, 38, 192-199; Tablin et al., 2001, Cryobiology, 43(2), 114-23). Некоторые из побочных эффектов криоконсервации могут быть ограничены с помощью антифризных агентов, таких как DMSO или глицерин или другие криоконсерванты (US 5, 5891, 617, Oh et al., Cornea, 26, 840-846), однако концентрация данных агентов должна быть адаптирована для ограничения их токсичности и побочных эффектов. Таким образом, существует потребность в новом или альтернативном способе получения клеток или тканей, подходящих для немедленного использования с одновременным сохранением их целостности, в частности в рамках способности выделения факторов роста и жизнеспособности.
Сущность изобретения
Изобретение относится к области регенерации биологических тканей. Оно касается, в частности, новых способов, пробирок и устройств для приготовления тромбина, тромбоцитарного концентрата и средства для заживления ран, а также композиций и их применения. Изобретение также относится к новым композициям клеток, новым композициям обогащенной тромбоцитами плазмы (PRP), способам приготовления новых композиций клеток или композициям PRP, вариантам использования данных композиций клеток или PRP, по выбору смешанным с клеточным экстрактом, таким как аутологичный экстракт кератиноцитов, клеток костного мозга, фибробластов, надкостницы или клеток роговицы, меланоцитов и клеток Лангерганса, жировых клеток, жировой ткани, мышечных клеток, таких как миобласты и сателлитные клетки, остеобластов, хондроцитов, клеток пуповины, мезенхимных стволовых клеток (MSC), преадипоцитов, эндотелиальных клеток-предшественников, шванновских клеток или клеток ахиллового сухожилия.
Кроме того, изобретение предусматривает способ приготовления композиции полностью аутологичного и готового для немедленного приема средства для заживления ран или средства для заживления тканей. Все компоненты крови, предназначенные для использования в композиции аутологичного средства для заживления ран или средства для заживления тканей, получают от того же пациента, по отношению к которому будут применяться композиции аутологичного средства для заживления ран или средства для заживления тканей (один и тот же пациент).
Кроме того, изобретение предусматривает способ приготовления сыворотки с тромбином, состоящий из следующих стадий:
a) Забор цельной крови в пробирку, содержащую тиксотропный гель,
b) Центрифугирование пробирки до высвобождения сыворотки с тромбином и
c) Сбор сыворотки с тромбином.
Другая особенность изобретения заключается в том, что изобретение предусматривает способ приготовления композиции средства для заживления ран или композиции средства для заживления тканей, состоящий из следующих стадий:
a) Забор цельной крови предпочтительно в пробирку, содержащую гиалуроновую кислоту, тиксотропный гель и/или антикоагулянт, предпочтительно цитрат натрия,
b) Центрифугирование пробирки, предпочтительно до миграции красных кровяных клеток под тиксотропный гель и, предпочтительно, до миграции гиалуроновой кислоты выше обогащенной плазмы,
c) Необязательное смешивание гиалуроновой кислоты и обогащенной плазмы, предпочтительно путем переворачивания пробирки,
d) Сбор супернатанта, содержащего гиалуроновую кислоту и обогащенную плазму.
Другая особенность заключается в том, что изобретение предусматривает пробирку для забора и сепарирования жидкого образца, состоящую из:
i) двух отдельных частей, отличающихся по размеру и диаметру,
ii) фильтра, разделяющего две части, и
iii) необязательно тиксотропного геля и антикоагулянта.
В предпочтительном варианте изобретения пробирка характеризуется признаками, проиллюстрированными на Фиг. 1-14.
Другая особенность заключается в том, что изобретение относится к системе контейнеров для крови или устройству с пробирками для забора крови, состоящему из нескольких контейнеров или пробирок, подходящих для забора, хранения, использования и доставки компонентов крови.
Предпочтительной особенностью изобретения является система контейнеров для крови или устройство с пробирками для забора крови в соответствии с Фиг. 15.
Другая особенность заключается в том, что изобретение предусматривает систему контейнеров для крови или устройство с пробирками для забора крови, состоящее из единственной входной трубки, соединенной с разветвителем и трубок разветвителя, соединенных, по меньшей мере, с двумя контейнерами или пробирками, причем каждая трубка разветвителя соединена с единственным контейнером или пробиркой.
Пробирки для забора крови предпочтительно вакуумируют, запечатывают и заполняют тиксотропным гелем и антикоагуляном.
Краткое описание чертежей
Чертежи, которые представлены здесь, и которые представляют собой часть описания, иллюстрируют предпочтительные варианты данного изобретения и, наряду с описанием, служат для раскрытия принципов изобретения.
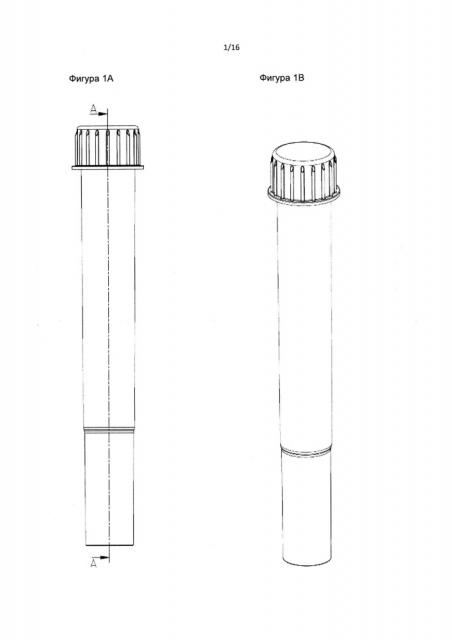
Фиг. 1А и 1В являются схематическими изображениями пробирки в соответствии с данным изобретением.
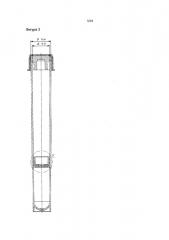
Фиг. 2 и 3 являются схематическими изображениями внутренней части пробирки в соответствии с данным изобретением.
Фиг. 4 является схематическим изображением внутренней части фильтра пробирки в соответствии с данным изобретением. Фильтр состоит из внутреннего слоя с воронками и внешнего слоя с трапециевидными конструкциями.
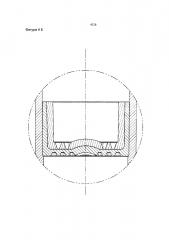
Фиг. 5A является схематическим изображением внутренней части пробирки в соответствие с данным изобретением.
Фиг. 5B является схематическим изображением колпачка и стыка пробирки. Фиг. 6 является схематическим изображением колпачка.
Фиг. 7А и 7В являются двумя детальными изображениями фильтра и пробирки в соответствии с данным изобретением.
Фиг. 8 является нижележащим изображением фильтра пробирки в соответствии с данным изобретением. Фиг. 8 также изображает четыре симметричных набора, состоящих из 3 диапазонов отверстий внешнего слоя или нижнего слоя в соответствии с данным изобретением.
Фиг. 9 изображает внешний вид фильтра пробирки в соответствии с данным изобретением. Фиг. 9 также изображает четыре симметричных набора, состоящих из 2 диапазонов отверстий внешнего слоя или верхнего слоя в соответствии с данным изобретением.
Фиг. 10 и 11 являются детальными изображениями фильтра пробирки в соответствии с данным изобретением.
Фиг. 12 является детальным изображением центральной части фильтра пробирки в соответствии с данным изобретением.
Фиг. 13 является детальным изображением внутренней части фильтра пробирки в соответствие с данным изобретением. Фильтр состоит из внутреннего слоя с воронками и внешнего слоя с трапециевидными конструкциями. Каждая воронка и трапеция встраивается в фильтр поочередно (первая трапеция, затем первая воронка, затем вторая трапеция, затем вторая воронка и, наконец, третья трапеция). Фиг. 14 является детальным изображением фильтра, включающего воронки и трапеции в пробирке в соответствии с данным изобретением.
Фиг. 15 является изображением системы контейнеров для крови или устройства с пробирками для забора крови в соответствии с данным изобретением. Фиг. 16 является схематическим изображением способа приготовления средства для заживления ран или тканей, включающего PRP и гиалуроновую кислоту.
Подробное описание изобретения
Нижеследующие параграфы содержат определения терминов в соответствии с данным изобретением и предназначены для единообразного применения по всему объему описания и формулы изобретения, за исключением случаев приведения более широких определений.
Термин «тиксотропный» означает гель, который становится более жидким в результате встряхивания или давления, т.е. гель, вязкость которого снижается в результате встряхивания или давления. Термин «вязкость» относится к тем характеристикам указанного материала(ов), которые определяют степень гелеобразования, такие как, например, жесткость или твердость материала, степень, в рамках которой материал сопротивляется жидкотекучести. В соответствии с данным изобретением, тиксотропный гель содержит полиэфирный гель или их смеси на его основе, который нерастворим в воде и химически инертен по отношению к компонентам крови, которые могут быть использованы в соответствии с данным изобретением. Типичные тиксотропные гели используются для отбора кровяных клеток в диагностических и протеомных целях. Тиксотропный гель также называется здесь гелем для отделения клеток. В настоящем изобретении могут быть использованы другие гели. Термин «место оказания помощи» означает все услуги, предоставляемые пациентам при постельном режиме.
Термин «инструменты для флеботомии» или «инструменты для осуществления венепункции» означает инструменты, которые позволяют осуществлять прокол вены иглой в целях забора крови.
Альтернативные термины «средство для заживления ран» или «запечатывающий раны материал» или «средство для заживления тканей» или «запечатывающий ткани материал» или «композиция для заживления ран» или «композиция для заживления тканей» означают «биоадгезивный запечатывающий материал» или «фибриновый клей».
Термин «средство для заживления ран» или «запечатывающий раны материал» или «средство для заживления тканей» или «запечатывающий ткани материал» или «композиция для заживления ран» или «композиция для заживления тканей» или «биоадгезивный запечатывающий материал» или «фибриновый клей» означает агент или композицию, которая способствует и/или увеличивает скорость и/или качество заживления раны. Средства для заживления ран или запечатывающие материалы способствуют регенерации ткани. Термин «рана» означает любую поврежденную ткань, например поврежденную в результате травмы или хирургии. У млекопитающих раны включают, например, пролежни, язвы, рваные раны и ожоги, места имплантации (места взятия и пересадки имплантатов), фистулы, повреждение периодонтальной ткани, хронические диабетические язвы, последствия травм или любого хирургического вмешательства. В общем случае, данный термин также используется для обозначения повреждений кожи, при которых поверхность кожи обладает некоторыми негативными признаками без непосредственного повреждения ее поверхности как, например, возрастные повреждения ткани (например, морщины) и рубцы как, например, акне (в частности, после дермабразии) или рубцы от краснухи. Термин «PRP» означает богатую тромбоцитами плазму, предпочтительно млекопитающего или человека, более предпочтительно аутологичную, приготовленную в рамках способа данного изобретения в целях осаждения и удаления эритроцитов и концентрирования лейкоцитов, тромбоцитов и адгезивных белков в плазме по сравнению с нативной цельной кровью. Термин «аутологичный» или «аутогенный» или «аутогенезный» означает in vivo способ, в рамках которого используется кровь, ткань и/или клетки одного пациента и при котором кровь, ткань и/или клетки забираются у этого донора и предназначаются для использования у того же донора. Противоположно, «аллогенные» способы предусматривают использование крови, ткани и/или клеток, забранных у одной или более третьих сторон для использования у донора («гомологично» или «гетерологично»). Аутологичный продукт позволяет избежать некоторых типичных проблем, связанных с использованием биологических материалов, полученных от третьих сторон, таких как, например, скрининг в целях подтверждения того, что донор являлся биологически и иммунологически совместимым с пациентом и что возможно потенциальное заражение гепатитом, ВИЧ, прионом, болезнью Крейтцфельдта-Якоба и им подобными заболеваниями. Термин «активатор коагуляции» означает агент, например энзим, который способен инициировать и активировать коагуляцию плазмы и агрегацию тромбоцитов. Активатор коагуляции представляет собой активатор тромбина и/или активатор фибриногена и/или тромбин и/или аутологичный тромбин и/или аутологичную сыворотку с тромбином и/или хлорид кальция и/или глюконат кальция. Коагуляция может быть комбинированной в целях изменения плотности композиций.
Термин «активатор тромбина» означает агент, который способен активировать тромбин и инициировать коагуляцию. Типичными активаторами тромбина являются определенные кофакторы, такие как натрий или кальций. В данном изобретении активация тромбина предпочтительно происходит в присутствии ионов кальция. Ионы кальция, как правило, добавляют в тромбоцитарный концентрат в виде солевого раствора для достижения итоговой концентрации, как правило, около 0.1 мг/мл тромбоцитарного концентрата. Подходящие соли кальция включают, без ограничения, СаСО3, CaSO4 или CaCl2. Предпочтительной кальциевой солью для использования в данном изобретении является глюконат кальция (CaGL). CaGL доступен в виде инъекции кальциевого геля, USP 10% (Regen Lab, Switzerland). Термин «активатор фибриногена» означает агент, который способен активировать превращение фибриногена в фибрин и инициировать образование сгустка. Типичными активаторами фибриногена являются тромбин или батроксобин. Термин «тромбин» может включать кальцинированный тромбин, в частности от около 100 до около 10 единиц тромбина на 1 мл 10% водного раствора глюконата кальция; он может включать кальцинированный бычий тромбин, аллогенный тромбин или рекомбинантный тромбин человека, предпочтительно аутологичный тромбин. Активатор фибриногена может быть обогащенной тромбином композицией, такой как композиции тромбина, описанные в US 6,472.162, или аутологичной сывороткой с тромбином в соответствии с данным изобретением. Термин «терапевтически эффективное количество» означает количество или количества компонентов или их комбинации, необходимые для стимулирования заживления ран, такого как, например, уменьшения размера или площади раны, увеличения объема гранулирующей ткани или другого биологического материала, облегчающего выстилание коллагена, развитие кровеносных сосудов, пролиферацию фибробластов или общее заживление. Предполагается, что все варианты изобретения, описанные здесь, включают терапевтически эффективные количество(а) компонентов или их комбинаций. Термин «фармацевтически приемлемый носитель» предназначено для определения фармацевтически приемлемого дополнительного ингредиента, такого как стабилизаторы, антимикробные агенты, буферы, вспомогательные лекарственные вещества, анестетики, кортикостероиды и им подобные. Термин «косметически приемлемый носитель» предназначено для определения косметически приемлемого дополнительного ингредиента, такого как стабилизаторы, буферы, красители, отдушки, вспомогательные лекарственные вещества и им подобные.
Термин «циклический сополимер олефина» (СОС) или «циклический полимер олефина» (СОР) означает аморфный полимер, сополимер этилена, СОС, СОР, циклический сополимер олефина, циклический полимер олефина, сополимер типа этилен/норборнен. В СОР используется единственный тип мономера, в то время как в СОС используются различные типы мономеров. Изобретение включает циклические сополимеры олефина, основанные на различных типах циклических мономеров и методах полимеризации. Циклические сополимеры олефина или полимеры настоящего изобретения могут быть получены с помощью кольцевой кополимеризации циклических мономеров, таких как 8,9,10-тринорборн-2-ен (норборнен) или 1,2,3,4,4а,5,8,8а-октагидро-1,4:5,8-диметанофталин с этеном, препарат TOPAS компании Ticona, APEL™™ компании Mitsui Chemicals, или с помощью раскрывающей кольцо обменной полимеризации различных циклических мономеров с последующей гидрогенизацией (например, с помощью Japan Synthetic Rubber's ARTON, Zeon Chemical's Zeonex и Zeonor).
Термин «гиалуроновая кислота» (также называемая гиалуронаном или гиалуронатом) означает анионный несульфированный гликозаминогликан, широко встречающийся во всех соединительных, эпителиальных и невральных тканях. Уникальное свойство гликозаминогликанов заключается в их способности, являясь несульфированными, образовывать плазматическую мембрану вместо аппарата Гольджи и достигать очень большого размера и молекулярного веса, зачастую достигающего миллиона. Один из основных компонентов экстраклеточного матрикса, гиалуронан оказывает заметное влияние на пролиферацию и миграцию клеток.
Термин «хитозан» означает линейный полисахарид, состоящий из произвольно распределенного β-(1-4)-связанного D-глюкозамина (деацетилированная единица) и N-ацетил-D-глюкозамина (ацетилированная единица). Для коммерческих целей хитозан получают путем деацетилирования хитина, который является структурным элементом экзоскелета ракообразных (крабов, креветок и так далее) и клеточных стенок грибов. Степень деацетилирования (%DD) может быть определена с помощью ЯМР спектроскопии, %DD в коммерчески доступных хитозанах находится в диапазоне 60-100%. В среднем, молекулярный вес коммерчески производимого хитозана находится в границах между 3800 и 20000 а. е. м. Типичным способом синтеза хитозана является деацетилирование хитина с помощью избытка гидроксида натрия в избытке в качестве реагента и воды в качестве растворителя. Данный путь течения реакции при завершении (полном деацетилировании) дает выход до 98% продукта. Аминогруппа хитозана имеет значение pKa ~6.5, что приводит к протонированию в кислых и нейтральных растворах с плотностью заряда, зависящей от рН и значения %DA. Это делает хитозан растворимым в воде и биоадгезивным, что обеспечивает немедленное прикрепление к отрицательно заряженным поверхностям, таким как слизистые оболочки. Хитозан улучшает транспорт полярных лекарственных веществ по эпителиальным поверхностям и является биосовместимым и поддающимся биологическому разложению.
Кроме того, изобретение предусматривает способ приготовления сыворотки с тромбином, состоящий из следующих стадий:
a) Забор цельной крови, предпочтительно в пробирку, предпочтительно содержащую тиксотропный гель,
b) Центрифугирование пробирки до высвобождения сыворотки с тромбином и
c) Сбор сыворотки с тромбином.
Забор крови инициирует реакции свертывания крови, и, если не предприняты превентивные меры для остановки данного процесса, сгусток образуется естественным путем.
Предпочтительно, тиксотропный гель расположен рядом с дном пробирки. В течение центрифугирования красные кровяные клетки будут мигрировать под действием геля. В то же время, происходит полимеризация фибриногена с образованием сгустка на геле. Под действием значительной силы центрифугирования и/или значительного времени центрифугирования данный сгусток далее выпадет в осадок, формируя фибриновую сетку, которая высвободит жидкий супернатант, называемый сывороткой, содержащей обогащенный активированный тромбин. Тромбин является энзимом, стимулирующим коагуляцию.
Преимущественно сыворотка с тромбином, в соответствии с данным изобретением, может быть получена в несколько стадий исключительно с помощью центрифугирования пробирки содержащей цельную кровь и тиксотропный гель, в течение значительного времени центрифугирования. Преимущественно способ приготовления сыворотки с тромбином в соответствии с данным изобретением предусматривает получение готовой к использованию сыворотки с тромбином. К сыворотке с тромбином здесь также относится препарат, обогащенный тромбином; сыворотка, обогащенная тромбином; обогащенная активированная сыворотка с тромбином; обогащенный активированный препарат с тромбином; обогащенная тромбином активированная сыворотка; активированный обогащенный тромбином препарат.
Другая особенность заключается в том, что изобретение предусматривает способ приготовления сыворотки с тромбином, состоящий из следующих стадий:
a) Забор цельной крови, предпочтительно в пробирку, предпочтительно содержащую тиксотропный гель,
b) Центрифугирование пробирки до тех пор, когда красные кровяные клетки мигрируют под тиксотропный гель и, предпочтительно, до образования фибриновой сетки на тиксотропном геле и
c) Сбор супернатанта или сыворотки с тромбином.
В одном из предпочтительных вариантов изобретения стадия центрифугирования выполняется при величине ускорения 1000 g в течение приблизительно 30 минут. В следующем варианте изобретения стадия центрифугирования выполняется при величине ускорения от около 1000 g до около 2000 g в течение периода времени, выбранного в диапазоне от около 20 минут до около 40 минут, предпочтительно при 1500 g в течение периода времени, выбранного в диапазоне от около 25 минут до около 35 минут, предпочтительно при 1500 g в течение около 30 минут.
Предпочтительно, стадия центрифугирования выполняется в течение значительного времени до высвобождения сыворотки с тромбином.
Преимущественно способы настоящего изобретения позволяют осуществлять консервацию жидкой сыворотки при сохранении тромбина в растворимом состоянии. Стандартные способы заключаются в измельчении сгустка до высвобождения сыворотки с тромбином. Преимущественно данный способ является необязательным для приготовления сыворотки с тромбином в соответствии с настоящим изобретением. Данная альтернативная сыворотка с тромбином может быть также использована в качестве препарата, обогащенного тромбином в контексте изобретения. Преимущественно агент коагуляции не используется, и коагуляция происходит самопроизвольно. Это имеет преимущества, заключающиеся в снижении стоимости и упрощении способа. Поскольку в пробирке отсутствует цитрат, агент коагуляции (также называемый агентом восстановления) преимущественно не требуется для начала коагуляции. Преимущественно не требуется раствор этилового спирта и/или хлорид кальция.
Преимущественно способ приготовления сыворотки с тромбином, описанный здесь, является простым, требующим меньшего времени присутствия человека, поскольку измельчение сгустка не требуется, что обеспечивает экономическое преимущество по сравнению с прежними способами приготовления.
Альтернативная аутологичная сыворотка с тромбином, предназначенная для использования в контексте изобретения в качестве препарата, обогащенного тромбином, приготовляется с помощью устаревшего способа, который включает добавление 95% раствора этилового спирта (например, 1 мл) и хлорида кальция 10% (например, 1 мл) в пробу цельной крови пациента (например, 10 мл), отобранную в пробирку. Затем смеси позволяют осесть в течение около 30 минут при комнатной температуре. После 30 минут почти 80% антитромбина (наряду с другими белками, такими как фибриноген) выпадает в осадок, затем пробирку центрифугируют при около 1500 g в течение от около 8 до 10 минут, после чего аутологичная сыворотка с тромбином становится готовой для использования в комбинации с тромбоцитарно-обогащенным концентратом.
Предпочтительно, изобретение предусматривает способ приготовления аутологичной сыворотки с тромбином. Предпочтительно, все аспекты и/или варианты настоящего изобретения предназначены для аутологичного использования. Соответственно, настоящее изобретение предусматривает способ приготовления полностью аутологичной сыворотки с тромбином, причем донор и реципиент являются одним и тем же человеком или животным.
В одном варианте изобретения пробирка для приготовления сыворотки с тромбином изготовлена из стекла, предпочтительно является стеклянной пробиркой для отбора клеток (пробиркой-сепаратором), содержащей тиксотропный гель на основе сложного полиэфира.
В наиболее предпочтительном варианте способ приготовления сыворотки с тромбином включает использование пробирки в соответствии с данным изобретением, в которую не добавляют цитрат.
Другая особенность заключается в том, что изобретение предусматривает способ приготовления композиции для заживления ран или тканей, включающий следующие стадии:
a) Забор цельной крови, предпочтительно в пробирку, предпочтительно содержащую тиксотропный гель,
b) Центрифугирование пробирки, предпочтительно до высвобождения сыворотки с тромбином,
c) Сбор супернатанта и сыворотки с тромбином и
d) Смешивание сыворотки с тромбином с PRP композицией или выделенной композицией тромбоцитарного концентрата.
Другая особенность заключается в том, что изобретение предусматривает способ приготовления композиции для заживления ран или тканей, клеточную композицию и/или клеточный препарат, включающий следующие стадии:
a) Забор цельной крови, предпочтительно в пробирку, предпочтительно содержащую тиксотропный гель,
b) Центрифугирование пробирки, предпочтительно до высвобождения сыворотки с тромбином,
c) Сбор сыворотки с тромбином,
d) Смешивание сыворотки с тромбином с PRP композицией или выделенной композицией тромбоцитарного концетрата и
e) Добавление полученной композиции по пункту d) в клеточный экстракт, клеточную композицию, TCP, хитозан, гиалуроновую кислоту, крем, кремовую маску, жировые клетки, жировую ткань, концентрат клеток костного мозга, любрицин, cd-желатин, ботулотоксин и/или стволовые клетки.
В одном из вариантов осуществления изобретения цельная кровь забирается, по меньшей мере, в одну пробирку. Пробирка может быть обозначена здесь как пробирка для отбора клеток (пробирка-сепаратор). Предпочтительно все способы настоящего изобретения могут включать использование одной или нескольких пробирок в соответствии с изобретением.
В одном из вариантов осуществления изобретения все способы настоящего изобретения могут включать использование цельной крови, собранной в систему контейнеров для крови или устройство с пробирками для забора крови в соответствии с данным изобретением или устройство или набор, состоящий из такой системы контейнеров для крови или устройства с пробирками для забора крови.
Термин «пустая» пробирка относится здесь к пробирке, в которую не были помещены и/или добавлены никакие вещества или композиции.
Любой способ настоящего изобретения может быть воспроизведен с использованием, по меньшей мере, одной пробирки в соответствии с данным изобретением.
Другая особенность заключается в том, что изобретение предусматривает способ приготовления композиции для заживления ран или композиции для заживления тканей, состоящий из следующих стадий:
a) Забор цельной крови в пробирку,
b) Центрифугирование пробирки,
c) Сбор сгустка.
Агент коагуляции преимущественно не используется для приготовления композиции для заживления ран или композиции для заживления тканей. Композиция для заживления ран или композиция для заживления тканей является преимущественно готовой к использованию композицией. Такая композиция может быть непосредственно нанесена на диабетические язвы.
Предпочтительно способ приготовления композиции для заживления ран или композиции для заживления тканей предназначен для использования в стоматологии и/или ортопедии.
Другая особенность заключается в том, что изобретение предусматривает композицию для заживления ран или композицию для заживления тканей, состоящую из сгустка, предназначенного для использования в стоматологии, ортопедии; лечении артрита, псевдоартрита и подобных им заболеваний. В одном из вариантов осуществления изобретения композиция для заживления ран или композиция для заживления тканей включает сгусток, предназначе