Способ получения мезо-3,4-ди(п-оксифенил)1,1,1,6,6,6- гексафторгексана(ф-эстрола)или его эфиров
Иллюстрации
Показать всеРеферат
"„IОЛ ИСАНИЕ
<11) 434732
Республик
ИЗОБРЕТЕН ИЯ
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ (61) Дополнительное к авт. свнд-ву(22) Заявлено 28.10.71(21) 1709539/23 4 с присоединением заявки № (23) Приоритет (43) Опубликовано 25.02.76.Бюллетень №7 (51) М. Кл.
С 07С .43/12
С 07С 39/12
С 07 С 69/86
Государственный комитет
Совета Министров СССР
h0 делам изобретений и открытий (53) УДК 547,27.07 (088.8) (45) Дата опубликования описания22.03.76. (72) Авторы изобретения
Г. Г. Шитов, Э. A. Рудзит, О. М. Кулябко, Л, М. Ягупольский и 10. A. Фиалков
Институт органической химии AH Украин< кой ССР, Всесоюзный научно-исследовательский химико-фар лацевтический институт им. Серго Орджоникидзе; Новокузнецкий химикоа мацевтический завод (71) Заяви; елн (54) СПОСОБ ПОЛУЧЕНИЯ МЕЗ0-3,4-ДИ- (п-01 СИФЕНИЛ)-1,1,1,6,6,6-ГЕКСАФТОРГЕКСАНА (F -ЭСТРОЛА)
ИЛИ ЕГО ЭФИРОВ
20
Изобретение относится к способу получения новых фторированн6".х аналогов синэстрола, в частностимезо-3,4-ди-(п-оксифенил)-1,1,1, 6,6,6 гексафторгексана и его эфиров, кото.рые могут найти применение в медицине, 5
Соединения типа синэстрола, содержашие в алифатической части молекулы атомы фто;ра или трифторметильные группы,не известны. ,Предлагаемый способ получения мезо-3,4- 1р
-ди- (и - оксифенил)-1, 1, 1,6,6,6-гексафтор-: гексана (P -эстрола) или его эфиров обшей фор Аулы
Cgj
СН, I
R0 СН-СН
1 сн, CF3 где R - Н; СН3, СН3СО; СН3СН >СО;
CF3CH2CO, основанный на использовании,известных реакций, заключается в том, что две молекулы 1-бром-1-фенил-3,3,3-трифтор-5
1пропана конденсируют друг с другом в услоI виях гпдрированич в присутствии катализато,ра Адамса, полученный при этом мезо-3,4дифенил-1,1,1,6,6,6-гексафтаргексан ннтруют, образовавшийся мезо-3,4-ди- (и-нитрофенил)-1,1,1,6,6,6-гексафторгексан последовательно восстанавливают, диазотируют, .полученное диазосоединение разлагают B кислой среде, а зачем ацилируют ангидридом или хлорангидридом в присутствии шелочных ,агентов или алкилируют. 11елевой продукт выделяют известными приемами.
Предложенный способ на основе доступных фторорганич ских соединений позволяет расширить ассортимент эстрогенных гормонов с новыми фармакологическими свойствами.
Полупрздукт61 вышеуказанного синтеза могут служить основой для получения разноочразных физиологически активных вешеств нового типа.
Все полученные соединения не уступают по эффективности гормона:1ьного действия известным синэстролу и диэтилстильбестролу, а в некоторых случаях даже превосходят их.
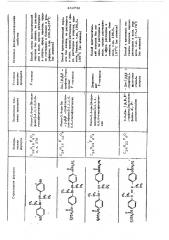
Данное изобретение иллюстрируется ннжепри434732 введенными приемами. Характеристика свойств полученных соединений представлена в таблице.
Пример 1. Мезо-3,4-дифенил-l,l, 1,6,6,6-гексафторгексан.
В склянку для гидрироваиия загружают
45 г l-бром- l-фенил-3,3; З-трифторпропана, 1 00 мп метанола, 0,25 г катализатора Адамса и гидрируют при атмосферном давлении до прекращения поглощения водорода. Катали- язатор отфильтровывают, фильтр и склянку промывают 1 00 мл эфира и смешиваютс основным раствором. Фильтрат разбавляют водой, эфирный слой отделяют, а из водного слоя дополнительно извлекают продукт реакции 15 эфиром (3х50 мл). Эфпрнь:е экстракты сушат хлористым кальцием эфир отгоняют, остаток охлаждают до 0 С и выдерживают при этой темпе стуре в течение 12 час.
Выпавший осадок отфильтровывают, пром „- 2О веют колодным метанолом и сушат. Выход сухого продукта 5,92 r; т.пл. 147-148 С.
После пе екристаппизации и, метанола получают 6,15 r мезо-3,4-дифенип-l,l,l, 6,6,6-гексафторгексана (16,7%); ", пп. 149-.И
150 С.
Пример 2. Мсзо-3,4--ди-(й-нитрофенип)-1,1,1,6,6,6-гексафторгексан.
В трехгорлую колбу емкостью 500 мп, снабженную мешалкой, термометром, капель» ной воронкой и ба ей дпя охлаждения, загружают 20 r мезо-3,4-дифенил-1,1,1,6,,6,6-гекса 9горгексана и 200 мл перегнанного уксусного а гидрида. Сусг.знзию слегка нагревают до растворения, охлаждают до о
0 С и при этой температуре пост пенно приливают 240 мл предварительно приготовленной нитруюшей смеси (1:1 ) перегнанной азотной кислоты (уд.вес. 1,52) и уксусного ангидрида. После добавления реакционную
40 о смес. выдерживают при 0-2 С в теч ние
6 час, после чего .оставляют на 12 час в холодильнике. Затем реакционную смесь выпивают в 700 г мелко измельченного льда
45 и перемешивают в течение 2 час. Выпавший осадок отфильтровывают, промывают водой до нейтральной реакции и сушат. Выход смеси изомеров 25,15 r (99,8%); т.пп. 2l7. 19,5 С. Дважды перекристаппизовывают о в ледяной укс сной киспоте. Выход параизомера 2 О, 42 г (81 %); т. пп. 2 36,5-2 37 С, При окислении азотной кислотой в запаянной ампуле при 220 С образуется f3-нитробензойиая кислота с выходом 60%. й5
1-найдено, %: Й 6,24; 6,36.
С18Н14 Г6 М20, Вычислено, %. Й 6,42.
Пример 3. Мезо-3,4-ди(й-аминофенип)-l, 1, 1,6,6,6-ге сафторгексан.
6О
В склянку для гидрирования загружают
4„36 г мезо 3, 1-ga-(й иисрафечил)-1,1,1, 6,6,6-гексафт ргексана, 250 мл метанола, 0,05 г катализатора Адамса и гидрируют при атмосферном давлении до прекращения поглощения водорода. Катализатор отфильтровывают, фильтрат разбавляют эфиром (1:1), промывают водой и экстрагируют 1%-ным раствором НС (Зх100 мл). Экстракты об» рабатывают активированным у. пек...;обавляют 300 мл концентрированной соляной кис» о лоты, охлаждают до 0 С и выпавший осадок отфильтровывают. Выход сухого дихлоргидрата мезо-3,4-ди- (й-аминофенил)«1, 1, 1,6,6,6гексафторгексана 4,07 r (90,6%); т.пп.
350ОС.
При обработке водного раствора дихлоргидрата раствором едкого натра получают мезо-3,4-ди-(й-аминофенил)-1, 1, 1,6,6,6-гексафторгексан; т.пп. 201-201,5 С (этаноп). о
Найдено, %: Р 30,30; 30,34.
С18Н18 Г6 Й2
Вычислено, %: F 30,33.
При ацетилировании уксусным ангидридом о получают диацетат; т.пл. > 350 С, Найдено, %: F 24,39; 24,65.
С22Н2 6 "202.
Вычислено, %: F 24,78.
Пример 4. Мезо-3,4-ди-(p-.оксифенил )-1, 1, 1, 6, 6, 6-гексафторгексан (Р-эс-рол).
В трехгорлую колбу емкостью 500 мл, снабженную мешалкой, термометром и капельной воронкой, загружают 1,8 г дихлоргидрата и постепенно приливают воду до полного растворения осадка. К полученному раствору при комнатной температуре приливают 15 мл концентрированной НС и постепенно 80 мл 1%«ного раствора нитрита нат« рия. Конец реакции диазотирования определяют ю йодокрахмальной бумаге. После слива раствора нитрита натрия смесь переме» шивают 1 час и полученный раствс,р диазосоединения постепенно <-кивают в 350 мл кипящей 50%-ной серной кислоты. После охлаждения осадок отфильтровывают, промывают водой до нейтральной реакции и сушат в вакууме при 70 С. Выход сухого технио ческого Р -эс-ропа 1,44 r; т. пл. 2272 9С.
Полу и-:.нный технический продукт ацетипируют 2(мл уксусного ангидрида в присутст . вии 0,5 мп пирпдина при 70 С в течение
2 час, Продукт реакции выделяют разбавле» нкзм водой, осадок отфильтровывают и промывают 10 мл эфира.
Сухой осадок диацетата F «эстрола кипятят с обработанным холодильником в 30 мл
3%-ного метанольного раствора едкого натра, после чего реакционную смесь разбавляют водой и обрабатывают активированнь..А г;лем. Фильтрат подкисляют соляной кислотой и, получают 1,23 г . Р -эстрола (82%}, бе:лый кристаллический порошок; т.пл, 236,5237 С (этанол).
Найдено, %: Р 30,1 ; 30,27.
С18Н1 602.
Вычислено, %: 30,18. Диацетат Р -эстрола получают по описанной выше методике, примененной для очистки технического продукта. Выход диацетата количественный; т.пл, 186,5187оС (уксусная кислота).
Найдено, %: 24,81; 24,92.
С22Н20 604
Вычислено, %: 24,65, Дипрогионат F -ecvpoxra. В трехгорлую колбу на 60 мл за. ружают 1,89 г эстрола, 10мл пропионового ангидрида и
CJ
0,5 мл пиридина. Смесь нагревают до 70 С, выдерживают при этой темпера.уре в течение 1 час, после чего разбавляют водой и полученный осадок оотфильтровывают. Выход о количественный; т.пл. "96,5-197 С (этанол).
Найдено, %: F 23,12; 23,30.
С24Н24 F604
Вычислено, %:: 23,28, 732
Ди - (P,P,6 - -трифтор)-пропионат t-эстрола, B трехгорлую колбу емкостью
250 мл загружают 1,89 г F эстрола, 100 мл сухого бензола и 1,6 г хлорьнгид-"
5 рида P q P yP -трифторпрогионовой кисло» .ты. Смесь охлаждают до 7оС, и постепенно
O приливают раствор 2 мл пиридина в 10 мл бензола. Реакционную смесь перемешивают
2 час, а затем выдерживают при комнатноя
lO температуре в течение,5 час и промыва кт водой (Зх100 мл}. Бензольный слой сушат хлористым кальцием, бензол упаривают, г остаток промывают эфиром и дважды КрНс тсллизуют из этанола, Выход ди (pp,ó - g»
15 фтор)-пропионата Г -эстрола 1,1 г (37%); т.пл. 198,5-199 С.
Найдено, %: F 38, 1 9; 38, 37.
С24Н1 8 1 204
Вычислено, %: Г 38,17.
Мезо 3,4-дп- (п-.,1етоксифенчл)-1,1,1,6,,6,6-гексафторгексян. В трехгорлую колбу на 100 мл загружают 1,89 r F -эстрола, 5 MJI 40 -Но 0 раствора едкого HGtpG H
1» мп диметилсульфата. Смесь нагревают о до 100 С, выдерживают при этой тмпера туре в течение 10 час, охлаждают до комнатной температуры и выливают в 50 мл
20%-ного раствора едкого натра. Выпавший
3(j ocBl1oK Отфильтровывают, промывают водой и кристаллнзуют нз 40".o-ного изопрппилово» го спирта. B, ход 1,24 г (61%}, т.пл. 192193 <;, 434732 И к о
Ж Ра о
Ф щ;Са.
Л и В
xgv5$
3;ою о
4 оаэи
3o" - e
1 QИ да.g ч
)CO и а. -» о
Д а.1о
Я -v! х о о о " " а. U И e ..д-,о -о
° ц <б Ф Ж Ф рфetйc
Я х и 3 а 0) g
Ь й. » о - а s I,U о t
2.В® и к
Я Ю х о
o о g t= а. а. щ оа" хорц оа Чц
XO "Iо Ф . и
Kl «, K. x
I 6» ф
4а.жд е
6)ko" f.ь
G Ж
CL, 4 Kà_#_ m
& Ф Ф
1 I .6 (434732
СИ, 3
СИ вЂ” СИ вЂ” QR
СИ
Ю
Составитель М. Меркулова
Редактор Е. Герасимова Техред М. Ликович Корректор Н. Зинзикова
Заказ 74 тираж 576 Подписное
БНИИПИ Государственного комитета Совета Министров СССР по делам иэобрете. ий и открытий
113035, Москва, Ж-35, Раушская наб., д. 4/5
Филиал ППП "Патент, г. Ужгород, ул. Гагарина. 101
Формула изобретения
Способ получения меэо-3,4 ди-(и-оксифенил}-1,1,1,6,6,6-гексафторгексана { Р эстрола} или его эфиров общей формулы
0PÇ б
3 где 2 - Н; СН3, .СН СО; СНЗСН СО;
С РЗСН2СО, отличающийся тем, 5 что две молекулы 1-бром-1-фенил-3,3,3-трифторпропана конденсируют друг с друго. в условиях гидрирования в присутствии квталиэатора Адамса, полученный при этом мезс 3,4-дифенил-1, 1, 1,6,6.,6-гексафторгексан нитруют, обраэовавшиися мезо-3,4-ди(г-нитрофенил)-1,1,1,6,6,6-гексафторгексан последовательно восстанавливают, диазотируют, полученное диазосоединение разлагают в кислой среде, а затем,апилируют ангидридом или хлоренгиаридом в присутствии щелочных агентов илп алкилируют и выделяют целевой продукт известными йриемами.