Способ получения 3-замещенных рифамицинов
Иллюстрации
Показать всеРеферат
ОП ИСАНИЕ
ИЗОБРЕТЕН ИЯ
К ПАТЕНТУ
Союз Советских
Сотеиалистицеских
Республик (11) 444372 (61) Зависимый от патента .! (22) Заявлено17.01.73 (21)1872137/23-4
32),Приоритет 19.01.7 Я. (31) 19525 А/72 (ЗЗ) Италия (43) Опубликовано25.09.74.Бюллетень № 35 (53) УЙК 547.89.07 (088.8) (45) Дата опубликования описания 29,10.75 (72) Авторы изобретения
Иностранцы
Николо Мадли и Ренато ричо (Италия) Иностранная фирма
Группо Лепетит, С. п. А. (Италия) (il) Заявитель (54) спОсОБ пт1лУчений 3-3Амешенных РиФАмицинОВ SV
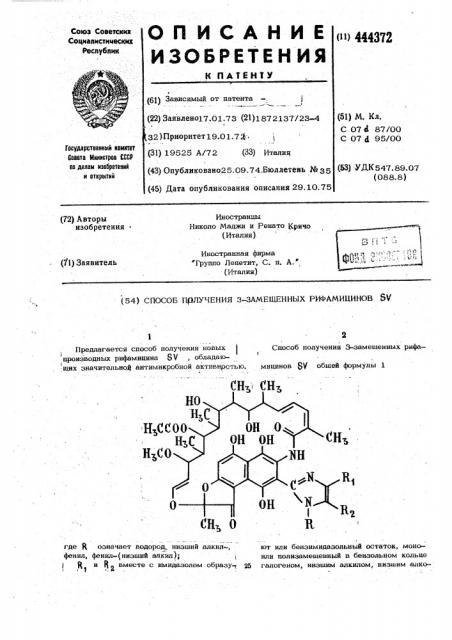
Способ получения 3-замешенных рифа-! мицинов Я общей формулы 1
Предлагается способ получения новых
) производных рифамицина 3V, обладаю-! щих эначительноЯ антимикробной активнрстью сн, Вт
l где Я означает водород„низший алкил, фенил, фенил-(низший алкнл);
Я и „вместе с имидазолом образу-
1 1 т 1..3 ют или бензимидазольный остаток, моноили полизамешенный в бензоньном кольце
25 галогеном, низшим алкилом, низшим алкоГосударственный комитет
Совета Министров СССР оо делам изооретеиий и открытий
ЯСС
К О (51) М. Кл.
С 07 8 87/00
С 07 с1 95/00
444372
2, ксилом, карбоксилом, карбалкоксилом, сульфо-, сульфамил-, нитро-, триф.орметил-, карбамил-, моно«или ди-(низший алкил),—:
-карбамилгрупаами, или поликонденсирован- ный ароматичес ий остаток, как замещенный, 5 так и незамещенный и cocTQHBIHM из 2-3 колец, каждое из которых содержит 5-6 ат,мов углерода, или метилендиоксиостаток, или их 25-дезацетил- и 16,17,18,19,;
28, 2 9-гексагидропрои зводных, заключает- Ip ся во взаимодействии 3-формилрифамицина:
$V или его 25-дезацетил- или 16,17,. . 1 8, 19,28,29-гексагидропроизводного с ароматическим о-диамином общей формулы 2
4. йЭ или его изомерный имидазолин затем окисляют и получают производное имидазола.
Наиболее применяемые окислители— кислород воздуха, соли меди (II), окись ртути (II); двуокись марганца, изоамилнитрит, феррицианид калия, тетраацетат свинца.
Если при окислении соединения формулы 3 o6pa3yeòñß нафтохиноновый фрагмент 445 то его- переводят. в соответствующий гидрохинон путем промывания раствором аскорбиновой кислоты..
В некоторых случаях выделения основания Шиффа формулы 3 или соответствующе- gp го изомерного имидазолина не требуется, так как при взаимодействии диамина формулы 2 с 3-формилрнфамицином в присутствии кислорода воздуха или других акцепторов водорода можно получать непосредственно производное имидазола.
Реакцию 3-формилрифамицина с диамиюм проводят, используя эквимолекулярные
=оотношения реагентов, в органическом растворителе цри температуре, которую 60 где R, p .и Я имеют указанные 2 значения.
Получаемое . при этом основание Шиф-. фа общей формулы 3 можно варьироват от комнатной до температуры кипения раСтворителя. Нродолжительность реакции 20 мин — 3 час, В качестве растворителей можно применять тетрагидрофуран, диоксан, низшие алканолы. Окисление промежуточного основания Шиффа фо,.мулы 3 лучше производить в смеси, состоящей из уксусной кислоты и хлорированного низшего углеводорода, применяя примерно эквимолекулярное количество окислителя, при минус 5 — плюс
10 С.
Пример 1. 3-(2-Бензимидазолил)рифамицин Я
Раствор 2,7 г 3-формилрифамицина
SV и 0,33 г о-фенилендиамина в 30 мл т трагидрофурана перемешивают в течение о
30 мин при 0-5 С. После выпаривания растворителя получают твердое основанное
Шиффа, т. пл. 252-255 С из. метанола, выход 80%.
1 .г полученного основания Шиффа растворяют в смеси 10 мл уксусной кислоты и 20 мл тетрахлорметана и после охлаждения в ледяной ванне прибавляют 0,5 i — .1
444372
1О
Таблица 1 макс 1 см
Е ммк
Температура о плавления С
Пример
Заместитель в положении 3 рифамици на $Ч
Амин
464 165,5
328 316,4
136-1 37
5-Метил-2-бен зим идазолил
3 3, 4-Тол уолдиа м ин
4 4, 4-Диметил-о-фенилендиамин 5, 6-Диметил-2-бензимидазолил
180
465 149,0
332 290,3
4, 5-Дигидро-7 1-1-аценафт 4,5-(Ц—
5 4, 5-Аценафтендиа мин
220 (разложение) 485 140,4
360 246,1 ) -имидазол-8-ил
5-Хлор-2-бензимидазолил
328
336
215-216 (разложение) 166,1
326,0
200 (разложение) .132,5
348,1
7 2,3-Флорендиамин
1, 9-Дигидрофнорено (-
2,3- g)-имидазол-2-ил
230 (разложение) 6, 1 1-Диоксоантра
1,2- Я) -имидазол-2-ил
429 176
1тетраацетата свинца. После 2 час ьыдеро живания при 0-5 С смесь разбавляют тетрахлорметаном и промывают, применяя
10%ный раствор водной аскорбиновой кислоты.
Органическую фазу сушат и выпаривают досуха. Твердый остаток перекристаллизовывают из ацетона или метанола, т. пл.
189-193 С (с разложением), выход 40%, макс ммк: 325; 46О; Е 322,5;
174,4.
Пример 2. 25-Дезацетил-3-(2бензимидазолил) рифамицин ЭЧ
Раствор 5 r 25-дезацетил-3-формил6 4-Хлор-о-фенилендиамин
8 1, 2-Диаминоантрахинон
Пример 9. 3-(1П-9-Оксофлорено 2,3- g /имидазол-2-ил) рифамицин $ Ч
Раствор 4,2 г 2,3-диаминофторен-9 -она и 14 г 3-формилрифамицина SV в
200 мл тетрагидрофурана нагревают в течение 3 час до кипения. После охлаждения вылавшее твердое вешество отфильтровывао ют, т. пл. 230 С (с разложением), выход
12,5 г; A.,ммк-470; 310; 256макс
1 о
Е1 см 139,2; 357,1;э388,3.
Пример . 10. 3-(5-КаРбокси-2-бензимидазолил) рифамицин SV
Это соединение получают аналогично рифамицина SV и 0,7. г о-фенилендиа- ) мина в 100 мл тетрагидрофурана перемешивают в течение 2 час в открытом сосуде при комнатной т мпературе. После выпаривания растворителя получают сырой продукт, который плавится после перекри,о. сталлизации из метанола при 195-196 С, выход 2,5 г, Я, ммк: Ж6; 462; макс
Е 351; 191.
1 см
11 р и м е р ы 3-8. Аналогично примеру 2, применяя соответствующие о-диамины и 3-формилрифамицин $Ч, получают
3-замешенные производные рифамицина
ЯЧ приведенные в табл. 1. l
1 примеру 10, применяя 3,4-диаминобензойную кислоту вместо 2,3-диаминофлорен-9о
-она, т. пл. 215 С (с разложением);
50 л, ммк: 462; 328: E 161
1% макс 1 см
310, 1.
Данные анализа описанных в примерах соединений соответствуют теоретическим
Аналогично получают 3 замешенные производные рифамицина 8Ч или их соответствуюшие 25-дезацетил-и 16, 17, 18, 19, 28, 29-гексагидросоединения, приведенные в табл. 2.
444372
Таблица2
Исходный амин
Заместитель рифамицина
B положении 3 н и я рифамиI
8, 4-Н итро-о-фенилендиамин
4-Диметикарбамило-фенилен дна мин
4-Б утин-о-фенилендиамин
4-Фенил-о-фенилендиамин
3-Н итро-о-фенилендиамин
4-Бром о-фенилендиамин
4-4>торо-фенилендиамйн
4,5-Дихлор-о-фенилендиамин
4, 5-Диметокси-о-фенилендиамин
4,5 Диэтокси-о-феннлендиамин
4,5 етилендиокси-о-фенилендиа мин
4,5-Дини rpo-о-фенилендиамин
4-Х:. ульфамоил-офенилендиамин и -Этил-о-фенилендиамин
К -Метил 4-трифторметил-офеиилендиамин
N -Метил-4,4-диметокси-офенилендиамин
N -Бензил-о-феыилендиамин .
Я -Фекл-о-фенилендиамин сложный этиловый эфир 3,4ди. минобензойной кислоты
2-Хлор-4,5-диаминобензолсульфоновая кислота
9, 10-Ф енантрендиамин
1,2-Нафталиндиамин
1,2-Диа мино-Ф-нафталинсульфоновая кислота
1,2-Дна мино-,4-фенантренсульфоцовая кислота предмет изобрете
Способ получения 3-замешенных нинов SV обшей формулы
5-Нутро -2-бенэамидазолил
5 -Цяметилкарбамил-2-бензим идаэолил
5-Бутил2-бензимидазолил
5 П ентил-2-бензимидазолил
4-Нитро-2-бенэимидазолил
5-5poM2
5Ф тор-2-бензимидазолил
5,6-Дихлор-2-бензимидазолил
5 6-Диметкоси-2-бензимидазолил
5,6-Диэтокси-2-6ензимидазолил
5,6-Метилендиокси-2-бензимида золил
5,6-Дни итрр-2-бензимидазолил
5-С ульфамоил-2-бензимидазолил
1-Этил-2-бензимидазолил
1-Метил-5 трифторметил-2бензимидазолил
1-Метил-5,6-диметокси-2бензимидазолил
1-Бензил-2-бензимидазолил
1-4> енил-2-бензимид аэолил
5-Карбэтоксй-бензимидазолил .
6-Хлор-5-сульфо-2-бензнмидаэолил
Фенантро/9, 10- Й /имидазол-2-ил
Нафто/1,2- В /нмидазол-2-ил
5-Сульфонафто /1,2- d, /ямнда зол-2-ил
5-Сульфофенантро /1,2-3/ имидазол 2-ил
;,где Я означает водород, низший алкил, . 40 фенил-(низший алкил); и Й вместе с имидазолом образу3 ют или бенэимидазольный остаток, моно или полизамешенный в бензольном кольце
t . 45, галогеном, низшим алкилом, низшим алко ксилом, карбоксилом, карбалкоксилом, сульI фо-, сульфамил-, нитро-, трифторметил-, карбамил-, моно- или ди-(низш ф алкил) !
:карбамилгруппами, или поликонденсирован Q) ный ароматический остаток, как замешенный, так и неэамешенный и состоящий из 2-3 колец, каждое иэ которых содержит
G-6 атомов углерода, или метилендиоксиостаток, И нли их 25-дезацетил-и 16, 17, 18, 19, 28, 29-гексагидропроизводных, о т-, I л и ч а ю ш и и с я тем, что 3-формил444372
HN
R.
Составитель Я. Цернов
Редактор О.Кужецова Техред Н XmeeBa лхм
Заказ Я6Х
Изд. М 8GQ
ЦНИИПИ Государственного комитета Совета Министров СССР но делам изобретений и открытий
Москва, 113035, Раушская наб., 4
11редприятне «Патент», Москва, Г-б9, Бережковская наб., 24 рифамицин или его 25-дезацетил и 16, : 17, 18, 19, 28, 29-гексагидропроизвод ное подвергают взаимодействию с о-диамином обшей формулы н К R) }О где Ц, Я и Я . имеют указанные значения, с поеледующими обработкой образую. шегося основания Шиффа окислителем, abr
1 бранным из рида: кислород воздуха, соль меди (ll), окись ртути (П), двуокись марганца, изоамилнитрит, феррициаыид калия, тетрацетат свинца, и восстановлением по- . лучаюшегося имидазольного производного аскорбиновой кислотой в соответствуюший . гидрохинон в случа,е, если имидазольное .. производное получают в хиноидной форме.
Тираж 506 Поднмсное