Способ получения тиолфосфонатов
Иллюстрации
Показать всеРеферат
ОЛ ИСАЙ ИЕ
ИЗОБРЕТЕН ИЯ
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ
Союз Советских
Социалистических ееслублик (») 450814 (6>) Зависимое от авт. свид-ва— (22) Заявлено 23.08.71(21) 1692725/23-4 с присоединением заявки № 169411 6/23-4 (32) Приоритет(51) М. Кл.
С 07(9/40
Государственный комитет
Совета Министров СССР по делам иэавретений и открытий (43) Опубликовано 25 11 74.Бюллетень № 43 (53) УДК 547.341, .26 118,07 (088,8) (45) Дата опубликования описания 24.12.75 (72) Авторы изобретения
3. H. Кваша, Л. М. Солнцева и Н. К. Близнюк (71) Заявитель Всесоюзный наУчно-исследовательский HHGTHTJT фитопатологии (54) СПОСОБ ПОЛУЧЕНИЯ ТИОЛфОСфОНД ГОВ
Г®.
RP u
10 где Р, — замешенный или неэамещенный фенил или бензил;
«незамещенный или замещенный фенил, аралкил, циклоалкил, 1а алкенил, алкинил, этилтиоэтил, алкоксиэтил, арилоксиэтил или группа — N С(СН )
3 2 !!
- алкил или арил.
Изобретение относится к фосфороргани-! ,ческой химии, а именно к способу получения новых тиолфосфонатов общей формулы
Известен способ получения тиолфосфона - тов взаимодействием дихлорфосфинов с сульфенилхлоридами, разложением аддукта сернистым газом и обработкой образующегося эфирхлорангидрида спиртами. lи
Однако соединения указанной формулы являются новыми. Они обладают физиологической активностью и могут найти применение в сельском хозяйстве.
Предлагаемый способ заключается в том, что соответствующий дихлорфосфин подвергают взаимодействию с сульфенилхлоридом в присутствии уксусной кислоты с последующей обработкой образующегося эфирхлорангидрида фенолом, спиртом или ацетоксимом в присутствии третичного амина.
Предлагаемый способ проводят смеш нием примерно эквимолярных количеств реагентов в инертном органическом раст» ворителе при минус 50 — плюс 80 С.
Целевые продукты выделяют известными приемами. Они представляют собой вязкие жидкости, растворимые в органических растворителях и нерастворимые в воде.
В качестве исходного сульфенилхлорида во многих случаях целесообразно испольэовать продукт взаимодействия соответст- ,вующего тиола или дисульфида с эквимо- l
4508И лярным количеством хлора или хлористого сульфурила.
Пример 1. Получение - 0-4-хлорфенил» $ -метилбензилтиофосфоната.
К раствору 0,52 г ° моль диметилдисульфида в 30 мл сухого хлороформа при минус 40-50оС добавляют эквимолярное количество хлора или хлористого сульфурила. Температуру смеси доводят до комнатной и получают раствор А.
К смеси 0,1 г ° моль бензилдихлорфос фина и 0,1 г ° моль ледяной уксусной кислоты в 30 мл хлороформа при минус
40-30 С приливают раствор А. Темперао туру смеси доводят до комнатной, раство,ритель и летучие удаляют в вакууме, в,. остатке получают промежуточный -метилбензилхлортиофосфонат. К смеси 0,25
r моль промежуточного эфирхлорангидри10
4 да и 0,25 г ° моль 4-.хлорфенола в 30 мл, бензола при, 1О-15оС прибавляют О,О25 г ° моль триэтиламийа и кийятят 2 час. Pw акционную массу промывают водой, сушат азеотропно, растворитель удаляют в вакууме и продукт выделяют перегонкой, т,кип.
230-232 С/2 мм рт. ст., вешество при о стоянии кристаллизуется, т. пл. 53-54 С, выход 72%, Найдено, %: Ci 11,10; P 9,65;
$10,40.
С Н Ci0 PS
14 14
Вычислено, %: Cl 11,35; P 9,94;
$10,22.
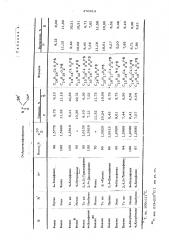
В условиях примера 1 получают другие тиолфосфонаты, выход и некоторые свойства которых приведены в таблице 1.
4 0814 в о ф л о
fQ л» л л Я о л
0) о" л» н
l СО
СО t о
fQ л
° -»
fQ
CD o
С4
fQ л»
СЧ
СО о ж (D
Ц
g
Ф
С4
1" »
О)" о
Я
О) fQ
° -» л и»
1-»
С0 о н»
hl о о л
Г
»О CD Ф »О
СО t
М а
hl о
СО а
CV о а о е
С0
fQ о л
С0
Ñ0 fQ
СО»
СО
fQ о лч
iV
l о л»
С0
0) о л о л л л»
c0 t с
Al о н» о
CD о
1-»
CD
fQ л
СО О
СО Л л»Q
С0 СО
° -» л» о о о
CQ
СО
fQ л» о о. о о
CU
СО (О о о а о о о о о л о о
Я а м о в
Д Ц1 4»
6 (Ц а ф
О. х
Q о
Х
4 а
М
Я
»ч аQ о
©
Ю о о m
1:
5 о а
Е: л х х
С0 с
u o
И а
CU о и х
Ф о с/) а Й о
Я х
Ñ 3 и
СО
hJ о
С о о х
03 н и
CG а
Я о и х
»0 о
CO а
X Ф о
0) а
hl о с4 л о
o u
0) а Ф о к
С0 о
М а
СЧ о о
Ф х
fQ о сО со а а л
rt O о
o u
СО CD х х
u o и
Д
o o о о л» сО
° -» л» О»
CD rl о
С4
Д»=
:С х
450814
Пример 2. Получение 0- й, -кре-) зил- $ -2,5-дихлорфенил-2,4-диметилбен зилтиофосфоната.
К смеси 0,03 г. моль 2,4-диметилбензилдихлорфосфина и 0,03 г . моль уксусной кислоты в 30 мл хлороформа при 0 — минус 5 С прибавляют раствор 0,03 r моль о
2,5-дихлорфенилсульфенилхлорида в 20 мл, хлороформа. Температуру смеси доводят до комнатной, растворитель и летучие удаляют в вакууме, в остатке получают промежуточный $ -2,5-дихлорфенил-2,4-ди метилбензилхлортиофосфонат.
В смесь 0,15 r. моль промежуточного эфирхлорангидрида и 0,015 г.моль tL—
-крезола в 30 мл бензола при 5-10 С вводят 0,015 г . моль триэтиламина. Смесь кипятят 2 час, промывают водой, органический слой сушат азеотропно, раствори1тель удаляют в вакууме при 100 С/1015 мм рт. ст., в остатке получают целевой продукт, д 20 1,5820; выход
98%. D
Найдено, %: С1 15,41; P 6,54;
Я 7,62.
2 2
Вычислено, %: С 15,75; P 6,87;
S7, 10.
Пример 3. Получение $ -бутил-0-(4-хлорфенокси)этилбензилтиофосфоната.
К раствору 0,026 г.моль дибутилдисульфида в 20 мл сухого хлороформа при о минус 40-50 С прибавляют эквимолярное количество хлора или хлористого сульфурила. Температуру смеси доводят до комнатной и получают раствор А, В раствор
0,05 r ° моль„бензилдихлорфосфина и
0,05 г. моль ледяной уксусной кислоты в о
30 мл хлороформа при минус 30-40 С вводят раствор А. Температуру смеси доводят до комнатной, растворитель и летуо чие удаляют в вакууме при 100 С/10-15 мм рт. ст. Остаток растворяют в 30 мл бензола и к полученному раствору при
0-5 С приливают раствор 0,05 г ° моль о
8 -(4-хлорфенокси)этанола и 0,05 г. моль гриэтиламина в 30 мл бензола. Смесь ! нагревают в течение 8 час при 50-60оС, промывают водой, органический раствор сушат азеотропно, растворитель удаляют в вакууме и в остатке получают целевой продукт, у 20 1,5660;
1,2233; MR найдено 106,0; вычислено 106,9, выход 98%.
Найдено, %: С 1 8,48; P 7,5 1;, 10 $8,36.
С Н С1 0 Р5
Вычислено %: CJ. 8,91; P 7,76;
S 8,03.
15 Пример 4. Получение 0-($ -этилбензилтиофосфонил ) ацетоксина.
В условиях примера 1 из 0,052 г. моль этилмеркаптана и эквимолярного количества хлора или хлористого сульфурила получают раствор " А.
К смеси 0,05 г ° моль бензилдихлорфосфина и 0,05 r ° моль ледяной уксусной кислоты при минус 30-40оС прибавляют раствор А. Температуру реакционной маср5 сы доводят до комнатной, растворитель и летучие удаляют в вакууме и остаток растворяют в 30 мл бензола. К полученному раствору при 5-10 С приливают о раствор 0,05 r ° моль ацетоксима и 0,05 ф) г. моль триэтиламина в 30 мл бензола. о
Смесь нагревают 2 час при 50 С, охлаждают, промывают водой, сушат азеотропно, растворитель удаляют в вакууме и в остатке получают целевой продукт, 35 20
1,555; <(1,1676; MR> найдено 74,6; вычислено 74,9; выход
96%
Найдено, %: Щ 5,36; P 11 14>
$1 1,59.
С Н N 0 Р$
Вычислено, %: hl 5,17; Р11.,,43;
В условиях примеров 3 и 4 получают другие вещества, выход и некоторые свойства которых приведены в табл. 2.
450814 о) (д сИ ж CD"
1-(tQ Ф о л1 (0 (Ч о
1-
hl л о л л1
Я
CD (4
tO
CD м и
CO а
CU о
t с4
:с
t и
И а
Л о
Я
X а с4 о (4 х (О о а
iV о а
С4 о
Я (0 CD
LQ Я
СЧ
Ю
t л
hl
° -1 с3 о
1-1 л л1 л
CD
Я о л1
CD л» л л
С4
t л
CD о Ф
h3
1-1
1 с9
Я
CO
1-1 о л1 л1 л1
1-1 (Ч
03 о л1 л о
Ю
t (О л о л1
Il3
1-1 о
CQ с
l0 о
Л
0)
И л о
EQ
IO
1-1
A л
" (7) I
00 у.
Ф о
Л о
\ о о
Э
I о
1 и
Q с4 о
Q»
Ц
Х
И о
С
В
Ж а
Р) о о
<д CO а а р 03 о о ж
1-1
:с х
С0 С4
1-1 о о
Я Я (0 GO о ч
CO а (Ч о
CD л х с9 л о с t
CO Й а
Щ о
Я о
03
CU
CD
h б о
Ж
В с(!
4 ( сЧ Al t со л о а о о с4 х
О) о (О
Щ
Ж
c I
И а
С4 о о с0
СМ о о
CD
LQ
Я л о о
LQ
° -1 о
C) с4
Я
Л с о
Ц
0 сО
450814
О! со
03 л о т 1 о. (4
fQ (О °
C4
0)
CQ л (О о л
tQ
0) о" т-1 о! о
CD (4 о 1 л
tQ о! л л о с!
t т-1 о л т-1 (О о л л
CD о л (О о
CQ а
CU о х
tO о а о о! х :! о о о (Ч 4 т! т-1 (О
t о" л (т3
tQ
oj л (О (О о т-1
СЯ т! о т-1
tO
С ) л л о о л
Я (1т
CD т- л л
CQ о
0) т-1 о
CQ Ф
03 т-1 л
Я т-1 о о
О) !т (О т-1 о
CD (O
И
1-т о
CO тй
tQ
Л1 о (т)
CO
tQ л о т3 (О
t0 л
1 ж
1»
2 о
И о (»е и
М
Ф
Г» о о
С4
Е р." о о о о
CD
l а !
I !
I !! !
I о (-ч х сл о а
СЧ о о со (ч
hl C4 х х ф CO т!
o o (О Ф с0 Я
O CQ о4
Ц (ч
"4 (Т)
CO а
СЧ о
03 т"1 х о
CD
СЧ
03 т-1 !
1 о, (т) о (4 т-1
CD (О о т-1
CD
CQ
10 т-1 л
CD
Я
0) а с4 о
03 о
CQ (Ч
Ж а (т3 о с9 о (О л х (О о
I о
Я q
"ф »».
l o 5
o o
4Д (O а
Я о х с9 о (O а о Ф о
CD
:с
CO о (I! а
Я о
СМ л о
СЧ х
CO о! -9
tQ O (4 1 .!
1: в о4 ц
450814
0R
ВР
И SR""
Составитель Д Карунина
Редактор O.Êóçíeöoâà Texpe> H.Ханеева Корректор А.дэесова
Заказ
Изд. И f/$P Тираж 506
Подписное
ЦНИИПИ Государственного комитета Совета Министров СССР по делам изобретений н открытий
Москва, 113035, Раушская наб., 4
Предприятие сПатеит». Москва. Г-б9. Беоежковекяя
Пример 5. Получение Я -2,5-дихлорфенил-О-пропаргил-2,4-диметилбензилтиофосфоната.
К смеси 0,03 г . моль 2,4-диметилбен эилдихлорфосфина и 0,03 г ° моль ледяной уксусной кислоты в 30 мл хлороформа при
0- минус 5оС прибавляют раствор 0,03 г .моль 2,5-дихлорфенилсульфенилхлорида в
30 мл хлороформа. Температуру смеси до
° водят до комнатной, растворитель и летучие удаляют в вакууме при 100 С/10-15 о мм рт. ст. и остаток растворяют в бензоле. В полученный раствор при 0-5оС вводят смесь 0,03 г . моль пропаргилового спирта и 0,03 r. моль триэтиламина в 20 мл бензола. Смесь нагревают 2 час при 50 С, о промывают водой, сушат азеотропно, растворитель удаляют в вакууме, в остатке получают целевой продукт, g 1,5750; 20 Э
С 1,2078, выход 96%.
Найдено, %; Cj 17,56; P 7,49;
$8,37.
С18Н17С 1 202Р $ .
Вычислено, %: СА 17,73; P 7,75;
$8,01.
В условиях примера 5 получают вещество, приведенное в табл. 2 последним.
14
Предмет изобретения
Способ получения тиолфосфонатов общей формулы
5 где Я - замешенный или незамещенный фенил или бензил;
Я вЂ” неэамещенный или замешенный
1 фенил, аралкил, циклоалкил, алкенил, алкинил, этилтиоэтил, алкоксиэтил, 20 арилоксиэтил или группа - К =C (СН ) 4
К вЂ” алкил или арил, о т л и ч а юЦ шийся тем, что соответствующий дихлорфосфин подвергают взаимодействию с сульфенилхлоридом в присутствии уксусной
25 кислоты с последующими обработкой образующегося эфирхлорангидрида фенолом, спиртом или ацетоксимом в присутствии третичного амина и выделением целевого продукта
30 известными приемами.