Способ получения галогенированных феноксициклопентендионов
Иллюстрации
Показать всеРеферат
1;
ОПИСАНИЕ
ИЗОБРЕТЕН ИЯ
Союз Советских
Социалистических
Республик (11) 47799 5
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ (61) Зависимое от авт. свидетельства(22) Заявлено 19.09.72 (21) 1829942/23-4 (51) М, Кл.
С 07.с 49/45 с присоединением заявки № (32)Прноритет—
Гасударственный намнтет
Саввтв Мнннстрав СССР
Ао делам нэааретеннй н атнрытнй
Опубликовано 25.07.75,Бюллетень № 27
Дата опубликования опнсання14.08.75 (53) УДК 547.514.472. .07 (088. S ) (72) Авторы изобретения
В. Д. Симонов и Г. М. Коновалова (7l) Заявитель Уфимский филиал Всесоюзного научно-исследовательского института химических средств зашиты растений (54) СПОСОБ ПОЛУЧЕНИЯ ГАЛОГЕЕИРОВАННЫХ
Ф ЕНОКСИПИКЛОПЕНТЕНДИОНОВ
1
Изобретение относится к способу получения галогенированных феноксициклопентендионов, которые могут найти применение в качестве биологически активных соединений. . Известен способ получения Р -арилоксивинилкетонов взаимодействием р -хлорвинилкетонов с фенолами.
На основе известной реакции получен ряд новых соединений.
Предложенный способ получения галогенированных феноксициклопентендионов общей формулы
СС1, подвергают взаимодействию с феноламп при 20-100оС в среде органического растворителя, например бензола, в присутствии акцептора галоидводорода с последующим выделением целевых продуктов известными д1 и собами.
Предложенный способ прост в исполне-. нии и позволяет получить новые биологически активные галогенированные феноксициклопентендионы с выходом 50-85% от теоретического.
Пример 1, Получение 2,3-дихлор-5-хлор (фенокси) метилен-2-циклопентен-.
-1,4-диона.
2,46 r (0,01 моль) 2,3-дихлор-5-(дихлорметилен) 2-циклоп ентен-1, 4-диона
С1 С1 С1
О - O" О
С1 С -0R
0 с-(oa) где Я вЂ” фенил, моно- и полихлорфенил, моно- и полинитрофенил, заключается в том, что галогенирован ный циклопентендион формулы
477995 растворяют в 65 t.û бензола и в течение
30 мин прн комнатной температуре смесь из 0,94 > (0,01 моля) фецола и 1,4 мл (0,01 моля) триэтиламина в 30 мл бензола. Реакционную массу перемешивают в течение 2 час при температуре окружающей среды. После отделения 1,3 г (95% от теоретического) осадка солянокислого триэтиламина If отгонки бензола получают
3,01 г остатка, который после перекристаллизац ги из н-гептана дает 2,5 г (82,5% от теоретического) желтоватого
-,,о вещества с т. пл. 161-163 С.
Пример 2. Получение 2,3-дихлор-
-5-ди (пентахлорфенокси) метилен-2-циклопентен-1,4-диона.
2,46 г (0,01 моля) 2,3-дихлор-5-(дихлорметилен) -2-циклопентен-1,4-диона растворяют в 65 л1л бензола и в течение .о
50 lvl)IH при температуре бани 5 э С прикицывают смесь из 5,34 г (0,02 моля) пентахлорфенола и 2,8 мл (0,02 моля) триэтиламнна в 90 мл бензола. Реакционную массу перемешивают в течение 5 час при этой же температуре. Отделяют 2,22 г (81% от теоретического) осадка co)IHllo кислого триэтнламина. После отгонки бепзола получают 7,4 г продукта, который промывают горячим ацетоном и выделяют
5,36 г (76% от теоретического) продукта с т. пл. выше 240оС.
ll р и м е р 3. Получение 2,3-дихлор-5-хлор (2,4-дицитрофенокси) метилен-2-циклонентен 1,4-диона.
2,46 r (0,01 моля) 2,3-дихлор--5— (дихлорметилен)-2-циклопентен-), ) дио на растворяют в 65 мл бензола и в .течение 30 мин при комнатной температуре прикапывают смесь из 1,85 г (0,01 моля)
2,4-динитрофенола и 1,4 мл (0,01 моля) триэтиламина в 50 мл бензола. Реакционную массу перемешивают в течение 5 час при температуре окружающей среды. После р отделения 4,03 г осадка солянокислого триэтиламина и отгонки бензола получают
1,22 г (89,5% от теоретического) остатка, который после перекристаллизации из и-гептана дает 2,75 г (70%о от теорети- к ческого) продукта с т. пл, 131-133 С. ! б
Пример 4. Получение 2 3-дихлор-5-ди (Я -нафтокси) метилеп-2-циклопентен-1,4-диона.
2,46 г (0,01 моля) 2,3-дихлор-5-(дихлорметилен)-2-циклопентен-l,4-диона растворяют в 65 мл бензола и в течение 40 мин прикапывают при комнатной температуре смесь из 2,89 r (0,02 мр25 ля) ф -нафтола и 2,8 мл (0,02 моля) триэтиламина в 100 мл бензола. Реакционную массу перемешивают в течение 6 час при комнатной температуре. После отделения 2,43 r (89% от теоретического) осадка солянокислого триэтиламина и отгонки бензола получают 4,23 г остатка, который после перекристаллизации из смеси н-гептан/бензол дает 3,61 г (78% от теорети ческого) продукта с т. пл.
95-197 С.
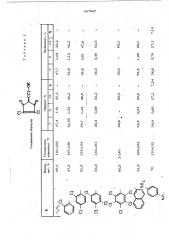
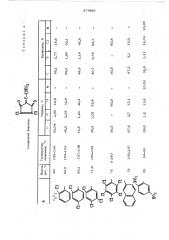
Характеристика полученных соединений приведена в табл. 1 и 2.
1 1
<Ч
CD Ф о (0
t о г1 (О о
03 о
ñ9 о о (О с4
СЯ
0) (О о (Ч о
СЯ
С ) i о о с л
fD о
Я о
Ю о
Ф
Ц о
Р (Я
М х
Z !
44799 (0 (O (-", ol ф l0
Щ . l0
g) tQ
Щ и (Ч со c4 (Q сЯ: (О
Я о
t с ( (g (Q д): ñ9
CD
ol л
CD
CD
l0 о
С о
С ) о
1-1 ф
1 о о
СО о ж
Ф
tf з (Д
oj о
СЧ с о о
IQ о
С
<О о Ф
Я
Р3
Е а
О р
6 о о
Д и р
А
Я о л а а <р
О д
477995
477995
СС, Составитель Г.Максимова
РедактоРН ДжаРагетти ТехРед И арандашова КоРРегтоР Л.БРахнина
Заказ g g07 Изд. М //35 Тираж Я29
Подписное
ЦИИИПИ Государственного комитета Совета Министров СССР по делам изобретений и открытий
Москва, И3035, Раушская наб., 4
Предприятие сПатент», Москва, Г-59, Бережковская наб., 24
-Предмет изобретения
Способ получения галогенированных феноксициклопентендионов обшей формулы
Cf Q Ci м
О О р 0
С1-С-ОВ.. С (ОК}г 1о где Я - фенил, моно-„полижорфенил, моно- и полинитрофенил, нафтил, мо-: но- и полиалкилфенил, отличающийся тем, что галогенированный циклопентендион формуС1 CI
О О подвергают взаимодействию с фенолами при 20-100оС в среде органического растворителя, например бензола, в присутствии акцептора галоидводорода с последующим выделением целевых продуктов известными способами.