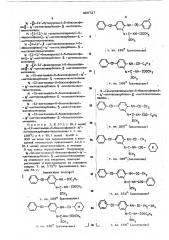
Способ получения замещенных бензоилфенилизотиомочевины
Иллюстрации
Показать всеРеферат
(61) Дополнительный к патенту (51) М. Кл, (22) Заявлено,23.0 1. 74 (21) .1990 756/23-4 (23) Приоритет2 3. 01. 73, 32) С 07 с 157/14
Гасудвратвеииый кватет
Саввтв Миииатрав СССР па делен изобретеиий и аткрытвй
Ф (Q) УДК 547.496.3,07 (088 8) (31) Р2303048.0 (33) ФРГ (43} Опубликовано 25.12.756толлетеиь № 47 (45} Дата опубликования описания 14.06,76 (72) Авторы Иностранцы изобретения Хайнрих Кйллинг, Арно Виддиг, Херберт Томас и Ханс (фРГ) Иностранная фирма
"Байер АГ" (ФРГ} (71) Заявитель
\ (54) СПОСОБ ЦОДУ 1ЕНИ 1 3ANEigEHI ib yi БЕНЗОИ Х! ФЕНИ ПИЗОТИОМОЧЕВИНЫ
Изобретение относится к способу получении замешенных бензоилфенилизотиомочевины обшей формулы где Я - алкил C -С, циклоалкил, содериаший до 8 атомов углерода, алкенил, содержа% ший до 12 атомов углерода или аралкил, не амешенный или замешенный в арильной части одной или несколькими
Группами алкила С1 С4 и/или алкоксила с С -С, и/или галогена;
- алкил С -С
- водород, Bnlllln С,-C, „, не2
Я замешенный или замешенный галогенциан -, алкоксигруппой с С -С > алкоксикарбонилом с С -С, феноксн-, галогенфенокси-, алкилфеноксн или алкоксифеноксигруппой, IIHKIloBFiIIHn С -С, арил- IITfH BpBIIIIHË, 1, незамешенные или замешенные, галоген, -алкил - С -С ил; алкоксигруппой с
1 4
С -С,, 1 фурил или группа - NR 5
И 1И
II ! в кОтОрОй R ВОдород или алкил
С -С,, (III — водород, алкил С -С неэамешенный или замешенный I MloleH, 16
1 циан-, алкоксигруппой с С -С, алкокси- .
1 4 карбонилом с С -С, пиклоалкил с
2 5, С -С,, аралкил, незамешенный или заме . шенный в арильной части галоген, низшей алкин- и/илн низшей алкоксигруппой, фенил, незамешенный или замешенный ГалО ген-, низшей алкил- и/или низшей алкоксигруппой, адил, содержаший до 18 атомов углерода, незамешенный и:пт замешенный Гал Ген, низшей алкоксигруттпой, ароил, . 496727 незамешенный или замещенный галоген-, ниэшей алкил-, низшей алкоксигруппой, апкилсульфонил, содержащий до 18 атомов углерода, арчлсупъфонил, незамещенный или замешенный галоген-, амино-, низшей алкил-, низшей . алкоксигруппой, диалкил-:, аминогруппа, содержащая до 4 атомов углерода, ипи Р" и P" образуют совмест! но с атомом азота гетероциклическое кольцо с С4-С7, которое может содержать l 10 другие гетероатомы, например кислород или серу, которые обладают антигельминт- ным действием, Получение соединений основано на известном способе ; алкилирования тцо ло-, 15 чевины. Однако применение соответствующих исходных веществ позволяет получать, новые соединения, обладающие уггучшенными свойствами по сравнению с из,вестными, Предлагаемый способ заключается в том, что тиомочевину общей формулы
20 со ин — сов
NH- С8 — СООЯ, где и R2 имеют указанные значе1 ния, гюдвергают Взаимодействию в щелочной I ag среде в присутствии разбавителя С соеди- нен11ел1 обшей формулы р где 3 имеет указанное значение;
У вЂ” галоген, арилсульфоцовая или gp алкилсупьфон вая группа, с последующим Выделением целевого продукта известными приемами. В качестве разбавитепей в способе могут применяться вода или органические растворитест, такие,как спирт, ацетон, диметипсульфоксид, диметипформамид или ацетонитрип IIIIII их смеси с ВОДОЙ, f1tI÷ создания щелочной среды можно применять любые щелочи, Однако предпоч- j5Q тительиее применение едких кали и нат, ра, карбоната ипи бикарбоната натрия. 1 ел111ература реакции От -10 до +40 С, О
: предпочтительно От 0 до ЗООС.
При Осуществлении способа, как пра-, Я випе„на 1 л1Оль амидобе 1оипфепиптпо. мочевииы Оеруг J, моль аг;килируюшего
Средства (ООединсиия Обшей формулы Н1)
И 1 мел1 1и:Jto÷tt, Однаке л1ожнО прил1е
1гять иаб1.г ток алкил11ру1егце1-О средстг1а zt, 60 щелочи. При переработке реакционной смеси ее выливают в воду, отжимают выпавший продукт, сунат и очищают перекристаллиэацией.
В качестве новых действующих начал могут быть названы следующие вещества:
hl -(2-ацетамидо-5-бенэоилфенил)— ) -метоксикарбонил- Я -метилизотиомоче( вина; -(2-ацетамидо-5-бензоилфенил)I
- g -этоксикарбонил- Я -метилиэотиомочевина;
111 -(2-ацетамидо-5-бенэоилфенил)- Ц -изо-пропоксикарбонил- $ -метилиэо-! тиомочевига;
Я -{ 2-ацетамидо-5-бенэоилфенил)I — Я -втор.-бутокснкарбонил- 3 -метилизотиомочевина;
N -{2-пропионамидо-5-бенэоилфенил)1 — Й -метоксикарбонил- 1 -метилизотиомочевина;
N -(2-бутирамидо-5-бензоилфенил)-!
- g -метоксикарбонил- Я -метилизотиомочевина;
Й -(1-иэо-бутирамидо-5-бензоилфенил)I — Я -метоксикарбонил- Я -метнлиэотиомоче- вина;
М -{ 2-ваперамидо-5-бенэоилфенил)I
- hJ -метоксикарбонип- g -метилизотиомочевина;
И вЂ” { 2-иэо-ваперамидо-5-бензоилфенил)-! — g -метоксикарбонил- Я -метилиэотиомочевина;
-(2-капронамидо-5-бензоилфенил)- д1-метоксикарбонил Я вЂ” метипиэотиомоче...
BHHG;
Я -(2-изо-капронамидо-5-бензоилфеI нип)- Q -метоксикарбонип- Q -метилизотиомоче вина;
Я -(2-циклопентанкарбонамидо-5-бенэои эоипфенил)- g --метоксикарбонип- $ -меI типиэотиомочеви11; (2 цикпогексанкарбонамидо-5 бен Я зоипфенил)- Q -метоксикарбонип- Я -метйй-!
I изотиомочевина;
)ч -(2-фенипац тамидо-5-бенэоилфенил)I
- (4 -метоксикарбонил- $ -метилизотиомоче-. вина;
-(2-феноксиацетамидо-5-бенэоилфенил)- Я -метоксикарбонил- Я -метилизотио-, 1 мочевина;
Я -(2-бенэамидо-5-бензоилфенил)- Q -, I
-метоксикарбонил- Я -метилизотиомочевина;
Я вЂ” 2- (2 -ме тилуреидо )-5-бензоилфе»
I нип — } -метоксикарбонил- Q -метилизотиомочевина;
Ц вЂ” 2-(2 -этилуреидо)-5-бенэоилфенил— N --метоксикарбонил- Я -метипизотиомо-! чевина;
496727
СО йв- (,"О й= С- ИН-С00СН
3 есв, NH-Ñ0- Св
3 ñî
®0 3
И=С- Йв- С00- H
Всв
С
1 . т. пл.
ЙН вЂ” ®С ) 7 о
152 (разложение) СО
NH- С0-С -св
2 3
- -(2 -бутииуреиио)-б-беиеоиифенил1- g -метоксикарбонил- 5 -метилиэо тиомочевина;
N -(2-(2 - Ю -цианпентилуреидо)-5I
I -бенэоилфенил)- N -метоксикарбонил- S - 5
-метилизотиомоче вина;
Я -(2-(2 - 3 -метоксиэтилуреидо )-5I бвнзоилфенил) - g -метоксикарбонил- 3; -метилизотиомочевина;
g -(2-(2 -бенэилуреидо)-5-бенэоилфе- . 19 нил1 - g метоксикарбонил- $ - метилизотио. мочевина, g -Q-(2 -фенилуреидо )-5-бенэоилфе, ни Д» g -метоксикарбонил- Я -метилизотио; мочевина; 35
Д -(2-ацетамидо-5-бенэоилфенил)- К—
-метоксикарбонил- 6 -этилиэотиомочевина;
Я -(2-ацетамидо-5-бенэоилфенил}- )) -метоксикарбонил- 8 -иэопропилиэотиомочевина; ю
К -(2-ацетамидо-5-бенэоилфенил)- Я -метоксикарбонил- Я. -аллилиэотиомочевина;
N -(2-ацетамидо-5-бенэоилфенил)- Ц -метоксикарбонил- Q -циклогексил1 И изотиомочевина;
Я -(2«ацетамидо-5-бензоилфенил)- N -метоксикарбонил- Я -бенэилизотио» мочевина.
Пример l. К 37 1 г (O 1 моля) -(2-ацетамидо-5-бензоилфенил)- NI . -метоксикарбонил-тиомочевины с т. пл.
199 С и 4 г (0,1 моля) ЯаОН в
300 мл воды при перемешивании и комнатной температуре прикапывают 12,6 r (0,1 моля) диметилсульфата, в течение
Э час смесь перемешивают, Полученную !
g -(2-ацетамидо-5-бензоил-фенил)-
-метоксикарбонил- Я -метилиэотиомочевину отжимают под вакуумом, повторно, растворяют и кристаллиэуют иэ зтилового спирта. Т. пл. 172 С (раэложение), выход 31 г.
Аналогично получают !
N-e NH-COO|:H
),SCH т. пл, 158о (разложение) И=С-ВН-ССоСн, I
SCH о т. пл, 140 (разложение) о
t т. пл. 139 (разложение) С0 NH-(. ()- С H g
1 N C -NH- ÑÎ0ÑÍ
g(, H о т. пл. 168 (разложение) и и -(2-пропиониламино-5-бенэоилфенил }
- N -метоксикарбонил- Д -метилизотиомоt чевина Ин- С00- С H
2 5
8СН
1 о т. пл. 205 (разложение) т. пл. 196,разложение) К=С-NH-СООС Н
2 5
3 т. пл. 168 (разложение)