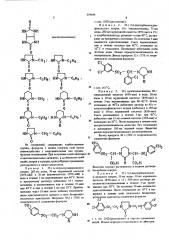
Способ получения сульфонильных соединений
Иллюстрации
Показать всеРеферат
ОП ИСАНИЕ
ИЗОЬРЕтЕНИЯ
К ПАТЕНТУ
Союз Советских
Социалистических
Республик (11-) -559646 (61) Дополнительный к патенту (22) Заявлено 02.06.72 (21) 1791397/04
2 (51) М. Кл.
С 07 С 147/00 (32) 05.06.71 (23) Приоритет
Государственный комитет
Совета Министров СССР
w делам изобретений и открытий (31) Р 2128011.5 (33) ФРГ (43) Опубликовано 25.05.77. Бюллетень №19 (45) Дата опубликования описания21.0Х,78 (53) УДК
547.544.07 (088 8) Иностранцы
Штеффен Пиш и Фридрих Энгелыардт (ФРГ) (72) Авторы изобретения
Иностранная фирма
"Каеселла Фарбверке Майикур" (ФРГ) (71) Заявитель (54) СПОСОБ ПОЛУЧЕНИЯ СУЛЬФОНИЛЬНЫХ СОЕДИНЕНИЙ
2,,Г
СН-К Ы- СН- О,-R5;
С
31 н 3»
О иог1, где  — низа,, алкил:
Изобретение относится к способу цолучения
Неописанных в литературе соединений формулы I
R SO,-X, где R ° арил, аралкнл, гетерил, циклоалкил с
4 — 8 атомами углерода, алкил с 1 — 8 атомами утлерода1 Z б
Х- -СН- К,; — СН-Эг Ы-Z,; с
Я! R .О сн — мн- соо-т — ооС-Йн-сн-so a:, I
В. Rg
R> — водород, арил, аралкил, гетерил, циклоалкил с 4- 6 атомами углерода, алкил с 1 — 8 атомами углерода, карбоксил, карбокснлат (в виде солей);
R, йз — арил, аралкил, циклоалкил е 4 — 8 атомами углерода, алкил с 1-8 атомами углерода и
R еще водород;
У вЂ” алкилен, цнклоалкилен, арилен;
Z — алкилен, оксиалкилен или
-CH — СИl
NH NH
ll
0 гтзвеетен способ получения к(си=си > Х вЂ” 802 (CHg CHg 0)g — Н i
ОН ! — 80 СН СН вЂ” СКЛОН i
559646 — 80 — С „Сн — сн,м, 1
t взаимодействием ароматического альдегида с соответствующим замешенным нитротолуолом при нагревании в присутствии основного катализатора, Однако способ получении соединений формулы 1 не известен.
Полученные соединения представляют интерес в, качестве физиологически активных соединений, а также могут найти применение в качестве восстановительного компонента в окислительно-восстановительных системах катализаторов, которые используются для получения гомо- и сополимеров с олефиновой связью.
Предлагается способ получения соединений формулы 1, заключающийся в том, что сульфиновую кислоту подвергают взаимодействию с соответствующим альдегидом и образовавшееся при этом оксисульфонильное соединение подвергают взаимодействию с тиолом, или циклической мочевиной, или производным мочевины, или соединекием общей формулы I1
Н и — СОΠ— Y — 0OC-NHg где У имеет указанное значение, с последующим выделением целевого продукта известным способом.
В качестве сульфиновых кислот общей формулы H можно применять, например, метан-, этан-, пропаи-, бутан-, бензол-, п-толуол-, n-хлорбензол-, 4-метоксибензол-, З-трифторметилбензол-, 4-нитробенэол-, З-цианбензол-, 4-ацетаминобензол-, 3,4-дихлор-, 2,5-дихлор- или 2,б-дихлорбенэол-, 2,3,4-трихлорбензол-, 2,5-диметоксибензол-, . 3,4,5-триметоксибензол-, ?;-метокси- 5-хлорбензол-, 2-хлор-5-нитробензол-, 2-хлор- 5-трифторметилбензол-, 2-хлор- б- метилбензол-, 4- гидрокси.
-5-карбокси бензол-,; 2-тиофен-, 2-нафталин- сульфоновые кислоты.
Можно применять также и соли сульфиновой кислоты, в особенности натриевые и калиевые.
Сульфиновые кислоты можно получать, например, восстановлением соответствующих хлоргидридов сульфоновой кислоты (их получают путем взаимодействия соответствующих эамещепных бензолов с хлорсульфо кисл отой или из соответствующих замешенных анилинов путем модифицированной реакции Зандмейера по Меервейну)или путем непосредственной реакции Зандмейера с получением сульфиновой кислоты. Таким образом получили, например, еще. неизвестную 2-хлор-6о
-метилбензолсульфиновую кислоту (т.пл. 110 С с разложением), исходя иэ 2-хлор-6- метиланилина через 2-хлор-6-метилбензолсульфохлорид (т. кип.
117 C/1,3 мм рт.ст.
В качестве альдегидов можно применять, например, формальдегид, ацетальдегид, пропионовый альдегид, К- или изо-бутиральдегид, Я- или изо-валериановый альдегид, капроновый альдегид, бензальдегид, хлораль, бромаль, и- и о-хлорбензальдегид, п-бромбеязальдегид, и- и о-метоксибензальдегид, 3,4,5- триметоксибенэальдегид, о-оксибенэальдегид, 2,5- и 3,4-дихлорбенэальдегид, и-диметиламинобензальдегид, п-ацетиламииобензальдегид, толилальдегид, .и- и и- нитробензальдегид, фурфуровый альдегид,фурфурол, акролеин, кротой вый альдегид, пиридил-3- альдегид, глиоксиловую кислоту (также в виде ее солей, в особенности яатриевой, калиевой, кальциевой, аммониевой, триэтаноламмоииевой H триэтиламмониевой соли) .
В качестве тиолов (меркаптанов) можно применять, например, метантиол, этантиол, пропантиол, бутаятиол, Р-оксиэтантиол, бензолтиол, и-хлорбензолтиол, п-оксибензолтиол, 3,4-дихлорбензолтиол, 2-хлор- 5- трифторметилбензолтиол, 3- трифторметилбензолтиол, 4-ацетиламинобензолтиол, 4-димет ила минобензолтиол, 2,3,4-трихлорбензолтиол, 4-бромбеяэолтиол, 2,5-диметоксибензолтиол,, S-хлор-2- метоксибензолтиол, 2-нафталинтиол, 2-хлор-6- метилбензолтиол, 4-метилбензолтиол, фенилметантиол, 3,4-диметилбенэолтиол, циклопентантиол, и- меркаптобензойную кислоту, меркаптоуксусную кислоту, метиловый, этиловый и пропиловый эфиры меркаптоуксусной кислоты.
Тиолы можно получать известными способами, например путем алкилирования или арилирования сероводорода и путем превращения других серных функций в группу — SH. При алкилировании сероводорода целесообразно замещение второго атома
Н легкоотщепляемыми радикалами. Алкилируют, например, тиосульфат натрия, тиомочевину или ксантогенаты и продукты алкилирования посредством подкисления или гидролиза переводят в тиолы. Ароматические тиолы предпочтительно получают восстановлением хлорангидрндов сульфокислоты.
В качестве циклической мочевины и ее производных можно применять, например, Г 1 нн .нн
45
Яй ИН
40 (этиленмочевина) (и ропиленмочевина1
50 (бутиленмочевина) - «о о«« с«, 9 нн нн нн,нн нн нн
: II iI П
60 0 О О
559646
О
II щ « щ (ацетиленмочевина, HN @NH
II
О
Г 3
НИ«И-СН ;, — C H
О
tl tt
О ОГ 1 в — a,,; н
О О !
Э 35
О
Из соединений, содержащих карбоксильиые группы, формулы 1 можно получать, соли путем взаимодействия с неорганическими или органическими основаниями. Прй получении солей щелочных 40 и щелочноземельных металлов, в особенности солей калия, натрия и кальция, целесосйразно применение растворенного в спирте алкоголята.
Пример 1. 35 г и-толуолсульфинкислого натрия, 00 мл воды, 30мл муравьиной кислоты 45 (85%.нв4) и 20 мл формальдегида (39 .нвй в воде в течение 3 час перемешивают при 40 С. Затем к прозрачному раствору добавляют 16 r этиленмочевины и перемешивают еше в течение 10 мин при 40 С и еше в течение.2 час при 10 С. Прибли- 50 зительно через 10 мин после добавки этиленмочевины кристаллизуется продукт в виде бесцветных игольчатых кристаллов. Получают 38,5 г (76% от теоретического) соединения формулы
so,-сн,- NB
6 с т.пл, i 58" (разложение) .
Пример 2. 24 г 3,№-дихлорбенэолсульфинкислого натрия, 10 г этиленмочеяины, 75 мл воды, 200 мл муравьиной киелоты (85 »ная) и 15 г о-хлорбензальдегида, размеши я при 40 С, растворяют до прозрачного состояния. По истечении 5 мин начинается кристаллизация. Смесь перемешивают еще в течение получаса при 40 С, охлаждают до о
10 С и отсасывают. Промывают небольшим количеством воды. Можно перекристаллизовывать из изопропанола. Выход продукта 32 г (77% от георетического) соединения формулы с т.пл. 161 С, Пример 3. 10 г пропиленмочевины, 40г глиоксиловой кислоты (45%-ная) в воде, 20 мл воды и 10мл муравьиной кислоты (85% ная) в течение Зчас перемешивают при 80 — 85 С, Затем охлаждают до 40 Си добавляют раствор из 40 r п толуолсульфинкислого натрия (избыток) s 150 мл воды и 50 мл муравьиной кислоты (85 o-ная). о
Смесь размешивают в течение 5 час при 40 С, добавляют еще 15 мл соляной кислоты (25%-ная) и охлаждают до 10 С. После выдержки в течение ночи выкристаллизовывается вещество. Его отсасывают и промывают 100 мл ледяной воды. Вещество можно перекристаллизовывать из изопропанола.
Выход продукта 30 г- (58% от теоретического) соединения формулы
Î -GV-И!
N-СК- SO
СО,Н о Со,н
Вещество хорошо растворяется в водном растворе бикарбоната натрия.
Пример 4. 25 r 3,4-дихлорбензожульф лнкислого натрия, 50 мл воды, 50 мл муравьиноь. кислоты (85 o-ная) и 15 г 50 o-ного раствора диоксиметилэтиленмочевинь| в течение 3 час размешивают при 50 С. По истечении 20 мин начинается о кристаллизация. После охлаждения до 10 С и выдержки в течение ночи отсасывают бесцветные игольчатые кристаллы соединения формулы
Cf
Cf / 3 so2 Сн,-N -сн вО, с
/ с т. пл. 210 (разложение) и хорошо промывают водой. Можно перекристалпиэовывать из пйоксана.
559646.7 выход продукта 22,6 г (87,5% от теоретического).
СоФдииени» формулы R 802 СН вЂ” Я
R$
Температура плавления, С вЂ” сн сн он
102 сн сн он
102
Таблица 2
/Z
®2 н 3 l
О
Температура плавления, О
188
-Снг СНг
190
--СН,-СН,—
Cl — СНг — СНг— Н
116
-сн -сн—
148 сн a-cHf
158
-СНг -СНгCl
161
Н., С1 н сн 3 н
О
cv — ® 3
Аналогичным способом получают соединения, приведенные в табл. 1-4.
Таблица 1
559646
Иралалженне таблнны
Темпе ра ту ра нлаялеиня, с я яэ
-сн,-сн,—
15О
06Н3 -сн,-сН,—
148
О НЗ
Таблица 3
Соединениа формулы Г
К вЂ” So< — н — я я — сн — 8o — к
Температура нлаиления, б
-сн,-б-он, 160 (разложение) 175 (разложенне) — сн — сн—
-сн, --сн,—
180 (разлеже;ене) -Со,н
127 (разложение) — сн — сн — сн210 (рааложенне) 148 (разложение) -Сн -СНз—
С1
СН3
СПАЙЗ
206
-сн, --сн,—
-сн — СНz
141
559646
Таблица
Соединение формулы
 — 8o> — сн — нн — соо — " — ooc — ин — сн — so к
R1 К1
Температура плавления, С сн,/
-(СН?) 2СН, 174 (разложение) СН сн -с" сн
2 4 3 сн
180 (разложение) (СН2 ) 6
140 (разложение) — (CH2) 6
163 (раэложение) 154
СН -СНФормула изобретения
Тираж 833
1lH>>WIH Закяз 1341/l l5
Подписное филиал! 1ПП Патент, r. Ужгород, ул. Проектная, 4
Способ получения сульфонильнмх соединений общей формулы X й-$02-Х
r где R — арил, аралкил, гетерил, циклоалкил с
4 — 8 атомами углерода, влкил с 1 — 8 атомами углерода, Х вЂ” радикал — С Н вЂ” Я(2
2-1 Z — СН вЂ” N N — R ;, г
R1 11
0 бЕ, — СН вЂ” М И вЂ” СН вЂ” go — я, 1 с
1) R
-СН-ИН-СОО-У-00C-NH-СН-60 -М
1 1
Я, Я1
R 11„ — водород, арил, аралкил, гетФрил, с циклоалкил с 4 — 6 атомами углерода, алкил с 1 — 8 атомами углерода, карбоксил, карбоксилат;
R2, йа — арил, аралкил, циклоалкил с 4 — 6 атомами углерода,алкил с 1-8 атомами углерода, фенил, иафтил, бензил, фенэтил или R2 — водород;
У вЂ” алкилен, циклоалкилен, арилен;
Z.— алкилен, оксиалкилен илн
-СН-СН-
ИН ИИ
4S с
И
О отличающийся тем, что сульфиновую кислоту подвергают взаимодействию с соот50 ветствующим альдегидом, а образовавшееся при этом оксисульфонильное соединение — взаимо,действию с тиолом, или циклической мочевиной, нлн производным мочевины, илн соединением общей формулы И .И
Н и — СОΠ— Y— - 00C NH?
2Р где У имеет указанное значетпте, с последующим выделением целевого продукта известным способом,