Способ получения замещенных кетокарбоновых кислот
Иллюстрации
Показать всеРеферат
ОП И
ИЗОБ
Союз Советских
Социалистичаских
Республик (61) Дополиительн (22) Заявлено 02.0 (23) Приоритет(31) 5001 9-А/74 (43) Опубликовано (45) Дата опубли
Гесударстаонный комитет
Соввтв Министров СССР оо делам изоорвтвннй и открытий (72) Авторы изобретения
Иностранцы
Джорджо Боттаччио, Джан Паоло Къюзоли и Марчелло Марки (Италия) Иностранная фирма
"Монтэдисон С.П.А" (Италия ) (71) Заявитель (54)- СПОСОБ ПОЛУЧЕНИЯ ЗАМЕШЕННЫХ КЕТОКАРБОНОВЫХ
КИСЛОТ
Изобретение относится к получению кето карбоновых кислот, которые могут быть ис» пользованы в производстве косметических препаратов, растворителей для нитрата целлюлозы, смол, лаков и т.п. б
Известны различные способы получения кетокарбоновых кислот, например, формулы.:
Я вЂ” C — С Н вЂ” CO0H
ll
0 R (н 10 где Я и К вместе образуют циклоалкиленовые кольца, карбоксилированием соответствующих кетонов двуокисью углерода в присутствии триметилфенолята, щелочного металла (илн крезолята) в среде полярного растворителя, например диметилфоомамида или диметипсульфоксида при 0-100 С (1.) .
Другой способ получения кетокарбоновых кислот основан на взаимодействии гидроперекисей циклоалканолов с альдегидами в окислительно-восстановительных условиях с последующей экстракцией 2 J., Однако в первом случае применяются растворители, смешиваюшиеся с водой, что
9 ведет к усложнению разделения и выделения целевого продукта. Во втором случае необходимос сь применения перекисей, экстракции и других приемов разделения и выделения
О целевого продукта приводит к его небольшому выходу (9-25%), а также вносит определенные технологические трудности для обеспечения взрывобезопасности процесса.
Известен также способ получения кетокар« боновых кислот путем карбоксилирования соответствующих кетонов, имеющих активный атом водорода, с помощью двуокиси углерода и фенолята щелочного металла.
По этому способу получают кетокарбоном вые моно- или дикислоты алифатического или аралифатического или циклоалифатичесо кого ряда. Процесс ведут при 0-100 С в среде биполярных апротонных растворителей 3 .
° ° ри осуществлении такого процесса обеспечивается высокая конверсия (80-99%), но по выходу и чистоте целевого продукта не достигают таких же высоких показателей из-за трудностей, возникающих при раз581859 делении смешивающихся с водой растворителей.
Для упрошения процесса предложено в качестве растворителя использовать другой .растворитель-алифатический, ароматический или аралифатический углеводород, т.кип. 80.
250 С.
Это позволяет получать кетокислоты.фьр мулы I или И
-О
Е1 !1 С вЂ” С вЂ” R.3 (Х)
R j
699Н
О
Rg j) И с-с-с» z к, !
СООН СООН!
5 где Я,ЯR,Я»,, Я -независимо друг от друга .представляют собой водород, алкил С»-С > арил или:R и R5 вместе образуют углеводородную алкиленовую цепь разветвленного или нормального строения; 25
R -алкил С вЂ” С, арил, О-алкил, О-арил, когда R» -арил, с лучшими: выходами и чистотой чистота 99%, выход 39%, а в известном щ способе (3 ) соответственно 90 и 37%.
B результате использования несмешиваю шихся с водой растворителей последние легко отделяются и выделение целевого продукта возможно одной экстракцией. Образую- 3s шийся в процессе фенол в органическом раст воре цреврейается в соответствуюший фенолят и рециклизуется в стадию карбоксили PoBBHKH
Кроме того, вместо незамешенного фено- 40 пята щелочного металла в процессе целе сообразно использовать его фенил или моно-, .ди-, и триалкилзамещенные, причем алкильные заместители могут быть "нормального .или изостроения и находятся в орто-, мета- 4 или пара-положениях.
В чроцессе целесообразно использовать исходные кетоиы формулы! Ц или И
К .. GH- G —, (щ) Rg
Ry I Rq
СН вЂ” С вЂ” СН. (K>
И. R$ где Р»- В f имеют:указанные значения, и замешенный или незамещенный фенолят щелочного. металла при мольном соотношении 1:1-4, В качестве растворителей целесообразно использовать толуол, гептан, триметилбензол или м вЂ,диизопропплбензол.
При осушествлении данного процесса можно также готовить предварительно раствор фенолята в органическом растворителе.
Пример 1. Берут 6,7 г 2„6-диберег,бутил- -крезолята калия в 50 мл толуола и загружают в колбу емкостью
100 мл, снабженную мешалкой, термометром и газовводной трубкой, . и в атмосфере СО вводят 3,1 г ацетофенона (мольно6 соотношение крезолята и кетона равно 1:1), Реакцио онную смесь перемешивают 4 ч при 20 С, затем подкисляют.холодной 10%-ной серной кислотой, отделяют органический слой и экстрагируют его 10%-ным раствором бикарбоната натрия. После подкисления экстракта ° из него экстрагируют эфиром целевую кис.лоту -бензоилуксусную (0,8г). Кроме того. из органической фазы выделяют 2,3-ацетофенон.
Осушествление процесса при разных температурах и использование. других исходных продуктов ведут аналогично.
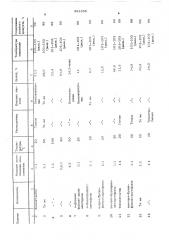
Условия и результаты представлены в таблице, при этом время процесса — 4 ч, конверсия — 25,8%; селективност ь — 8 2,3%, о т.пл. 10-103 С (разл.); кетоглутаровую кислоту (пример 6) получают в виде соли, а бензоилуксуснач кислота (примеоы 10.—
12, 16) содержит кристаллизационную воду.
ggyggo
cD а Ж Ж ж а
1 р ) о
1 о
Я о т щ
В. о
03 б) о —. o
1-1 С
А Ак
O- O—о
Ж
O л
С Н
Т !!
03 о
С!
С!
CO
Ч с1
Е!
Й
fQ м
C x
L" о
М
g !
» е
С-н! о !
>ъ
О (-
1 I
I !
1 о
СJ
<Ц
1 а Ъ
Э 03
2 (ц ао
4 Т 1
Ф" -1 (Q т!
С|о
Ф
1 Ф х
l
c;i
1(Q Ф
Ф
М о
О
C-< а
Р
Ы а
& ,Ъ, а
О (ч
rA и
Ф
0»
1
О
О О
Ф (D
О ж
° Ь
A Ф
3 о ,«» Ж м
Ф
6.)
Д о ! и
2!
Ф
М
Я ж
Ф х (-с
g !
Ф
" «з.
М л ъ
О и ж
Ф о а
1- о р Q>
1 с
1.И
О о «ф
Р со
Ф
l5
Щ
1-! (Ц
I а о 1
О
О
А Ф
С.
У ф
И .1
Q; а (м
С, Y
С ) Р о о1-1 г-!
° Ч %-4
O O
1 о ф З,д !
"- О ж
«Ъ,Я. !!!
К о к
Ф е а Й
Ж Ф л—
А
O"- O—
° 1!
I а
Ъ !
1"
„1 Ф е о
О
Ж о а,е !О о о о л1 Я
Рч
И.8.
1ч я Ф
Ф & а к
С» о
581859
2, имеют указанные значения, Составитель 1 . Лндион
Редактор Т. Загребельная ТехредН. Анцрейчук Корректор А, Лакнда
Заказ 3940/2 Тираж 553 Подписное
ЦНИИПИ Государственного комитета Совета Министров СССР по делам изобретений и открытий
113035, Москва, Ж-35, Раушская наб., д. 4/5Филиал ППП "Патент,. г, Ужгород,. ул, Проектная, 4.
Формула изобретения
1. Способ получения замешенных кетокарбоновых кислот обшей формулы I или 9
О
3.1 к 0 — С вЂ” R (Х)
С 00Н (М1. i! Ь (,— Q —,, Б
Rg i Rs
СООК ОООН 2, Я,, R независимо . друг
От друга представляют собой водор д, а
О
ii сн — с — z. (m)
Rg с помошью двуокиси углерода и феноляга щелочного металла при 20-100 С в срео це растворителя, о т л и ч а ю ш и и с я тем, что, с целью упрошения процесса, в качестве растворителя используют алифатический, ароматический или аралифатический углеводород с т. кип. 80-250 С.
2. Способ по и, 1, о т л и ч а ю ш и йс я тем, что в качестве фенолята щелочного металла используют его фенил или моно. ди- и триалкильные замешенные, причем алкильные заместители могут быть нормального или изостроения и могут находиться в орто-, пара или мета- положении.
3, Способ по пп, 1 н 2, о т л и ч а юш и и с я тем, что, в процессе используют соединение формулы )Tt или Й и замешенlIbN или незамещенный фенолят щелочного металла при мольном соотношении 1:1-4;
4.. Способ по пп. 1-3, о т л и ч а ю— ш и и с я тем, что в качестве растворителя в процессе используют толуол, гептан, триметилбензол или м диизопропилбензол.
Источники информации, принятые во внимание прп экспертизе .
1. Заявка ФРГ % 1668378, кл. С 07 С 59/32, 1973.
2. Патент США % 3197488, кл. 260-347.3, 1965.
3, Bottmccio 6 и др. Органические синтезы в растворителях. Карбоксилирование двуокисью углерода в апротонных диполярных растворителях, Оо z 2 е tt а
СВеа1 са Ма 1 3 а д сх, 103, ". 105116. 19 3.