Производные 6н-дибензо пиран-6-она и способ их получения
Иллюстрации
Показать всеРеферат
ОПИСАНИЕ
ИЗОБРЕТЕНИЯ
Союз Советских
Социалистических
Республик
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ (61) дополнительное к авт. свид-ву (22) Заявлено 02.0975 (21) 2168594 /23-04
С ПРИСОЕДИНЕНИЕМ ЗаЯВКИ РЙ— (23) Приоритет—
Гаардаратввнный номнтвт
Соввтв 1йнннатрав СССР на,двнвм нвабрвтвннр н отнрытнй (43) Опубликовано о 502,78.Бюллетень р(х (45) Дата опубликования описания 020278 (72) Двторьв изобретения
Pl) Заявитель (54) ПРОИЗВОДНЫЕ 6Н-ДИБЕНЗО-(0,Д) -ПИРАН-6-ОНА-ПОЛУПРОДУКТЫ В СИНГЕЗЕ КРАСИРЕЛЕИ
И СПОСОБ ИХ ПОЛУЧЕНИЯ
2 своей структуре они отличаются от известных соединений бифенильного ряда (11 наличием одного или двух ! лактонных мостиков. в 0,0 -положениях бифенильного ядра. Поэтому данные. соединения копланарны и на их основе можно получить дис- и ттолиазокрасители, обладающие повыщенным срод твсм к волокну. Данные соединения т0 могут быть частично использованы для замены бензидина и его производных, обладающих сильной канцерогенностью.
Спссоб получения производных 6Ндибензо- t b, о 1 -писан-6-она состоит
IS в том, что 2 -нитрозамещенную бифенил-2-карбоновую кислоту нли ее соль общей формулы
ХООС БОв
Ф и
Изобретение отно"ится к новым ароматическим лактонам и способу их получения, а именно к производным 6Н-дибенэо- ((), g j -пиран-б-она, которые могут найти применение в синтезе новых органических красителей.
Производные .6Н-днбензо- (т1,$$» .
-пиран-6-она общей формулы н
0 где и н ЯЗ вЂ” Н, НО.- и и М вЂ” Н, СООН или
1 образуют группу - -С - О- 20 о
0 причем Й =И,= к -> Н быть не может, и способ их получения в литературе не описан
Данные соединения могут быть использованы в качестве промежуточных продуктов в синтезе красителей, причем красители на их основе обладают повышенной светостойкостью (4-6 баллов) и вытнраемостью (60%). По 30
01 R2 где к и "З вЂ” Н,ко
R и R — Н 802, СООХ, причем ,1
I(=тт =R =тт = Н быть не может, Х-Ет
1 2 3 или катион металла, нагревают прн
130-330 С, предпочтительно в среде органического полярного растворителя.
Г. И. Мигачев, A. М. Андриевский, A. Н.Поплавский и Н. С. Докунихин
591473
Известный способ получения лакто. на 2-оксифенил-2-карбоновой кислоты, основанный на реакции- окисления дифеновой кислоты перекисью водорода в среде серной кислоты (2 1, существенно отличается от предлагаемого способа тем, что в данном случае найдено новое, неожиданное превращение
6-нитро- и 6,6 -динитроэамещенной дифеновой кислоты. l0
В основе этого превращения лежит внутримолекулярное нуклеофильное замещение нитрогруппй. Предлагаемый способ прост в использовании и позволяет получить целевые продукты с высоким выходом.
В качестве полярного растворителя применяют диметилформамид,. диметилсульфоксид, хинолин, ацетамид. диметилацетамид и другие 20 растворители. Когда исходное сырье нагревают без растворителя, применяют преимущественно натриевые или калиевые соли используемых кислот °
II ри мер 1. 3 r 4,6,4,6 —
25 тетранитродифеновой кислоты кипятят в 30 мл диметилформамида до прекращения выделения окислов азота, охлаждают и выливают в 250 мл во ды. Выпавший желтый продукт от- 30 фильтровывают, промывают водой и сушат. Получают 2,26 r (97%) 2,7динитро-6,10-диоксо-4,9-диоксапнрена, т. лл. 331-332ОС (желтые иглы из диоксана)р Я 0,6 (бенэол) .
Найдцнс, Ъ: С 51,61; 51,88;
П 1,37; 1,52; К 8,40 ; 8, 60. с14н4 М;Оа
Вычислено, Ъ: С 51, 23; Я 1, 23;
8.64. ИК-спектр (КВp) см : с. 3090, с. 1780 (СО), с. 1625, с. 1550 (.НС ), сл. 1460, ср. 1420, с. 1370, с. 1350 (ЙОэ), с. 1315, с. 1210, сл, 1155, с. 1120, с. 1090, ср. 1020, cp. 980, сл. 930, ср. 915, с. 820, ср. 775, с. 745 с. 720.
Пример 2. 3 г 4,6,4,6 - тетра нитродифеновой кислоты кипятят в
25 мл диметилсульфоксида до прекращения выделения окислов азота. Далее реакционную,массу обрабатывают аналогично; примеру 1 и получают 2,2 r (953) 2,7-динитро-5,10-диоксо-4,9фиоксапирена, т. пл. 331-332 С.
Пример 3. 0,2 г калиезой соли 4,6 6 -тринитродифенофой кислоты нагревают в сублиматоре при 210 С и остаточном давлении 2-3 мм рт.ст.
Через 30 мин обогрев прекращают и получают в качестве сублиматора
0,06 г 2-нитро-5,10-диоксо-4,9диоксапирена, т. пл. 260-261 С (из бензола); М О, 56 (бензол) .
Найдено, %: С 59,43; 59,88;
Н 2,05; 2,09; и 4,77; 4,80.
С14Н Иоь«
ВычисленО, В: С 59,37, H 1,78, и 4,95.
ИК-спектр (KBp) см : 3095, 3070, 3055. 1760, 1610, 1540, 1480, 1450, 1425 1350, 1335, 1300, 1255, 1200, 1130, 1090, 1080, 1060, 1030, 1010г
945; 920, 830, 820, 790, 760, 745.
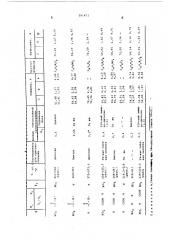
В примерах 4-11 получают соедине" ния, .свойства которых приведены в таблице..
591473
«Ф
iCL
С0
Г Ъ
CO с
1 »
\ л м
С0 с
4 о
4 с
ГЧ 0
Г Ъ
\ м о
Ю с о
Г»
Г«1
ГЧ
iCL
ГЧ
ОЪ с
Ю
ОЪ
1 » м
«
Ch
СГЪ
Г 4
ОЪ с
Ю
О ) Ф
LA с
° э
ОЪ и о
М, l» х
3 4
Х
З
Cj х и
r- o
I» C0 с
«3 Ф (»4 О
«Ф «I
С0 С0
«ф л
Г ГО с
ОЪ ОЪ Ф Г
С0 (О с
«1 «Ф а1Ъ Со
4 Г4 с
CCj Г0
ЮЮ
cl 0
С0 00 л м
ГО CJl с с
«I
СО Г
ОЪ O с
W C«4
М 10 о Ъ ИЪ с
Г«1 М («4 ««
М «I с с
ГЧ ГЧ
C«I «3
4 л с
ГЧ (4 iO
Г » CO с с
ГЧ ГЧ
14Ъ ОЪ оо с
Г«1 С 4
1 ГЧ м Оъ с с
i «\
4 Ъ ОЪ 0 1 с
СО ОЪ иЪ 44Ъ
«4 1Д>
Ch (»4 с
ОЪ Ю iO I»
C 4 Г
C0 Ch с. с
ЮЮ
44Ъ СГЪ
° 4 Ю
Оъ Ch с
Ю Ю
LA LA
Оi Г»
Г Ъ «Г с с
«Ф Ф
ОЪ С4Ъ
14Ъ 4Ъ
У ГГЪ с
ОЮ
Г м ш
«Ф CO с с
О\ ОЪ
0Ъ СГЪ
СО
«й 0 с с л л
У ОЪ к о х
Э
6 о х <Съ I
Г4Ъ ХЛ
C»I ф
СГЪ
14Ъ
Ф
ГЧ с
LO с
«й с о
LCL с
Г«4 с
Ю и
Щ и
Х о к о х
Э
1
Ю
1 4
С4 о х о к
С 1 о м о
С4 м х о о и.1.СЭ
o=u
С4 г
» »i
СГ х х ж о о ,о о . u u х х х о о и
СР «и
I х о о я g о х о х
IIj к
z
Щ о к
4;ь
f i,С.
>, n. а,о
1Д & с о
Э
Ц
tg
61 х
Ф о х х
Ф х о
1 ф о о с х о о а
f» X о ф х
И х 0)
«4
lCI 1 х и
O, A а ах
0) х
4«н иХГЪ
is о
С4 л
«С х
Lj х о х
Р
4«4 м
ГЪ К
СС4
ftj o.
Г"l
Ю
Ю.=Г >
С4 о
М
Х
t) dL с
Г»4
Г м
ГЧ С"Ъ
CCI о
Г«
М .0
«С
4 и
Х б к н оо
v r„
Ik
Ф ЪС х
I CC дР П1
ГГЪ с
С0 4 "Ъ
Г4 1
ОЪ пъ CCI м 0
С»4
Г
° т
Г«4 I
CCj
С7 41
° а 04
ГЧ
0L
Г»4
4Ъ К и
43
«»4
0 о
Х
-0 х
4 Ъ
Г«4
1 о
Г«4 о
С« и
-0
Х
i0 а3
Ч о
1 Цм
dP I ° °
ГГЪ ХЛ
CIj о и
Ф Х х
Ф дР CCI
LA с
ОЪ
Г Ъ (3 1«
C4I
4СЪ Clj
Г«Ъ Д4
591473
Для тонкослойной хроматографии используют пластины Si1мfoE МО 254. . Пример 12 ° 2,38 г 5,10диоксо-4,9-диоксапнрена растворяют в 20 мл 5%-ной щелочи, добавляют .5
25 мл спирта, затем 303-ным раствором уксусной кислоты доводят рН до 8,5. 4,8г 4-нитроанилина диаэотируют рассчитанным количеством нитрита натрия и полученный раствор I0 диазосоединения приливают по каплям к раствору 5,10-диоксо-4,9-диоксацирена, . поддерживая раствором соды значения рН 8-8,5. Получают оранжевый краситель, ко,торый отфильтровывают, промывают ,водой и сушат при 60 С. Краситель окрашивает поливинилхлоридную пленку в оранжевый цвет.
, н 2- Н, СООТГ, или образуют группу -..ОХООС
Ж гдеА Я>-НИ02, К ий1-HH02,,COOÕ, прнчемЯ = ki = Rz = Rp "-Н быть не может
Х=Н или катион металла, нагревают при
130-330 С.
3 Способ по и 2 o b л и ч а ю— д5 шийся тем, что процесс ведут в присутствии органического полярногс растворителя.
Источники информации, принятые во внимание при экспертизе:
1. Венкатараман К., Химия синтетических красителей, Л., изд. Хим.
° литература, т. 1, с. 531, 1956.
2. Патент CIIIA Р 3106567, кл, 264 34, 1963.
Формула изобретения где К и R — Н, нОа
Составитель Р, Марголина
Редактор Т. Шарганова Техред Н.Андрейчук Корректор Е.Папп
Заказ 528/21 Тираж 559 Подписное
ЦНИИПИ Государственного комитета Совета Министров СССР пб делам изобретений и открытий
113035, Москва, Ж-35, Раушская наб, д. 4/5
Филиал ППП Патент, r. Ужгород, ул. Проектная, 4
1. Производные 6Н-дибензо-;.Ь.Ю„
-пиран-6-она общей формулы а, я причем Я = Ф, = Rq- R = Н быть не может, — полупродукты в синтезе красителей. 2. Способ получения соединений по п.l, отличающий с я тем, что 2-нитрозамещенную бифенил-2-карбоновую кислоту или ее соль общей формулы