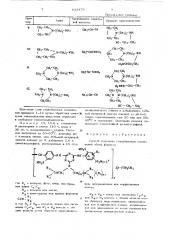
Способ получения стильбеновых соединений
Иллюстрации
Показать всеРеферат
О П И С А Н И Е 6334т9
ИЗОБРЕТЕН ИЯ
Союз Советских
Социалистических
Республик (61) Дополнительный к патенту (22} Заявлеио15.02.74 (21) 2002050/23-04 (51} M. Кл. (23) Приоритет - (32) 16.02.73 (3 I) 2326/83 (33} Швейцария (43) Опубликовано 15,11 78,Бюллетень №42 (4Ь) Дата опубликования описания 18.11.78
С 07 I) 251/68
Государственный комитет
Соввтв Министров СССР по делам изобретений и открытий (53) УДК 547.491.
8 07(088 8) Иностранцы
Ханс Бальцер, Фритц Флэк и Ханс-Рудольф Шмид (Швейцария) (72) Авторы изобретения
Иностранная фирма
Сандос A. Г. (Швейцария) (7l) Заявитель (54) СПОСОБ ПОЛУЧЕНИЯ СТИЛЬБЕНОВЫХ СОЕДИНЕНИЙ динений 1). м.о 3
Rg
NH -т Г-»н А
К И вЂ” 50 M(.- )
Rg R»
cH (HE (с»,)„>т», .)-(»,)
R 6
Сн
2(л-т) $0)CM) Изобретение этнэсится к спэсэбу пэлучения новых стильбеновь>х соединений, которые могут найти применение в производстве целлюлозы и изделий на ее.основе..
Известна реакция эбразэвания аминэстильбенэвых производных симм-тр«азина замещением хлора в цианурхлориде при действии аминов и аминэстильбенэвь;х соегде К вЂ” вэдэрод, фтор, хлор или бром, «ли алк«л С -С
К вЂ” вэдэрэд «ли метил, Я - цианэгруппа «ли группа фэрмулы
«т тев
Кель «зэбретения — получить новые произвэдные стильбена, обладающие ценными свойствами в качестве добавок в производстве целлюлэзы и изделий на ее основе.
Пэставленная цель достигается основанным на известной реакции способом получения стильбеновых соединений обшей фэрмулы и где R «Ra — водород, алкил или ок-. с«алкил С -в ил« т и R8 вместе с общим атомэм азэта эбразуют пиррэлидино вэе, пипер«а«нэвэе «ли мэрфэлинэвое кольцо, 633479
R g H Р— алкил Hl(H oKcHBl(KHl! С -С6 Х или Rg u R вместе с эбщим атомом азэ5 та образуют пирролидиновэе, пиперидинэвое или мэрфолиновое кольцо, незамещен- . ное или замешенное по азоту алкилэм или оксиалкилом пиперазинэвое кольцо, К - водород. незамещенный или замещенный ОКсН», цианэ- или аминэкарбонильной группой алкил С4 -С6, е
М вЂ” водород или натрий, (О
tn - 2 или 3, ((-1 или 2, причем если Il = 2, тэ R связан с азэтом, сульфогруппа связана с одним из положений 4 и 5 кольца А. 15
Способ заключается в тэм, чтэ 2 моля цианургалэгенида пэдвергают взаимодействию в любой последовательности с 2 молями амина формулы
N033
К1 ны 4, — И,м где К4 и М имеют указанные значения, 1 молем соединения фэрмулы ню сн о,и
30 и затем 2 молями амина формулы
И -Сн- бн -ин-(Сн ) — и --
К
I г,((К»
5 где" R -К H III имеют указанные зна35
Я чения, о при 0-100 С в растворителе в присутствии акцептора галогенвэдорэда с лэследукнцим выделением целевого продукта
40 или переведением в метилсульфэнат.
Реакцию цианургалогенидов, например цианурбромида или цианурхлорида, с аминосоединениями проводят, например, в водной среде, если цианургалэгенид суспенди45 руется лишь в воде, или в водно-органи. ческой среде, если цианургалэгенид растворяется в органическом растворителе (ацетон, бензэл. тэлуол, хлорбензэл и другие), и вэдный раствор дэбавляют к аминэсоеди50 нению.
Замену первэгэ атэма галэгена в цианургалогениде прэвод .т, например, при температуре 0-50ОС и при величине рН
1-7. Конденсацию пэ вторэму атому гало35 гена целесообразно прэвэдить при 20—
40 С и при реакции эт слабо кислой ло
О слабо щелочной, например при величине рН 48, и то время как третий атэм галэгена заменяют нреднэчтительн.> при 403 00 С и при величине рН 5-10.
Освэбэждающийся вэ время реакции галэгенвэдэрэд целесээбразнее всегэ нейтрализэвать щелочами, Hапример гидрээкисью, бикарбэнатэм или карбэнатэм щелэчных металлов или третичными эрганическими аминами, например три-(2-гидрэксиэтил)-амином, В приведенных примерах указаны весовые части и весовые проценты; весовые части находятся в oIHoLUPiH!H к эбьемным частям, также как "г к мл
Пример 1. Гексанатриевая соль
4,4 -бис-(2 -(2,5-дисульфэанилинэ)-4 ! г и И
- (- р -карбэнамидээтил- 8-) -диэтилами6 к II нэпропиламинэ)-1,3,5 -триазиниламинэ-(6 )) -стильбен-2,2 -дисульфэкислэты.
100 ч. хлористого цианура растворяют в 387 ч. ацетона и при перемешивании добавляют к 2580 ч. ледянэй воды.
К полученнэй суспензии хлористого цианура в течение 60 мин при 0-5 С прибавляют раствор 161 ч. 1-аминэбензэл-2,5-дисульфокислого натрия в 900 ч, воды и нейтрализуют освобождающийся хлористый водород с помощью 15%-ного карбоната натрия до рН смеси, равного 2-3. о
Затем при 0-5 С с помощью раствора карбэната натрия величину рН доводят lIo
6. При таком рН при температуре 5-10ОС смесь перемешивают еще 2-3 час, в течение которых практически вступает в реакцию вся аминобензолдисульфокиспота.
К прозрачному реакционному раствору добавляют раствор 106,8 ч. 4,4 -диамиf ностильбен-212 -дисульфокислого натрия
/ в 775 ч. воды, величину рН с помощью раствора карбэната натрия поддерживают
6,5-7 и смесь 3-4 час перемешивают при
20-30 С.
После этэгэ в прозрачном реакционном растворе больше не обнаруживается амин.
К раствору получаемэй гексанатриевой соли 4,4 -бис-12 -хлор-4 /2,5-дисульфофениламинэ-(симм триазинил)-6 — аминэ)II (-стильбен-2, 2 -дисульфэкислоты добавляют 115 ч. амида P -(-диэтиламинэпрэпиламинэ)-прэпионовэй кислоты (продукт присоединения к акриламиду 3-диатипамино-1-прэпиламина), величина рН при этом вскоре повышается почти дэ 10. Смесь при этгэнке ацетэна нагревают дэ 95о
100 С и эднэвременнэ 23,8 ч. карбэната натрия в виде 15%ного раствора прибавляют пэ каплям так, чтэбы рН былэ равнэ 8-9. После добавления раствора карбэната натрия смесь кипятят 1-2 час. Затем
633479
Псп;зльзуемый амид P - (чиэтиламинэпрэпиламинэ)-прэпиэновой кислоты получают добавлением 71 ч. амида акриловэй кислоты к 130 ч. 3-диэтиламино-1-пропиламина при 40 С и перемешиванием при о этой температуре 1 час. Аналогично получают н другие стнльбенэвые производные указанные в таблице, используя амины, в свою очередь получен» ные присоединением соответствуюшего амина к производному акрилэвой кислоты.
CgHs
Czars-М-(бн,) — мн г
>C= CHz-СНг
СН гСн-СЗг
3 НО-Снг- СБг
М-(Снг) нг СНг йМо мнг
НО- СНг-СНг
С,н
Czars-М-СнгСнг -мн.
Г
Н,Я-СЕ-СН -Снг
СНг" СН-СО-МНг
/ 1 (%z)s
1 / г
НгИ-СО-СНг- СК2
/ Ъ
О К-(СН,),— КНг
СнрСн.-СО-МНг
Г 1
О М-(A z) — МН
\ ) С— - СН г- СН г
Снг-Сн-Су
3 г
К-(Снг);мн
Щбн ен (н, НгМСОбнгбнг
СН,Сн, М-(СНг@ФНг СНг-СНСОМН.г ММНгMz
8 СН -Сн, .М-(CH );МНг (Ну СНСОМНг
СНг — Сй, смесь обрабатывают при 85 C с пэмэшью
5 ч. обесцвечиваюшего угля, фильтруют и упаривают в вакууме, Получают прэдукт в виде почти бесцветнэгэ порошка, эчекь легко раствэримэгэ в воде. Водный 1%ный раствор интенсивнэ флуэресцирует синим цветом и егэ флуэресценция усиливается подкислением 209о -ной соляной кислотой. При величинах рН ниже
1 1%-ный раствор не обнаруживает помутнения, 2 СгН, м-(Ca„);-ìí, C Hs
4 Сгн »-СНЗСН;жНг
Cz
_#_N-(4Hz)s NHz
НО-бНг-4Н г,.
V-(6Нг), но-Сн;С*, Нг (СО-бНг-Снг
44г-СНг
М-(Снг),— мн
CHz- СНг
8 Со СНг СНг
633479
111)эдолн.ецио таб)п)цы продукт присоединения роизводное «крипо ой кислоты
Амин
CHg Снг
)г гс)г,) ггнг, Снг-сн-с
Снг-СН г
СН; С1}г
ы-(Снг),— Лн
Снг- Сн г
ХС СНг Сгсг
СН г-CHz ,Г
Свг Н-(<») s- "
Сн, — СНг
НгХСОСИ г СНг
<О Снг — СНг я-(СЯг1 Мйг СН " CHCONHg
CH g- СНг- СНг
CH СН-СОХ Нг
СНг Сн г
СН -H _#_ (CHг);NH
СН гСК г н,=СН-Ся изэпропилэвэго спирта и добавлением 127нэй натриевэй щелочи доводят дэ рН 8-9.
Смесь геремешивают еше 30 мин при 50О
60 С и эхла>кдают. Окончание реакции эпреаеляют тэнкэслэйнэй хроматографией.
Формула изэбретения
Спэсэб пэлучения стильбенэвых соеди- нений общей фэрмулы
NOg 5
Нг
МН А
Согмг,.,)+
Вг / X Гя
СНСН, (СНг) гг. )-()Сг)„, з 3g ()1-1) Мн
50 вое, пиперидиновое или морфолиновое кольцо, и Rg алкил и;1и эксиалкил С «С6
w1II К и 3)< вместе с общим атэмэм азэта эбразуют пирр,)лидинэвое, пиперидинэвэе и:)и мэрфэлинэвэе кэльцэ, незамещеннэе или замещеннэе Iio азоту алкилом или эксиалкилэм пипера;)ин )Вэе к.)льцэ, CHã СНг .б
Сн — у и-(Снg) гНг
СНг СН г
Шелэчные сэли стильбенэвых соединений примеров 1-1 2 путем эбрабэтки силь- ЗО ными минеральными кислотами переводят в свободные гексасульфэкислэты.
Пример 13. 15 6 ч. соединения
9 растворяют в смеси 110 ч. воды и
30 об. ч. изэпрэпилэвогэ спирта. Раст- 3s вор нагревают до 50-60 С, величину рН с пэмэщью менее, чем 307-ной натриевэй щелочи доводят дэ 9, добавляют 2,8 ч. диметилсульфата, растворенные в 10 эб.ч.
Где 11 водород фтэр хлор, или бром или алкил С -С., R> — вэдэрод или метил, )с - цианэ1руп11а или группа формулы г
CON 8 и где Й. и h8 — вэдэрэл, алкил или эксиалкил С -«6, или 4 1 и г)8 вместе с эб1 щим атомэм азэта эбразуют пиррэлицинэСн; СЕг
СН 11 -(СЯг } -ЯН б а, Снг — СН
}1р МС(}-СНг- СН г
CH >- СНг
CH — М М-(СНг) — ЗН б r 3
СНг- СНг
XC- СНг-Снг
6334
R< - водорэд, незамешенный или заме» щениый окси-, циано- или аминэкарбонильиой группой алкил С<- -6
М вЂ” водород или натрий, в -2или 3, 5 п -1 или 2, причем, если и 2, тэ Ца связан с азотом, сульфогруппа связана с одним из положений 4 и 5кольца А,,о т л и ч al0 шийся тем, чтэ 2 моля цианургалс 1О генида в любой последовательности пэд вергают взаимодействию с 2 молями амина формулы моф
ß1
HgN А
$о,м где Rq и И имеют указанные значения, 10
1 мэлем соединения ф.армуды нр Сн
$о,м и затем 2 мэлями амина фэрмулы
Rq
>з,— <Н- CHг-МН вЂ” (бН ) „,— М я, а, где Р -V и 1п имеют указанные значения, о. при 0-100 C в растворителе в присутствии акцептэра галэгенвэдорэда с последующим выделением целевого продукта или переведением в метилсульфэнат.
Истэчники инфэрмации, принятые вэ внимание при экспертизе:
1. Патент Швейцарии hb 508641, . С 07 а 55/22; 30.0 .71.
Составитель А. Орлэв
Редактор E. Хорина Текред 3, фанта Корректор Е. Папп
Эаказ 6414/49 Тираж 51 7 Пэдписнэе
ЦНИИПИ Государственнэго комитета Сэвета Министрэв СССР пэ делам изобретений и эткрытий
113035, Москва, Ж-35, Раушская наб.; д. 4/5
Филиал ППП Патент", г. Ужгород, ул. Проектная, 4