О-тозиламинозамещенные 2,5-диарил-1,3,4-оксадиазолон в качестве органических люминофоров
Иллюстрации
Показать всеРеферат
Союз Советсинн
Социал истичесинн
Республни ())) 1
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ (6l ) Дополнительное к авт. саид-ву (22) Заявлено 20.05,77 (21) 2489697/23-04 с присоединением заявки М (51) м. к.
С 07 З 27 1/10
С 09 К 11/06
Гаоударстюпай квинтет
СССР по долаи изобретений и открытий (23) Приоритет (53) УДК 621.3. .032.35 (088. 3) ) Опубликовано 30.03.82. Бюллетень J4 12
) Дата опубликования описания 02.0.82
):,, ..",, E ц с.
Л 4
И. К.т - :.:-. - .:
5 ; .; . )- -, (72) Авторы изобретения
Б. М. Красовицкий, Л. Ш. Афанасиааи (7I ) Заявитель (54) О -ТОЗИЛ АМИНОЗАМЕЩЕНН ЫЕ 2,5-gjHAPH31 -1,3,4-ОКСАДИАЗОЛОВ B КАЧЕСТВЕ ОРГАНИЧЕСКИХ ЛЮМИНОФОРОВ
Изобретение относится к новым химическим соеаннениям, конкретно к 0-този" ламинозамешенным 2,5-аиарил-1,3,4-оксааиазолов, облвааюшим свойствами органических люминофоров.
Укаэанные соеаинения проявляют лю- минесценции аномально высокий сток овый савиг в rrpeaenax 11430-12330 см . Буаучи бесцветными при аневном свете, они как в твераом состоянии, твк и в органических растворителях флуоресцируют
l0 при облучении УФ-светом в виаимой области спектра.
Отсутсвие у этих веществ окраски при аневном освешении позволяет ввоаить их в цветные к ом по эицни бе з иск аж ения цвеl5 та послеаннх. Это свойство может быть использовано, например, при созаании люминесцентных марок и печатных красок аля автоматической сортировки писем, 20 аля соэаания коанрованных люминесцентными красками географических карт, аля люмннесцентной метки преаметов в криминалистике н т.п.
Наиболее близкими по структуре к новым соеаинениям являются 2,5-аиарил1,3,4-оксааиазолы 11), которые известны как эффективные органические люминофоры фиолетового свечения. Они применяются в качестве активаторов в жиаких и пластмассовых сцинтилляторах, используются как активные среаы в оптических квантовых генераторах, оанако из-зв коротковолнового свечения не нвхоаят применения в тех областях науки и техники, гае необхоаимы люминофоры бесцветные при аневном свете, но люминесцируюшие в виаимом аиапазоне алин волны.
Uemü изобретения - органические люминофоры с аномально бото шим стоксовым савигом в преаелах 11430-12330 см, а также расширение ассортимента органических люминофоров, люминесцируюших в алннноволновой области спектра.
Это постигается новой химической структурой О -тозиламинозамещенных
3 68
2,5-аиари -1,3,4-оксациаэолов, которая выражается общей формулой м102/ 1Н
Ю вЂ” К гае Ь " С6Н, 4-Bl" -С6 Н4, 4- CH -C6H4 4-СН О 634, 4-(Н9, 1-(оН
Указанные соеаинейия обшей формулы получабт слеауюшим образом.
0-Тоэиламиноэамешенные 2,5-аиарил1,3,4-оксациазолов получают конценса- цией соответствуюшего моноароилгиараэина с хлорангиариаом hl -тозилантрвни. ловой кислоты и послеауюшей циклоаегицратацией несимметричных циароилгиаразинов воаоотнимаюшими срецствами.
g -Тозиламинозамешенные 2,5-циарил-1,.3,4-оксааиаэолов являются органическими люминофорами с аномально большим стоксовым сцвигом. Они поглошают в той же области спектра, что и их аналоги - 2,5-пиарил-1,3,4-оксааиазолы, не соаержашие р- тозиламиногрупйы, а люминесцируют в значительно более алинноволновой области. Слецовательно, получают люминофоры, облацаюшие нева» кономерными цля 2,5-пиарил-1,3,4- окс апиа эолов с войс твами.
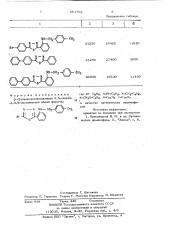
В таблице привецены спектральные характеристики преалагаемых люминофоров в хлороформе и аля сравнения аналогичных произвоцных 1,3,4-оксааиаэо- ла, не соаержвших O -тозиламиногруппу, при этом 0 — максимум цлинноволновой полосы, П.р и м е р 1 ° Получение 2-(2-този лам ин офени л) -5-фен ил- 1, 3, 4-окса аиа зола.
К раствору 1,4 г бензгицразина в
40 мл пирицина прибавляют в несколько приемов при перемешивании 3,1 г хлорангиарипа М- тоэилантраниловой кислоты. Смесь выаерживают 20- 30 мин о при 60 С, после чего охлвжпают и выливают в вопу.
Выпавший осааок отфильтровывают, промывают воцой цо исчезновения запаха пириаина и сушат. Полученный процукт кипятят с 40 мл хлорокиси фосфора в течение 1 ч 30 мин, выливают в леа, фильтруют, промывают воаой ао нейтральной реакции промывных воц на лакмус и сушат. После хроматографироввния бензольного раствора на окиси алюминия
1792 4 и нослеауюшей перекристаллизации из метилового спирта получают процукт с т. пл. 155-156 С. Выхоц 1,3 r (35%).
Найпено, %: С 64,52; Н 3,87;
Й 10,69; S 8,20.
Д6 К О Б
ычислено, %: С 64,62; Н 4, 10; и 10,77, S8,21.
4 рдкс поглощение в хлороформе
lð 31750 см;
4рлс1Кс люминесценции в хлороформе
19420 см; д 0 12330 см .
Пример 2, Получение 2-(2-то15 зиламинофенил)-5-(4-метоксифенил) -1,3,, 4-окс ааиазо ла.
Продукт получают аналогично проаукту, описанному в примере 1. Для реакции бе.— рут 1,66:г гиаразипа анисовой кислоты, 2р 3,1 г хлорангиарипа М -тозилантраниловой кислоты.
Выхоп 1,25 г (30%), т. пл. 173 С.
Найдено, %. С.62,67> Н 4,48>
М 10,09; 6 7,80.
25 С Н 9 13(»
Вычислено, %: С 62,71; Н 4,51;
Ì 9,98; Я 7,60.
4 к поглошения в хлороформе 31250 см; 9 a
Зр 19800 см в дМ 11450 см .
-1
Пример 3. Получение 2-(2-тоI зиламинофенил) -5-(4-топил) -1,3,4-оксааиазола.
Пропукт получают аналогично описанному в примере 1. Для реакции берут
1,5 г гицразиаа Yl- толуиловог кислоты, 3, 1 r хлорангиприцв N — тозилантраниловой кислоты.
Выхоа 2,15 г (53%); т. пл. 184185 С.
Найаено, %. С 65,23; Н 4.,57;
Й 10,39; » 7,90.
С22.Н19 3Оз S
Вычислено, %: С 65, 19; Н 4,69;
М 10,37 5 7.90. ) „роглошения в хлороформе 31750 см; 0 с люминесценции в хлороформе
19670 см; д 0 12140 см.
5Р
Пример 4. Получение 2-(2-тозиламинофенил) -5-(4-бромфенил) — 1, 3, 4-оксапиазолв.
Пропукт получают аналогично описцн55 ному в примере 1. Для ревкци:, берут
2, 15 r гиаразиаа 4-бромбензойной кислоты, 3,1 г хлорвнгицрица Я -тозилвнтрвниловой кислоты. -И сн, 31750
28570
3 180
С и—
3 1750 19420
12330
4220
31250 27030 н,сю ън- о б сн
31250
Н(0 Г
11450
19800
31750
27030
4720
3 1750
БС
19610
12 140
31750
3970
27780
5 68 17
Выхоа 2,2 г (46%); т. пл. 184 С, Найдено, %: С 53,81, Н 3,29; К 8,89;
Bi" 16,95; Я 6,68.
Cg„H 6Br
Вычислено, %: С 53,62; Н 3,40; 5
N 8,94; Вг17,02; 5 6,81. „роглошения в хлороформе 31280 см;
4,цК люминесценции в хлороформе 19420 см; ) 11830 см . о
Пример 5. Получение 2-(2-тозила мино фенил) -5-(4-бифенилил) - 1, 3,4-юксациазола.
Процукт получают. аналтично описанному в примере 1. Для реакции берут
1 н,ф
»-И, 6н, 92 6
2,12 г 4-6ифенилилгицразица, 3,1 г хлор ангицрица И -тозилантраниловой кис лоты.
Выхоц 1,7 г (36%); т. пл. 185 С.
Найцено, %: С 59,51j Н 4,66; 8,81; 6,73. с, н,„и,о
Вычислено, %: С 69,38; Н 4,49;
N8,99; S 6,85. О, сц<с поглошения в хлороформе
30960 см
4 с кс люминесценции в хлороформе
19530 см; д4 11430 см .
68 1792
Продолжение таблицы ян — й, 1н, 31250
11830
19420
3850
27400
31250
МН-$02 / 1нз
30960
1 1430
19530 и чн sO Сн, Составитель Г. Шагалова
Рецактор П. Горькова Техрец Т. Маточка, Корректор H. Швыцкая
Тираж 448 Поцписное
ВНИИПИ Госуцарственного комитета СССР по целам изобретений и открытий
113035, Москва, Ж-35, Раушская Маб., ц. 4/5
Заказ 638
Филиал ППП "Патент, г. Ужгороц, ул. Проектная, 4
Фор мула изобретения
0 -Т озиламинозамешенные 2, 5-циарил-1,3,4-оксациазолов обшей формулы гце А " Ce HS 4-Вг-СьНд, 4-СНЗ-С Ц
4-СН О-С Н, 4-С 2 Н, 1-С1оН, 25 в качестве органических люминофо5 ров.
Источники информации принятые во внимание при экспертизе
° 1. Красовицкий Б. М. и цр. Органические люминофоры, Л., Химия, с. 8.