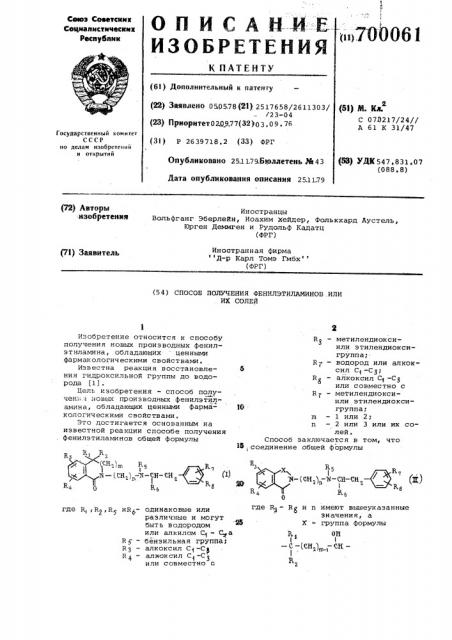
Способ получения фенилэтиламинов или их солей
Иллюстрации
Показать всеРеферат
ОПNCAHNE
ИЗОБРЕТЕНИЯ
Сеюз Советским
Сециапистичесиик
Республик (61) Дополнительный к патенту (22) Заявлено 050578 (23) 2517658/2611303/ (5!) N. Кл.
С 07D217/24// (23) Приоритет02Щ77(32)03.09 ° 76 61 К 31/47
Государственный комитет
СССР но делам изобретений и открытий (3l) P 2639718.2 (33} ФРГ (53) УДК 547,831,07 (088. 8) Опубликовано 25,1 179.Бюллетень РЙ 43
Дата опубликования описанмя 25,1179
Иностранцы
Вольфганг Эберлейн, Иоахим грейдер, Фолькхард Аустель, Юрген Деммген и Рудольф Кадатц (ФРГ) Иностранная фирма Д-р Карл Томэ Гмбх (ФРГ) P3) Заявитель (54) СПОСОБ ПОЛуЧЕНИй ФЕНИЛЭТИЛЛМИНОВ,ИЛИ
ИХ СОЛЕЙ
R — метилендиоксиили этилендиоксигруппа;
R — водород или алкокб сил CI -Cg;
R — алкоксил С -С е или совместно с
R — метилендиоксиили этилендиокси1Î группа;
m — 1 или 2;
n — 2 или 3 или их солей.
Способ заключается в том, что
; соединение общей формулы
R(К
СН2, К 7 ж — (Сн )„-я-СН-СН (1)
1 /
s, йв
В,6 8 гДе Н<,Н7,Rg иН6Ф
0Н
I I — с-(сн21 ;ск—
В2
В
R3
Из обретение относ итс я к способу получения новых производных фенилэтиламина, обладающих ценными фармакологическими свойствами, Известна реакция восстановления гидроксильной группы до водорода (1) .
Цель изобретения — способ полученкл новых производных фенилэтиламина, обладающих ценными фармакологическими свойствами, Это достигается основанным на известной реакции способе получения фенилэтиламинов общей формулы одинаковые или различные и могут быть водородом или алкилом С С а бензильная группа; алкоксил С -С алкоксил С -С3 или совместно с
) +7 м- (сн,1 -1 -сн-си (й)
2 и 2
R, 8
0 б где Н вЂ” R и и имеют вышеуказанные значения, а
Х вЂ” группа формулы
700061 или ФорМулы
ОН
-С- (СН2)щ
Р где R4, R и m имеют вышеукаэ анные значения, подвергают восстановлению с последующим выделением целевого продукта в виде основания или соли.
Восстановление предпочтительно осуществляют в растворителе, таком, например, как ледяная уксусная кислота, вода, этанол или этилацетат, водородом в момент, выделения при использовании например, .цинка (ледяной уксусной кислоты), олова (соляной кислоты) или дихлорида олова (соляной кислоты) или водородом в присутствии катализатора, такого, например, как палладий на угле при температуре. 0-150ОС.
Обычно процесс проводят при дав лении 1-7 атм. Соединения общей -фоРмулы. 1 могут быть переведены в их соли, например, соли соляной, фосфорной, бромистоводородной, серной, мОлочной, винной или малеиновой кислот.
Пример 1, Гидрохлорид
1-(4,4-диметил-б,7-диметокси-3,4-дигидро-2Н-изохинолин-1-он-2-ил) г
-3- (И-метил-N-2- (3, 4-диметоксйфенил) -этиламино) пропана . а) 1 (3-окси-4, 4-диметил-б, 7-диметокси-З, 4-дигидро-2Н-изохинолин-1-он-2-ил) -3-) N-метил-N-2- {3,4-диметок сифенил) -этиламино) -пропан, К. раствору 4,0 г (8,2 моля) .
1- (4,4-диметил-б, 7-диметокси-1, 3-диоксо- (2Н, 4Н) - изохинолин-2-ил) — 40
- 3- (N-метил-Л-2- (3, 4-диметоксифенил) -этиламино)-пропана в смеси
I00 мп диоксана..и 20 мл воды при
0 С добавляют 0,49 r (13 молей) боргидрида натрия. Перемешивают 45
8 ч при комнатной температуре, а затем добавляют 100 мл 2н,соляной кислоты. После экстрагирования хлороформом органическую фазу сушат сульфатом натрия и упаривают в ва- 50 кууме, получают 3,25 г (80%) продукта. . б) гидрохлорид 1- (4, 4-диметил-б, 7-диметокси- 3, 4-дигидро-2Н-и зохинолин-1 -он-2-ил)-3-(N-метил-N-2-(3 4-диметоксифенил) -этиламино)55
-пропана.
3,25 r .{6, 7 ммоля) -1-(3-окси-4,4-.
-диметил-б, 7-диметокси-З, 4-,цигидро-2Н-изохинолин-1-он-2-ил) - 3- (N-метил-N-2- (3, 4-диметоксифенил) -этил- 60 амино)-пропана растворяют в 80 мл ледяной уксусной кислоты и смешивают с 2, 3 г цинковой пыли, а затем в течение четырех часов кипятят с обратным холодильником. Для отделения цинковой пыли, горячий раствор фильтруют, фильтрат упаривают в вакууме досуха. Затем остаток растворяют в хлороформе и хлороформовую фазу промывают насыщенным водным раствором гидрокарбона-. та натрия и водой при встряхивании, сушат сульфатом натрия и упаривают.
Полученный продукт очищают хроматографией на силикагеле (хлороформ:метанол 19:1), Прибавлением эфирного раствора хлористого водорода переводят в гидрохлорид, получают 2,2 г (70В) продукта, т.пл ° 70 С (раэл), (хлороформ:метанол 9:1) = 0,45.
Пример 2. Гидрохлорид
1-(6,7-диметокси-3,4-дигидро-2Н-изозинолин-1-он-2-wrg3-5-этил-N-2-(3,4-диметоксифенил)-этил-амино)— пропана.
Раствор 5,0 r (10,7 ммолей) гидрохлорида 1- (б, 7-диметокси-3, 4-дигидро-2Н.-и зохинолин-1-он-2-ил) — 3-
- (N-2- (3, 4-диметоксифенил) -этиламино) -пронана в смеси 1, 38 r (30 ммолей) муравьиной кислоты и 1,5 r (20 ммолей) формалина и в течение часа нагревают до 100 С. После охлаждения реакционный раствор подщелачивают ,2н. раствором едкого натра, экстрагируют хлороформом, объединенные, органические фазы промывают водой, сушат и упаривают в вакууме. Остаток хроматографируют на силикагеле (хлороформ:метанол 50:1), основные фракции упаривают и основание действием эфирного раствора хлористого водорода переводят в гидрохлорид, получают 2,7 r (52%) продукта, т.пл. 178-1 7ФС.
Пример 3. Гидрохлорид
1- (б, 7-диметок си-З, 4-дигидро-2Н-изохин олин-1-он-2-ил) -3- (И-2— (3, 4-диметоксифенил) -этиламино)пропана.
В. раствор 2, 17 r (4,2 ммоля)
1- (б, 7-диметокси-З, 4-дигидро-2Н-изохинолин-1-он-2-ил) -3- (N-бенэил-N" 2- (3, 4-диметоксифенил) — этил амино) пропана,.; в 50 мл. метанола вводят 1 r палладия на угле (30%-ный) и .при комнатной температуре и давлении 5 атм в течение четырех часов гидрируют. По окончании поглощения водорода отфильтровывают катализатор и раствор упаривают в вакууме. Остаток .растворяют в ацетоне, гидрохлорид получают добавлением эфирного раствора хлористого водорода, получают 0,62 r (32% теории) продукта, т.пл, 132134 С.
Аналогично получают следующие соединения.
Гидрохлорид 1-(6,7-этилендиокси-3,4-дигидро-2Н-изохинолин-1-он-2-ил)—
-3"(N-метил-N-2-(3,4-диметоксифенил) -Зтиламино)-пропана Й = 0,40
700061 (хлороформ:метанол 19:1) ; гидрохлорид
2-(6,7-метилендиоксн-3,4-дигидро-2Н-изохинопин-1-он-2-ил)-3-(N-метил-N-2-(3,4-диметоксифенил)-этиламнно) -пропана Q 0,25 (хлороформ:метанол 19:1); гидрохлорид 1-(6,7-диметокси-3,4-дигндро-2Н-изохинолин-1.-он-2-ил)-2-(N-метил-М-2-(3,4-диметоксифенил)-этиламино|-этан Rg-=Î 25 (хлороформ:метанол 29:1); гидрохлорид 1-(6,7-диметокси-3,4-дигидро -2Н-Иэохинолин-1-он-2-ил)-2-(N-2-(3,4-диметоксифенил) -этиламино)этана Иу 0,15 (хлороформ:метанол
1Я 1); гидрохлорид 1- (6, 7-диметокси-3, 4-дигидро-2Н-иэохинолии-1-он-2-ил ) -3- (22-метил-N-2- (3-метоксифенил) -этиламино) -пропана R «О, 35 (хлороформ метанол 19:1) 1 гидрохлорид 1- (6,-7-диметокси-3, 4-дигидро-2Н-изохинолин-1-он-2-ил) -3- (й-метил-N-2- (3-метоксифенил) -этиламино)—
-пропана Rg= О, 30 (хлороформ:метанол 19:1); гидрохлорид 1- (6, 7-диметокси-3, 4-ди гидро-2Н-и зохинолин-1-он-2-ил) -3- (N-метил-N-2- (3, 4-мети-. лендис ксифенил) -этиламино) -пропана, Rf =0,40 (хлороформ:метанол 19:1); гидрохлорид 1-(4,4-диметил-б,7-диметокси-3,4-дигидро-2Н-изохинолин-1-он-2-ил)-3-(N-метил-N-2-.(3,4-диметоксифенил)-этиламино)-пропана, Кf = 0,25 (хлороформ:метанол 19:1); гидрсхлорнд 1-(4,4-диметил-б,7-диметокси-3,4-дигидро-2Н-изохинолин-1-он-2-ил)-3- .N-2-(3,4-диметоксифенил) зтиламино)-пропана, y= 0,20 (хлороформ:метанол 19:1); гидрохлорид
1-(4,4-днметил-б,7-диметокси-3 4-дигидро-2Н-изохинолин-1-он-2-ил) -2(N -метил-N-2-(3,4 -диметоксифенил)— этиламино| -этана Rf = 0,40 (хлороформ:метанол 19:1); гидрохлорид
1-(4,4-диметил-б,7-диметокси-3,4-дигидро-2Н-изохинолин-1-он-2«ил)-2— (N-2-(3,4-дииетоксифенил)-этилаииHGj -зтана, R$ = 0,20 (хлороформ:, метаноя 19."1); rидрохлорид
1-(7,8-диметокси-1,2,3,4-тетрагидро-5Н-2-бенэазепин-1-он-2- ил|-3-(N-метил-6-2-(3,4-диметокснфенил)-этиламино)-пропана, В(=0,20(хлороформ: метанол 19:1)гидрохлорид 1-(7,8-днметокси-1,2,3,4-тетрагидро-5Н-2-бензазепин -1-он-2-ил) -3- (N-2-(3, 4-диметокси фенил)-этиламино)-пропана,Rf=.0 10(хлороформ:метанол=.3:.1):гипоохлооил l-(6,7-диметокси-3,4-дигидро-2Н-изохинолин -1-он-2-ил) -3-(N-метил-й-2-(3,4-диметоксифенил) -этнламино)-пропав 78;
179 C,ãèäðoõëoðèä 1-(6,7-днметок -3,4-дигидро-2Н-изохинолин-1-он-2-ил)«
-3-(N-бензнл-И-2-(3,4-диметоксифенил)-этиламино) -пропана, R f =0, 8 (хлороформ метанол 19:1); гидрохлорид 1-(6,7-диметоксн-3,4-дигидро-2Н-изохинолин-1-он-2-ил) -3-(N-2-(3,4-диметоксифенил)»
-этиламино)-пропана т.пл. 132-134 С..
Формула изобретения
1. Способ пи учения фвнилэтиламинов общей формулы
СНа)ю Kg
-(cH ) — 5 — CH-СН
1 / (x)
3 1 I 1 6
О
10 где R«R,R@ и Вбодинаковые или различные и могут быть водородом или алкилом
С -С, а бензильная группа;
С6 СЗ алкок сил С4 -С3 или совместно с метилендиоксиили этилендиоксигруппа; водород или алкоксигруппа с
1-3 атомами углерода; алкоксил С -С3 илн совместно с метилендиоксиипи этнлендиоксигруппаг
1 или 2;
2 или 3, В8R4
ВуЗО
В. ОН
I 1 — С вЂ” (СНг) — СН—
) 2
50 М и формулы
ОН !
-С вЂ” (СН )
Kg где R, Ку и re. имеют вышеуказанные значения, подвергают восстановлению с последующим выделением целевого продукта в виде основания или соли.
2. Способ по п.l, о т л и ч а юд и и с я тем, что процесс восстановления проводят в растворителе при температуре О-150 С водородом
37 нлйнхсолей отличающийся что соединение общей формулы
К
5 Х i5 Р„
Fi,40 м (сн 1 ъ-сн-сн / (х)
zn г
4 2 6
О. где Rg-Rg и и имеют вышеуказанные значения, а Х вЂ” группа формулы
4S аООВ1
Составитель А.Орлов
Техред Э.Чужик КорректорГ Решетник
Редактор Р Антонова
Заказ 7260/62
Тираж 513 Подписное
ЦНИИПИ Государственного комитета СССР по делам изобретений и открытий
113035, Москва, Ж-35, Расейская наб ° »4/5
Филиал ППП Патент, г.ужгород, ул.Проектная,4 в момент выделения или водородом в присутствии катализатора.
Источники информации, принятые Во внимание при экспертизе
1.Вгеаз1ег z.í.спи bunco A.м.ы е ic еК ес1 1п,1Ъе reduction от И- пе1И t-3,2-парИо ИтпЫе vitttzAhe. J.Îrö. CtlGYn. 19Ьь 28
p-so<.