2-(п-аминофенил)-5-нитробензимидазол как промежуточный продукт для синтеза мономеров
Иллюстрации
Показать всеРеферат
:ъ
ОПИСАНИЕ
ИЗОБРЕТЕНИЯ
К АВТОИ:КОМУ СВИ ЕТЕЛЬСТВУ
Союз Советскик
Социалистических
Республик ()749834 (бт ) Дополнительмое к авт. саид-ву (22) Заявлено 141277 (21) 2555259/23-04 с присоединением заявки Но (23) Приоритет
Опубликовано 23.07.80. бюллетень М 27 (з )м. к,,з
С 07 D 235/18
1осударствениый комитет
СССР ио делам изобретений и открытий (53) УДН 547. 7811 .785(088.8) Дата опубликования описанию 230780
Л. С. ЭФрос, М. Х. Стрелец, Ю. И. Акулин, М. М. Рельмонт и А. М. Евдокимов (72) Авторы изобретения (71) Заявитель (54) 2-(и-АМИНОФЕНИЛ)-5-НИТРОБЕНЗИМИДАЗОЛ
КАК ПРОМЕЖУТОЧНЬЯ ПРОДУКТ ДЛЯ СИНТЕЗА
МОНОМЕРОВ
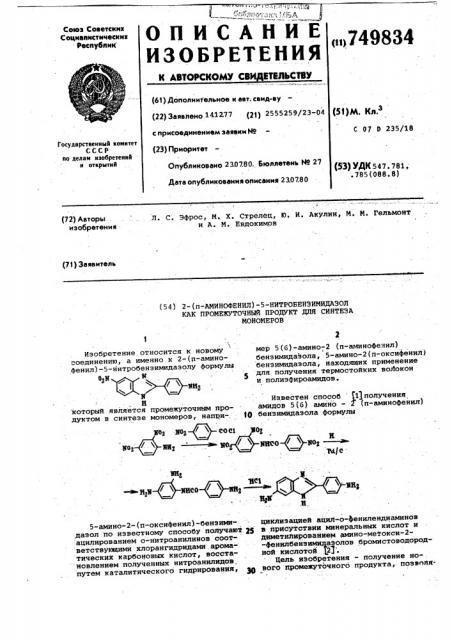
Изобретение относится к новому соединению, а именно к 2-(и-аминоФенил)-5-нитробензимидазолу формулы
I / ми
М
Н который является промежуточным продуктом в синтезе мономеров, напри-. 10 о мой / с г
38QO l E Мог ъцс юг
3П ая3 / МИС0 / МИг г
Hg циклиэацией ацил-о-фенилендиаминов
„ 5 в присутствии минеральных кислот и диметилированием амино-метокси-2-@eHshdeHsmaegjasozros бромистоводородной кислотой 2 ;
Цель изобретения - получение нового промежуточного продукта, позвс ля5-амино-2-(п-оксифенил)-бензимидазол по известному способу получают ацилированием о-нитроанилинов соответствующими хлорангидридами.ароматических карбоновых кислот, восста новлением полученных нитроанилидов путем каталитического гидрирования, 2 мер 5 (б) -амино-2 (п-аминофенил) бенэнмидазола, 5-амино-2(п-оксифенил) бензимидазола, находящих применение для получения термостойких воЛокон и полиэфироамидов.
Иэвестеи способ (1 получения амидов 5(б) амино - Е (п-аминофенил) бенэимидаэола формулы
834 ледуюцим нитрованием полученного 2 (п-аминофенил)-бензимидаэола в 70
85% серной кислоте при 0 — 5oC.
Синтез 5(б)-амино-2 (и-аминофенил)—
-бензимидазола с использованием заявляемого соединения происходит по следуюшей схеме:
t Е вн, — " — -- ©" о- )-юв, 3? И z и
Предлагаемый способ йолучения ами нофенилнитробензимидазола пОзволяет 20 получать без дополнительной перекристаллизации продукт высокой степени
- чистоты без примеси изомероВ ° .
Заявляемое амййонитропроизводное легко йревраЫается в мономер 5(б)—
-амино-2-(и-аминофенил) бензимидазол известным способом-каталитическим
--- восстановлением (Pd/С) водородом под атмосферным давлением в среде органйческого растворителя, например диметилформамиде и спирте с выходом
94%, т. пл. 234-235 °, Преимуцество заявляемого промежу"точного продукта при синтезе данного мойомера состоит . so-ïåðâblõ, в использовании менее дефицитйых о-фени-" лендиамина в,сравнении с 2,4-дийитроанилином, так как о-фенилейдиамин получается восстановлением о-нитроанилина,-который образуется в качестве побочного продукта при нитровании 40 анилина йаряду с .п-нитроанилином, на содяшим гораздо более-широкое применение в органическом синтеза? вовторых, в возможности синтеза 2-(п-,, -аминофенил)-5-йитробензимидазола без примеси иэомеров; в-третьих, в сушественио большем выходе, на стадиях 2-3-9б,и 94% против 90 и 91%, по известному способу . Что .касается синтеза другого мономера-5-амино-2(п-оксифенил)-бензимидазола, то синтез его на "основе предлагаемого
2-(и-аминофенил)-5-нитробенвимидазола также более прост, исключает использование дефицйтных исходных продуктов, концентрированной брОмйстоводо- родной кислоты (ам. полученйе 5-ами- но-2-(и-оксифенил)-бензимидазола s. примерах .4 и 5). на основании полученного йроме?куточйого продукта можно получить и 60 другйе мономвры.:--:::-:..
Пример 1. 2-(п-аминофенил).-бенэимидазол.,;, В 300 г полифосфориой Ййслоты (124% H®po ) перемешивании и 65
3 749 ющего более простым способом Получать мономеры высокой степени чистоты.
Это достигается 2-(п-аминофенил)-5-нитробензимидазолом указанной формулы, получаемым циклизацией о-фенилендиамина, п-аминобензойной кислотой в полифосфорной кислоте,с постемпературе 100-120 C загружают смесь 14,0 r (0,102 моля) п-аминобензойной кислоты и 10,8 г (0,1 моля) о-фенилендиамина, температуру реакционной массы повышают до 160 С, йосле-чего"дают охладиться до 120130 С,далее загрузку с последуюшим йагреванием до 160 повторяют. Всего за 4 приема загружают 56 г. (0,408 моля) п-аминобензойной кислоты и 43;2 r (О 4 моля) о-фенилендиамина. После
l о чего перемешивают при 160-165 С
0 5 ч, охлаждают до 120-130©С и осторожйо выливают при перемешивании в 100 мл горячей воды. Полученный раствор охлаждают и нейтрализуют приливанием к 1,6 л 12%-ного водного аммиака. Белый осадок отфильтровывают, промывают водой и сушат при
150 С. Выход 79 r(94%), т. пл. 244246© С, Л р и м е р 2. 2(п-аминофенил)-5-"йитробен з ймидаз ол.
В 300 мл серной кислоты (С-70-85%) йри охлаждении водой растворяют 62,7г (0,3 моля) 2-(п-аминофенил)бензимидазола. Полученный раствор охлаждают до 0©С и нитруют при перемешивании смесью 13 мл азотной кислоты (А . 1,5) (0.,305 моля) в 50 мл -серной кислоты, йоддерживая теьшературу 0-5: С. Пос-. ле окойчанйй приливания раствор перемешивают 1 час при 0"С и выливают в смесь 1,3 л воды и 1 л аммиачной воды. Орайжевый осадок отфильтровывают; тщательно проьиавают водой и сушат при 120бС, т, пл. 272-274 С. Выход 74 г (96%).
Хроматографйя на силуфоле: метилацетат, М 0,35; хлороформ-пропанол 10:1 Rf .0,46. Спектр ПИР в диметилацетамиде + 3% 1.1С1, о. 4Í 8 42, д 8,02, Ф„» 7,66, б 48,28; 0"У л 6,73, бнин. 6,28," 44 Е- 2 г,:ГВ,79 гц З.ij з
8 гцр
1 "Пример 3. 5(6)-амино-2-(п-амииофенил)бензимидазол. В 150 мл зтанола растворяют 12,7 г (0,05 моля) ,5(б)-нитро-2- - -.-. нил) бензими-1
749834
Формула изобретения
Составитель Г. Жукова
Редактор Л. Лашкова Техредй . Хастелевич Корректор, М арошн
Подписйое
Заказ 4972/50 Тираж 495
ЦИНИПИ Государственного комитета СССР по делам изобретений и Открытий
113035, Москва, Ж-35, Раушская наб., д. /
4/5
Филиал ППП "Патент", r- ужгород, ул . Ро
П ектная, 4
\ даэола, гндрируют водородом под атмосферным давлением в присутствии 2 г
1,7% катализатора Pd/C в течение 2 ч.
Раствор отфильтровывают, отгоняют
80 мл этанола, охлаждают, отфильтровывают выпавшие кристаллы, IlpoMHвают 50%-ным этанолом. Получают 10,5г (94%) мономера 5(6)-амино-2-(и-аминофенил) бензимидаэола, т. пл. 234235 С.
Пример 4. 5-нитро-2-(н-оксифенил) бензимидаэол.
К смеси 6 мп Н 504 в 50 мл воды при перемешивании добавляют 5,1 г (20 ммоля) 2(п-аминофенил)-5-нитробенэимидазола, образовавшуюся соль
s суспенэии диазотируют 1,3 г (20 ммо. ля) нитрита натрия при 0-5 С., Полученную желтую суспензию диазосоединения постепенно приливают к 100 мл кипя@ей 10% Н 50 . После окончания выделения азота отфильтровывают оранжевый осадок, растворяют в 25% МН ОН, красный раствор фильтруют и нейтрализуют соляной кислотой. Выпавший желтый осадок Отфильтровываюту промы- д вают водой и сушат при 150бС. Попу- чают 3,5 г (70%) 5-нитро-2-(и-оксифенил) бензимидазола, т.. пл. 338340еС (раэл.).
Найдено: 16,4%, С Н9Й 0 . 30
Вычислено и 16,3%.
Пример 5. 5-амино-2-(и-оксифенил) бенэимидазол.
В 30 мл этанола растворяют 2 r
5-нитро-2(п-оксифенил)бенэимидаэола, гидрируют водородом под атмос- ферным давлением в присутствии 0,5 г катализатора Pd/Ñ в течение 2 ч.
Раствор отфильтровывают, упариваЮт, получают 1,5 г (85%) 5-амино-2-(и-оксифенил)-бензимидазола, т. пл.
196-197 С (лит. т. пл. 195 С) °
Предлагаемое соединение позволяет получать мономеры высокой степени чистоты простым, доступньм способом.
У
2-(п-аминофенид)-5-нитробензимидьзол формулы
/X вк» и как промежуточный продукт для синтеза мономеров., Источники информации, принятые so внимание при экспертизе
1. Авторское свидетельство СССР
Ю 522602, кл. С 07 Р 235/04 1974.
2. Авторское свидетельство СССР
В 510474, кл. С 07 Р 235/18, 1974.