Способ измерения каталитической активности дисперсного катализатора
Иллюстрации
Показать всеРеферат
ОП ИСАНИЕ
ИЗОБРЕТЕНИЯ
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ
Союз Советскик
Социалистических
Республик о»789721 (61) Дополнительное к авт. сеид-ву (22) Заявлено 20. 11. 78 (21) 2687772/18-25 с присоединением заявки ¹ (23) Приоритет
Опубликовано 2 31280. Бюллетень Йо 47 (51)М. Кл.З
G 01 N 27/30
Государственный комитет
СССР но деяам нзооретеннй и открытии (53) УДК 543 253 (088 8) Дата опубликования описания 26.1280 ю.м.волвфвоввч, В.с.Дубасова, В.if.íèù>íåâ„,„
I ! (72) Авторы изобретения
1 !.* ) ! (73 ) Заявитель (54 ) СПОСОБ ИЗМЕРЕНИЯ КАТАЛИТИЧЕСКОЙ АКТИВНОСТИ
ДИСПЕРСНОГО КАТАЛИЗАТОРА
Изобретение относится к электрохимии .и касается способов измерения констант скорости каталитических реакций на дисперсных катализаторах, где необходимым условием является обеспечение равнодоступности поверхности
Известен способ измерения констан- . ты скорости элактрокаталитической реакции, при котором после изготовле» tO ния электрода производят измерение электрохимических характеристик. $1) .
Известен способ измерения электрохимических характеристик пористого электрода при изменении степени за- 15 топления (2) .
Однако в данном способе не были достигнуты условия равнодоступности поверхности катализатора.
Известен также способ измерения 20 каталитической активности дисперсногс катализатора, включающий измерение потенциала катализатора и тока реакции в условиях равнодоступности катализатора. 25
Изготавливают тонкослойные вращающиеся электроды, содержащие гидрофильный слой из исследуемого катализатора на гидрофобной фторопластовой основе, имеющие контролируемую и вос- 30 производимую. структуру и на них измеряют электрохимические характеристики: ток и потенциал. Из полученных данных определяют ток обмена, являющийся мерой активности. Критерием отсутствия внутридиффузионных ограничений в данном случае является независимость скорости реакции от толщины электрода (31
Недостатком этого способа является необходимость изготовления электродов строго воспроизводимой структуры различной толщины, что практически трудно осуществить. Измерения активности также необходимо проводить на электродах различной толщины. Кроме того, технологические операции, используемые для изготовления электродов, затрудняют достижение внутрикинетического режима и искажают результаты измерений.
Цель изобретения — упрощение спо» соба определения каталитической активности и повышение его точности.
Указанная цель достигается тем, что исследуемый катализатор вводят в водородно-кислородный матричный топливный элемент или электролизер в качестве одного иэ электродов и .поляризационные кривые электроды изме789721 ряют при изменении эатопленности порового пространства, причем для оценки активности выбирается область влагосодержаний и токов, где потенциал не зависит оТ стенки затопления.
Изменение затопленности порогового пространства осуществляется либо за счет проведения электрохимического процесса без отвода и подвода воды извне, либо путем прямого дозированного введения или выведения воды в исследуемый электрод с после- 1О дующей регистрацией характеристик.
Предлагаемый способ основан на следующих положениях теоретической макрокинетики.
Неравнодоступность поверхности катализатора определяется замедленностью диффузии газового реагента, растворенного в электролите, к поверхности катали3атора (внутридиффузионные потери энергии) и замед- 20 ленностью переноса ионов (внутриоммические потери энергии). Обычно и те и другие потери возрастают с ростом тока в газодиффузионных пористых электродах, оба эти вида потерь за- Q$ висят от степени затопленности порогового пространства электродов (Ч).
С ростом происходит возрастание внутридиффузионных потерь и уменьшение внутриоммических потерь энергии. ЗО
Поэтому зависимость, поляризации (q,) от V при постоянном и достаточно большом токе имеет вид кривой с минимумом. Во внутрикинетическом режиме, т,е. когда поверхность катализатора является равнодоступной, иными словами, изоконцентрационной и изопотенциальной, зависимость ), и всей (1) .кривой от V исчезает. Внутрикинетический режим газодиффузионного электрода достигается только при не очень больших токах и в области средних величин V, где оба вида потерь энергии пренебрежимо малы по сравнению с активиционными потерями энергии, т.е. активиционной поляризацией.4$
В этом случае зависимость q, от Ч при 1= const изображается кривой, имеющей нисходящую ветвь, плато (, =const) и восходящую ветвь.
Область плато и является областью $р равнодоступности поверхности катализатора, т.е. отвечает внутрикинетическому режиму.. Чем ниже ток, тем шире зоне внутрикинетического режима па шкале V.
$$
Таким образом, согласно теорети-. ческой макрокинетике, можно контро- лировать Наличие внутрикинетического режима, измеряя электрохимические характеристики электрода. При прове дении электрохимического процесса 60 в водородно-кислородном топливном элементе или электролизере без отвода и подвода воды извне определение увеличивающейся,генерируемой в ТЭ) или ум< пытающейся (потребляемой в 65 электролизере) величины V рассчитывается по закону Фарадея
М=эЛт где Ф вЂ” время измеряемое с момен,. та включения тока d) . Хотя происходящее при этом изменение концентрации электролита в принципе влияет на электрохимические характеристики, однако, практически это влияние очень мало по сравнению с влиянием Р
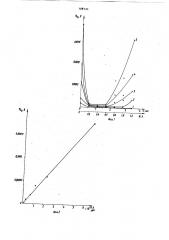
На фиг. 1 показана зависимость потенциала (Р) водородного электрода из платинового катализатора от влагосодержания при различных токах; на фиг. 2 - поляризационная кривая, построенная по данным фиг.1; на фиг.
3 — то же, для никелевого катализатора; на фиг. 4 — поляризационная кривая, построенная по данным фиг.3; на фиг. 5 — зависимость потенциала кислородного электрода из платинового катализатора от влагосодержания при различных токах, на фиг. б — поляризационная кривая, построенная по данным фиг. 5.
На фиг. 1 кривые 1 — 5 соответствуют токам 0,05; 0,1;, 0,3 0,5;
1,0мА; на фиг. 3 кривые 1-6 соответствуют токам 0,1; 0,3; 0,5; 1,05, 3,0 и 10,0 мА; на фиг. 5 кривые 113 соответствуют токам 20,50,100, 300,500 мкА; 1,3,5,10 30,50,100 и
150 мА.
Пример 1. Для измерения активности платинового катализатора. в реакции водорода порошок платины, имеющий поверхность 1,7 м /г в количестве 25 мг/см через сито с размерами ячейки 70 ммк просеивают на поверхность асбестовой матрицы, предварительно пропитанной раствором электролита (7н KOH). В качестве противоэлектрода (кислородного электрода) используют жесткогидрофобный платиновый электрод. ЭлЕктродом сравнения служит платиновый электрод, размещенный в центре мембраны в водородной камере. От элемента отбирают ток 100 мА каждые 30 мин регистрируют характеристики. Потенциал. (или поляризация) зависит от влагосодержания при различных токах (фиг.1), но при токах 0 05-0,50 мА поляризация электрода в широкой. зоне влагосодержаний не зависит от степени затопления и, следовательно, процесс лимитируется скоростью электрохимической реакции. Поляризационная кривая (фиг.2), из которой найдена плотность тока обмена по фор-, муле ъ =, равна 1,7. 10 А/см
1 о Р
Пример 2..Для измерения активности скелетного никелевого ката-. лизатора в реакции ионизации водорода порошок никеля с поверхностью
789721
4,6 м /г в количестве 100 мг/GM+ по примеру 1 наносят на асбестовую мембрану и процесс ведут при токе 10 мА.
Плотность тока обмена, найденная из .данных фиг. 4, составляет
1,9 10 A/ñì .
Пример 3. Для измерения активности платинового катализатора в реакции восстановления кислорода, порошок платины с поверхностью
19 м /г в количестве 25 мг/см по примеру 1 наносится на асбестовую матрицу. В качестве водородного электрода используется жесткогидрофобный платиновый электрод. Электрохимический процесс ведут при токе
150 мА. Характер регистрируют через каждый час. Потенциал электрода зависит от влагосодержания (фиг.5) ток обмена, равный 10 ® А, находят электрополяризацией на бесточный потенциал поляризационных кривых (фиг.6). Предлагаемый способ проще „ чем известный, поскольку в этом случае исключается операция изготовления электродов, которая является довольно сложной и обычно представляет собой технологический процесс, состоящий из нескольких стадий.
Исключение операции изготовления электродов в предлагаемом способе делает его также более точным, так как технологические операции затрудняют достижение внутрикинетического режима (например при прессовании уменьшается пористость катализатора, а значит, ухудшается его равнодоступность), а также вообще искажают сами результаты измерений (термообработка или введение смачивателя при гидрофобизации), Кроме того., контроль за равнодоступностью поверхности в предлагаемом способе осуществляется на одной и той же навеске катализатора, что также повышает точность метода, поскольку при изменении толщины катализатора или другого пористого тела очень трудно сохранять неизменной его структуРу. !
О
Формула изобретения
Способ измерения каталитической активности дисперсного катализатора, включающий измерение потенциала !
5 катализатора и тока реакции в условиях равнодоступности катализатора, отличающийся тем, что, с целью повышения точности способа и его упрощения, исследуемый катализа;щ тор вводят в водородно-кислородный матричный топливный элемент или электролизер в качестве одного из электродов и поляризационные кривые электрода измеряют при изменении затопленности порового пространства, причем для оценки активности выбирают область влагосодержаний и токов, при которых потенциал не зависит от степени затопления.
Источники информации, принятые во внимание при экспертизе
1.Авторское свидетельство СССР
Р 542131, кл. Q 01 Й 27/30, опублик. 1973.
2.Бурштейн P.М. и др. Кинетика электродных процессов. Сборник "Топливные элементы". N. 1968.
3. Stonebo t.Ð Ross Ч .м. ЕЬвс4 оhim a Acta. 21,441, 1976 (прототип) .