Способ определения субстрата или фер-ментативной активности b биологическомматериале
Иллюстрации
Показать всеРеферат
Всесо»оз» «» я и иС ЁЖ-и4 .
Союз Советских
Социалистических
Республик
{»»»797592
К ПАТЕИТУ (6») Дополнительный к патенту (51)М. Кл.з
С 12 Я 1/26 (22) Заявлено 06.05. 77 (2») 2481956/28-13 (23) Приоритет - (32) 09 ° 06 ° 76 (31) .Р 26 25 834 . 4 (33) ФРГ
Государственный комитет
СССР по делам изобретеннй н открытий
Опубликовано 15.0181.Бюллетень М 2 (53) УДК 6 12. 015 . 1 (088.8) Дата опубликования описания 1701,81
Иностранцы
Иозеф Даннингер, Ульферт-Денеке, Гунтер Ланг, Герхард М хал и Петер Решлау (И Г) (72) Авторы изобретения
Иностранная фирма
"Берингер Маннхайм ГМБХ" (71) Заявитель (ФРГ) (54) СПОСОБ ОПРЕДЕЛЕНИЯ СУБСТРАТА ИЛИ ФЕРМЕНТАТИВНОИ
АКТИВНОСТИ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ
Изобретение относится к биохимии, в частности к способам определения субстрата или ферментативной активности.
Известен способ определения субстрата или ферментативной активности в биологическом материале путем проведения окислительно-восстановительной реакции |1) .
Однако известный способ не позволяет провести точные определения, поскольку в биологическом материале имеются другие восстановительные вещества, которые создают помехи. Наиболее часто встречается аскорбиновая кислота, которая нарушает течение окислительно-восстановительных реакций с использованием НоОо образуюшего фермента, тетразолия или фенола.
Цель изобретения — повышение точности способа определения.
Поставленная цель достигается тем, что в реакционную смесь вносят аскор-25 батоксидаэу в Количестве 100 Ео/мл исходной смеси, а учет реакции ведут по образованию окрашенного продукта.
Кроме того, для получения окрашенного продукта аскорбатоксидаэу вводят одновременно или с НоОо. образуюшим ферментом, или с солью тетраэолия или же с феьолом.
Используемую аскорбатоксидазу можно получить иэ Zucchini (Cucurbuta реро »»»edullosa).
Предпочитаемыми методами для предлагаемого способа являются определение глюкозы с пероксидаэой или глюкозаоксидаэой и о-дианизидином или
2,2-азино-ди-3 -этилбензтиазс инсульфонатом (ABTS), определение глюкозы по методу гексокинаэы глюкоза-6-фосфатдегидрогеназы), обнаружение мочевой кислоты посредством фенола, аминоантипирина, пероксидаэы и уриказы, определение тироэина или пирокатехина посредством SMBTH (4-метил-б-калийсульфонил-бензтиазолонгидразона(2)) и тирозиназы или дифенолокси дазы.
Пример 1. Определение глюкозы с о.-дианизидином, пероксидазой, (POD) и глюкоэаоксидазой (GOD), изм ренное в фотометре, с длиной волны
432 нм, с температурой измерения
25оС (см. табл.1).
Кювета 1 соответствует ненарушенному измерению (нет аскорбиновой кислоты). Кюветы 2 и 3 показывают, 797592
Таблица 1
2,5 2,5
0,1 0,1
0,05 0,05
2,5
2,5
2,5 о-Дианизидин,, 0,5%
0,1
0,1
0,1
0,05
0 05
0,05
POD, О, 18% что 0,00573 или 0,000573% аскорбата практически полностью тормозят тест до 41,5%,кюветы 4 и 5-пок зывают полное устранение нарушения этих концентраций аскорбата добавкой по
0,0003% аскорбатоксидазы.
Пример 2..Обнаружение глюкозы с 2,2,-азино-ди(З-этил-бензтиазолинсульфонатом(6) ) (ASTS), РОЗ и ЯОЭ в фотометре, с длиной волны 432 ни, с температурой измерения 250С (см. табл. 2 .
Кювета 1 соответствует ненарушенному измерению (нет аскорбата). Кюветы 2 и 3 показывают, что 0,000573% или 0,0000573 мол.% аскорбата полностью тормозят тест до 2,1%.
Кюветы 4 и 5 показывают полное устранение нарушения этих концентраций аскорбата добавкой ro 0,ОООЗЪ аскорбатоксидазы.
Пример 3. Обнаружение моче- 26 вой кислоты посредством фенола, аминоантипирина, РО0 и урикаэы на аналитическом автомате (Aute Ana1уzar).
Принцип теста; Мочевая кислота +
+ O + H
+ Н О 2 Н Од + 2,4-дихлорфенал +
+ 4-аминоантипирин — хинодный краситель + 2 Н О
Изготовление растворов.
Реактив аскорбатоксмддэы. 9 600 мп З© бидистиллированиой воды растворяется содержимое флакона 1. Добавка О,З мл
Вг Ц-35. Затем смесь выдерживается в темном флаконе приблизительно щж
40С четыре недели,при 25оС одну не-9 делю.
Реактив уриказы. В 800 ил биднс тиллированной воды растворяется содержимое флакона 2. Добавка 2,0 мп
8rij-35. Затем смесь выдерживается в темном флаконе приблизительно нри 49
4 оС четыре недели, приблизительно при 25ОС одну неделю.
Концентрация растворов.
0,63% фосфатного буферного раствора, рН 5,6. g$
О, 35% трис/лимонной кислоты, рН 8,9, уриказы ) 0,001%, Р00 yi 0,000015%, 0,05% 2,4-дихлорфенола, 0,08% 4-аминоантйпирина.
Пример 4 ° Обнаружение глюкозы с НК/Я 6Р-ОА, МАРР, (NT и диа-, l
Фосфатный буферный раствор, рН 7,01, 1,368% форазой в фортометре. Измеряемая длина волны 492 нм, температура инкубацин 25оС (см. табл. 3) .
Кювета 1 соответствует ненарушенному измерению. Кювета 2 показывает, что 0 0000573% аскорбата может тормозить тест на 34% кювета 3 пока1 зывает, что 0,0003% аскорбатоксидазы полностью устраняет это нарушение.
П р и и е р 5. Определение глутамата посредствои диафоразы в фотоиетре. Измеряемля длина волны 492 нм, температура 25оС(см. табл. 4).
Кювета 1 соответствует ненарушенному измерению.
Кюветы 2 и 3 показывают, что
0,0029Ъ нли 0,00029Ъ аскорбата тормозят тест на 7003 или на 100%.
Кюветы 4 и 5 показывают полное устранение этого нарушения добавкой
0,00006Ъ аскорбатоксидазы.
П р и и е р 6. Определение тнрозина с 3-метил-6-калийсульфонил-бензтиазолон-гидраэоном-(2)(SNBTH) и тнрозиназой в фотометре, измеряемая длина волны 492 ни, измеряемая температура 25оС (си, табл. 5) .
Кювета 1 соответствует ненарушенному измерению, в кювете 2 0,00573 аскорбата снижает теоретическую величину на 35%, в кювете 3 это нарушение полностью устраняется добавкой
О,ООЗЪ аскорбатоксндазы.
Пример 7. Определение нирокатехина с SNBTH и дифенол-оксидаэой(см. табл. 6) .
Кювета 1 соответствует ненарушенному измерению, В кювете 20,011453 аскорбата снижают теоретическую величину на 47%, это нарушение полностью устраняется в кювете 3 добавкой 0,0003% аскорбатоксидаэы.
Полученный способ позволяет полностью устранить вызванные ошибки наличием аскорбиновой кислоты при проведении окислительно-восстановительных реакций.
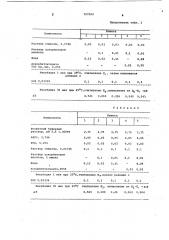
797592
Продолжение табл. 1 вета
Компоненты
Раствор глюкозы, 0,172%
0,03 0,03
0,03
О „03 0,03
Раствор аскорбиновой кислоты
0,1 0,01
0,1 Оф01
0,02 0,11 — . 0,09
0,12
Вода
0,02 . 0,02
Аскорбатоксидаза
500 ед./мл, 0,054
Инкубация 1 мин при 25оС, считывание Е, затем начинается реакция с
G0D О,ОЗЗЗЪ
0,1 0,1 0,1 0,1
Инкубация 30 мин при 25оС,считывание Е .,вычисление из Е -Е =6E
0,541 0,010 0,31б 0,540 0,543
ДЕ
Таблица 2
Фосфатный буферный раствор, рН 5,6 1,3609%
2,75
2,75
2,75
0,05
0 05
0,02
0,02
0,1
0,1
0,1
0,1
0,1
Раствор аскорбиновой кислоты, 1 ммоль
0,1 0,01 0,1 0,01
0,02 0,11 — 0,09
0,12
0,02 0,02
Инкубация 1 мин при 25 C,ñ÷èòûâàíèå Е, начало реакции с
0,1 0,1 0,1 0,1 0,1
600 0,0333%
Инкубация 30 мин при 25оС считывание Е, вычисление из Е -Е, = д Е
0,505 0,000 0,40 0,502 0,504
ABTS 2,74%
POD, 0,25%
Раствор глюкозы, 0,0172%
Вода
Аскорбатоксидата,005%
0,05
0,02
2,75 2,75
0,05 0,05
0,02 О 02
79Уг 9) Т а с и и ii 3
Компо
Кюветд
Фосфатный буферный раствор, рН 7,5, 1,36%
1,7
1,7
1,7
0,1
0,1
0,1
0,1
0,1
0,1
0,1
0,1
0,1
0,01 0,01
Аскорбатоксидаза, 0,00035%
0,03
0,04
0,03
Вода
Инкубация 3 мин при 25 С, считывание Е на ало реакции с
НК/G6P-DH-раствор по 0,14%
0,05 0,05 0,05
Ннкубация 15 мин, считывание Е, вычисление из E -E> = Ь E
0,234 0,307 0,230 Таблица 4
Фосфатный буферный раствор рН 5,6, 0,14%
1,30
1,20 1,29
0,1
0,1
0,1
0,1
0,01
Инкубация 3 мин при 25ОС, затем раствор набирается пипеткой в отдельные кюветы
3,7
TRA
1,0
1,0
1,0
0,68
NA0-раствор 0,5
Р ас твор ди афор азы О, 2
0,2
0,2
0,2
0,05
0,05
0 05
0,05
О, 0. i
0,05
0,8 с он
NADP INT по 0,1%
Диафораза 5 E/ìë, 0,1%
Раствор глюкозы, 0,005%
Раствор аскорбата 0,17%
Раствор глутамата, 0,02%
Раствор аскорбата, 0,086%
Аскорбатоксидаза, 0,01%
Калийфосфатный буферный раствор рН 8,6 с 1,5%. тритона-Х-100
1,18 1,27
0,1 0,1
0,1 0,01
0,02 0,02
1,0 1,0
0,2 0,2
0,05 0,05
0,05 0,05
797592
Продолжение табл. 4
Кювета
Компоненты
Считывание Е, начало реакции с
0,05 0,05 0,05
1 Т вЂ” раствор 0,2
0,05
0,05
Инкубация 15 мин при 25 С, считывание Е вычисление из Е -Z, = d Е о
Таблица 5
Фосфатный буферный, раствор рН 5,2, 3,44
2,77
2,77
2,77
0,05
0,05
0,05
SMBTH 0,1 мол, за
Раствор аскорбиновой кислоты, 0,172%
0,1
0 1
0,02
Вода
Аскорбатоксидаза
500 Е/мл 0,05%
0,02
0,05
0,05
0,05
Тироэиназа, 0,2
Инкубация 1 мин при 25ОС считывание Е>, начало реакции с
0,036% тирозин
0 05 0,05 0,05
Инкубация 1 час при 25ОС считывание Е, вычисление из Е>-E„ = AE
1t113 0,728 1,100
ЬЕ
Т а б л и ц а 6.
Фосфорный буферный раствор, рН 5 2, 3,4%
2,68
2,70.2,80
0,05
0,05
0i05
0,10
0,10
0,10
0,1, 0 i 3.
0,02
SMBTE1 0,1, З,ОЪ .
Пирокатехин, 0,0056%
Раствор аскорбата 20 ммоль
Аскорбатоксидаза 500 Е/мл
0 184 1г560 0ñ 380 Ог186 О ° 182
В! . 4Г". а °:- ° ° t з
° Е ЕР,Е 9» "Е Ре, ь. р р" "" " " 1675 92
Продолжение табл. >
Кювета
Компоненты
Инкубация 1 мин при 25 СР считывание Е, начало реакции с дефенолоксидаэа, 0,23 0,05 0,05 0 05
Инкубация 17 мин при 25 С считывание Е, вычисление из Е -Е = ЬЕ
О
IR 1
ЬЕ
0,890 0,485 Г,896
Формула изобретения
Составитель Морозова
T д . сталош Ко екто И. Муска
Редактор
Заказ 982
539 Подписное
ВНИИПИ Государственного комитета СССР по делам изобретений и открытий
113035 Москва Ж-35 Ра сная наб., д. 4 5
Филиал ППП "Патент", r. Ужгород, ул. Проектная, 4
1 ° Способ определения субстрата или ферментативной активности в биологическом материале путем проведения окислительно-восстановительной реакции, отличающийся тем,что, с целью повышения точности способа, в реакционную смесь вносят аскорбатоксидаэу в количестве
100 Eg/ìë исходной смеси, а учет реакции ведут по образованию окрашенного продукта.
2. Способ по п.1, о т л и ч а юшийся тем, что для получения окрашенного продукта аскорбатоксидазу вводят одновременно с Н Оаобразукщим ферментом.
3. Способ по п.1, о т л и ч а юшийся тем, что для получения окрашенного продукта аскорбатоксн2О даэу вводят одновременно с солью тетразолия.
4. Способ по п.1, о т л и ч а юшийся тем, что для получения окрашенного продукта аскорбатоксидаэу вводят одновременно с фенолом.
5. Способ по п.1, о т л и ч а юшийся тем, что используют аскорбатоксидазу иэ zucchini (Cucurbuta
pepo medullos.à).
30, Источники информации, принятые во внимание при экспертизе
1. В !ochemiса1 Сорреr Рroceedings
Иагкi292en И.Ч. 1965, с. 305-337.